Momelotinib:モメロチニブ(オムジャラ®)
| 投与量 | コース | 投与日 |
|---|---|---|
| 200mg/body 1日1回 | 1~ | Day 1~ |
前投薬
| なし |
その他
| 重度の肝機能障害 (Child Pugh分類C)を有する患者に投与する場合、 開始用量は150mg. |
| 副作用による減量後、 忍容性が認められ、 十分な効果が認められない場合は、 50mgずつ増量可能. |
2024年8月15日、 「骨髄線維症」 に対して薬価収載 (200mg1錠 4万2428.00円 / 1日薬価 4万2428.00円)
本コンテンツは特定の治療法を推奨するものではございません. 個々の患者の病態や、 実際の薬剤情報やガイドラインを確認の上、 利用者の判断と責任でご利用ください.
薬剤情報
JAK/ACVR1阻害薬 モメロチニブ塩酸塩水和物錠
グラクソ・スミスクライン株式会社の外部サイトに遷移します.
主な有害事象
SIMPLIFY-1試験 (二重盲検無作為化期における副作用)¹⁾、 総合製品情報概要より引用
骨髄抑制
- 血小板減少症 (18.7%、≧Grade3 7.0%)
- 貧血 (14.5%、≧Grade3 6.1%)
- 好中球減少症 (4.7%)
主な有害事象 10%以上
- 下痢 (18.2%、≧Grade3 2.8%)
- 頭痛 (17.8%、≧Grade3 0.5%)
- 悪心 (15.9%、≧Grade3 0.9%)
- 浮動性めまい (15.9%、≧Grade3 0%)
- 疲労 (14.5%、≧Grade3 0.5%)
- 腹痛 (10.3%、≧Grade3 1.4%)
その他重大な有害事象
- 感染症 (2.3%)
- 肝機能障害 (6.4%)
- 間質性肺疾患 (頻度不明)
特徴と注意点
他の抗悪性腫瘍剤との併用について、 有効性及び安全性は確立していない。
注意すべき相互作用
主にCYP3A4により代謝されるため薬物相互作用に注意。 また、 有機アニオン輸送ポリペプチド (OATP)1B1/1B3の基質であり、 乳癌耐性タンパク (BCRP)の阻害作用を示すため関連する薬剤との相互作用に注意。
作用機序
モメロチニブはJAK1/2およびACVR1に対する阻害作用を有する低分子化合物であり、 JAK1/2の下流のシグナル伝達物質 (STAT等)のリン酸化を阻害することで腫瘍増殖抑制作用を示す。
ACVR1の下流シグナル伝達分子 (SMAD)のリン酸化を阻害することでへプシジン産生を抑制し循環血中の鉄濃度を増加させ造血を促進する。
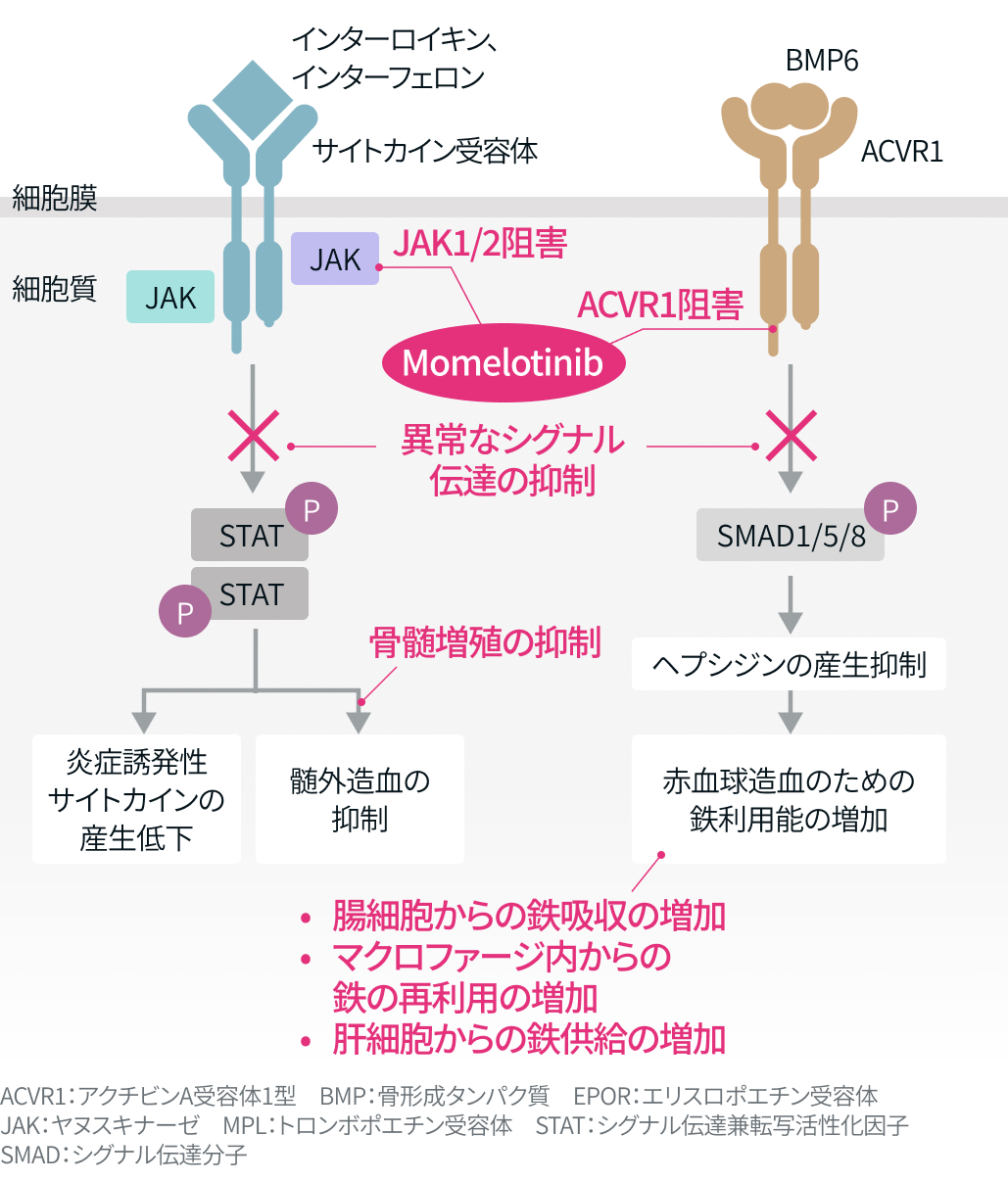
ACVR1 : アクチビンA受容体1型 LAK : ヤヌスキナーゼ STAT : シグナル伝達兼転写活性化因子 SMAD : シグナル伝達分子
用法・用量
モメロチニブとして200mgを1日1回経口投与する。 なお、 患者の状態により適宜減量する。
重度の肝機能障害 (Child Pugh分類C)を有する患者に投与する場合、150mgを開始用量とする。
また、 副作用が発現した場合には下表を参考に休薬又は減量する。 副作用による減量後、 忍容性が認められ、 十分な効果が認められない場合は、 50mgずつ増量することが可能である。
休薬・減量基準

オムジャラ®電子添文を基に作表
その他の注意点
肝炎ウイルス、 結核等が再活性化するおそれがあるので、 投与前に適切な感染症のスクリーニングを考慮。
投与開始前に患者に対して帯状疱疹の初期症状について説明し、 異常が認められた場合には速やかに連絡し適切な処置を受けるように指導。
関連する臨床試験の結果
SIMPLIFY-1試験¹⁾
多施設、 国際共同、第Ⅲ相、 無作為化、 二重盲検、 実薬対照試験。 JAK阻害剤による治療歴のないMF (骨髄線維症)患者を対象に、 SRR (脾臓縮小割合)に基づき、 モメロチニブとルキソリチニブの有効性を比較。
- 24週時の≧35% SRR (脾臓縮小割合) : モメロチニブ群26.5% vs ルキソリチニブ群29.5%、 p=0.014.
- 24週時のTSS (総症状スコア)改善割合 : モメロチニブ群28.4% vs ルキソリチニブ群42.2%、 p=0.98.
- 24週時のRBC-TI (赤血球輸血非依存)割合 : モメロチニブ群66.5% vs ルキソリチニブ群49.3%、 p<0.001.
- 24週時の輸血依存割合 : モメロチニブ群2% vs ルキソリチニブ群40.1%、 p=0.019.
SIMPLIFY-2試験²⁾
多施設、 第Ⅲ相、 無作為化、 非盲検、 BAT (best available therapy)対照試験。 ルキソリチニブによる治療中または治療歴のある貧血および/または血小板減少症を有するMF患者を対象にモメロチニブとBATの有効性および安全性を比較。
- 24週時の≧35% SRR (脾臓縮小割合) : モメロチニブ群6.7% vs BAT群5.8%、 p=0.90.
- 24週時のTSS (総症状スコア)改善割合 : モメロチニブ群26.2% vs BAT群5.9%、 p<0.001.
- 24週時のRBC-TI (赤血球輸血非依存)割合 : モメロチニブ群43.3% vs BAT群21.2%、 p=0.001.
MOMENTUM試験³⁾
多施設、 国際共同、 第Ⅲ相、 無作為化、 二重盲検、 実薬対照試験。 JAK阻害剤による治療歴があり、 症状および貧血を有するMF患者を対象に、 TSS (総症状スコア)の改善に基づき、 モメロチニブとダナゾール (骨髄線維症に対して本邦未承認)との有効性および安全性を評価。
- 24週時のTSS (総症状スコア)改善割合 : モメロチニブ群24.6% vs ダナゾール群9.2%、 p=0.0095.
- 24週時のTI (輸血非依存)割合 : モメロチニブ群30.0% vs ダナゾール群20.0%、 p=0.0116.
- 24週時の≧25% SRR (脾臓縮小割合) : モメロチニブ群39.2% vs ダナゾール群6.2%、 p<0.0001.
- 24週時のTSS (総症状スコア)のベースラインからの変化量 : モメロチニブ群-9.36 vs ダナゾール群-3.13、 p=0.0014.
- 24週時の≧35% SRR (脾臓縮小割合) : モメロチニブ群22.3% vs ダナゾール群3.1%、 p=0.0011.
- 二重盲検無作為化期赤血球輸血量がゼロ単位であった患者の割合 : モメロチニブ群35.4% vs ダナゾール群16.9%、 p=0.0012.
出典
- J Clin Oncol. 2017;35(34):3844-3850.
- Lancet Haematol. 2018;5(2):e73-e81.
- Lancet. 2023;401(10373):269-280.
関連コンテンツ
🔢DIPSS-PLUS / DIPSS
原発性骨髄線維症の国際的予後分類
骨髄増殖性腫瘍の症状を評価
最終更新:2025年4月14日
執筆担当 : 小澤病院薬剤部 長剛広
監修医師 : 東海大学血液腫瘍内科 扇屋大輔
Momelotinib
Momelotinib:モメロチニブ(オムジャラ®)
| 投与量 | コース | 投与日 |
|---|---|---|
| 200mg/body 1日1回 | 1~ | Day 1~ |
前投薬
| なし |
その他
| 重度の肝機能障害 (Child Pugh分類C)を有する患者に投与する場合、 開始用量は150mg. |
| 副作用による減量後、 忍容性が認められ、 十分な効果が認められない場合は、 50mgずつ増量可能. |
概要
2024年8月15日、 「骨髄線維症」 に対して薬価収載 (200mg1錠 4万2428.00円 / 1日薬価 4万2428.00円)
本コンテンツは特定の治療法を推奨するものではございません. 個々の患者の病態や、 実際の薬剤情報やガイドラインを確認の上、 利用者の判断と責任でご利用ください.
薬剤情報
JAK/ACVR1阻害薬 モメロチニブ塩酸塩水和物錠
グラクソ・スミスクライン株式会社の外部サイトに遷移します.
主な有害事象
SIMPLIFY-1試験 (二重盲検無作為化期における副作用)¹⁾、 総合製品情報概要より引用
骨髄抑制
- 血小板減少症 (18.7%、≧Grade3 7.0%)
- 貧血 (14.5%、≧Grade3 6.1%)
- 好中球減少症 (4.7%)
主な有害事象 10%以上
- 下痢 (18.2%、≧Grade3 2.8%)
- 頭痛 (17.8%、≧Grade3 0.5%)
- 悪心 (15.9%、≧Grade3 0.9%)
- 浮動性めまい (15.9%、≧Grade3 0%)
- 疲労 (14.5%、≧Grade3 0.5%)
- 腹痛 (10.3%、≧Grade3 1.4%)
その他重大な有害事象
- 感染症 (2.3%)
- 肝機能障害 (6.4%)
- 間質性肺疾患 (頻度不明)
特徴と注意点
他の抗悪性腫瘍剤との併用について、 有効性及び安全性は確立していない。
注意すべき相互作用
主にCYP3A4により代謝されるため薬物相互作用に注意。 また、 有機アニオン輸送ポリペプチド (OATP)1B1/1B3の基質であり、 乳癌耐性タンパク (BCRP)の阻害作用を示すため関連する薬剤との相互作用に注意。
作用機序
モメロチニブはJAK1/2およびACVR1に対する阻害作用を有する低分子化合物であり、 JAK1/2の下流のシグナル伝達物質 (STAT等)のリン酸化を阻害することで腫瘍増殖抑制作用を示す。
ACVR1の下流シグナル伝達分子 (SMAD)のリン酸化を阻害することでへプシジン産生を抑制し循環血中の鉄濃度を増加させ造血を促進する。

ACVR1 : アクチビンA受容体1型 LAK : ヤヌスキナーゼ STAT : シグナル伝達兼転写活性化因子 SMAD : シグナル伝達分子
用法・用量
モメロチニブとして200mgを1日1回経口投与する。 なお、 患者の状態により適宜減量する。
重度の肝機能障害 (Child Pugh分類C)を有する患者に投与する場合、150mgを開始用量とする。
また、 副作用が発現した場合には下表を参考に休薬又は減量する。 副作用による減量後、 忍容性が認められ、 十分な効果が認められない場合は、 50mgずつ増量することが可能である。
休薬・減量基準

オムジャラ®電子添文を基に作表
その他の注意点
肝炎ウイルス、 結核等が再活性化するおそれがあるので、 投与前に適切な感染症のスクリーニングを考慮。
投与開始前に患者に対して帯状疱疹の初期症状について説明し、 異常が認められた場合には速やかに連絡し適切な処置を受けるように指導。
関連する臨床試験の結果
SIMPLIFY-1試験¹⁾
多施設、 国際共同、第Ⅲ相、 無作為化、 二重盲検、 実薬対照試験。 JAK阻害剤による治療歴のないMF (骨髄線維症)患者を対象に、 SRR (脾臓縮小割合)に基づき、 モメロチニブとルキソリチニブの有効性を比較。
- 24週時の≧35% SRR (脾臓縮小割合) : モメロチニブ群26.5% vs ルキソリチニブ群29.5%、 p=0.014.
- 24週時のTSS (総症状スコア)改善割合 : モメロチニブ群28.4% vs ルキソリチニブ群42.2%、 p=0.98.
- 24週時のRBC-TI (赤血球輸血非依存)割合 : モメロチニブ群66.5% vs ルキソリチニブ群49.3%、 p<0.001.
- 24週時の輸血依存割合 : モメロチニブ群2% vs ルキソリチニブ群40.1%、 p=0.019.
SIMPLIFY-2試験²⁾
多施設、 第Ⅲ相、 無作為化、 非盲検、 BAT (best available therapy)対照試験。 ルキソリチニブによる治療中または治療歴のある貧血および/または血小板減少症を有するMF患者を対象にモメロチニブとBATの有効性および安全性を比較。
- 24週時の≧35% SRR (脾臓縮小割合) : モメロチニブ群6.7% vs BAT群5.8%、 p=0.90.
- 24週時のTSS (総症状スコア)改善割合 : モメロチニブ群26.2% vs BAT群5.9%、 p<0.001.
- 24週時のRBC-TI (赤血球輸血非依存)割合 : モメロチニブ群43.3% vs BAT群21.2%、 p=0.001.
MOMENTUM試験³⁾
多施設、 国際共同、 第Ⅲ相、 無作為化、 二重盲検、 実薬対照試験。 JAK阻害剤による治療歴があり、 症状および貧血を有するMF患者を対象に、 TSS (総症状スコア)の改善に基づき、 モメロチニブとダナゾール (骨髄線維症に対して本邦未承認)との有効性および安全性を評価。
- 24週時のTSS (総症状スコア)改善割合 : モメロチニブ群24.6% vs ダナゾール群9.2%、 p=0.0095.
- 24週時のTI (輸血非依存)割合 : モメロチニブ群30.0% vs ダナゾール群20.0%、 p=0.0116.
- 24週時の≧25% SRR (脾臓縮小割合) : モメロチニブ群39.2% vs ダナゾール群6.2%、 p<0.0001.
- 24週時のTSS (総症状スコア)のベースラインからの変化量 : モメロチニブ群-9.36 vs ダナゾール群-3.13、 p=0.0014.
- 24週時の≧35% SRR (脾臓縮小割合) : モメロチニブ群22.3% vs ダナゾール群3.1%、 p=0.0011.
- 二重盲検無作為化期赤血球輸血量がゼロ単位であった患者の割合 : モメロチニブ群35.4% vs ダナゾール群16.9%、 p=0.0012.
出典
- J Clin Oncol. 2017;35(34):3844-3850.
- Lancet Haematol. 2018;5(2):e73-e81.
- Lancet. 2023;401(10373):269-280.
関連コンテンツ
🔢DIPSS-PLUS / DIPSS
原発性骨髄線維症の国際的予後分類
骨髄増殖性腫瘍の症状を評価
最終更新:2025年4月14日
執筆担当 : 小澤病院薬剤部 長剛広
監修医師 : 東海大学血液腫瘍内科 扇屋大輔
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
がん薬物療法における治療計画をまとめたものです。
主要論文や適正使用ガイドをもとにした用量調整プロトコール、 有害事象対応をご紹介します。
なお、 本ツールは医師向けの教育用資料であり、 実臨床での使用は想定しておりません。 最新の添付文書やガイドラインを必ずご確認下さい。
また、 一般の方への情報提供ではないことを予めご了承ください。
