本コンテンツは特定の治療法を推奨するものではありません。 個々の患者の病態や、 実際の薬剤情報やガイドラインを確認の上、 利用者の判断と責任でご利用ください。
薬剤情報
スチバーガ® (レゴラフェニブ)
*バイエル薬品株式会社の外部サイトへ遷移します
投与スケジュール
【1コース】28日間
【催吐性】軽度³⁾、 最小度~軽度 (NCCN)⁴⁾
【FN発症】低リスク*
*GRID試験⁵⁾ではFNの報告がなく、 編集部で分類した。

レゴラフェニブ : 4週を1サイクルとして、 1日1回160mgを食後に3週間連日経口投与し、 その後1週間休薬する (空腹時投与や高脂肪食後投与は避ける)。
イマチニブ及びスニチニブによる治療後の患者を対象とし、 手術の補助化学療法としての有効性及び安全性は確立していない。
スチバーガ®電子添文情報¹⁾を基に編集部作成
Key Data|臨床試験結果
📊 GRID試験
Lancet. 2013;381(9863):295-302.
イマチニブ及びスニチニブ治療後に増悪した切除不能又は転移性消化管間質腫瘍を対象とした第III相無作為化比較試験である。 レゴラフェニブ+至適支持療法群133例、 プラセボ+至適支持療法群66例に2:1で割り付け、 主要評価項目は中央判定によるPFSとした。
プラセボ群の85%では、 増悪後にレゴラフェニブが投与された。
【有効性】レゴラフェニブ群 (vs プラセボ群)
- PFS中央値 4.8ヵ月 (vs 0.9ヵ月)
- HR 0.27 (95%CI 0.19–0.39、 p<0.0001)
- OS中央値 未到達 (vs 未到達)
- HR 0.77 (95%CI 0.42–1.41、 p=0.199)
- DCR 52.6% (vs 9.1%)
- ORR 4.5% (vs 1.5%)
【安全性】主な有害事象 : 全Grade (Grade≧3)
- 手足症候群 56.1% (19.7%)
- 高血圧 48.5% (23.5%)
- 下痢 40.2% (5.3%)
- 疲労 38.6% (2.3%)
- 口腔粘膜炎 37.9% (1.5%)
- 脱毛 23.5% (1.5%)
- 嗄声 22.0% (0%)
- 食欲減退 20.5% (0%)
- 斑状丘疹状皮疹 18.2% (2.3%)
- 悪心 15.9% (0.8%)
- 便秘 15.2% (0.8%)
- 筋肉痛 13.6% (0.8%)
- 発声障害 10.6% (0%)
各プロトコル
適格基準
GRID試験⁵⁾の主な適格基準
- イマチニブ及びスニチニブの前治療歴あり
- 18歳以上
- ECOG PS 0–1
- 好中球数≧1,500/mm³
- 血小板数≧10万/mm³
- Hb≧9.0g/dL
- 肝機能 : T-Bil≦1.5×ULN、 AST/ALT≦3.0×ULN
- 腎機能 : Cre≦1.5×ULN、 GFR≧30mL/min/1.73m²
用量レベル
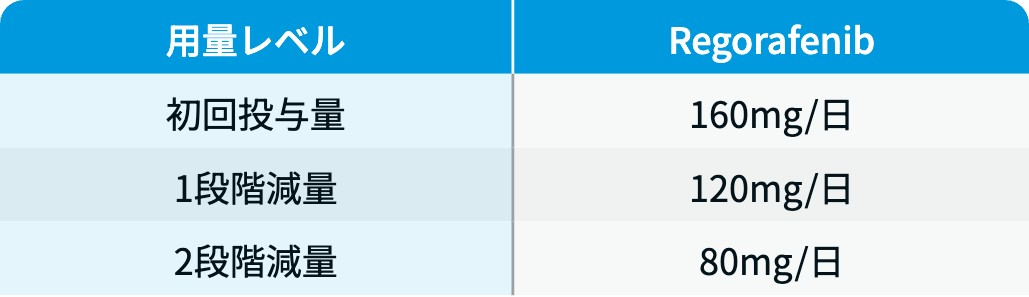
スチバーガ®電子添文情報¹⁾を基に編集部作成
減量は40mgずつ行い、 1日1回80mgを下限とする。
腎障害患者に対する用量調整
軽度腎機能障害 (eGFR 60–89mL/min/1.73m²) では、 未変化体・M-2・M-5のAUCおよびCmaxは腎機能正常患者と類似¹⁾しており、 用量調整は不要と考えられる。 中等度腎機能障害の薬物動態データは限られ、 重度腎機能障害・末期腎疾患では検討されていない¹⁾。
有害事象発現時の減量・休薬・中止基準

スチバーガ®電子添文情報¹⁾を基に編集部作成
レジメンの特徴と注意点
作用機序の特徴
レゴラフェニブは、 腫瘍血管新生 (VEGFR1–3、 TIE2)、 腫瘍微小環境 (PDGFR、 FGFR)、 腫瘍形成 (KIT、 RET、 RAF-1、 BRAF) に関わるキナーゼを阻害する (in vitro)。 また、 変異型KIT (V560G、 V654A、 D816H、 D820Y、 N822K) の活性も阻害する (in vitro)。 腫瘍移植マウスまたはラットでは、 腫瘍血管新生を抑制し、 腫瘍細胞増殖に関わるシグナル伝達経路を阻害した¹⁾。
レジメン適用時の注意事項
スチバーガ®電子添文¹⁾ 「重要な基本的注意」 の要約
皮膚障害 : 手足症候群、 中毒性表皮壊死融解症 (TEN)、 皮膚粘膜眼症候群 (SJS)、 多形紅斑等があらわれることがあるため、 必要に応じて皮膚科を受診するよう指導する。
肝機能障害 : 劇症肝炎、 肝不全、 肝機能障害、 黄疸があらわれることがあるため、 投与開始前及び投与中は定期的に肝機能検査を行い患者の状態を観察する。
肝機能異常を伴わない高アンモニア血症があらわれることがある。 意識障害を認めた場合は、 アンモニア値の測定を考慮する¹⁾。
高血圧 : 血圧上昇が認められることがあるため、 投与開始前及び投与中は定期的に血圧測定を行う。
創傷治癒遅延 : 創傷治癒を遅らせる可能性があるため、 手術が予定されている場合は手術前に投与を中断する。
FDA添付文書⁶⁾では、 予定手術の少なくとも2週間前には中止することが推奨されている。 術後の再開時期については、 十分な創傷治癒が確認されたうえで判断する。
タンパク尿 : タンパク尿があらわれることがあるため、 投与開始前及び投与中は定期的に尿タンパクを観察し異常時は適切な処置を行う。
甲状腺機能低下 : 甲状腺機能低下があらわれることがあるため、 投与中は定期的に甲状腺機能を検査する。
骨髄抑制 : 血小板減少、 好中球減少、 白血球減少があらわれることがあるため、 投与中は定期的に血液検査を実施する。
間質性肺疾患 : 咳嗽、 呼吸困難、 発熱等の臨床症状を十分に観察する。
出典
1) バイエル薬品株式会社. スチバーガ®錠40mg 電子添文. 2026年4月改訂 第5版.
2) バイエル薬品株式会社. スチバーガ適正使用ガイド〈大腸癌・消化管間質腫瘍 編〉. 2024年11月作成 第11版.
3) 日本癌治療学会. 制吐薬適正使用ガイドライン. 2023年10月改訂 第3版. 金原出版.
4) NCCN Clinical Practice Guidelines in Oncology (NCCN Guidelines®): Antiemesis. Version 1.2026.
5) Lancet. 2013;381(9863):295-302.
6) Stivarga® (regorafenib) prescribing information. Bayer HealthCare Pharmaceuticals Inc.; 2012.
最終更新日 : 2026年4月30日
執筆 : HOKUTO編集部 がん専門・指導薬剤師
執筆協力 : 国立がん研究センター中央病院 消化管内科 廣瀬俊晴
監修 : 国立がん研究センター中央病院 頭頸部・食道内科 加藤健
Regorafenib
本コンテンツは特定の治療法を推奨するものではありません。 個々の患者の病態や、 実際の薬剤情報やガイドラインを確認の上、 利用者の判断と責任でご利用ください。
薬剤情報
スチバーガ® (レゴラフェニブ)
*バイエル薬品株式会社の外部サイトへ遷移します
投与スケジュール
【1コース】28日間
【催吐性】軽度³⁾、 最小度~軽度 (NCCN)⁴⁾
【FN発症】低リスク*
*GRID試験⁵⁾ではFNの報告がなく、 編集部で分類した。

レゴラフェニブ : 4週を1サイクルとして、 1日1回160mgを食後に3週間連日経口投与し、 その後1週間休薬する (空腹時投与や高脂肪食後投与は避ける)。
イマチニブ及びスニチニブによる治療後の患者を対象とし、 手術の補助化学療法としての有効性及び安全性は確立していない。
スチバーガ®電子添文情報¹⁾を基に編集部作成
Key Data|臨床試験結果
📊 GRID試験
Lancet. 2013;381(9863):295-302.
イマチニブ及びスニチニブ治療後に増悪した切除不能又は転移性消化管間質腫瘍を対象とした第III相無作為化比較試験である。 レゴラフェニブ+至適支持療法群133例、 プラセボ+至適支持療法群66例に2:1で割り付け、 主要評価項目は中央判定によるPFSとした。
プラセボ群の85%では、 増悪後にレゴラフェニブが投与された。
【有効性】レゴラフェニブ群 (vs プラセボ群)
- PFS中央値 4.8ヵ月 (vs 0.9ヵ月)
- HR 0.27 (95%CI 0.19–0.39、 p<0.0001)
- OS中央値 未到達 (vs 未到達)
- HR 0.77 (95%CI 0.42–1.41、 p=0.199)
- DCR 52.6% (vs 9.1%)
- ORR 4.5% (vs 1.5%)
【安全性】主な有害事象 : 全Grade (Grade≧3)
- 手足症候群 56.1% (19.7%)
- 高血圧 48.5% (23.5%)
- 下痢 40.2% (5.3%)
- 疲労 38.6% (2.3%)
- 口腔粘膜炎 37.9% (1.5%)
- 脱毛 23.5% (1.5%)
- 嗄声 22.0% (0%)
- 食欲減退 20.5% (0%)
- 斑状丘疹状皮疹 18.2% (2.3%)
- 悪心 15.9% (0.8%)
- 便秘 15.2% (0.8%)
- 筋肉痛 13.6% (0.8%)
- 発声障害 10.6% (0%)
各プロトコル
適格基準
GRID試験⁵⁾の主な適格基準
- イマチニブ及びスニチニブの前治療歴あり
- 18歳以上
- ECOG PS 0–1
- 好中球数≧1,500/mm³
- 血小板数≧10万/mm³
- Hb≧9.0g/dL
- 肝機能 : T-Bil≦1.5×ULN、 AST/ALT≦3.0×ULN
- 腎機能 : Cre≦1.5×ULN、 GFR≧30mL/min/1.73m²
用量レベル

スチバーガ®電子添文情報¹⁾を基に編集部作成
減量は40mgずつ行い、 1日1回80mgを下限とする。
腎障害患者に対する用量調整
軽度腎機能障害 (eGFR 60–89mL/min/1.73m²) では、 未変化体・M-2・M-5のAUCおよびCmaxは腎機能正常患者と類似¹⁾しており、 用量調整は不要と考えられる。 中等度腎機能障害の薬物動態データは限られ、 重度腎機能障害・末期腎疾患では検討されていない¹⁾。
有害事象発現時の減量・休薬・中止基準

スチバーガ®電子添文情報¹⁾を基に編集部作成
レジメンの特徴と注意点
作用機序の特徴
レゴラフェニブは、 腫瘍血管新生 (VEGFR1–3、 TIE2)、 腫瘍微小環境 (PDGFR、 FGFR)、 腫瘍形成 (KIT、 RET、 RAF-1、 BRAF) に関わるキナーゼを阻害する (in vitro)。 また、 変異型KIT (V560G、 V654A、 D816H、 D820Y、 N822K) の活性も阻害する (in vitro)。 腫瘍移植マウスまたはラットでは、 腫瘍血管新生を抑制し、 腫瘍細胞増殖に関わるシグナル伝達経路を阻害した¹⁾。
レジメン適用時の注意事項
スチバーガ®電子添文¹⁾ 「重要な基本的注意」 の要約
皮膚障害 : 手足症候群、 中毒性表皮壊死融解症 (TEN)、 皮膚粘膜眼症候群 (SJS)、 多形紅斑等があらわれることがあるため、 必要に応じて皮膚科を受診するよう指導する。
肝機能障害 : 劇症肝炎、 肝不全、 肝機能障害、 黄疸があらわれることがあるため、 投与開始前及び投与中は定期的に肝機能検査を行い患者の状態を観察する。
肝機能異常を伴わない高アンモニア血症があらわれることがある。 意識障害を認めた場合は、 アンモニア値の測定を考慮する¹⁾。
高血圧 : 血圧上昇が認められることがあるため、 投与開始前及び投与中は定期的に血圧測定を行う。
創傷治癒遅延 : 創傷治癒を遅らせる可能性があるため、 手術が予定されている場合は手術前に投与を中断する。
FDA添付文書⁶⁾では、 予定手術の少なくとも2週間前には中止することが推奨されている。 術後の再開時期については、 十分な創傷治癒が確認されたうえで判断する。
タンパク尿 : タンパク尿があらわれることがあるため、 投与開始前及び投与中は定期的に尿タンパクを観察し異常時は適切な処置を行う。
甲状腺機能低下 : 甲状腺機能低下があらわれることがあるため、 投与中は定期的に甲状腺機能を検査する。
骨髄抑制 : 血小板減少、 好中球減少、 白血球減少があらわれることがあるため、 投与中は定期的に血液検査を実施する。
間質性肺疾患 : 咳嗽、 呼吸困難、 発熱等の臨床症状を十分に観察する。
出典
1) バイエル薬品株式会社. スチバーガ®錠40mg 電子添文. 2026年4月改訂 第5版.
2) バイエル薬品株式会社. スチバーガ適正使用ガイド〈大腸癌・消化管間質腫瘍 編〉. 2024年11月作成 第11版.
3) 日本癌治療学会. 制吐薬適正使用ガイドライン. 2023年10月改訂 第3版. 金原出版.
4) NCCN Clinical Practice Guidelines in Oncology (NCCN Guidelines®): Antiemesis. Version 1.2026.
5) Lancet. 2013;381(9863):295-302.
6) Stivarga® (regorafenib) prescribing information. Bayer HealthCare Pharmaceuticals Inc.; 2012.
最終更新日 : 2026年4月30日
執筆 : HOKUTO編集部 がん専門・指導薬剤師
執筆協力 : 国立がん研究センター中央病院 消化管内科 廣瀬俊晴
監修 : 国立がん研究センター中央病院 頭頸部・食道内科 加藤健
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
がん薬物療法における治療計画をまとめたものです。
主要論文や適正使用ガイドをもとにした用量調整プロトコール、 有害事象対応をご紹介します。
なお、 本ツールは医師向けの教育用資料であり、 実臨床での使用は想定しておりません。 最新の添付文書やガイドラインを必ずご確認下さい。
また、 一般の方への情報提供ではないことを予めご了承ください。