Epcoritamab:エプコリタマブ(エプキンリ®)
| 投与量 | コース | 投与日 |
|---|---|---|
| 0.16mg 皮下投与 | 1 | day 1 |
| 0.8mg 皮下投与 | 1 | day 8 |
| 3mg 皮下投与 | 1 | day 15 |
| 48mg 皮下投与 | 1 | day 22 |
| 48mg 皮下投与 | 2、 3 | day 1、 8、 15、 22 |
| 48mg 皮下投与 | 4-9 | day 1、 15 |
| 48mg 皮下投与 | 10- | day 1 |
前投薬
| 1サイクル目 (day 1、8、15、22):副腎皮質ホルモン剤、 抗ヒスタミン剤、 解熱鎮痛剤 (30-120分前). |
| 1サイクル目のepcoritamab投与後1、 2、 3日目:副腎皮質ホルモン剤. |
| 2サイクル目以降:前回投与時にGrade2以上のCRSを認めた場合、 1サイクル目と同様の副腎皮質ホルモン剤を使用する. |
| より詳細なCRS軽減のための薬剤投与は概要欄参照. |
| CRS:cytokine release syndrome (サイトカイン放出症候群) |
その他
| CRSの緊急時に備えてトシリズマブを速やかに使用できるよう準備する. |
本コンテンツは特定の治療法を推奨するものではございません。 個々の患者の病態や、 実際の薬剤情報やガイドラインを確認の上、 利用者の判断と責任でご利用ください。
2025年2月20日、 再発又は難治性の濾胞性リンパ腫 (FL) Grade 1~3Aに対する適応が追加された。
薬剤情報
*アッヴィ製薬株式会社の外部サイトへ遷移します
投与スケジュール
【1コース】28日間
【催吐性】 軽度*
【FN発症】低リスク**
*NCCN Guidelines Version 2.2025 Antiemesisを引用
**EPCORE NHL-1試験³⁾のFN発生率1.2%を基に編集部が分類
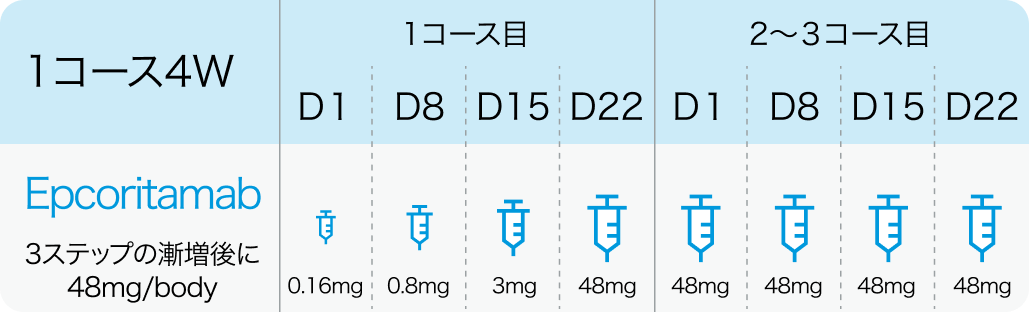
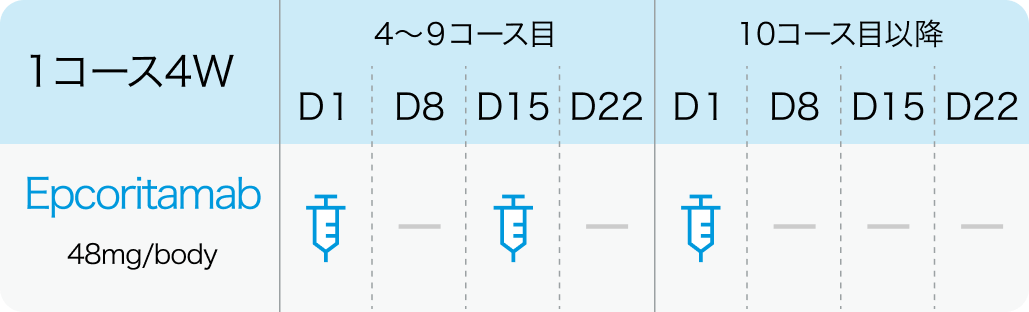
エプキンリ®電子添文¹⁾を基に編集部作成
- 28日間を1サイクルとして投与
- 1サイクル目は1日目に0.16mg、 8日目に0.8mg、 15日目に3mg、 22日目に48mgを皮下投与 (3ステップで漸増)
DLBCLやFL Grade 3Bに対する2ステップ漸増法とは異なる点に注意
- 2・3サイクル目は各週 (1、 8、 15、 22日目) に48mg、 4~9サイクル目は隔週 (1、 15日目) に48mg、 10サイクル目以降は4週ごと (1日目) に48mgを皮下投与
Key Data|臨床試験結果
📊 EPCORE NHL-1試験³⁾
Lancet Haematol. 2024;11(8):e593-e605.
2ライン以上の治療歴を有する再発又は難治性CD20陽性FL Grade 1~3A患者を対象とした国際共同の単群第I/II相試験 の第2相パートでは、 主要コホート (128例) と初回サイクル最適化コホート (86例) に皮下エプコリタマブ48mgを投与。 主要コホートでは初回サイクルに段階的増量とプレドニゾロンを用いたサイトカイン放出症候群 (CRS) 予防を行い、 主要評価項目は独立判定による全奏効率 (ORR) とされた。 最適化コホートでは3mgの中間用量追加、 水分管理、 デキサメタゾン予防を併用し、 CRSの発現割合を主要評価項目とした。
【有効性】主要コホート128例
- ORR 82.0%
【安全性】主な有害事象 : 全Grade (≧Grade3)
FL最適化コホート86例のデータ²⁾より一部抜粋
- サイトカイン放出症候群 48.8% (0%)
- 好中球減少症 17.4% (16.3%)
- 貧血 11.6% (2.3%)
- 血小板減少症 9.3% (2.3%)
- リンパ球減少症 4.7% (4.7%)
- 注射部位反応 26.7%
- 疲労 19.8%
- 発熱 14.0%
- 注射部位紅斑 8.1%
- 末梢性浮腫 14.0%
- 倦怠感 4.7%
- COVID-19 18.6%
- 上気道感染 4.7%
- 尿路感染 4.7%
- 下痢 11.6%
- 悪心 12.8%
- 便秘 20.9%
- 頭痛 14.0%
- 浮動性めまい 8.1%
- ALT増加 9.3%
- AST増加 8.1%
- 咳嗽 16.3%
- 呼吸困難 5.8%
- 関節痛 12.8%
- 背部痛 9.3%
- 筋肉痛 1.2%
- 不眠症 10.5%
- 発疹 9.3%
- 紅斑 3.5%
- 高血糖 5.8%
各プロトコル
適格基準
EPCORE NHL-1試験³⁾の主な選択基準
- 年齢 : 18歳以上
- 抗CD20抗体を含む全身抗腫瘍療法を含め、 2レジメン以上の前治療歴を有する
- 腎機能: CrCl ≧45mL/min/1.73m²
- 肝機能: 総ビリルビン ≦1.5x ULN、 ALT/AST ≦3x ULN
休薬・中止基準
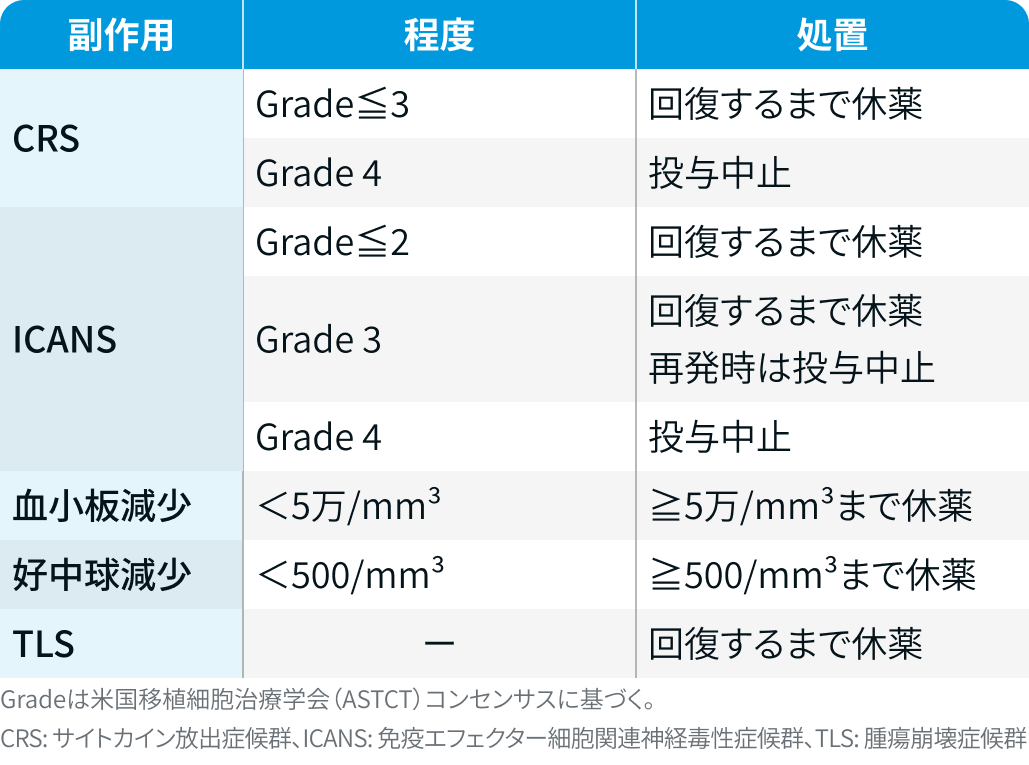
エプキンリ®電子添文¹⁾を基に編集部作成
休薬期間を踏まえた投与スケジュールの調整方法
CRS軽減のため、 以下のいずれかに該当する場合は、 1サイクル目の投与方法に戻して再開¹⁾²⁾ :
- 0.16mgと0.8mg、 又は0.8mgと3mgの投与間隔が8日超
- 3mgと48mgの投与間隔が14日超
- 48mgの投与間隔が6週間超
レジメンの特徴と注意点
🧑⚕️エプコリタマブが再発又は難治性のCD20陽性FL Grade 1~3Aにも使用可能となり、 同疾患における治療選択肢が広がりました。
東海大学医学部血液腫瘍内科 扇屋大輔先生
作用機序
エプコリタマブは、 T細胞表面のCD3およびB細胞腫瘍表面のCD20の双方に結合する、 ヒト化IgG1型二重特異性モノクローナル抗体である。
これによりT細胞の増殖と活性化が誘導され、 CD20陽性腫瘍細胞の傷害が引き起こされると考えられている。
CRS予防を目的とした前投薬
1サイクル目 (1、 8、 15、 22日目) : 全患者が対象
- 副腎皮質ホルモン剤
- エプコリタマブ投与30~120分前
- エプコリタマブ投与後1~3日目
- 解熱鎮痛薬・抗ヒスタミン薬
- エプコリタマブ投与30~120分前
2サイクル目以降
- 対象 : 前回投与後にGrade 2–3のCRSが出現した患者は、 Grade≧2のCRSが認められなくなるまで以下の前投薬を継続
- 副腎皮質ホルモン剤
- エプコリタマブ投与30~120分前
- エプコリタマブ投与後1~3日目
EPCORE NHL-1試験の最適化コホートでは、 1サイクル目のエプコリタマブ投与に際し、 デキサメタゾン15mgの静脈内投与が推奨されていた。 必要に応じて、 同薬の投与量は12mgまで減量可能とされた。 また、 エプコリタマブ投与前24時間には2~3Lの水分摂取および降圧薬の中断、 投与当日の等張輸液500mLの投与、 さらに投与後24時間における2~3Lの水分摂取も推奨された²⁾。
レジメン適用時の注意事項
- 第1サイクルの各投与後は入院管理を検討
- 1サイクル22日目 (初回の48mg投与日) は、 投与後48時間の入院管理が必須
- CRS発現時に備えてトシリズマブを速やかに使用できるよう準備する
- 免疫エフェクター細胞関連神経毒性症候群 (ICANS) があらわれることがあるため、 失語症、 意識レベルの変化、 認知能力の障害、 筋力低下、 痙攣発作、 脳浮腫等について、 観察を行う
- エプコリタマブ投与前にニューモシスチス・イロベチイなどの感染の有無を確認し、 適切な処置を行う。 投与中は、 感染症 (帯状疱疹等の再活性化や日和見感染を含む) の発現・悪化に十分注意する
- 腫瘍崩壊症候群の発現に留意し、 血清電解質や腎機能の検査を実施するなど、 患者の状態を十分に観察する
- 進行性多巣性白質脳症 (PML) が報告されているため、 意識障害、 認知機能障害、 麻痺、 構音障害、 失語などが出現した場合には、 MRIや脳脊髄液検査を実施し、 エプコリタマブの投与を中止のうえ、 適切に対処する
- 大腿部、 腹部等に左右交互に投与するなど同一注射部位を避ける
RMP【重要な特定されたリスク】
エプキンリ®医薬品リスク管理計画書 (RMP)
- CRS
- ICANS
- 感染症
- 腫瘍崩壊症候群
- 血球減少
- 進行性多巣性白質脳症
出典
- エプキンリ®皮下注4mg, 48mg 適正使用ガイド (2025年2月改訂) [最終閲覧 : 2025/5/28]
- エプキンリ®皮下注4mg, 48mg 適正使用ガイド (2025年2月改訂) [最終閲覧 : 2025/5/28]
- Lancet Haematol. 2024;11(8):e593-e605.
最終更新 : 2025年5月28日
執筆 : HOKUTO編集部 がん専門・指導薬剤師
監修医師 : 東海大学血液腫瘍内科 扇屋大輔
Epcoritamab (Grade 1~3A)
Epcoritamab:エプコリタマブ(エプキンリ®)
| 投与量 | コース | 投与日 |
|---|---|---|
| 0.16mg 皮下投与 | 1 | day 1 |
| 0.8mg 皮下投与 | 1 | day 8 |
| 3mg 皮下投与 | 1 | day 15 |
| 48mg 皮下投与 | 1 | day 22 |
| 48mg 皮下投与 | 2、 3 | day 1、 8、 15、 22 |
| 48mg 皮下投与 | 4-9 | day 1、 15 |
| 48mg 皮下投与 | 10- | day 1 |
前投薬
| 1サイクル目 (day 1、8、15、22):副腎皮質ホルモン剤、 抗ヒスタミン剤、 解熱鎮痛剤 (30-120分前). |
| 1サイクル目のepcoritamab投与後1、 2、 3日目:副腎皮質ホルモン剤. |
| 2サイクル目以降:前回投与時にGrade2以上のCRSを認めた場合、 1サイクル目と同様の副腎皮質ホルモン剤を使用する. |
| より詳細なCRS軽減のための薬剤投与は概要欄参照. |
| CRS:cytokine release syndrome (サイトカイン放出症候群) |
その他
| CRSの緊急時に備えてトシリズマブを速やかに使用できるよう準備する. |
概要
本コンテンツは特定の治療法を推奨するものではございません。 個々の患者の病態や、 実際の薬剤情報やガイドラインを確認の上、 利用者の判断と責任でご利用ください。
2025年2月20日、 再発又は難治性の濾胞性リンパ腫 (FL) Grade 1~3Aに対する適応が追加された。
薬剤情報
*アッヴィ製薬株式会社の外部サイトへ遷移します
投与スケジュール
【1コース】28日間
【催吐性】 軽度*
【FN発症】低リスク**
*NCCN Guidelines Version 2.2025 Antiemesisを引用
**EPCORE NHL-1試験³⁾のFN発生率1.2%を基に編集部が分類


エプキンリ®電子添文¹⁾を基に編集部作成
- 28日間を1サイクルとして投与
- 1サイクル目は1日目に0.16mg、 8日目に0.8mg、 15日目に3mg、 22日目に48mgを皮下投与 (3ステップで漸増)
DLBCLやFL Grade 3Bに対する2ステップ漸増法とは異なる点に注意
- 2・3サイクル目は各週 (1、 8、 15、 22日目) に48mg、 4~9サイクル目は隔週 (1、 15日目) に48mg、 10サイクル目以降は4週ごと (1日目) に48mgを皮下投与
Key Data|臨床試験結果
📊 EPCORE NHL-1試験³⁾
Lancet Haematol. 2024;11(8):e593-e605.
2ライン以上の治療歴を有する再発又は難治性CD20陽性FL Grade 1~3A患者を対象とした国際共同の単群第I/II相試験 の第2相パートでは、 主要コホート (128例) と初回サイクル最適化コホート (86例) に皮下エプコリタマブ48mgを投与。 主要コホートでは初回サイクルに段階的増量とプレドニゾロンを用いたサイトカイン放出症候群 (CRS) 予防を行い、 主要評価項目は独立判定による全奏効率 (ORR) とされた。 最適化コホートでは3mgの中間用量追加、 水分管理、 デキサメタゾン予防を併用し、 CRSの発現割合を主要評価項目とした。
【有効性】主要コホート128例
- ORR 82.0%
【安全性】主な有害事象 : 全Grade (≧Grade3)
FL最適化コホート86例のデータ²⁾より一部抜粋
- サイトカイン放出症候群 48.8% (0%)
- 好中球減少症 17.4% (16.3%)
- 貧血 11.6% (2.3%)
- 血小板減少症 9.3% (2.3%)
- リンパ球減少症 4.7% (4.7%)
- 注射部位反応 26.7%
- 疲労 19.8%
- 発熱 14.0%
- 注射部位紅斑 8.1%
- 末梢性浮腫 14.0%
- 倦怠感 4.7%
- COVID-19 18.6%
- 上気道感染 4.7%
- 尿路感染 4.7%
- 下痢 11.6%
- 悪心 12.8%
- 便秘 20.9%
- 頭痛 14.0%
- 浮動性めまい 8.1%
- ALT増加 9.3%
- AST増加 8.1%
- 咳嗽 16.3%
- 呼吸困難 5.8%
- 関節痛 12.8%
- 背部痛 9.3%
- 筋肉痛 1.2%
- 不眠症 10.5%
- 発疹 9.3%
- 紅斑 3.5%
- 高血糖 5.8%
各プロトコル
適格基準
EPCORE NHL-1試験³⁾の主な選択基準
- 年齢 : 18歳以上
- 抗CD20抗体を含む全身抗腫瘍療法を含め、 2レジメン以上の前治療歴を有する
- 腎機能: CrCl ≧45mL/min/1.73m²
- 肝機能: 総ビリルビン ≦1.5x ULN、 ALT/AST ≦3x ULN
休薬・中止基準

エプキンリ®電子添文¹⁾を基に編集部作成
休薬期間を踏まえた投与スケジュールの調整方法
CRS軽減のため、 以下のいずれかに該当する場合は、 1サイクル目の投与方法に戻して再開¹⁾²⁾ :
- 0.16mgと0.8mg、 又は0.8mgと3mgの投与間隔が8日超
- 3mgと48mgの投与間隔が14日超
- 48mgの投与間隔が6週間超
レジメンの特徴と注意点
🧑⚕️エプコリタマブが再発又は難治性のCD20陽性FL Grade 1~3Aにも使用可能となり、 同疾患における治療選択肢が広がりました。
東海大学医学部血液腫瘍内科 扇屋大輔先生
作用機序
エプコリタマブは、 T細胞表面のCD3およびB細胞腫瘍表面のCD20の双方に結合する、 ヒト化IgG1型二重特異性モノクローナル抗体である。
これによりT細胞の増殖と活性化が誘導され、 CD20陽性腫瘍細胞の傷害が引き起こされると考えられている。
CRS予防を目的とした前投薬
1サイクル目 (1、 8、 15、 22日目) : 全患者が対象
- 副腎皮質ホルモン剤
- エプコリタマブ投与30~120分前
- エプコリタマブ投与後1~3日目
- 解熱鎮痛薬・抗ヒスタミン薬
- エプコリタマブ投与30~120分前
2サイクル目以降
- 対象 : 前回投与後にGrade 2–3のCRSが出現した患者は、 Grade≧2のCRSが認められなくなるまで以下の前投薬を継続
- 副腎皮質ホルモン剤
- エプコリタマブ投与30~120分前
- エプコリタマブ投与後1~3日目
EPCORE NHL-1試験の最適化コホートでは、 1サイクル目のエプコリタマブ投与に際し、 デキサメタゾン15mgの静脈内投与が推奨されていた。 必要に応じて、 同薬の投与量は12mgまで減量可能とされた。 また、 エプコリタマブ投与前24時間には2~3Lの水分摂取および降圧薬の中断、 投与当日の等張輸液500mLの投与、 さらに投与後24時間における2~3Lの水分摂取も推奨された²⁾。
レジメン適用時の注意事項
- 第1サイクルの各投与後は入院管理を検討
- 1サイクル22日目 (初回の48mg投与日) は、 投与後48時間の入院管理が必須
- CRS発現時に備えてトシリズマブを速やかに使用できるよう準備する
- 免疫エフェクター細胞関連神経毒性症候群 (ICANS) があらわれることがあるため、 失語症、 意識レベルの変化、 認知能力の障害、 筋力低下、 痙攣発作、 脳浮腫等について、 観察を行う
- エプコリタマブ投与前にニューモシスチス・イロベチイなどの感染の有無を確認し、 適切な処置を行う。 投与中は、 感染症 (帯状疱疹等の再活性化や日和見感染を含む) の発現・悪化に十分注意する
- 腫瘍崩壊症候群の発現に留意し、 血清電解質や腎機能の検査を実施するなど、 患者の状態を十分に観察する
- 進行性多巣性白質脳症 (PML) が報告されているため、 意識障害、 認知機能障害、 麻痺、 構音障害、 失語などが出現した場合には、 MRIや脳脊髄液検査を実施し、 エプコリタマブの投与を中止のうえ、 適切に対処する
- 大腿部、 腹部等に左右交互に投与するなど同一注射部位を避ける
RMP【重要な特定されたリスク】
エプキンリ®医薬品リスク管理計画書 (RMP)
- CRS
- ICANS
- 感染症
- 腫瘍崩壊症候群
- 血球減少
- 進行性多巣性白質脳症
出典
- エプキンリ®皮下注4mg, 48mg 適正使用ガイド (2025年2月改訂) [最終閲覧 : 2025/5/28]
- エプキンリ®皮下注4mg, 48mg 適正使用ガイド (2025年2月改訂) [最終閲覧 : 2025/5/28]
- Lancet Haematol. 2024;11(8):e593-e605.
最終更新 : 2025年5月28日
執筆 : HOKUTO編集部 がん専門・指導薬剤師
監修医師 : 東海大学血液腫瘍内科 扇屋大輔
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
がん薬物療法における治療計画をまとめたものです。
主要論文や適正使用ガイドをもとにした用量調整プロトコール、 有害事象対応をご紹介します。
なお、 本ツールは医師向けの教育用資料であり、 実臨床での使用は想定しておりません。 最新の添付文書やガイドラインを必ずご確認下さい。
また、 一般の方への情報提供ではないことを予めご了承ください。

