2022年8月24日に新たに 「EGFR遺伝子変異陽性の非小細胞肺癌における術後補助療法」 への適応が追加された
本コンテンツは特定の治療法を推奨するものではございません。 個々の患者の病態や、 実際の薬剤情報やガイドラインを確認の上、 利用者の判断と責任でご利用ください。
薬剤情報
タグリッソ®錠 (オシメルチニブ)
*アストラゼネカ株式会社の外部サイトへ遷移します
投与スケジュール
【1コース】連日内服投与
【催吐性】 最小度催吐性
【FN発症】低リスク
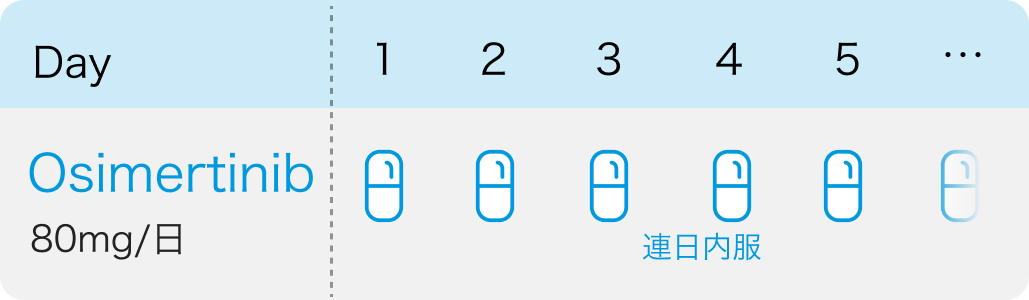
術後補助療法では、投与期間は36ヵ月間まで
タグリッソ®適正使用ガイド²⁾より引用
Key Data|臨床試験結果
📊ADAURA試験³⁾⁴⁾
病理病期ⅠB~ⅢA期※のEGFR変異陽性NSCLC術後患者を対象に、 オシメルチニブ3年投与とプラセボを比較した国際第Ⅲ相試験 [オシメルチニブ群 339例、プラセボ群343例]
※病理病期 AJCC/UICC第7版 切除検体の病理診断に基づくため、日本では病理病期ⅠB期患者は対象外である
【有効性】オシメルチニブ群
- Ⅱ~ⅢA期 DFS : 未到達 [主要評価項目]³⁾
プラセボ群 : 19.6ヵ月、 HR 0.17、 P<0.0001

タグリッソ®電子添文¹⁾より引用
更新されたDFS報告は65.8ヵ月であった⁴⁾
プラセボ群 : 21.9ヵ月、 HR 0.23、 P<0.0001
- Ⅱ~ⅢA期 4年DFS率 : 70%³⁾
プラセボ群 : 29%、 HR 0.23、 P<0.0001
- Ⅱ~ⅢA期 5年OS率 : 85%³⁾
プラセボ群 : 73%、 HR 0.49、 P=0.0004
【安全性】
- 主な有害事象³⁾
下痢、 皮疹(ざ瘡様皮疹・爪周囲炎)、 肝機能障害、 白血球減少、 血小板減少
- 注意すべき有害事象³⁾
薬剤性肺障害、 心毒性 (QTc延長、 心機能低下、 心嚢液貯留)
減量の目安

タグリッソ®電子添文情報¹⁾を基に編集部作表
有害事象発現時の用量調節基準
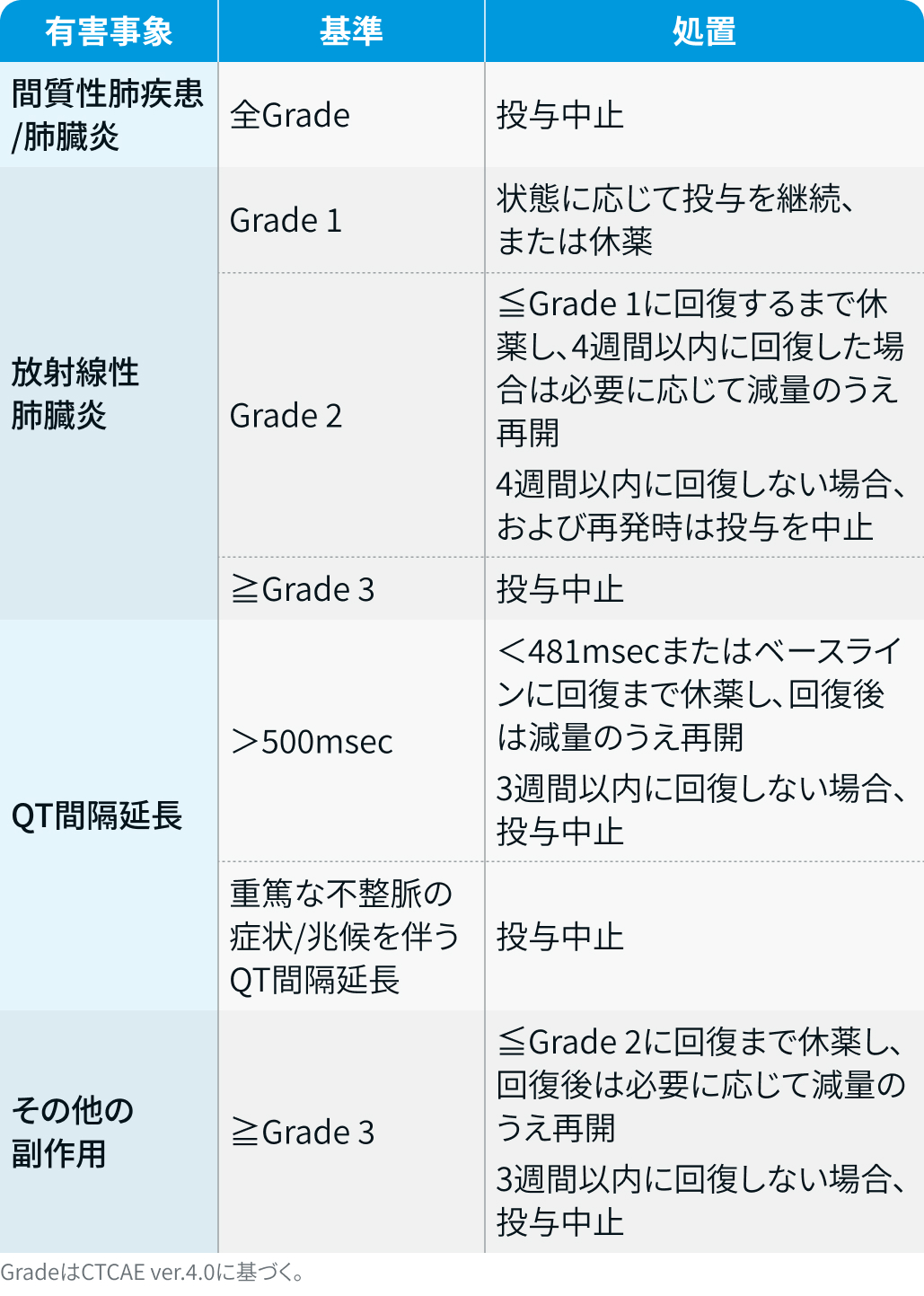
タグリッソ®電子添文情報¹⁾を基に編集部作表
レジメンの特徴と注意点
2022年8月にADAURA試験により 「術後補助化学療法」 としての使用が可能となった。 投与期間は最長36ヵ月であるため留意すること。
コンパニオン診断
コンパニオン診断の最新情報について、 こちらのコンテンツを参照ください。
肺癌コンパニオン診断薬一覧ページへ遷移
有害事象の特徴
日本人における薬剤性肺障害の発現割合は全体集団より高い傾向が見られた。 また、 ICI投与歴がある場合、 薬剤性肺障害の発現率が高まるとの報告あり。 また、 一過性無症候性肺陰影 (TAPO)が報告されている。
Chest 2022 : オシメルチニブ起因の薬剤性肺炎発症率18%、半数はTAPO の記事を読む
肺癌診療ガイドライン2025
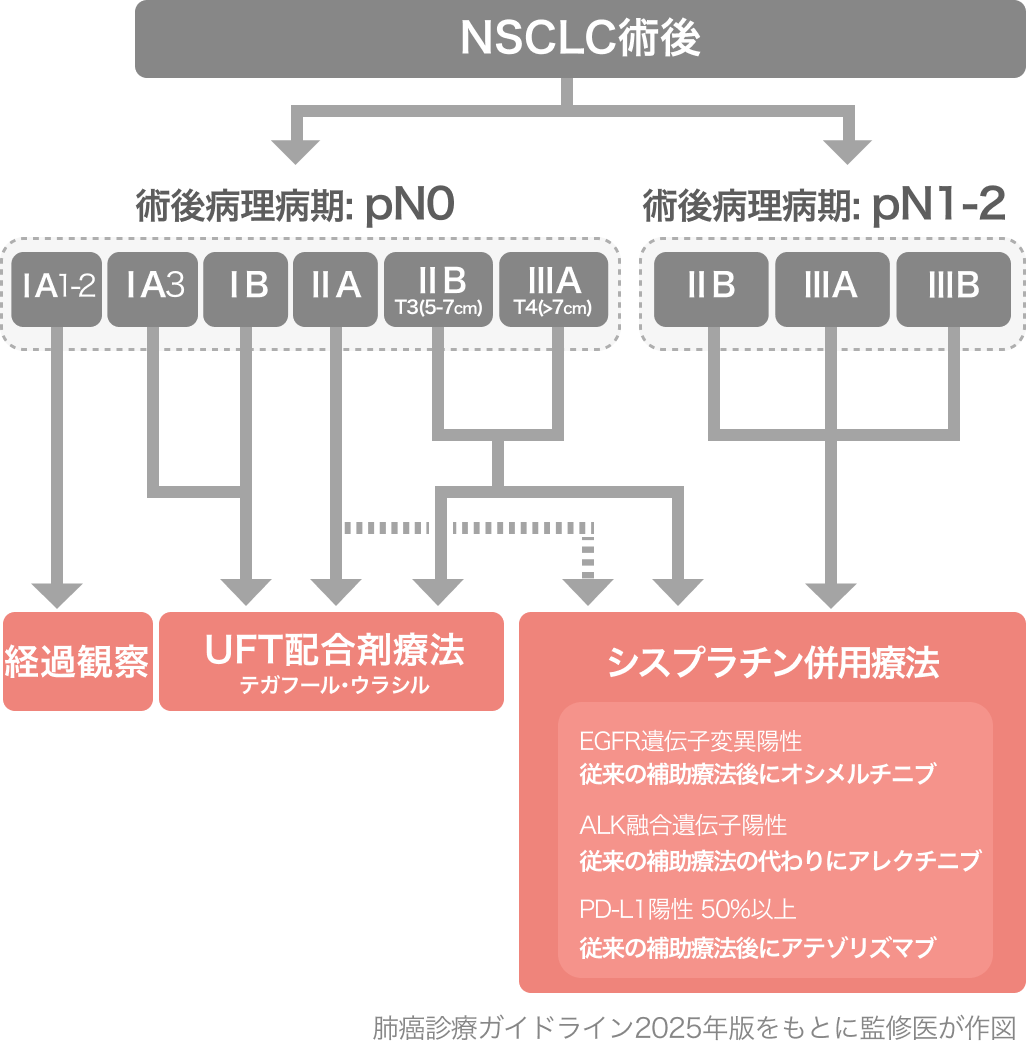
EGFR遺伝子変異陽性の病理病期Ⅱ-ⅢB期 (第9版)*N3は除く 完全切除例に対する術後療法については、 従来の術後補助化学療法後に、 オシメルチニブによる治療追加が弱く推奨 [2B]⁵⁾
日本肺癌学会. 肺癌診療ガイドライン-胸膜中皮腫・ 胸腺腫瘍含む-2025年版より引用
出典
- アストラゼネカ株式会社. タグリッソ®電子添文. 2026年01月改訂 第8版.
- アストラゼネカ株式会社. タグリッソ®適正使用ガイド. 2025年10月作成
- N Engl J Med. 2023;389(2):137-147.
- J Clin Oncol. 2023;41(10):1830-1840.
- 日本肺癌学会. 肺癌診療ガイドライン-胸膜中皮腫・ 胸腺腫瘍含む-2025年版
最終更新日 : 2026年1月13日
監修・作図 : HOKUTO編集部専門医
Osimertinib
2022年8月24日に新たに 「EGFR遺伝子変異陽性の非小細胞肺癌における術後補助療法」 への適応が追加された
本コンテンツは特定の治療法を推奨するものではございません。 個々の患者の病態や、 実際の薬剤情報やガイドラインを確認の上、 利用者の判断と責任でご利用ください。
薬剤情報
タグリッソ®錠 (オシメルチニブ)
*アストラゼネカ株式会社の外部サイトへ遷移します
投与スケジュール
【1コース】連日内服投与
【催吐性】 最小度催吐性
【FN発症】低リスク

術後補助療法では、投与期間は36ヵ月間まで
タグリッソ®適正使用ガイド²⁾より引用
Key Data|臨床試験結果
📊ADAURA試験³⁾⁴⁾
病理病期ⅠB~ⅢA期※のEGFR変異陽性NSCLC術後患者を対象に、 オシメルチニブ3年投与とプラセボを比較した国際第Ⅲ相試験 [オシメルチニブ群 339例、プラセボ群343例]
※病理病期 AJCC/UICC第7版 切除検体の病理診断に基づくため、日本では病理病期ⅠB期患者は対象外である
【有効性】オシメルチニブ群
- Ⅱ~ⅢA期 DFS : 未到達 [主要評価項目]³⁾
プラセボ群 : 19.6ヵ月、 HR 0.17、 P<0.0001

タグリッソ®電子添文¹⁾より引用
更新されたDFS報告は65.8ヵ月であった⁴⁾
プラセボ群 : 21.9ヵ月、 HR 0.23、 P<0.0001
- Ⅱ~ⅢA期 4年DFS率 : 70%³⁾
プラセボ群 : 29%、 HR 0.23、 P<0.0001
- Ⅱ~ⅢA期 5年OS率 : 85%³⁾
プラセボ群 : 73%、 HR 0.49、 P=0.0004
【安全性】
- 主な有害事象³⁾
下痢、 皮疹(ざ瘡様皮疹・爪周囲炎)、 肝機能障害、 白血球減少、 血小板減少
- 注意すべき有害事象³⁾
薬剤性肺障害、 心毒性 (QTc延長、 心機能低下、 心嚢液貯留)
減量の目安

タグリッソ®電子添文情報¹⁾を基に編集部作表
有害事象発現時の用量調節基準

タグリッソ®電子添文情報¹⁾を基に編集部作表
レジメンの特徴と注意点
2022年8月にADAURA試験により 「術後補助化学療法」 としての使用が可能となった。 投与期間は最長36ヵ月であるため留意すること。
コンパニオン診断
コンパニオン診断の最新情報について、 こちらのコンテンツを参照ください。
肺癌コンパニオン診断薬一覧ページへ遷移
有害事象の特徴
日本人における薬剤性肺障害の発現割合は全体集団より高い傾向が見られた。 また、 ICI投与歴がある場合、 薬剤性肺障害の発現率が高まるとの報告あり。 また、 一過性無症候性肺陰影 (TAPO)が報告されている。
Chest 2022 : オシメルチニブ起因の薬剤性肺炎発症率18%、半数はTAPO の記事を読む
肺癌診療ガイドライン2025
EGFR遺伝子変異陽性の病理病期Ⅱ-ⅢB期 (第9版)*N3は除く 完全切除例に対する術後療法については、 従来の術後補助化学療法後に、 オシメルチニブによる治療追加が弱く推奨 [2B]⁵⁾
日本肺癌学会. 肺癌診療ガイドライン-胸膜中皮腫・ 胸腺腫瘍含む-2025年版より引用

出典
- アストラゼネカ株式会社. タグリッソ®電子添文. 2026年01月改訂 第8版.
- アストラゼネカ株式会社. タグリッソ®適正使用ガイド. 2025年10月作成
- N Engl J Med. 2023;389(2):137-147.
- J Clin Oncol. 2023;41(10):1830-1840.
- 日本肺癌学会. 肺癌診療ガイドライン-胸膜中皮腫・ 胸腺腫瘍含む-2025年版
最終更新日 : 2026年1月13日
監修・作図 : HOKUTO編集部専門医
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
がん薬物療法における治療計画をまとめたものです。
主要論文や適正使用ガイドをもとにした用量調整プロトコール、 有害事象対応をご紹介します。
なお、 本ツールは医師向けの教育用資料であり、 実臨床での使用は想定しておりません。 最新の添付文書やガイドラインを必ずご確認下さい。
また、 一般の方への情報提供ではないことを予めご了承ください。