Tazemetostat:タゼメトスタット(タズベリク®)
| 投与量 | コース | 投与日 |
|---|---|---|
| 800mg 1日2回 経口 | 1~ | Day 1~ |
その他
| 少なくとも2つ以上の標準的な治療が無効となったEZH2遺伝子変異陽性の濾胞性リンパ腫患者が適応. |
| 有害事象発現時の減量・休薬・中止基準は概要を参照. |
2026年3月27日、 エーザイは、 再発/難治性濾胞性リンパ腫におけるR²療法へのタゼメトスタット上乗せを検証する確認試験SYMPHONY-1を含む安全性データの精査により、 併用投与・単剤投与のいずれでも血液系二次悪性腫瘍の複数例が確認されたことから、 本邦での販売中止を決定した。
本コンテンツは特定の治療法を推奨するものではありません。 個々の患者の病態や、 実際の薬剤情報やガイドラインを確認の上、 利用者の判断と責任でご利用ください。
薬剤情報
タズベリク®錠 (タゼメトスタット)
*エーザイ株式会社の外部サイトへ遷移します
投与スケジュール
【1コース】28日間
【催吐性】最小度
【FN発症】不明*
ピボタル試験³⁾では、 FN発生率は報告されていない。
1回800mgを1日2回、 連日経口投与
Key Data|臨床試験結果
📊 海外第I/II相試験
Lancet Oncol. 2020;21(11):1433-1442.
再発又は難治性のFL (grade 1/2/3a/3b) で≧2レジメンの前治療歴を有するEZH2変異陽性患者45例を対象にタゼメトスタットを連日投与した単群非盲検多施設試験の第II相パート。 主要評価項目はIRC評価による客観的奏効率 (ORR) とした。
【有効性】
- ORR 69% (95%CI 53–82)
- CR 13%
- PR 56%
- 病勢コントロール率 98%
- 奏効期間中央値 10.9ヵ月 (95%CI 7.2–NE)
- PFS中央値 13.8ヵ月 (95%CI 10.7–22.0)
- OS中央値 NR (95%CI NE–NE)
【安全性】主な有害事象 : 全Grade (Grade≧3)
Treatment-emergent adverse events (TEAE) のうち、 全Gradeで5%以上に認めた有害事象を抜粋 (99例、 EZH2変異陽性群と野生型群の合算)。
- 悪心 23% (0%)
- 下痢 18% (0%)
- 脱毛症 17% (0%)
- 咳嗽 16% (0%)
- 無力症 18% (3%)
- 疲労 17% (2%)
- 上気道感染 15% (0%)
- 気管支炎 15% (0%)
- 腹痛 13% (1%)
- 頭痛 12% (0%)
- 嘔吐 12% (1%)
- 背部痛 11% (0%)
- 発熱 10% (0%)
- 貧血 14% (5%)
- 血小板減少 10% (5%)
- 好中球減少 7% (4%)
各プロトコル
適格基準
海外第I/II相試験³⁾の主な適格基準
- 18歳以上
- ECOG PS 0–2
- 好中球数≧750/μL
- 血小板数≧7.5万/μL
- Hb≧9g/dL
- 肝機能: T-Bil≦1.5×ULN、 AST/ALT≦3×ULN
- 腎機能: CrCl≧40mL/min
用量レベル
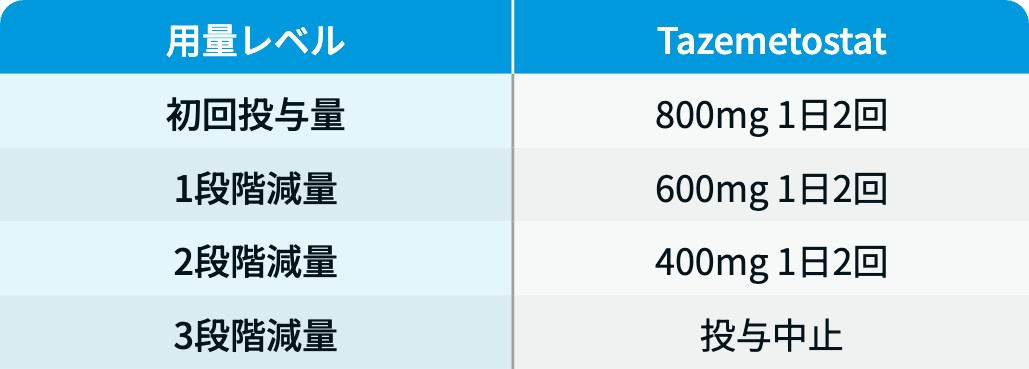
タズベリク®電子添文情報¹⁾を基に編集部作成
腎障害患者に対する用量調整
尿中未変化体排泄率は1.4%と低く、 腎クリアランスの寄与は小さいため、 腎障害時の用量調整は不要と考えられる。
タズベリク®インタビューフォームに基づく編集部の見解
有害事象発現時の減量・休薬・中止基準
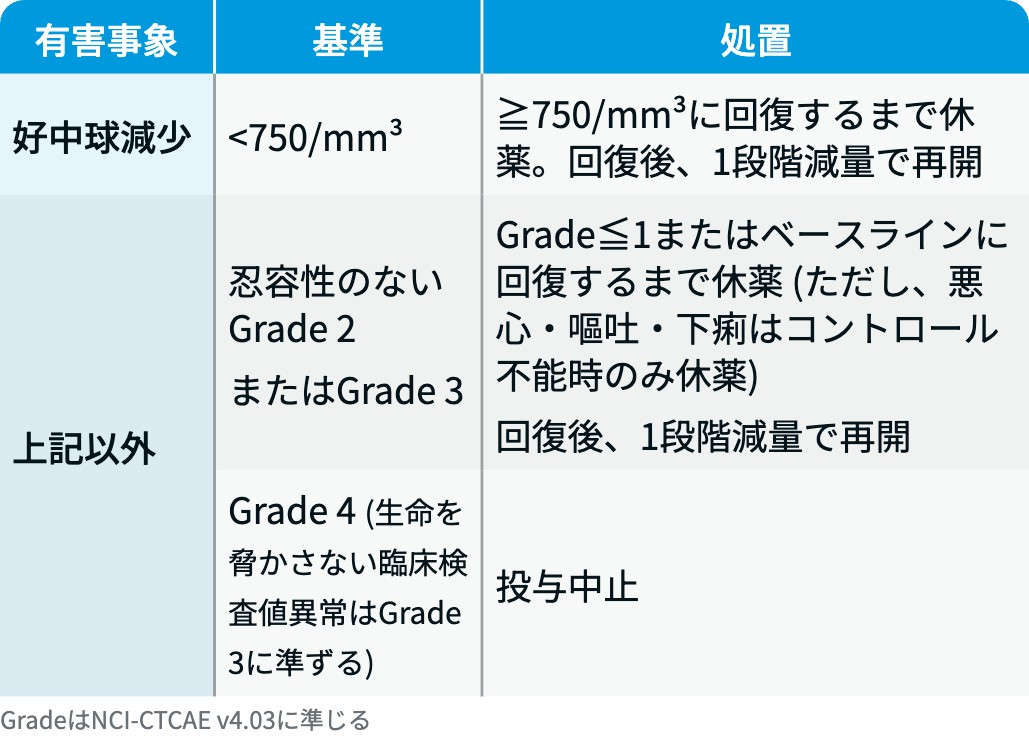
タズベリク®電子添文情報¹⁾を基に編集部作成
ピボタル試験³⁾における対応方法 (補足情報)
好中球減少 (ANC<750/μL) 発現時は、 初回はANC≧750/μLに回復後600mgを1日2回で再開し、 2回目は同基準に回復後400mgを1日2回で再開、 3回目は投与中止とする。
レジメンの特徴と注意点
作用機序の特徴
タゼメトスタットは、 ヒストンなどのメチル基転移酵素であるEZH2の酵素活性を阻害する低分子化合物である。 変異型EZH2 (Y646Fなど) のメチル化活性を阻害し、 ヒストンH3の27番目のリジン残基などのメチル化を抑制することで、 細胞周期停止やアポトーシス誘導を介した腫瘍増殖抑制作用を示すと推測されている。 ただし、 詳細な作用機序は解明されていない。
レジメン適用時の注意事項
骨髄抑制 : 投与開始前及び投与期間中は定期的に血液学的検査を実施し、 患者の状態を十分に観察する。
血液系二次癌のリスク : T細胞リンパ芽球性リンパ腫/白血病、 MDS、 AMLなどの血液系二次悪性腫瘍が報告されている。 2026年3月19日、 エーザイは、 再発/難治性濾胞性リンパ腫におけるR²療法へのタゼメトスタット上乗せを検証する確認試験SYMPHONY-1を含む安全性データの精査により、 併用投与・単剤投与のいずれでも血液系二次悪性腫瘍の複数例が確認されたことから、 本邦での投与中止を決定した。 投与中患者には速やかな中止検討、 新規投与は行わないよう案内されている。
RMP【重要な特定されたリスク】
タズベリク®RMP : 医薬品リスク管理計画書
- 骨髄抑制
- 感染症
コンパニオン診断薬の情報
本剤の適応判定に利用可能なコンパニオン診断薬は以下のとおり。
- コバス EZH2 変異検出キット
出典
1) エーザイ株式会社. タズベリク®電子添文. 2025年9月改訂 第6版.
2) エーザイ株式会社. タズベリク®適正使用ガイド. 2025年10月作成.
3) Lancet Oncol. 2020;21(11):1433-1442.
最終更新 : 2026年3月19日
執筆 : HOKUTO編集部 がん専門・指導薬剤師
監修医師 : 東海大学血液腫瘍内科 扇屋大輔
Tazemetostat (2026年3月27日より販売中止)
Tazemetostat:タゼメトスタット(タズベリク®)
| 投与量 | コース | 投与日 |
|---|---|---|
| 800mg 1日2回 経口 | 1~ | Day 1~ |
その他
| 少なくとも2つ以上の標準的な治療が無効となったEZH2遺伝子変異陽性の濾胞性リンパ腫患者が適応. |
| 有害事象発現時の減量・休薬・中止基準は概要を参照. |
概要
2026年3月27日、 エーザイは、 再発/難治性濾胞性リンパ腫におけるR²療法へのタゼメトスタット上乗せを検証する確認試験SYMPHONY-1を含む安全性データの精査により、 併用投与・単剤投与のいずれでも血液系二次悪性腫瘍の複数例が確認されたことから、 本邦での販売中止を決定した。
本コンテンツは特定の治療法を推奨するものではありません。 個々の患者の病態や、 実際の薬剤情報やガイドラインを確認の上、 利用者の判断と責任でご利用ください。
薬剤情報
タズベリク®錠 (タゼメトスタット)
*エーザイ株式会社の外部サイトへ遷移します
投与スケジュール
【1コース】28日間
【催吐性】最小度
【FN発症】不明*
ピボタル試験³⁾では、 FN発生率は報告されていない。

1回800mgを1日2回、 連日経口投与
Key Data|臨床試験結果
📊 海外第I/II相試験
Lancet Oncol. 2020;21(11):1433-1442.
再発又は難治性のFL (grade 1/2/3a/3b) で≧2レジメンの前治療歴を有するEZH2変異陽性患者45例を対象にタゼメトスタットを連日投与した単群非盲検多施設試験の第II相パート。 主要評価項目はIRC評価による客観的奏効率 (ORR) とした。
【有効性】
- ORR 69% (95%CI 53–82)
- CR 13%
- PR 56%
- 病勢コントロール率 98%
- 奏効期間中央値 10.9ヵ月 (95%CI 7.2–NE)
- PFS中央値 13.8ヵ月 (95%CI 10.7–22.0)
- OS中央値 NR (95%CI NE–NE)
【安全性】主な有害事象 : 全Grade (Grade≧3)
Treatment-emergent adverse events (TEAE) のうち、 全Gradeで5%以上に認めた有害事象を抜粋 (99例、 EZH2変異陽性群と野生型群の合算)。
- 悪心 23% (0%)
- 下痢 18% (0%)
- 脱毛症 17% (0%)
- 咳嗽 16% (0%)
- 無力症 18% (3%)
- 疲労 17% (2%)
- 上気道感染 15% (0%)
- 気管支炎 15% (0%)
- 腹痛 13% (1%)
- 頭痛 12% (0%)
- 嘔吐 12% (1%)
- 背部痛 11% (0%)
- 発熱 10% (0%)
- 貧血 14% (5%)
- 血小板減少 10% (5%)
- 好中球減少 7% (4%)
各プロトコル
適格基準
海外第I/II相試験³⁾の主な適格基準
- 18歳以上
- ECOG PS 0–2
- 好中球数≧750/μL
- 血小板数≧7.5万/μL
- Hb≧9g/dL
- 肝機能: T-Bil≦1.5×ULN、 AST/ALT≦3×ULN
- 腎機能: CrCl≧40mL/min
用量レベル

タズベリク®電子添文情報¹⁾を基に編集部作成
腎障害患者に対する用量調整
尿中未変化体排泄率は1.4%と低く、 腎クリアランスの寄与は小さいため、 腎障害時の用量調整は不要と考えられる。
タズベリク®インタビューフォームに基づく編集部の見解
有害事象発現時の減量・休薬・中止基準

タズベリク®電子添文情報¹⁾を基に編集部作成
ピボタル試験³⁾における対応方法 (補足情報)
好中球減少 (ANC<750/μL) 発現時は、 初回はANC≧750/μLに回復後600mgを1日2回で再開し、 2回目は同基準に回復後400mgを1日2回で再開、 3回目は投与中止とする。
レジメンの特徴と注意点
作用機序の特徴
タゼメトスタットは、 ヒストンなどのメチル基転移酵素であるEZH2の酵素活性を阻害する低分子化合物である。 変異型EZH2 (Y646Fなど) のメチル化活性を阻害し、 ヒストンH3の27番目のリジン残基などのメチル化を抑制することで、 細胞周期停止やアポトーシス誘導を介した腫瘍増殖抑制作用を示すと推測されている。 ただし、 詳細な作用機序は解明されていない。
レジメン適用時の注意事項
骨髄抑制 : 投与開始前及び投与期間中は定期的に血液学的検査を実施し、 患者の状態を十分に観察する。
血液系二次癌のリスク : T細胞リンパ芽球性リンパ腫/白血病、 MDS、 AMLなどの血液系二次悪性腫瘍が報告されている。 2026年3月19日、 エーザイは、 再発/難治性濾胞性リンパ腫におけるR²療法へのタゼメトスタット上乗せを検証する確認試験SYMPHONY-1を含む安全性データの精査により、 併用投与・単剤投与のいずれでも血液系二次悪性腫瘍の複数例が確認されたことから、 本邦での投与中止を決定した。 投与中患者には速やかな中止検討、 新規投与は行わないよう案内されている。
RMP【重要な特定されたリスク】
タズベリク®RMP : 医薬品リスク管理計画書
- 骨髄抑制
- 感染症
コンパニオン診断薬の情報
本剤の適応判定に利用可能なコンパニオン診断薬は以下のとおり。
- コバス EZH2 変異検出キット
出典
1) エーザイ株式会社. タズベリク®電子添文. 2025年9月改訂 第6版.
2) エーザイ株式会社. タズベリク®適正使用ガイド. 2025年10月作成.
3) Lancet Oncol. 2020;21(11):1433-1442.
最終更新 : 2026年3月19日
執筆 : HOKUTO編集部 がん専門・指導薬剤師
監修医師 : 東海大学血液腫瘍内科 扇屋大輔
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
がん薬物療法における治療計画をまとめたものです。
主要論文や適正使用ガイドをもとにした用量調整プロトコール、 有害事象対応をご紹介します。
なお、 本ツールは医師向けの教育用資料であり、 実臨床での使用は想定しておりません。 最新の添付文書やガイドラインを必ずご確認下さい。
また、 一般の方への情報提供ではないことを予めご了承ください。
