本コンテンツは特定の治療法を推奨するものではありません。 個々の患者の病態や、 実際の薬剤情報やガイドラインを確認の上、 利用者の判断と責任でご利用ください。
2024/8/25時点で、 悪性黒色腫に対して本邦適応外
薬剤情報
- パラプラチン® (添付文書¹⁾)
- タキソール® (添付文書²⁾)
用法用量 ※適応外
悪性黒色腫に対して、 これまでに複数の投与方法が報告されている³⁾⁴⁾⁵⁾。
メイヨー・クリニック 後ろ向き試験³⁾

28日サイクル:カルボプラチンAUC2とパクリタキセル100mg/m²を1、 8、 15日目に投与
Cancer. 2006 Jan 15;106(2):375-82³⁾より引用
第III相ランダム化比較試験⁴⁾
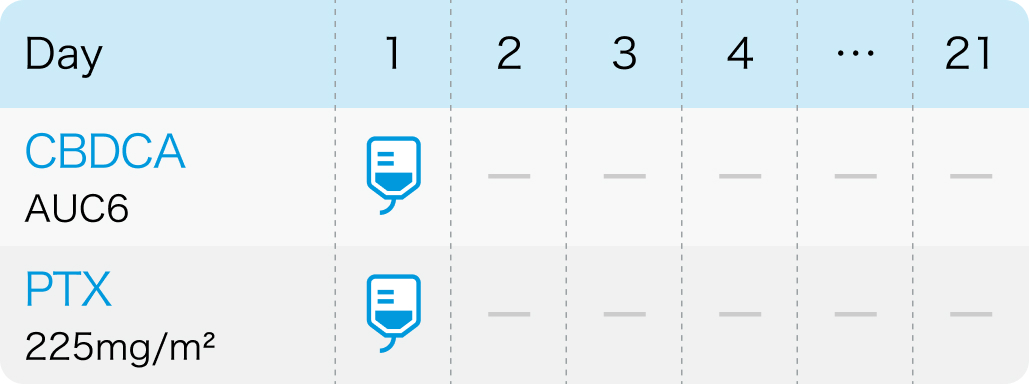
21日サイクル:カルボプラチンAUC6とパクリタキセル225mg/m²を3週間間隔で投与
J Clin Oncol. 2013 Jan 20;31(3):373-9⁴⁾より引用
第II相ランダム化比較試験⁵⁾
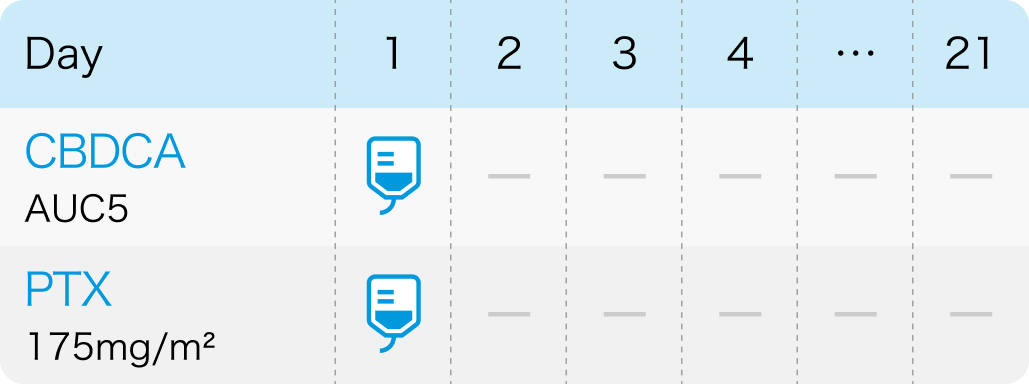
21日サイクル:カルボプラチンAUC5とパクリタキセル175mg/m²を3週間間隔で投与
J Clin Oncol. 2012 Jan 1;30(1):34-41⁵⁾より引用
エキスパートによるワンポイント
悪性黒色腫の4次治療以降程度の選択肢
免疫チェックポイント阻害薬や低分子性分子標的薬が承認される以前、 細胞障害性の抗がん薬としてダカルバジン (DTIC) が唯一の保険適用薬であったころにはダカルバジン単剤 (DTIC単剤)やダカルバジンを含む多剤併用療法 (DAV、DAC-Tam)に続く、 第2選択薬として位置づけられていた。 保険適用はなく、 現在は4次治療以降程度の治療法である。
上記に記載のとおり、 各診療試験において複数の投与方法が報告されている³⁾⁴⁾⁵⁾。
臨床試験における有効性
①メイヨー・クリニック 後ろ向き試験³⁾
ダカルバジンまたはテモゾロマイドで効果認められなかった31例の悪性黒色腫患者に対し、 パクリタキセル100mg/m²とカルボプラチンAUC2を投与する方法の後ろ向き試験において奏効率26% (8名に部分奏効) および病勢制御率45%であった。 無増悪生存期間の中央値は3か月(範囲、 0~7ヵ月)、 全生存期間の中央値は7.8か月(範囲、 1~14ヵ月)であった。
Cancer. 2006 Jan 15;106(2):375-82³⁾より引用
②第III相ランダム化比較試験⁴⁾
CBDCA + PTX併用療法と本療法へのソラフェニブの上乗せ効果を検討した第III相ランダム化比較試験でCBDCA + PTX併用療法群とソラフェニブ上乗せ群の2群間において奏効率(18% vs 20%, p=0.427), 無増悪生存期間 (中央値:4.2ヵ月 vs 4.9ヵ月, p=0.092),全生存期間 (中央値: 11.3ヵ月 vs 11.1ヵ月, p=0.86) のいずれも有意差はなかった。
J Clin Oncol. 2013 Jan 20;31(3):373-9⁴⁾より引用
③第II相ランダム化比較試験⁵⁾
CBDCA + PTX併用療法と本療法へのベバシツマブの上乗せ効果を検討した第II相ランダム化比較試験でCBDCA + PTX併用療法群とベバシツマブ上乗せ群の2 群間において 奏効率 (16.4% vs 25.5%, p=0.1577),無増悪生存期間(中央値: 4.2ヵ月 vs 5.6ヵ月, p=0.1414),全生存期間(中央値: 8.6ヵ月 vs 12.3ヵ月,p=0.366) といずれも有意差はなかった。
J Clin Oncol. 2012 Jan 1;30(1):34-41⁵⁾より引用
前向きランダム化比較試験である②と③の結果から投与量は異なるもののCBDCA + PTX併用療法の奏効率は16-18%程度、 無増悪生存期間は4ヵ月程度であった。
主な副作用としては、 食欲不振、 末梢神経障害、 骨髄抑制、 下痢、 疲労感などが挙げられる。
出典
- クリニジェン株式会社. パラプラチン®電子添文 (2023年5月改訂 第3版) [最終閲覧 : 2024/04/03]
- クリニジェン株式会社. タキソール®電子添文 (2023年7月改訂 第2版) [最終閲覧 : 2024/03/21]
- Combination of paclitaxel and carboplatin as second-line therapy for patients with metastatic melanoma. Cancer. 2006 Jan 15;106(2):375-82. PMID: 16342250
- Phase III trial of carboplatin and paclitaxel with or without sorafenib in metastatic melanoma. J Clin Oncol. 2013 Jan 20;31(3):373-9. PMID: 23248256
- BEAM: a randomized phase II study evaluating the activity of bevacizumab in combination with carboplatin plus paclitaxel in patients with previously untreated advanced melanoma. J Clin Oncol. 2012 Jan 1;30(1):34-41. PMID: 22124101
その他情報は随時更新予定です
最終更新日 : 2024年9月4日
監修医師 : 国立がん研究センター中央病院皮膚腫瘍科長 山崎直也先生
CP (CBDCA + PTX)
本コンテンツは特定の治療法を推奨するものではありません。 個々の患者の病態や、 実際の薬剤情報やガイドラインを確認の上、 利用者の判断と責任でご利用ください。
2024/8/25時点で、 悪性黒色腫に対して本邦適応外
薬剤情報
- パラプラチン® (添付文書¹⁾)
- タキソール® (添付文書²⁾)
用法用量 ※適応外
悪性黒色腫に対して、 これまでに複数の投与方法が報告されている³⁾⁴⁾⁵⁾。
メイヨー・クリニック 後ろ向き試験³⁾

28日サイクル:カルボプラチンAUC2とパクリタキセル100mg/m²を1、 8、 15日目に投与
Cancer. 2006 Jan 15;106(2):375-82³⁾より引用
第III相ランダム化比較試験⁴⁾

21日サイクル:カルボプラチンAUC6とパクリタキセル225mg/m²を3週間間隔で投与
J Clin Oncol. 2013 Jan 20;31(3):373-9⁴⁾より引用
第II相ランダム化比較試験⁵⁾

21日サイクル:カルボプラチンAUC5とパクリタキセル175mg/m²を3週間間隔で投与
J Clin Oncol. 2012 Jan 1;30(1):34-41⁵⁾より引用
エキスパートによるワンポイント
悪性黒色腫の4次治療以降程度の選択肢
免疫チェックポイント阻害薬や低分子性分子標的薬が承認される以前、 細胞障害性の抗がん薬としてダカルバジン (DTIC) が唯一の保険適用薬であったころにはダカルバジン単剤 (DTIC単剤)やダカルバジンを含む多剤併用療法 (DAV、DAC-Tam)に続く、 第2選択薬として位置づけられていた。 保険適用はなく、 現在は4次治療以降程度の治療法である。
上記に記載のとおり、 各診療試験において複数の投与方法が報告されている³⁾⁴⁾⁵⁾。
臨床試験における有効性
①メイヨー・クリニック 後ろ向き試験³⁾
ダカルバジンまたはテモゾロマイドで効果認められなかった31例の悪性黒色腫患者に対し、 パクリタキセル100mg/m²とカルボプラチンAUC2を投与する方法の後ろ向き試験において奏効率26% (8名に部分奏効) および病勢制御率45%であった。 無増悪生存期間の中央値は3か月(範囲、 0~7ヵ月)、 全生存期間の中央値は7.8か月(範囲、 1~14ヵ月)であった。
Cancer. 2006 Jan 15;106(2):375-82³⁾より引用
②第III相ランダム化比較試験⁴⁾
CBDCA + PTX併用療法と本療法へのソラフェニブの上乗せ効果を検討した第III相ランダム化比較試験でCBDCA + PTX併用療法群とソラフェニブ上乗せ群の2群間において奏効率(18% vs 20%, p=0.427), 無増悪生存期間 (中央値:4.2ヵ月 vs 4.9ヵ月, p=0.092),全生存期間 (中央値: 11.3ヵ月 vs 11.1ヵ月, p=0.86) のいずれも有意差はなかった。
J Clin Oncol. 2013 Jan 20;31(3):373-9⁴⁾より引用
③第II相ランダム化比較試験⁵⁾
CBDCA + PTX併用療法と本療法へのベバシツマブの上乗せ効果を検討した第II相ランダム化比較試験でCBDCA + PTX併用療法群とベバシツマブ上乗せ群の2 群間において 奏効率 (16.4% vs 25.5%, p=0.1577),無増悪生存期間(中央値: 4.2ヵ月 vs 5.6ヵ月, p=0.1414),全生存期間(中央値: 8.6ヵ月 vs 12.3ヵ月,p=0.366) といずれも有意差はなかった。
J Clin Oncol. 2012 Jan 1;30(1):34-41⁵⁾より引用
前向きランダム化比較試験である②と③の結果から投与量は異なるもののCBDCA + PTX併用療法の奏効率は16-18%程度、 無増悪生存期間は4ヵ月程度であった。
主な副作用としては、 食欲不振、 末梢神経障害、 骨髄抑制、 下痢、 疲労感などが挙げられる。
出典
- クリニジェン株式会社. パラプラチン®電子添文 (2023年5月改訂 第3版) [最終閲覧 : 2024/04/03]
- クリニジェン株式会社. タキソール®電子添文 (2023年7月改訂 第2版) [最終閲覧 : 2024/03/21]
- Combination of paclitaxel and carboplatin as second-line therapy for patients with metastatic melanoma. Cancer. 2006 Jan 15;106(2):375-82. PMID: 16342250
- Phase III trial of carboplatin and paclitaxel with or without sorafenib in metastatic melanoma. J Clin Oncol. 2013 Jan 20;31(3):373-9. PMID: 23248256
- BEAM: a randomized phase II study evaluating the activity of bevacizumab in combination with carboplatin plus paclitaxel in patients with previously untreated advanced melanoma. J Clin Oncol. 2012 Jan 1;30(1):34-41. PMID: 22124101
その他情報は随時更新予定です
最終更新日 : 2024年9月4日
監修医師 : 国立がん研究センター中央病院皮膚腫瘍科長 山崎直也先生
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
がん薬物療法における治療計画をまとめたものです。
主要論文や適正使用ガイドをもとにした用量調整プロトコール、 有害事象対応をご紹介します。
なお、 本ツールは医師向けの教育用資料であり、 実臨床での使用は想定しておりません。 最新の添付文書やガイドラインを必ずご確認下さい。
また、 一般の方への情報提供ではないことを予めご了承ください。