RopegIFNα-2b:ロペグインターフェロン アルファ-2b(ベスレミ®)
| 投与量 | コース | 投与日 |
|---|---|---|
| A法またはB法で漸増 | 1~ | 2週毎 |
その他
| 2026年2月19日、 B法 (開始用量250μg) の用法・用量が追加承認. |
| 他のインターフェロン製剤で間質性肺炎の発現が報告されているため小柴胡湯とは併用禁忌. |
2026年2月19日、 B法 (開始用量250μg) の用法・用量が追加承認された。
本コンテンツは特定の治療法を推奨するものではありません。 個々の患者の病態や、 実際の薬剤情報やガイドラインを確認の上、 利用者の判断と責任でご利用ください。
薬剤情報
ベスレミ® (ロペグインターフェロン アルファ-2b : RopegIFNα-2b)
ファーマエッセンシアジャパンの外部サイトへ遷移します
投与スケジュール
【1コース】 14日間

▼A法またはB法で皮下投与
A法 : 成人には1回100μg (他の細胞減少療法薬投与中は50μg : 下表参照) を開始用量とし、 2週ごとに投与する。 増量は50μgずつ行い、 1回500μgを超えない。

臨床試験で切り替え対象として想定されているのは、 ヒドロキシウレア (HU) のみである。 ベスレミ®電子添文情報¹⁾を基に編集部作成。
B法 : 成人には1回250μgを開始用量とし、 忍容性が良好であれば2週後に1回350μg、 さらに2週後に1回500μgとし、 以降は2週ごとに1回500μgを投与。
他の細胞減少療法薬投与中の場合は、 ベスレミ®投与前に他の細胞減少療法薬を終了する。
Key Data|臨床試験結果
📊 PROUD-PV試験
Lancet Haematol. 2020;7(3):e196-e208.
HU未治療または3年未満の治療歴を有するJAK2 V617F変異陽性の真性多血症患者254例を対象とした第III相無作為化非劣性比較試験PROUD-PVでは、 RopegIFNα-2b群127例とHU群127例に1 : 1に割り付け、 主要評価項目は12ヵ月時点の瀉血を要しない完全血液学的奏効 (CHR) および脾臓サイズの正常化とした。 さらに、 本試験完遂例を対象に延長試験CONTINUATION-PVが実施され、 長期の有効性および安全性が評価された。 延長試験では、 RopegIFNα-2b群は治療を継続し、 投与間隔は患者の状態に応じて2~4週ごとに個別化された一方、 対照群はHUを含むBest Available Therapy (BAT) で治療を継続した。
【有効性】RopegIFNα-2b群 (vs HU群)
- 12ヵ月CHRおよび脾臓サイズ正常化 21% (vs 28%)
- 差 -6.57% (95%CI -17.23–4.09、 p=0.23)
- 12ヵ月CHR 43% (vs 46%)
- 36ヵ月CHR 71% (vs 51%)
- RR 1.38 (95%CI 1.07–1.79、 p=0.012)
CONTINUATION-PV試験
【安全性】主な有害事象 : 全Grade (Grade≧3)
ベスレミ®適正使用ガイド²⁾より引用
- 血小板減少症 14.2% (0.8%)
- GGT増加 9.4% (3.9%)
- 白血球減少症 8.7% (1.6%)
- ALT増加 5.5% (0.8%)
- 肝酵素上昇 5.5% (0.8%)
- 貧血 5.5% (0%)
- そう痒症 5.5% (0%)
- AST増加 4.7% (0.8%)
- 脱毛症 4.7% (0%)
- 白血球数減少 2.4% (0%)
- 肝障害 1.6% (0%)
- 紅斑 1.6% (0%)
- 乾癬 1.6% (0.8%)
- 乾皮症 1.6% (0%)
- 血小板数減少 1.6% (0%)
- 好中球減少症 1.6% (0.8%)
- ALP増加 0.8% (0%)
- 顆粒球減少症 0.8% (0%)
- 血球減少症 0.8% (0%)
- 発疹 0.8% (0%)
- 湿疹 0.8% (0%)
- 多汗症 0.8% (0%)
- 光線過敏性反応 0.8% (0%)
- 全身性そう痒症 0.8% (0%)
- 皮膚剥脱 0.8% (0%)
📊 A23-301試験 (国内第III相試験)²⁾
既存治療が効果不十分または不適当な日本人真性多血症患者21例を対象とした多施設共同単群非盲検第III相試験。 RopegIFNα-2bを250μg、 350μg、 500μgの順に2週ごとに急速増量し、 以降24週まで1回500μgを2週ごとに維持投与した。 主要評価項目は24週時の瀉血を要しないCHR達成率とした。
【有効性】
- 24週時CHR達成率 57% (95%CI 35–78)
【安全性】主な有害事象 : 全Grade (Grade≧3)
- 尿中β2ミクログロブリン増加 76.2% (0%)
- 脱毛症 47.6% (0%)
- AST増加 28.6% (0%)
- ALT増加 23.8% (0%)
- 貧血 19.0% (0%)
- 白血球数減少 19.0% (0%)
- 下痢 14.3% (0%)
- 上咽頭炎 14.3% (0%)
- 疲労 9.5% (0%)
- インフルエンザ様疾患 9.5% (0%)
各プロトコル
適格基準²⁾
PROUD-PV試験の主な適格基準 :
- JAK2 V617F変異陽性
- 18歳以上
- HU治療歴がある場合は、 ノンレスポンダーで、 治療期間が3年未満、 かつHU抵抗性または不耐容ではない患者
A23-301試験の主な適格基準 :
- 18歳以上
- 既存治療が効果不十分または不適当
- 十分な肝機能
- Hb≧10g/dL (女性)、 Hb≧11g/dL (男性)
- 好中球≧1500/μL
- 血清Cre≦1.5×ULN
用量レベル
A法で投与する場合は50μgずつ増減し、 B法で投与する場合は、 下表に従い増減する。
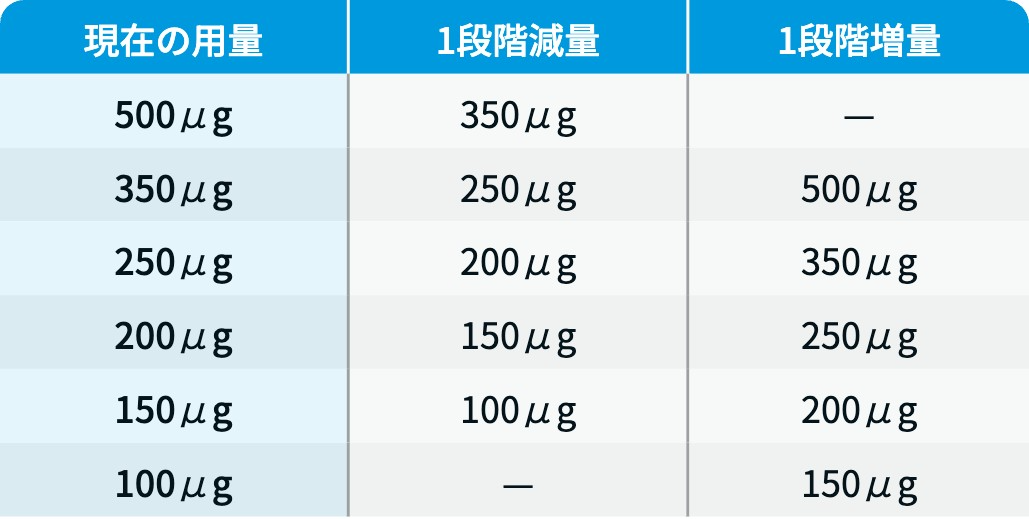
ベスレミ®電子添文情報¹⁾を基に編集部作成。
有害事象発現時の減量・休薬・中止基準
A法で投与する場合は50μg、 B法で投与する場合は1段階減量する。
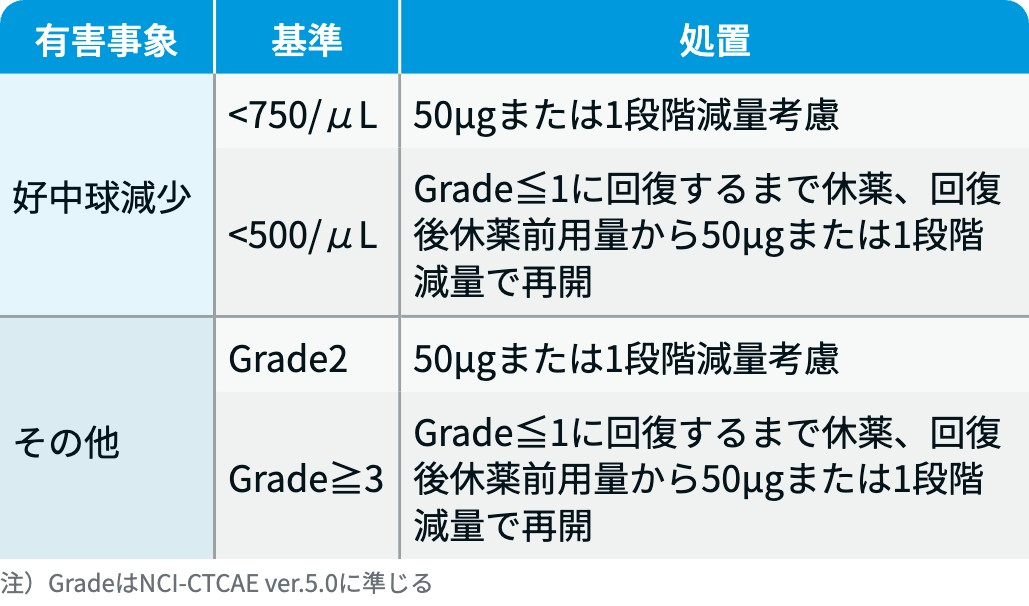
ベスレミ®電子添文情報¹⁾を基に編集部作成。
レジメンの特徴と注意点
🧑⚕️ベスレミ®の急速増量方法が新たに承認されました。 3段階のスムーズな増量で、 すみやかに最大用量である 500µg まで増量し、 自己注射に移行できるようになり利便性が改善されました。
東海大学医学部血液腫瘍内科 扇屋大輔先生
作用機序の特徴
RopegIFNα-2bはI型インターフェロン (IFN) 受容体に結合し、 ヤヌスキナーゼ (JAK) 1およびチロシンキナーゼ (TYK) 2の活性化を介して下流シグナル伝達分子のリン酸化を増加させ、 IFN誘導遺伝子の発現を増加させることで、 細胞周期の停止やアポトーシス誘導などを通じて腫瘍増殖抑制作用を示すと推測されている。 一方、 真性多血症 (PV) 患者における効果発現機序は不明である。
皮下注射時の注意事項
皮下注射時のポイント : 冷蔵庫から取り出して15~30分かけて室温に戻し、 薬液の濁りや変色、 シリンジの損傷の有無を確認する。 注射部位はへそから5cm以上離れた下腹部または左右の大腿部とし、 毎回変更し、 あざ、 傷あと、 赤みのある皮膚は避ける。 消毒後に皮膚をつまみ、 45~90度で刺入してプランジャーが止まるまでゆっくり注入する。
在宅自己注射時のポイント : 医師の指導を受け手順を習得したうえで実施する。 2~8℃で冷蔵保管し冷凍を避け、 持ち運びは保冷バッグを用いる。 使用後のプレフィルドシリンジは針を付けたままシェルパックに戻すか、 専用の廃棄容器に捨てる。 副作用が疑われる場合や薬液を多く廃棄した場合は速やかに医療機関へ連絡し、 めまいや意識障害の恐れがあるため運転や機械操作は注意する。
レジメン適用時の注意事項
過量投与 : 過量投与を防ぐため、 あらかじめプリフィルドシリンジ内の過量の薬液を廃棄して、 必要投与量を投与。
精神神経障害 : 抑うつ、 自殺企図、 躁状態、 攻撃的行動、 不眠、 不安等があらわれる可能性があるため、 患者および家族に十分理解させ、 症状発現時は直ちに連絡するよう注意する。
意識障害 : 失神、 昏睡、 錯乱等を発現することがあるため、 自動車の運転や機械の操作に従事させないよう注意する。
臨床検査値異常 : 骨髄機能抑制、 肝機能障害、 急性腎障害、 甲状腺機能障害等があらわれることがあるため、 投与前および投与中は定期的に血液検査、 肝機能検査、 腎機能検査、 甲状腺機能検査等を行う。
糖尿病 : 糖尿病が増悪または発症することがあるため、 定期的に血糖値、 尿糖等の検査を行う。
心臓障害 : 心臓障害があらわれることがあるため、 定期的に心電図検査を行う。
間質性肺炎 : 発熱、 咳嗽、 呼吸困難等の呼吸器症状に注意し、 既往歴のある患者では特に定期的な聴診や胸部X線検査を行う。
眼障害 : 網膜症等があらわれることがあるため、 定期的に眼底検査を行う。
HUS/TTP : 溶血性尿毒症症候群、 血栓性血小板減少性紫斑病があらわれることがあるため、 定期的な血液検査および腎機能検査を行う。
過敏症 : 反応を予測するため十分な問診を行い、 あらかじめプリック試験または皮内反応試験を行うことが望ましい。
発熱 : 投与初期に一般的にみられ、 高熱を呈することもあるため、 電解質を含む水分補給等に配慮する。
自己投与 : 医師の管理指導の下、 十分な教育訓練を実施し、 患者が自ら確実に投与できることを確認した上で実施する。
RMP【重要な特定されたリスク】
ベスレミ®RMP : 医薬品リスク管理計画書
- 肝機能障害
- 甲状腺機能障害
- 精神神経障害
- 眼障害
- 心臓障害
- 間質性肺疾患
- 重度の皮膚障害
- 骨髄抑制
- 感染症
- 消化管障害
- 糖尿病
- 出血
- 急性腎障害
- 血栓塞栓症
- 自己免疫疾患
- 溶血性尿毒症症候群・血栓性血小板減少性紫斑病
- 過敏症
出典
1) ファーマエッセンシアジャパン株式会社. ベスレミ®皮下注250μg・500μgシリンジ 電子添文 2026年2月改訂 第4版.
2) ファーマエッセンシアジャパン株式会社. ベスレミ®皮下注 適正使用ガイド 2026年2月改訂.
3) Lancet Haematol. 2020;7(3):e196-e208.
最終更新 : 2026年2月19日
執筆 : HOKUTO編集部 がん専門・指導薬剤師
監修医師 : 東海大学血液腫瘍内科 扇屋大輔
Ropeginterferon alfa-2b
RopegIFNα-2b:ロペグインターフェロン アルファ-2b(ベスレミ®)
| 投与量 | コース | 投与日 |
|---|---|---|
| A法またはB法で漸増 | 1~ | 2週毎 |
その他
| 2026年2月19日、 B法 (開始用量250μg) の用法・用量が追加承認. |
| 他のインターフェロン製剤で間質性肺炎の発現が報告されているため小柴胡湯とは併用禁忌. |
概要
2026年2月19日、 B法 (開始用量250μg) の用法・用量が追加承認された。
本コンテンツは特定の治療法を推奨するものではありません。 個々の患者の病態や、 実際の薬剤情報やガイドラインを確認の上、 利用者の判断と責任でご利用ください。
薬剤情報
ベスレミ® (ロペグインターフェロン アルファ-2b : RopegIFNα-2b)
ファーマエッセンシアジャパンの外部サイトへ遷移します
投与スケジュール
【1コース】 14日間

▼A法またはB法で皮下投与
A法 : 成人には1回100μg (他の細胞減少療法薬投与中は50μg : 下表参照) を開始用量とし、 2週ごとに投与する。 増量は50μgずつ行い、 1回500μgを超えない。

臨床試験で切り替え対象として想定されているのは、 ヒドロキシウレア (HU) のみである。 ベスレミ®電子添文情報¹⁾を基に編集部作成。
B法 : 成人には1回250μgを開始用量とし、 忍容性が良好であれば2週後に1回350μg、 さらに2週後に1回500μgとし、 以降は2週ごとに1回500μgを投与。
他の細胞減少療法薬投与中の場合は、 ベスレミ®投与前に他の細胞減少療法薬を終了する。
Key Data|臨床試験結果
📊 PROUD-PV試験
Lancet Haematol. 2020;7(3):e196-e208.
HU未治療または3年未満の治療歴を有するJAK2 V617F変異陽性の真性多血症患者254例を対象とした第III相無作為化非劣性比較試験PROUD-PVでは、 RopegIFNα-2b群127例とHU群127例に1 : 1に割り付け、 主要評価項目は12ヵ月時点の瀉血を要しない完全血液学的奏効 (CHR) および脾臓サイズの正常化とした。 さらに、 本試験完遂例を対象に延長試験CONTINUATION-PVが実施され、 長期の有効性および安全性が評価された。 延長試験では、 RopegIFNα-2b群は治療を継続し、 投与間隔は患者の状態に応じて2~4週ごとに個別化された一方、 対照群はHUを含むBest Available Therapy (BAT) で治療を継続した。
【有効性】RopegIFNα-2b群 (vs HU群)
- 12ヵ月CHRおよび脾臓サイズ正常化 21% (vs 28%)
- 差 -6.57% (95%CI -17.23–4.09、 p=0.23)
- 12ヵ月CHR 43% (vs 46%)
- 36ヵ月CHR 71% (vs 51%)
- RR 1.38 (95%CI 1.07–1.79、 p=0.012)
CONTINUATION-PV試験
【安全性】主な有害事象 : 全Grade (Grade≧3)
ベスレミ®適正使用ガイド²⁾より引用
- 血小板減少症 14.2% (0.8%)
- GGT増加 9.4% (3.9%)
- 白血球減少症 8.7% (1.6%)
- ALT増加 5.5% (0.8%)
- 肝酵素上昇 5.5% (0.8%)
- 貧血 5.5% (0%)
- そう痒症 5.5% (0%)
- AST増加 4.7% (0.8%)
- 脱毛症 4.7% (0%)
- 白血球数減少 2.4% (0%)
- 肝障害 1.6% (0%)
- 紅斑 1.6% (0%)
- 乾癬 1.6% (0.8%)
- 乾皮症 1.6% (0%)
- 血小板数減少 1.6% (0%)
- 好中球減少症 1.6% (0.8%)
- ALP増加 0.8% (0%)
- 顆粒球減少症 0.8% (0%)
- 血球減少症 0.8% (0%)
- 発疹 0.8% (0%)
- 湿疹 0.8% (0%)
- 多汗症 0.8% (0%)
- 光線過敏性反応 0.8% (0%)
- 全身性そう痒症 0.8% (0%)
- 皮膚剥脱 0.8% (0%)
📊 A23-301試験 (国内第III相試験)²⁾
既存治療が効果不十分または不適当な日本人真性多血症患者21例を対象とした多施設共同単群非盲検第III相試験。 RopegIFNα-2bを250μg、 350μg、 500μgの順に2週ごとに急速増量し、 以降24週まで1回500μgを2週ごとに維持投与した。 主要評価項目は24週時の瀉血を要しないCHR達成率とした。
【有効性】
- 24週時CHR達成率 57% (95%CI 35–78)
【安全性】主な有害事象 : 全Grade (Grade≧3)
- 尿中β2ミクログロブリン増加 76.2% (0%)
- 脱毛症 47.6% (0%)
- AST増加 28.6% (0%)
- ALT増加 23.8% (0%)
- 貧血 19.0% (0%)
- 白血球数減少 19.0% (0%)
- 下痢 14.3% (0%)
- 上咽頭炎 14.3% (0%)
- 疲労 9.5% (0%)
- インフルエンザ様疾患 9.5% (0%)
各プロトコル
適格基準²⁾
PROUD-PV試験の主な適格基準 :
- JAK2 V617F変異陽性
- 18歳以上
- HU治療歴がある場合は、 ノンレスポンダーで、 治療期間が3年未満、 かつHU抵抗性または不耐容ではない患者
A23-301試験の主な適格基準 :
- 18歳以上
- 既存治療が効果不十分または不適当
- 十分な肝機能
- Hb≧10g/dL (女性)、 Hb≧11g/dL (男性)
- 好中球≧1500/μL
- 血清Cre≦1.5×ULN
用量レベル
A法で投与する場合は50μgずつ増減し、 B法で投与する場合は、 下表に従い増減する。

ベスレミ®電子添文情報¹⁾を基に編集部作成。
有害事象発現時の減量・休薬・中止基準
A法で投与する場合は50μg、 B法で投与する場合は1段階減量する。

ベスレミ®電子添文情報¹⁾を基に編集部作成。
レジメンの特徴と注意点
🧑⚕️ベスレミ®の急速増量方法が新たに承認されました。 3段階のスムーズな増量で、 すみやかに最大用量である 500µg まで増量し、 自己注射に移行できるようになり利便性が改善されました。
東海大学医学部血液腫瘍内科 扇屋大輔先生
作用機序の特徴
RopegIFNα-2bはI型インターフェロン (IFN) 受容体に結合し、 ヤヌスキナーゼ (JAK) 1およびチロシンキナーゼ (TYK) 2の活性化を介して下流シグナル伝達分子のリン酸化を増加させ、 IFN誘導遺伝子の発現を増加させることで、 細胞周期の停止やアポトーシス誘導などを通じて腫瘍増殖抑制作用を示すと推測されている。 一方、 真性多血症 (PV) 患者における効果発現機序は不明である。
皮下注射時の注意事項
皮下注射時のポイント : 冷蔵庫から取り出して15~30分かけて室温に戻し、 薬液の濁りや変色、 シリンジの損傷の有無を確認する。 注射部位はへそから5cm以上離れた下腹部または左右の大腿部とし、 毎回変更し、 あざ、 傷あと、 赤みのある皮膚は避ける。 消毒後に皮膚をつまみ、 45~90度で刺入してプランジャーが止まるまでゆっくり注入する。
在宅自己注射時のポイント : 医師の指導を受け手順を習得したうえで実施する。 2~8℃で冷蔵保管し冷凍を避け、 持ち運びは保冷バッグを用いる。 使用後のプレフィルドシリンジは針を付けたままシェルパックに戻すか、 専用の廃棄容器に捨てる。 副作用が疑われる場合や薬液を多く廃棄した場合は速やかに医療機関へ連絡し、 めまいや意識障害の恐れがあるため運転や機械操作は注意する。
レジメン適用時の注意事項
過量投与 : 過量投与を防ぐため、 あらかじめプリフィルドシリンジ内の過量の薬液を廃棄して、 必要投与量を投与。
精神神経障害 : 抑うつ、 自殺企図、 躁状態、 攻撃的行動、 不眠、 不安等があらわれる可能性があるため、 患者および家族に十分理解させ、 症状発現時は直ちに連絡するよう注意する。
意識障害 : 失神、 昏睡、 錯乱等を発現することがあるため、 自動車の運転や機械の操作に従事させないよう注意する。
臨床検査値異常 : 骨髄機能抑制、 肝機能障害、 急性腎障害、 甲状腺機能障害等があらわれることがあるため、 投与前および投与中は定期的に血液検査、 肝機能検査、 腎機能検査、 甲状腺機能検査等を行う。
糖尿病 : 糖尿病が増悪または発症することがあるため、 定期的に血糖値、 尿糖等の検査を行う。
心臓障害 : 心臓障害があらわれることがあるため、 定期的に心電図検査を行う。
間質性肺炎 : 発熱、 咳嗽、 呼吸困難等の呼吸器症状に注意し、 既往歴のある患者では特に定期的な聴診や胸部X線検査を行う。
眼障害 : 網膜症等があらわれることがあるため、 定期的に眼底検査を行う。
HUS/TTP : 溶血性尿毒症症候群、 血栓性血小板減少性紫斑病があらわれることがあるため、 定期的な血液検査および腎機能検査を行う。
過敏症 : 反応を予測するため十分な問診を行い、 あらかじめプリック試験または皮内反応試験を行うことが望ましい。
発熱 : 投与初期に一般的にみられ、 高熱を呈することもあるため、 電解質を含む水分補給等に配慮する。
自己投与 : 医師の管理指導の下、 十分な教育訓練を実施し、 患者が自ら確実に投与できることを確認した上で実施する。
RMP【重要な特定されたリスク】
ベスレミ®RMP : 医薬品リスク管理計画書
- 肝機能障害
- 甲状腺機能障害
- 精神神経障害
- 眼障害
- 心臓障害
- 間質性肺疾患
- 重度の皮膚障害
- 骨髄抑制
- 感染症
- 消化管障害
- 糖尿病
- 出血
- 急性腎障害
- 血栓塞栓症
- 自己免疫疾患
- 溶血性尿毒症症候群・血栓性血小板減少性紫斑病
- 過敏症
出典
1) ファーマエッセンシアジャパン株式会社. ベスレミ®皮下注250μg・500μgシリンジ 電子添文 2026年2月改訂 第4版.
2) ファーマエッセンシアジャパン株式会社. ベスレミ®皮下注 適正使用ガイド 2026年2月改訂.
3) Lancet Haematol. 2020;7(3):e196-e208.
最終更新 : 2026年2月19日
執筆 : HOKUTO編集部 がん専門・指導薬剤師
監修医師 : 東海大学血液腫瘍内科 扇屋大輔
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
がん薬物療法における治療計画をまとめたものです。
主要論文や適正使用ガイドをもとにした用量調整プロトコール、 有害事象対応をご紹介します。
なお、 本ツールは医師向けの教育用資料であり、 実臨床での使用は想定しておりません。 最新の添付文書やガイドラインを必ずご確認下さい。
また、 一般の方への情報提供ではないことを予めご了承ください。
