本コンテンツは特定の治療法を推奨するものではありません。 個々の患者の病態や、 実際の薬剤情報やガイドラインを確認の上、 利用者の判断と責任でご利用ください。
薬剤情報
第2世代抗アンドロゲン薬 アパルタミド
*ヤンセンファーマ株式会社の外部サイトへ遷移します
用法用量
添付文書¹⁾の用法および用量
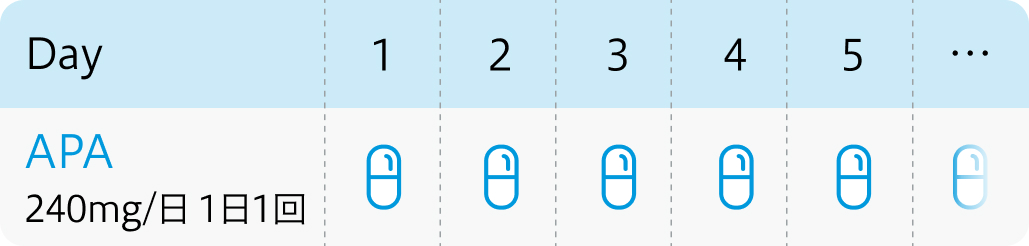
アパルタミド1日1回240mgを経口投与する
アーリーダ®電子添文 (2023年10月改訂 第4版)¹⁾より作図
特徴と注意点
2019年5月から日本で発売された第2世代抗アンドロゲン剤 (ヤンセンファーマ株式会社) である。 皮疹、 消化器毒性、 倦怠感などに注意。
監修 : 国立がん研究センター東病院 腫瘍内科 近藤 千紘先生
各プロトコル
投与開始基準
TITAN試験³⁾⁴⁾のプロトコル例
組織学的または細胞学的に前立腺癌と診断された18歳以上の患者 (骨シンチグラフィで骨病変2個以上の転移性疾患、 PS 0~2など)
ただし、 以下の場合を除く
- CT/MRIで肝臓または肺に転移あり
- 骨シンチグラフィで骨病変4個以上
- 骨盤または椎骨を超える病変1個以上
- その他以下の検査値
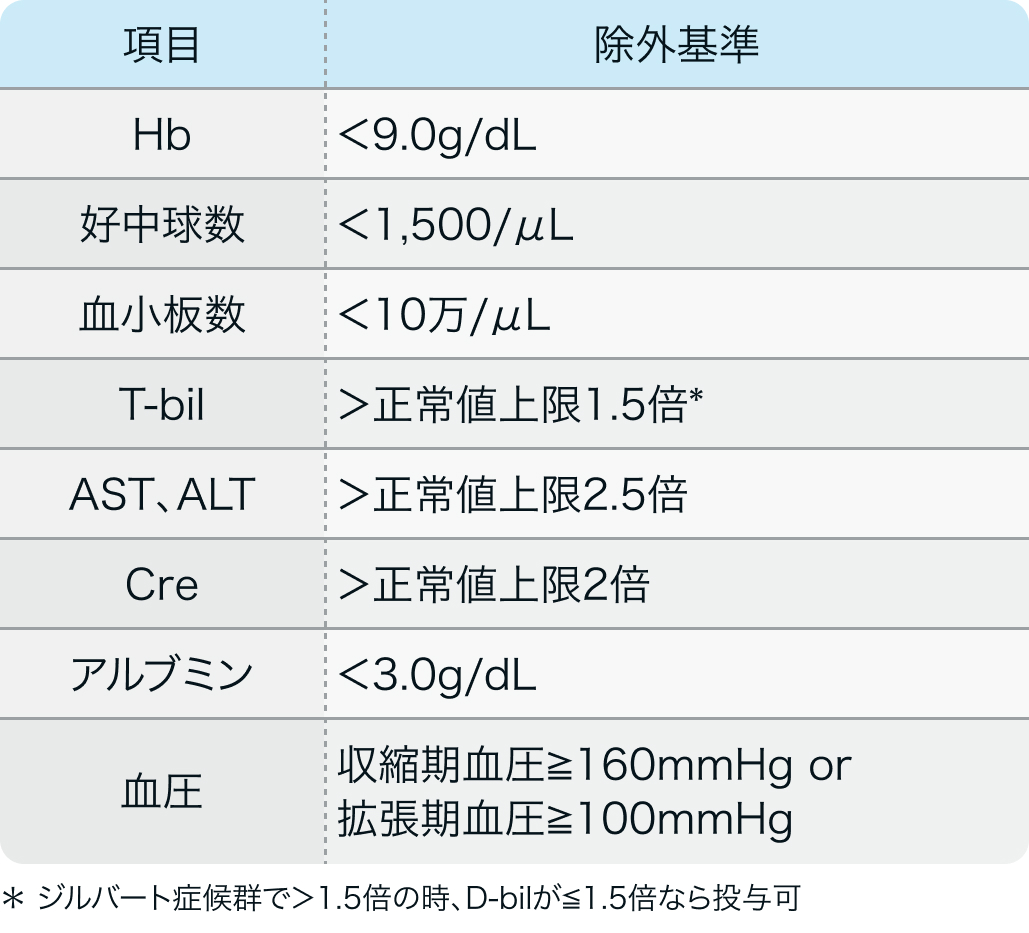
N Engl J Med. 2019 Jul 4;381(1):13-24³⁾、 J Clin Oncol. 2021 Jul 10;39(20):2294-2303⁴⁾より引用
減量・休薬・中止基準
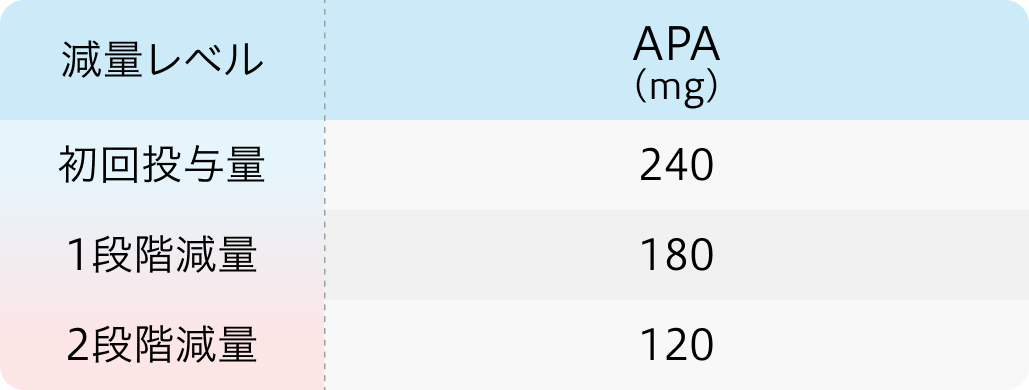
アーリーダ®電子添文 (2023年10月改訂 第4版)¹⁾より作図
痙攣発作 中止
痙攣発作以外の副作用 (Grade3、 4)
休薬 (Grade1以下またはベースラインに回復するまで)。 再開する場合には、 減量等を考慮すること。 (初回発現後に回復し再開する場合は減量せずに投与、 再発後に回復し再開する場合は1段階減量)
アーリーダ®電子添文 (2023年10月改訂 第4版)¹⁾より引用
KeyData|臨床試験結果
TITAN試験³⁾⁴⁾
³⁾ N Engl J Med. 2019;381(1):13-24.
⁴⁾ J Clin Oncol. 2021;39(20):2294-2303.
治療歴のあるホルモン感受性の転移性前立腺癌患者において、 アパルタミド+ADTの効果を、 プラセボ+ADTを対照に検証した第Ⅲ相無作為化比較試験TITANの結果より、 画像上の無増悪生存期間 (rPFS) と全生存期間 (OS) に対する有効性が示された。
主な有害事象 (カッコ内はGrade3~4)
- 倦怠感 19.7% (1.5%)
- 体重増加 10.3% (1.1%)
- 貧血 9.2% (1.7%)
- 便秘 9.0% (0%)
注意すべき有害事象 (カッコ内はGrade3~4)
- 高血圧 17.7% (8.4%)
- 甲状腺機能低下症 6.5% (0%)
N Engl J Med. 2019 Jul 4;381(1):13-24³⁾より引用
rPFS中央値
- アパルタミド+ADT群 : 未到達
- プラセボ+ADT群 : 22.1ヵ月
(95%CI 18.5-32.9ヵ月)
rPFS率 (24ヵ月時)
- アパルタミド+ADT群 : 68.2%
(95%CI 62.9-72.9%)
- プラセボ+ADT群 : 47.5%
(95%CI 42.1-52.8%)
HR 0.48 (95%CI 0.39-0.60)、 p<0.001
rPFSのサブグループ解析
腫瘍量に関わらず、 アパルタミド群で良好
OS中央値
- アパルタミド+ADT群 : 未到達
- プラセボ+ADT群 : 52.2ヵ月
(95%CI 41.9ヵ月-未到達)
HR 0.65 (95%CI 0.53-0.79)、 p<0.0001
OS率 (24ヵ月時、 48ヵ月時)
- アパルタミド+ADT群 : 82.4%、 65.1%
- プラセボ+ADT群 : 73.5%、 51.8%
HR 0.67 (95%CI 0.51-0.89)、 p=0.005
OSのサブグループ解析
腫瘍量に関わらず、 アパルタミド群で良好
化学療法までの期間
両群とも未到達
HR 0.47 (95%CI 0.35-0.63)、 p<0.0001
痛みの増悪までの期間
両群とも未到達
HR 0.87 (95%CI 0.70-1.08)、 p=0.197
オピオイド使用までの期間
両群とも未到達
HR 0.79 (95%CI 0.58-1.09)、 p=0.156
骨関連事象までの期間
両群とも未到達
HR 0.86 (95%CI 0.62-1.19)、 p=0.361
PSA値上昇までの期間
- アパルタミド+ADT群 : 未到達
- プラセボ+ADT群 : 12.9ヵ月
(95%CI 10.2-14.8ヵ月)
HR 0.27 (95%CI 0.22-0.33)、 p<0.0001
PFS2
- アパルタミド+ADT群 : 未到達
- プラセボ+ADT群 : 44ヵ月
(95%CI 38.9ヵ月-未到達)
HR 0.62 (95%CI 0.51-0.75)、 p<0.0001
出典
- ヤンセンファーマ株式会社. アーリーダ®電子添文 (2025年8月改訂 第6版)
- ヤンセンファーマ株式会社. アーリーダ®適正使用ガイド (2024年12月改訂)
- Apalutamide for Metastatic, Castration-Sensitive Prostate Cancer. N Engl J Med. 2019 Jul 4;381(1):13-24. PMID: 31150574
- Apalutamide in Patients With Metastatic Castration-Sensitive Prostate Cancer: Final Survival Analysis of the Randomized, Double-Blind, Phase III TITAN Study. J Clin Oncol. 2021 Jul 10;39(20):2294-2303. PMID: 33914595
最終更新日 : 2025年9月11日
監修医師 : 国立がん研究センター東病院 腫瘍内科 近藤 千紘先生
APA (Apalutamide)
本コンテンツは特定の治療法を推奨するものではありません。 個々の患者の病態や、 実際の薬剤情報やガイドラインを確認の上、 利用者の判断と責任でご利用ください。
薬剤情報
第2世代抗アンドロゲン薬 アパルタミド
*ヤンセンファーマ株式会社の外部サイトへ遷移します
用法用量
添付文書¹⁾の用法および用量

アパルタミド1日1回240mgを経口投与する
アーリーダ®電子添文 (2023年10月改訂 第4版)¹⁾より作図
特徴と注意点
2019年5月から日本で発売された第2世代抗アンドロゲン剤 (ヤンセンファーマ株式会社) である。 皮疹、 消化器毒性、 倦怠感などに注意。
監修 : 国立がん研究センター東病院 腫瘍内科 近藤 千紘先生
各プロトコル
投与開始基準
TITAN試験³⁾⁴⁾のプロトコル例
組織学的または細胞学的に前立腺癌と診断された18歳以上の患者 (骨シンチグラフィで骨病変2個以上の転移性疾患、 PS 0~2など)
ただし、 以下の場合を除く
- CT/MRIで肝臓または肺に転移あり
- 骨シンチグラフィで骨病変4個以上
- 骨盤または椎骨を超える病変1個以上
- その他以下の検査値

N Engl J Med. 2019 Jul 4;381(1):13-24³⁾、 J Clin Oncol. 2021 Jul 10;39(20):2294-2303⁴⁾より引用
減量・休薬・中止基準

アーリーダ®電子添文 (2023年10月改訂 第4版)¹⁾より作図
痙攣発作 中止
痙攣発作以外の副作用 (Grade3、 4)
休薬 (Grade1以下またはベースラインに回復するまで)。 再開する場合には、 減量等を考慮すること。 (初回発現後に回復し再開する場合は減量せずに投与、 再発後に回復し再開する場合は1段階減量)
アーリーダ®電子添文 (2023年10月改訂 第4版)¹⁾より引用
KeyData|臨床試験結果
TITAN試験³⁾⁴⁾
³⁾ N Engl J Med. 2019;381(1):13-24.
⁴⁾ J Clin Oncol. 2021;39(20):2294-2303.
治療歴のあるホルモン感受性の転移性前立腺癌患者において、 アパルタミド+ADTの効果を、 プラセボ+ADTを対照に検証した第Ⅲ相無作為化比較試験TITANの結果より、 画像上の無増悪生存期間 (rPFS) と全生存期間 (OS) に対する有効性が示された。
主な有害事象 (カッコ内はGrade3~4)
- 倦怠感 19.7% (1.5%)
- 体重増加 10.3% (1.1%)
- 貧血 9.2% (1.7%)
- 便秘 9.0% (0%)
注意すべき有害事象 (カッコ内はGrade3~4)
- 高血圧 17.7% (8.4%)
- 甲状腺機能低下症 6.5% (0%)
N Engl J Med. 2019 Jul 4;381(1):13-24³⁾より引用
rPFS中央値
- アパルタミド+ADT群 : 未到達
- プラセボ+ADT群 : 22.1ヵ月
(95%CI 18.5-32.9ヵ月)
rPFS率 (24ヵ月時)
- アパルタミド+ADT群 : 68.2%
(95%CI 62.9-72.9%)
- プラセボ+ADT群 : 47.5%
(95%CI 42.1-52.8%)
HR 0.48 (95%CI 0.39-0.60)、 p<0.001
rPFSのサブグループ解析
腫瘍量に関わらず、 アパルタミド群で良好
OS中央値
- アパルタミド+ADT群 : 未到達
- プラセボ+ADT群 : 52.2ヵ月
(95%CI 41.9ヵ月-未到達)
HR 0.65 (95%CI 0.53-0.79)、 p<0.0001
OS率 (24ヵ月時、 48ヵ月時)
- アパルタミド+ADT群 : 82.4%、 65.1%
- プラセボ+ADT群 : 73.5%、 51.8%
HR 0.67 (95%CI 0.51-0.89)、 p=0.005
OSのサブグループ解析
腫瘍量に関わらず、 アパルタミド群で良好
化学療法までの期間
両群とも未到達
HR 0.47 (95%CI 0.35-0.63)、 p<0.0001
痛みの増悪までの期間
両群とも未到達
HR 0.87 (95%CI 0.70-1.08)、 p=0.197
オピオイド使用までの期間
両群とも未到達
HR 0.79 (95%CI 0.58-1.09)、 p=0.156
骨関連事象までの期間
両群とも未到達
HR 0.86 (95%CI 0.62-1.19)、 p=0.361
PSA値上昇までの期間
- アパルタミド+ADT群 : 未到達
- プラセボ+ADT群 : 12.9ヵ月
(95%CI 10.2-14.8ヵ月)
HR 0.27 (95%CI 0.22-0.33)、 p<0.0001
PFS2
- アパルタミド+ADT群 : 未到達
- プラセボ+ADT群 : 44ヵ月
(95%CI 38.9ヵ月-未到達)
HR 0.62 (95%CI 0.51-0.75)、 p<0.0001
出典
- ヤンセンファーマ株式会社. アーリーダ®電子添文 (2025年8月改訂 第6版)
- ヤンセンファーマ株式会社. アーリーダ®適正使用ガイド (2024年12月改訂)
- Apalutamide for Metastatic, Castration-Sensitive Prostate Cancer. N Engl J Med. 2019 Jul 4;381(1):13-24. PMID: 31150574
- Apalutamide in Patients With Metastatic Castration-Sensitive Prostate Cancer: Final Survival Analysis of the Randomized, Double-Blind, Phase III TITAN Study. J Clin Oncol. 2021 Jul 10;39(20):2294-2303. PMID: 33914595
最終更新日 : 2025年9月11日
監修医師 : 国立がん研究センター東病院 腫瘍内科 近藤 千紘先生
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
がん薬物療法における治療計画をまとめたものです。
主要論文や適正使用ガイドをもとにした用量調整プロトコール、 有害事象対応をご紹介します。
なお、 本ツールは医師向けの教育用資料であり、 実臨床での使用は想定しておりません。 最新の添付文書やガイドラインを必ずご確認下さい。
また、 一般の方への情報提供ではないことを予めご了承ください。