本コンテンツは特定の治療法を推奨するものではありません。 個々の患者の病態や、 実際の薬剤情報やガイドラインを確認の上、 利用者の判断と責任でご利用ください。
薬剤情報
キイトルーダ® (ペムブロリズマブ)
MSD株式会社の外部サイトへ遷移します
投与スケジュール
【1コース】 21日間
【催吐性】CDDP : 高度、 CBDCA : 中等度
【FN発症】 未報告*
KEYNOTE-189試験³⁾では、 FN発生率は未報告
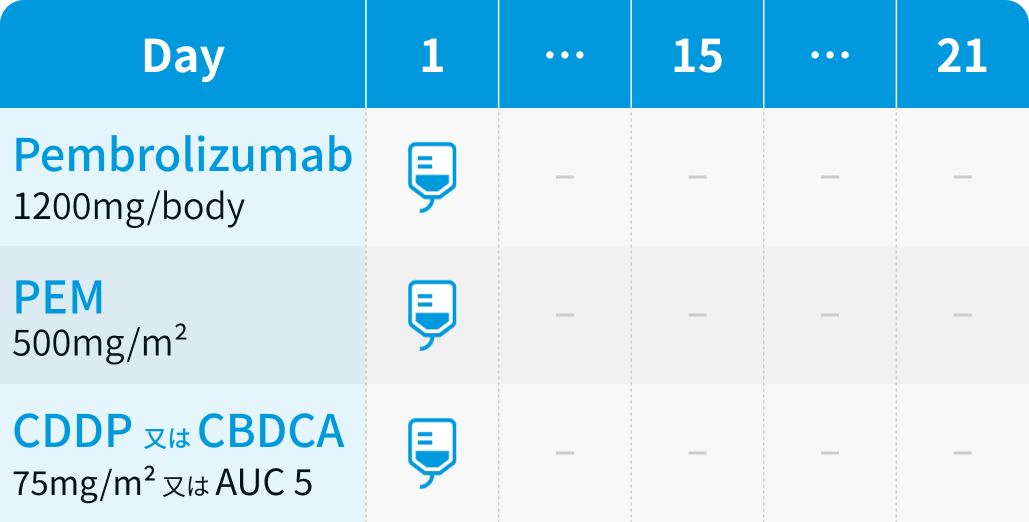
ペムブロリズマブ : 200mgを30分かけて点滴静注し、 3週ごとに投与
ペメトレキセド (PEM) : 500mg/m²を10分かけて点滴静注し、 3週ごとに投与
白金剤 : シスプラチン (CDDP) 75mg/m²またはカルボプラチン (CBDCA) AUC 5mg/mL/minを点滴静注し、 3週ごとに投与
白金剤は4コースまで投与。 以降は維持療法として、 PEMを病勢進行または忍容不能な毒性まで継続。 ペムブロリズマブは病勢進行または忍容不能な毒性まで投与し、 投与回数は最大35回まで。
Key Data|臨床試験結果
📊 KEYNOTE-189試験
N Engl J Med. 2018;378(22):2078-2092.
未治療の転移性・非扁平上皮NSCLCを対象に、 ペムブロリズマブ+プラチナ製剤+ペメトレキセド併用療法の有効性と安全性を検討した第III相無作為化比較試験。 介入群410例、 対照群 (プラセボ+化学療法) 206例が割り付けられ、 主要評価項目はOSおよびPFSとした。
【有効性】ペムブロリズマブ群 (vs プラセボ群)
- OS中央値 未到達 (vs 11.3ヵ月)
- HR 0.49 (95%CI 0.38–0.64、 p<0.001)
- PFS中央値 8.8ヵ月 (vs 4.9ヵ月)
- HR 0.52 (95%CI 0.43–0.64、 p<0.001)
- ORR 47.6% (vs 18.9%)
【安全性】主な有害事象 : 全Grade (Grade≧3)
- 悪心 55.6% (3.5%)
- 貧血 46.2% (16.3%)
- 倦怠感 40.7% (5.7%)
- 便秘 34.8% (1.0%)
- 下痢 30.9% (5.2%)
- 食欲減退 28.1% (1.5%)
- 好中球減少 27.2% (15.8%)
- 嘔吐 24.2% (3.7%)
- 咳嗽 21.5% (0%)
- 呼吸困難 21.2% (3.7%)
- 無力症 20.5% (6.2%)
- 発疹 20.2% (1.7%)
- 発熱 19.5% (0.2%)
- 末梢浮腫 19.3% (0.2%)
- 血小板減少 18.0% (7.9%)
- 流涙増加 17.0% (0%)
各プロトコル
適格基準
KEYNOTE-189試験³⁾の主な適格基準
- 18歳以上
- 未治療の転移性非扁平上皮NSCLC
- ECOG PS 0–1
- 好中球数≧1500/μL
- 血小板数≧10万/μL
- Hb≧9.0g/dL
- 腎機能 CrCl≧50mL/min
- 肝機能 T-Bil≦1.5×ULN、 AST/ALT≦2.5×ULN (肝転移例では≦5.0×ULN)
用量レベル
ペムブロリズマブ : 減量規定なし (固定用量)
化学療法 :
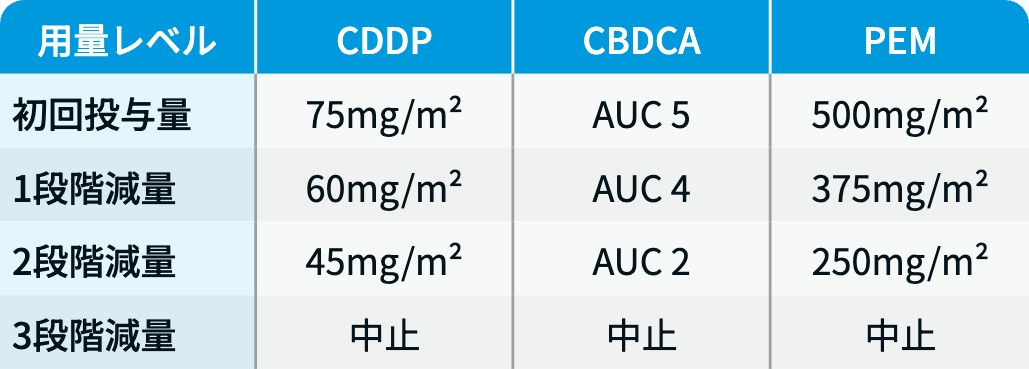
腎障害患者に対する用量調整
ペムブロリズマブ : 抗体薬は多様な細胞でのエンドサイトーシスとリソソーム分解により消失するため、 一般に減量は不要と考えられる。
編集部の見解
CDDP⁴⁾ :
- 重篤な腎障害例への投与は禁忌
- CrCl 46~60mL/minでは75%、 31~45mL/minでは50%に減量し、 CrCl≦30mL/minでは投与を推奨しない
- 別の報告 : CrCl 30~49mL/minでは75%、 10~29mL/minでは投与が必要な場合に75%、 CrCl<10mL/minでは投与が必要な場合に50%に減量
CBDCA : Calvert式で投与量を算出する
PEM : 重度の腎機能障害患者には投与しない。 なお、 CrCl<45mL/minの患者は別の臨床試験で除外されている
FDA添付文書 : CrCl<45mL/minの患者には投与しない
有害事象発現時の減量・休薬・中止基準
サイクル開始基準 :
- 毒性がGrade≦1又はベースラインに回復
- CrCl≧45mL/min*
*前回投与後42日以内にCrClが45≧mL/minに回復しない場合、 白金製剤および/またはPEMは中止
ペムブロリズマブ :

キイトルーダ®電子添文¹⁾を基に編集部作成
化学療法 :
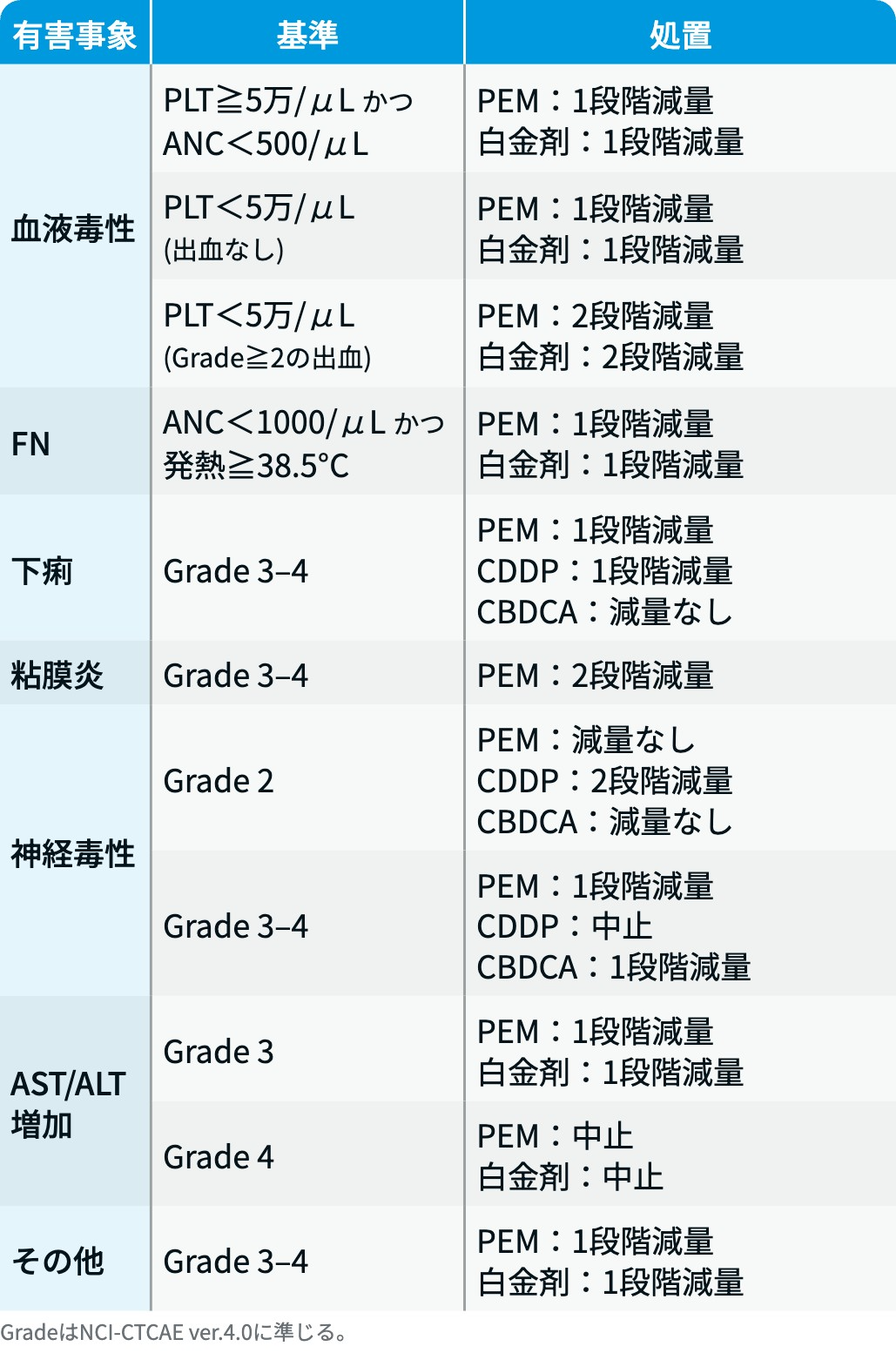
KEYNOTE-189試験³⁾のプロトコルを基に編集部作成
レジメンの特徴と注意点
作用機序の特徴
ペムブロリズマブは、 T細胞上のPD-1受容体に結合し、 腫瘍細胞上のPD-L1およびPD-L2との結合を阻害することで、 PD-1経路を介した抗腫瘍免疫応答の抑制を解除し、 T細胞の活性化を促進する。
レジメン適用時の注意事項
CDDPによる腎障害予防 : 十分な水分負荷と利尿管理を行い、 水分負荷に対する心機能の耐容性は事前に確認する。
PEMの副作用予防 : 重篤な副作用を軽減するため、 初回投与7日以上前から葉酸0.5mgを1日1回連日経口投与し、 最終投与日から22日目まで可能な限り継続する。 ビタミンB12は初回投与少なくとも7日前に1mgを筋肉内投与し、 投与期間中および中止後22日目まで9週ごと (3コースごと) に追加投与する。
免疫関連有害事象 : T細胞活性化により、 多様な免疫関連有害事象が発現することがある。 異常時は鑑別診断を行い、 必要に応じて副腎皮質ホルモンを投与する。 本剤終了後も発現しうるため、 継続的に観察を行う。
間質性肺疾患 : 息切れ・呼吸困難・咳などに注意し、 胸部X線、 必要に応じてCTや血清マーカーを実施する。
内分泌障害 : 甲状腺・下垂体・副腎機能低下が起こりうるため、 TSH、 FT3、 FT4、 ACTH、 コルチゾールなどを定期的に測定し、 必要に応じて画像検査を行う。
肝障害 : 劇症肝炎、 肝不全、 硬化性胆管炎などが報告されており、 特にアキシチニブ併用時は肝機能検査を頻回に実施し観察する。
1型糖尿病 : 口渇、 悪心、 嘔吐、 血糖上昇に注意し、 血糖モニタリングを行う。
腎障害 : 腎機能を定期的に検査し、 状態を観察する。
筋障害 : 筋炎や横紋筋融解症に注意し、 筋力低下、 筋痛、 CKやミオグロビンの上昇を観察する。
重症筋無力症 : 筋力低下、 眼瞼下垂、 呼吸困難、 嚥下障害などを観察する。
心筋炎 : 胸痛、 CK上昇、 心電図異常に注意し、 状態を観察する。
眼障害 : ぶどう膜炎などの重篤な障害に注意し、 定期的な眼の確認を行う。 異常時は速やかに受診を促す。
RMP【重要な特定されたリスク】
キイトルーダ®RMP : 医薬品リスク管理計画書
- 間質性肺疾患
- 大腸炎、 小腸炎、 重度の下痢
- 劇症肝炎、 肝不全、 肝機能障害、 肝炎、 硬化性胆管炎
- 腎機能障害 (尿細管間質性腎炎、 糸球体腎炎等)
- 内分泌障害 (垂体機能低下症、 副腎皮質機能不全、 甲状腺機能障害、 1型糖尿病)
- 1型糖尿病
- 筋炎、 横紋筋融解症
- 重症筋無力症
- 心筋炎
- 脳炎、 髄膜炎、 脊髄炎
- 重度の皮膚障害
- 神経障害 (ギラン・バレー症候群等)
- 膵炎・膵外分泌機能不全
- Infusion reaction
- 臓器移植歴 (造血幹細胞移植歴を含む) のある患者への使用
- 結核
出典
1) キイトルーダ®点滴静注100mg 電子添文 (2025年7月改訂 第25版)
2) キイトルーダ®点滴静注100mg 適正使用ガイド (2025年10月作成)
3) N Engl J Med. 2018;378(22):2078-2092.
4) 日本腎臓学会、 日本癌治療学会、 日本臨床腫瘍学会、 日本腎臓病薬物療法学会編 : がん薬物療法時の腎障害診療ガイドライン2022. ライフサイエンス出版.
最終更新日 : 2026年1月30日
執筆 : HOKUTO編集部 がん専門・指導薬剤師
監修 : HOKUTO編集部監修医師
Pembrolizumab+CDDP/CBDCA+PEM
本コンテンツは特定の治療法を推奨するものではありません。 個々の患者の病態や、 実際の薬剤情報やガイドラインを確認の上、 利用者の判断と責任でご利用ください。
薬剤情報
キイトルーダ® (ペムブロリズマブ)
MSD株式会社の外部サイトへ遷移します
投与スケジュール
【1コース】 21日間
【催吐性】CDDP : 高度、 CBDCA : 中等度
【FN発症】 未報告*
KEYNOTE-189試験³⁾では、 FN発生率は未報告

ペムブロリズマブ : 200mgを30分かけて点滴静注し、 3週ごとに投与
ペメトレキセド (PEM) : 500mg/m²を10分かけて点滴静注し、 3週ごとに投与
白金剤 : シスプラチン (CDDP) 75mg/m²またはカルボプラチン (CBDCA) AUC 5mg/mL/minを点滴静注し、 3週ごとに投与
白金剤は4コースまで投与。 以降は維持療法として、 PEMを病勢進行または忍容不能な毒性まで継続。 ペムブロリズマブは病勢進行または忍容不能な毒性まで投与し、 投与回数は最大35回まで。
Key Data|臨床試験結果
📊 KEYNOTE-189試験
N Engl J Med. 2018;378(22):2078-2092.
未治療の転移性・非扁平上皮NSCLCを対象に、 ペムブロリズマブ+プラチナ製剤+ペメトレキセド併用療法の有効性と安全性を検討した第III相無作為化比較試験。 介入群410例、 対照群 (プラセボ+化学療法) 206例が割り付けられ、 主要評価項目はOSおよびPFSとした。
【有効性】ペムブロリズマブ群 (vs プラセボ群)
- OS中央値 未到達 (vs 11.3ヵ月)
- HR 0.49 (95%CI 0.38–0.64、 p<0.001)
- PFS中央値 8.8ヵ月 (vs 4.9ヵ月)
- HR 0.52 (95%CI 0.43–0.64、 p<0.001)
- ORR 47.6% (vs 18.9%)
【安全性】主な有害事象 : 全Grade (Grade≧3)
- 悪心 55.6% (3.5%)
- 貧血 46.2% (16.3%)
- 倦怠感 40.7% (5.7%)
- 便秘 34.8% (1.0%)
- 下痢 30.9% (5.2%)
- 食欲減退 28.1% (1.5%)
- 好中球減少 27.2% (15.8%)
- 嘔吐 24.2% (3.7%)
- 咳嗽 21.5% (0%)
- 呼吸困難 21.2% (3.7%)
- 無力症 20.5% (6.2%)
- 発疹 20.2% (1.7%)
- 発熱 19.5% (0.2%)
- 末梢浮腫 19.3% (0.2%)
- 血小板減少 18.0% (7.9%)
- 流涙増加 17.0% (0%)
各プロトコル
適格基準
KEYNOTE-189試験³⁾の主な適格基準
- 18歳以上
- 未治療の転移性非扁平上皮NSCLC
- ECOG PS 0–1
- 好中球数≧1500/μL
- 血小板数≧10万/μL
- Hb≧9.0g/dL
- 腎機能 CrCl≧50mL/min
- 肝機能 T-Bil≦1.5×ULN、 AST/ALT≦2.5×ULN (肝転移例では≦5.0×ULN)
用量レベル
ペムブロリズマブ : 減量規定なし (固定用量)
化学療法 :

腎障害患者に対する用量調整
ペムブロリズマブ : 抗体薬は多様な細胞でのエンドサイトーシスとリソソーム分解により消失するため、 一般に減量は不要と考えられる。
編集部の見解
CDDP⁴⁾ :
- 重篤な腎障害例への投与は禁忌
- CrCl 46~60mL/minでは75%、 31~45mL/minでは50%に減量し、 CrCl≦30mL/minでは投与を推奨しない
- 別の報告 : CrCl 30~49mL/minでは75%、 10~29mL/minでは投与が必要な場合に75%、 CrCl<10mL/minでは投与が必要な場合に50%に減量
CBDCA : Calvert式で投与量を算出する
PEM : 重度の腎機能障害患者には投与しない。 なお、 CrCl<45mL/minの患者は別の臨床試験で除外されている
FDA添付文書 : CrCl<45mL/minの患者には投与しない
有害事象発現時の減量・休薬・中止基準
サイクル開始基準 :
- 毒性がGrade≦1又はベースラインに回復
- CrCl≧45mL/min*
*前回投与後42日以内にCrClが45≧mL/minに回復しない場合、 白金製剤および/またはPEMは中止
ペムブロリズマブ :

キイトルーダ®電子添文¹⁾を基に編集部作成
化学療法 :

KEYNOTE-189試験³⁾のプロトコルを基に編集部作成
レジメンの特徴と注意点
作用機序の特徴
ペムブロリズマブは、 T細胞上のPD-1受容体に結合し、 腫瘍細胞上のPD-L1およびPD-L2との結合を阻害することで、 PD-1経路を介した抗腫瘍免疫応答の抑制を解除し、 T細胞の活性化を促進する。
レジメン適用時の注意事項
CDDPによる腎障害予防 : 十分な水分負荷と利尿管理を行い、 水分負荷に対する心機能の耐容性は事前に確認する。
PEMの副作用予防 : 重篤な副作用を軽減するため、 初回投与7日以上前から葉酸0.5mgを1日1回連日経口投与し、 最終投与日から22日目まで可能な限り継続する。 ビタミンB12は初回投与少なくとも7日前に1mgを筋肉内投与し、 投与期間中および中止後22日目まで9週ごと (3コースごと) に追加投与する。
免疫関連有害事象 : T細胞活性化により、 多様な免疫関連有害事象が発現することがある。 異常時は鑑別診断を行い、 必要に応じて副腎皮質ホルモンを投与する。 本剤終了後も発現しうるため、 継続的に観察を行う。
間質性肺疾患 : 息切れ・呼吸困難・咳などに注意し、 胸部X線、 必要に応じてCTや血清マーカーを実施する。
内分泌障害 : 甲状腺・下垂体・副腎機能低下が起こりうるため、 TSH、 FT3、 FT4、 ACTH、 コルチゾールなどを定期的に測定し、 必要に応じて画像検査を行う。
肝障害 : 劇症肝炎、 肝不全、 硬化性胆管炎などが報告されており、 特にアキシチニブ併用時は肝機能検査を頻回に実施し観察する。
1型糖尿病 : 口渇、 悪心、 嘔吐、 血糖上昇に注意し、 血糖モニタリングを行う。
腎障害 : 腎機能を定期的に検査し、 状態を観察する。
筋障害 : 筋炎や横紋筋融解症に注意し、 筋力低下、 筋痛、 CKやミオグロビンの上昇を観察する。
重症筋無力症 : 筋力低下、 眼瞼下垂、 呼吸困難、 嚥下障害などを観察する。
心筋炎 : 胸痛、 CK上昇、 心電図異常に注意し、 状態を観察する。
眼障害 : ぶどう膜炎などの重篤な障害に注意し、 定期的な眼の確認を行う。 異常時は速やかに受診を促す。
RMP【重要な特定されたリスク】
キイトルーダ®RMP : 医薬品リスク管理計画書
- 間質性肺疾患
- 大腸炎、 小腸炎、 重度の下痢
- 劇症肝炎、 肝不全、 肝機能障害、 肝炎、 硬化性胆管炎
- 腎機能障害 (尿細管間質性腎炎、 糸球体腎炎等)
- 内分泌障害 (垂体機能低下症、 副腎皮質機能不全、 甲状腺機能障害、 1型糖尿病)
- 1型糖尿病
- 筋炎、 横紋筋融解症
- 重症筋無力症
- 心筋炎
- 脳炎、 髄膜炎、 脊髄炎
- 重度の皮膚障害
- 神経障害 (ギラン・バレー症候群等)
- 膵炎・膵外分泌機能不全
- Infusion reaction
- 臓器移植歴 (造血幹細胞移植歴を含む) のある患者への使用
- 結核
出典
1) キイトルーダ®点滴静注100mg 電子添文 (2025年7月改訂 第25版)
2) キイトルーダ®点滴静注100mg 適正使用ガイド (2025年10月作成)
3) N Engl J Med. 2018;378(22):2078-2092.
4) 日本腎臓学会、 日本癌治療学会、 日本臨床腫瘍学会、 日本腎臓病薬物療法学会編 : がん薬物療法時の腎障害診療ガイドライン2022. ライフサイエンス出版.
最終更新日 : 2026年1月30日
執筆 : HOKUTO編集部 がん専門・指導薬剤師
監修 : HOKUTO編集部監修医師
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
がん薬物療法における治療計画をまとめたものです。
主要論文や適正使用ガイドをもとにした用量調整プロトコール、 有害事象対応をご紹介します。
なお、 本ツールは医師向けの教育用資料であり、 実臨床での使用は想定しておりません。 最新の添付文書やガイドラインを必ずご確認下さい。
また、 一般の方への情報提供ではないことを予めご了承ください。