本コンテンツは特定の治療法を推奨するものではありません。 個々の患者の病態や、 実際の薬剤情報やガイドラインを確認の上、 利用者の判断と責任でご利用ください。
薬剤情報
【催吐性】 軽度催吐性
ベプシド® (添付文書¹⁾)
用法用量
第Ⅱ相試験²⁾のプロトコル
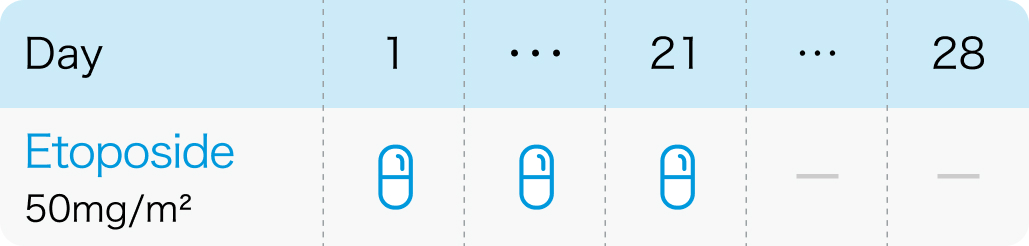
放射線治療歴の患者には、 30mg/m²で治療が行われ、 耐容された場合は増量可
後続のサイクルにおいてはGrade3、 4の毒性がなく、 血液学的毒性 (≦Grade2) の経験がある患者には最大60mg/m²までの増量処方
J Clin Oncol. 1998 Feb;16(2):405-10²⁾より作図、 引用
電子添文の用法及び用量
1日50mg/m²を21日間連続経口投与し、 1週間休薬
手術あるいは放射線治療の補助化学療法における有効性・安全性は確立していない
ベプシド®電子添文 (2023年2月改訂第1版)¹⁾より引用
投与開始基準
第Ⅱ相試験²⁾のプロトコル
エトポシドを除く化学療法が1回以下の身体検査または放射線学的検査で測定可能な腫瘍がある以下に該当する患者
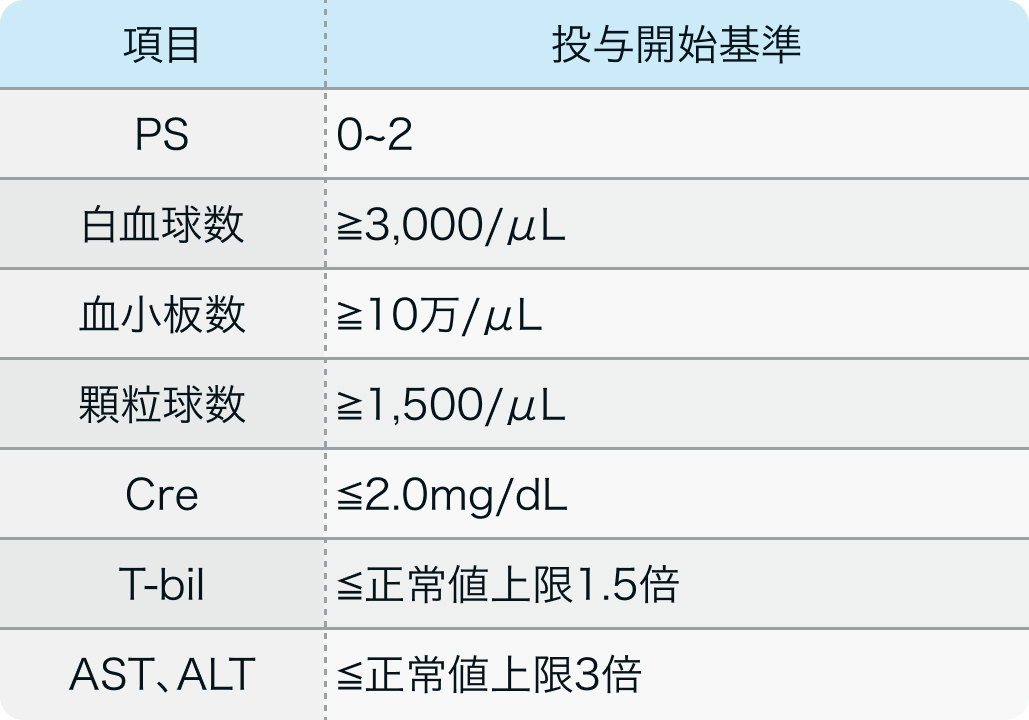
J Clin Oncol. 1998 Feb;16(2):405-10²⁾より作図
減量・休薬・中止基準
第Ⅱ相試験²⁾のプロトコル
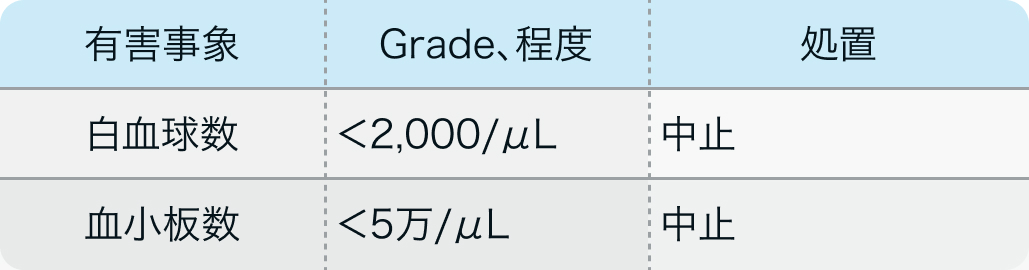
J Clin Oncol. 1998 Feb;16(2):405-10²⁾より作図
KeyData|臨床試験結果
第Ⅱ相試験²⁾
対象: プラチナベースの化学療法中に進行または治療完了後6ヵ月以内に再発した卵巣癌患者99例
方法: Oral Etoposide 50mg/m²/日 (以前に放射線療法を受けた場合、 30mg/m²/日) を21日間、 28日ごとに投与
【有効性】
- ORR 26.8%
- mPFS 5.7ヵ月
- mOS 10.8ヵ月
【安全性】主な有害事象 (カッコ内 Grade3~4)
- 白血球数減少 83.5% (41.2%)
- 好中球数減少 74.2% (45.4%)
- 貧血 44.3% (13.4%)
- 血小板数減少 34.0% (9.3%)
- AST増加 1.0% (0%)
- 発熱 8.2% (2.1%)
- 倦怠感 4.1% (1.0%)
- 体重減少 2.1% (1.0%)
- 脱毛症 13.4% (0%)
- 高血圧 1.0% (0%)
J Clin Oncol. 1998 Feb;16(2):405-10²⁾より引用
エキスパートによるワンポイント
プラチナ抵抗性再発卵巣癌の治療選択肢
第Ⅱ相試験²⁾では、 奏効率26.8% (11/41名) でした。 主な副作用としては、 骨髄毒性になります。 薬事承認はありませんが、 保険適応 (社会保険支払基金) になっている薬剤です。 プラチナ抵抗性になった患者さんで、 PSがよく、 前治療にもよく効いていた患者さんには、 選択肢の一つと考えてもよいと思います。
治療選択のポイント
プラチナ抵抗性再発卵巣癌に対するレジメンは、 PLDをはじめ複数存在しますが、 どのレジメンが最もよいのかは、 結論が得られていません。 また、 BSC (Best supportive care)との比較も行われていませんので、 プラチナ抵抗性再発卵巣癌に対して、 化学療法を行うことのベネフィットも示されていないとも言えます。 プラチナ抵抗性再発卵巣癌患者さんに、 どのレジメンを使用するかは、 副作用のプロファイル、 投与スケジュールなどを考慮して、 患者さんと相談しながら、 考えていくのがよいと思います。
監修 : 日本医科大学 武蔵小杉病院 腫瘍内科教授 勝俣 範之先生
出典
- 小野薬品工業株式会社. ベプシド®電子添文 (2023年2月改訂第1版) [最終閲覧 : 2024/03/25]
- Prolonged oral etoposide as second-line therapy for platinum-resistant and platinum-sensitive ovarian carcinoma: a Gynecologic Oncology Group study. J Clin Oncol. 1998 Feb;16(2):405-10. PMID: 9469322
最終更新日 : 2024年8月3日
監修医師 : 日本医科大学 武蔵小杉病院 腫瘍内科教授 勝俣 範之先生
Oral Etoposide
本コンテンツは特定の治療法を推奨するものではありません。 個々の患者の病態や、 実際の薬剤情報やガイドラインを確認の上、 利用者の判断と責任でご利用ください。
薬剤情報
【催吐性】 軽度催吐性
ベプシド® (添付文書¹⁾)
用法用量
第Ⅱ相試験²⁾のプロトコル

放射線治療歴の患者には、 30mg/m²で治療が行われ、 耐容された場合は増量可
後続のサイクルにおいてはGrade3、 4の毒性がなく、 血液学的毒性 (≦Grade2) の経験がある患者には最大60mg/m²までの増量処方
J Clin Oncol. 1998 Feb;16(2):405-10²⁾より作図、 引用
電子添文の用法及び用量
1日50mg/m²を21日間連続経口投与し、 1週間休薬
手術あるいは放射線治療の補助化学療法における有効性・安全性は確立していない
ベプシド®電子添文 (2023年2月改訂第1版)¹⁾より引用
投与開始基準
第Ⅱ相試験²⁾のプロトコル
エトポシドを除く化学療法が1回以下の身体検査または放射線学的検査で測定可能な腫瘍がある以下に該当する患者

J Clin Oncol. 1998 Feb;16(2):405-10²⁾より作図
減量・休薬・中止基準
第Ⅱ相試験²⁾のプロトコル

J Clin Oncol. 1998 Feb;16(2):405-10²⁾より作図
KeyData|臨床試験結果
第Ⅱ相試験²⁾
対象: プラチナベースの化学療法中に進行または治療完了後6ヵ月以内に再発した卵巣癌患者99例
方法: Oral Etoposide 50mg/m²/日 (以前に放射線療法を受けた場合、 30mg/m²/日) を21日間、 28日ごとに投与
【有効性】
- ORR 26.8%
- mPFS 5.7ヵ月
- mOS 10.8ヵ月
【安全性】主な有害事象 (カッコ内 Grade3~4)
- 白血球数減少 83.5% (41.2%)
- 好中球数減少 74.2% (45.4%)
- 貧血 44.3% (13.4%)
- 血小板数減少 34.0% (9.3%)
- AST増加 1.0% (0%)
- 発熱 8.2% (2.1%)
- 倦怠感 4.1% (1.0%)
- 体重減少 2.1% (1.0%)
- 脱毛症 13.4% (0%)
- 高血圧 1.0% (0%)
J Clin Oncol. 1998 Feb;16(2):405-10²⁾より引用
エキスパートによるワンポイント
プラチナ抵抗性再発卵巣癌の治療選択肢
第Ⅱ相試験²⁾では、 奏効率26.8% (11/41名) でした。 主な副作用としては、 骨髄毒性になります。 薬事承認はありませんが、 保険適応 (社会保険支払基金) になっている薬剤です。 プラチナ抵抗性になった患者さんで、 PSがよく、 前治療にもよく効いていた患者さんには、 選択肢の一つと考えてもよいと思います。
治療選択のポイント
プラチナ抵抗性再発卵巣癌に対するレジメンは、 PLDをはじめ複数存在しますが、 どのレジメンが最もよいのかは、 結論が得られていません。 また、 BSC (Best supportive care)との比較も行われていませんので、 プラチナ抵抗性再発卵巣癌に対して、 化学療法を行うことのベネフィットも示されていないとも言えます。 プラチナ抵抗性再発卵巣癌患者さんに、 どのレジメンを使用するかは、 副作用のプロファイル、 投与スケジュールなどを考慮して、 患者さんと相談しながら、 考えていくのがよいと思います。
監修 : 日本医科大学 武蔵小杉病院 腫瘍内科教授 勝俣 範之先生
出典
- 小野薬品工業株式会社. ベプシド®電子添文 (2023年2月改訂第1版) [最終閲覧 : 2024/03/25]
- Prolonged oral etoposide as second-line therapy for platinum-resistant and platinum-sensitive ovarian carcinoma: a Gynecologic Oncology Group study. J Clin Oncol. 1998 Feb;16(2):405-10. PMID: 9469322
最終更新日 : 2024年8月3日
監修医師 : 日本医科大学 武蔵小杉病院 腫瘍内科教授 勝俣 範之先生
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
がん薬物療法における治療計画をまとめたものです。
主要論文や適正使用ガイドをもとにした用量調整プロトコール、 有害事象対応をご紹介します。
なお、 本ツールは医師向けの教育用資料であり、 実臨床での使用は想定しておりません。 最新の添付文書やガイドラインを必ずご確認下さい。
また、 一般の方への情報提供ではないことを予めご了承ください。