2024年6月24日に「METex14スキッピング変異陽性の切除不能な進行・再発の非小細胞肺癌 (METex14 : MET遺伝子エクソン14)」 を対象として承認。 2024年10月11日に発売。
本コンテンツは特定の治療法を推奨するものではありません。 個々の患者の病態や、 実際の薬剤情報やガイドラインを確認の上、 利用者の判断と責任でご利用ください。
薬剤情報
MET阻害薬 グマロンチニブ水和物
*大鵬薬品工業株式会社の外部サイトへ遷移します
投与スケジュール
【1コース】連日内服投与
【催吐性】 調査中
【FN発症】調査中
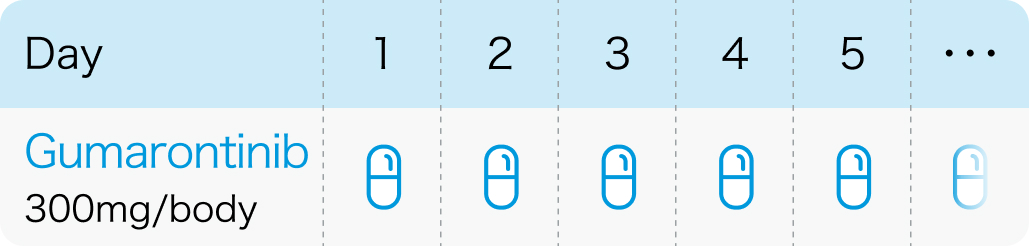
1回300mgを1日1回空腹時に経口投与する
ハイイータン®電子添文 (2024年9月改訂 第2版)¹⁾より作図
KeyData|臨床試験結果
📊GLORY試験²⁾
MET遺伝子エクソン14スキッピング変異陽性の局所進行または転移を有するNSCLC患者84例 (日本人患者10例を含む)、 うち1次治療 46例、 既治療 38例に対するグマロンチニブ300mg 1日1回投与の有効性と安全性を検証
【有効性】全体集団
- ORR 66%
1次治療例 71%、 既治療例 60%
- mPFS 8.5ヵ月
1次治療例 11.7ヵ月、 既治療例 7.6ヵ月
- mOS 17.3ヵ月
1次治療例 未到達、 既治療例 16.2ヵ月
【安全性】全体集団
主な有害事象 (カッコ内 Grade3~4)
- 浮腫 79.8% (21.4%)
- 低アルブミン血症 38.1% (0%)
- 頭痛 32.1% (2.4%)
- 食欲減少 32.1% (1.2%)
- 悪心 28.6% (1.2%)
- 血中ビリルビン上昇 27.4% (0%)
- ALT上昇 26.2% (1.2%)
- 嘔吐 23.8% (1.2%)
- AST上昇 21.4% (1.2%)
- 高血糖 17.9% (0%)
- 倦怠感 16.7% (3.6%)
- 貧血 16.7% (3.6%)
- 低カリウム血症 15.5% (3.6%)
- 白血球数減少 15.5% (1.2%)
- 好中球数減少 14.3% (4.8%)
- 低Na血症 14.3% (3.6%)
- 血小板数減少 14.3% (0%)
- 高尿酸血症 14.3% (0%)
- 便秘 13.1% (0%)
- 血清Cre上昇 13.1% (0%)
- 低Ca血症 11.9% (0%)
- 発疹 11.9% (2.4%)
- 手足の痛み 11.9% (0%)
- タンパク尿 10.7% (0%)
- 心電図QT延長 9.5% (3.6%)
- 背部痛 9.5% (2.4%)
- 胸水 9.5% (3.6%)
- 体重減少 8.3% (1.2%)
- ALP上昇 8.3% (1.2%)
- 不快 8.3% (1.2%)
- 呼吸困難 6.0% (1.2%)
EClinicalMedicine. 2023 Apr 6:59:101952²⁾より引用
各プロトコル
投与開始基準
GLORY試験²⁾のプロトコル
MET遺伝子エクソン14スキッピング変異陽性の局所進行または転移を有するNSCLC患者
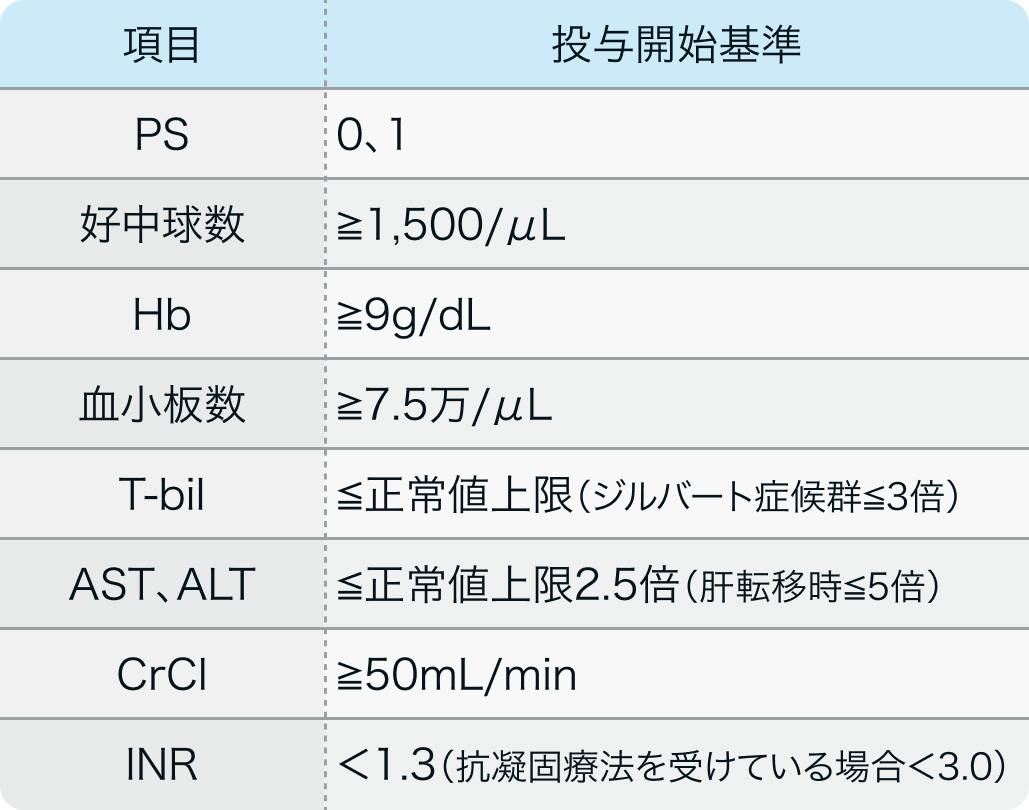
EClinicalMedicine. 2023 Apr 6:59:101952²⁾より作図
減量・休薬・休薬基準
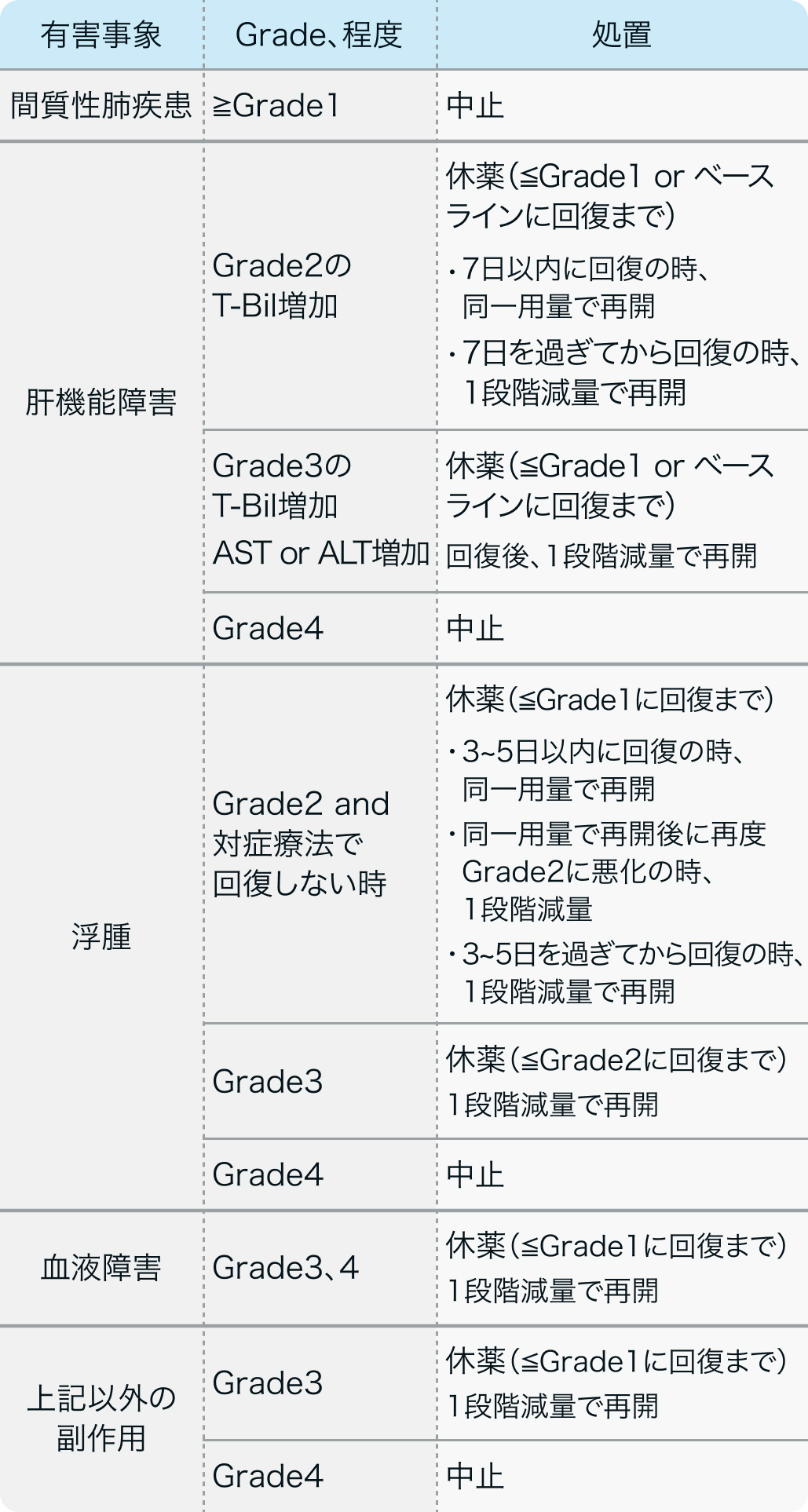
ハイイータン®電子添文 (2024年9月改訂 第2版)¹⁾より作図
初回基準量と減量レベル
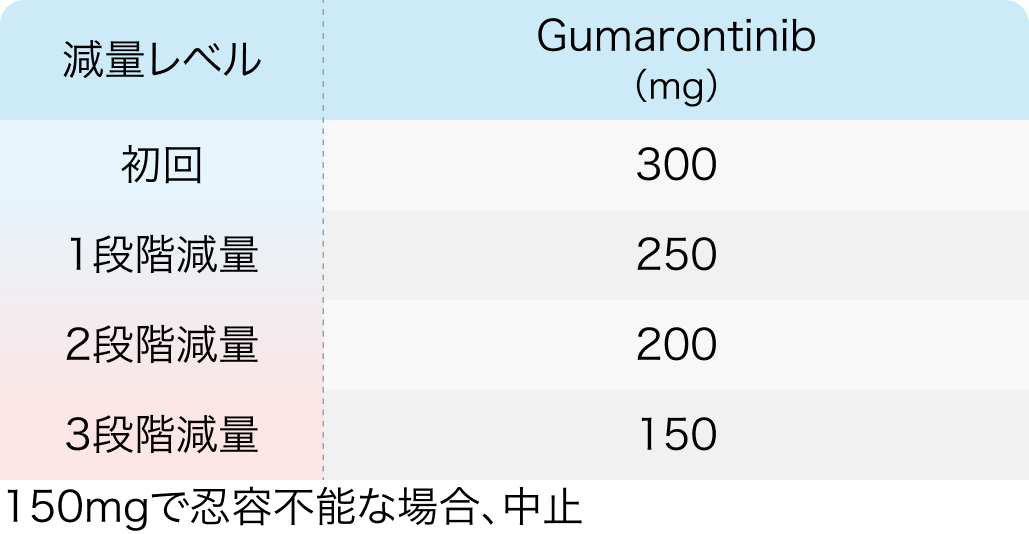
ハイイータン®電子添文 (2024年9月改訂 第2版)¹⁾より作図
特徴と注意点
MET阻害薬3剤の比較
臨床試験成績から直接比較は難しいものの、 各薬剤の治療成績はほぼ同等と考えられている。
- Tepotinib (テプミトコ®︎ VISION試験)
- Capmatinib (タブレクタ®︎ GEKMETRY試験)
- Gumarontinib (ハイイータン® GLORY試験)
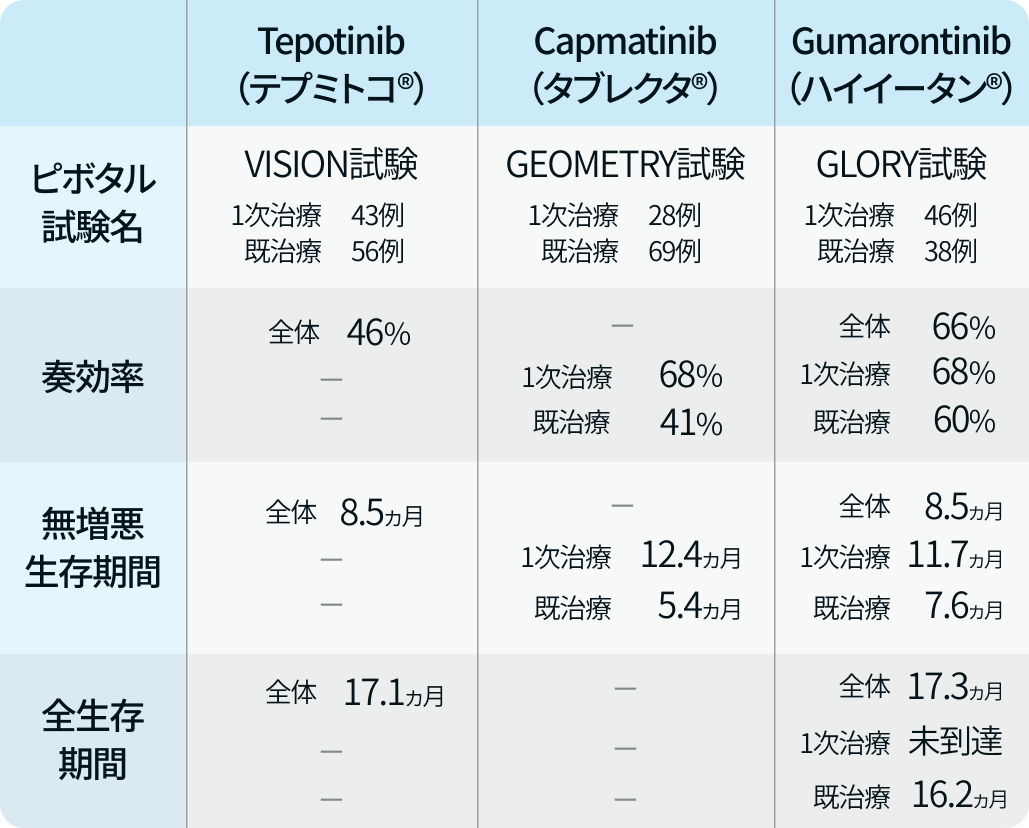
各臨床試験結果をもとにHOKUTO編集部で作表
コンパニオン診断薬
各MET阻害剤で適応となるCDxは異なる。
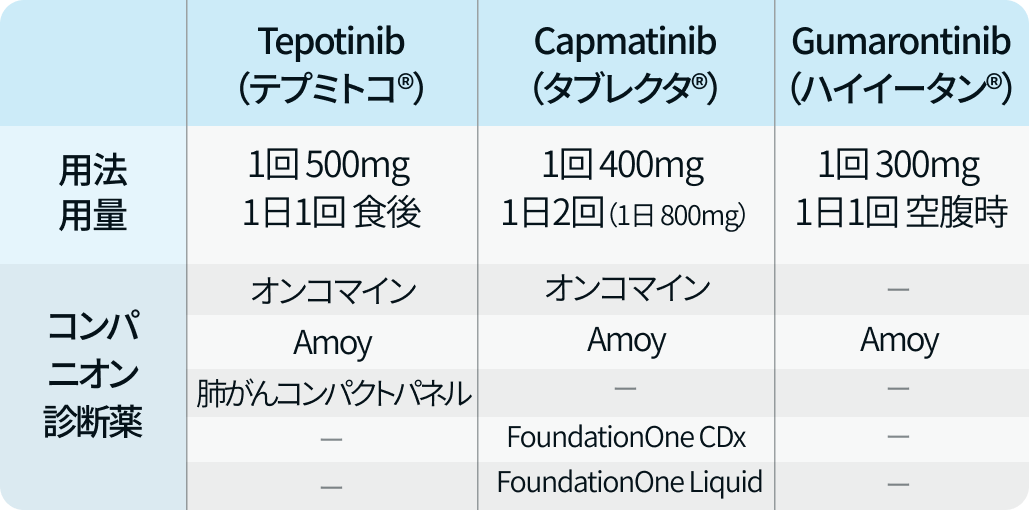
最新情報は日本肺癌学会の各種手引きや編集部まとめコンテンツを参照ください。
肺癌遺伝子パネル検査・コンパニオン診断薬一覧ページへ遷移
MET阻害薬の副作用マネジメント
MET阻害薬の特徴的な副作用としては、 末梢性浮腫、 肝機能障害、 消化器毒性 (嘔気、 嘔吐)、 クレアチニン上昇、 低アルブミン血症が挙げられる。 MET阻害薬の有害事象の管理としては、 原則として忍容不能なGrade2の有害事象が発症した際に休薬・減量を行っていくことである。
肺癌診療ガイドライン2024の推奨⁴⁾
1次治療として、 MET-TKI単剤療法 (テポチニブ、カプマチニブ、 グマロンチニブのいずれか) を行うよう強く推奨されている。 いずれも推奨とエビデンスの強さは横並びの1Cである。 なお、 グマロンチニブはGLORY試験の結果と承認に基づく2024年版からの記載である。
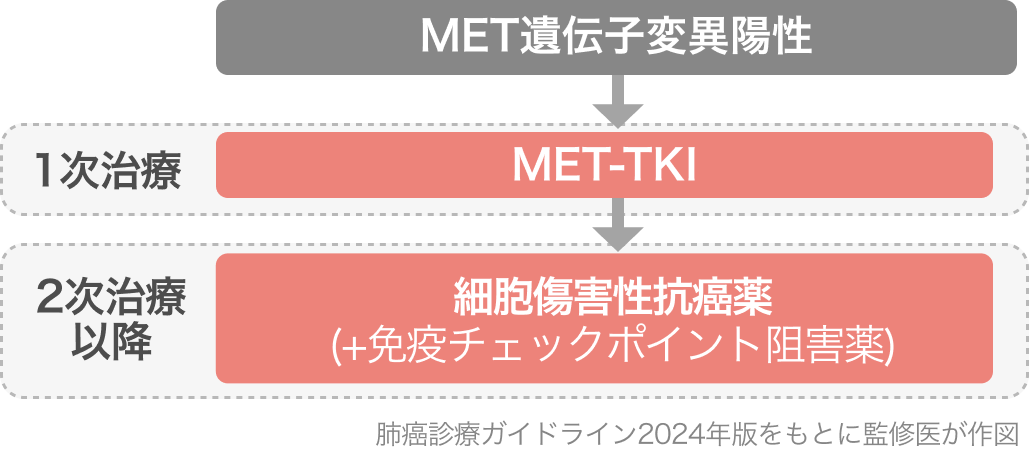
- Tepotinib (テプミトコ®︎)
- Capmatinib (タブレクタ®︎)
- Gumarontinib (ハイイータン®)
出典
1) 海和製薬株式会社. ハイイータン®電子添文 (2024年9月改訂 第2版) [最終閲覧 : 2025/04/10]
2) 海和製薬株式会社. ハイイータン®適正使用ガイド (2024年6月作成) [最終閲覧 : 2025/04/10]
*大鵬薬品工業株式会社の外部サイトへ遷移します
4) 日本肺癌学会. 肺癌診療ガイドライン-悪性胸膜中皮腫・ 胸腺腫瘍含む-2024年版
最終更新日 : 2025年4月10日
監修医師 : HOKUTO編集部監修医師
Gumarontinib
2024年6月24日に「METex14スキッピング変異陽性の切除不能な進行・再発の非小細胞肺癌 (METex14 : MET遺伝子エクソン14)」 を対象として承認。 2024年10月11日に発売。
本コンテンツは特定の治療法を推奨するものではありません。 個々の患者の病態や、 実際の薬剤情報やガイドラインを確認の上、 利用者の判断と責任でご利用ください。
薬剤情報
MET阻害薬 グマロンチニブ水和物
*大鵬薬品工業株式会社の外部サイトへ遷移します
投与スケジュール
【1コース】連日内服投与
【催吐性】 調査中
【FN発症】調査中

1回300mgを1日1回空腹時に経口投与する
ハイイータン®電子添文 (2024年9月改訂 第2版)¹⁾より作図
KeyData|臨床試験結果
📊GLORY試験²⁾
MET遺伝子エクソン14スキッピング変異陽性の局所進行または転移を有するNSCLC患者84例 (日本人患者10例を含む)、 うち1次治療 46例、 既治療 38例に対するグマロンチニブ300mg 1日1回投与の有効性と安全性を検証
【有効性】全体集団
- ORR 66%
1次治療例 71%、 既治療例 60%
- mPFS 8.5ヵ月
1次治療例 11.7ヵ月、 既治療例 7.6ヵ月
- mOS 17.3ヵ月
1次治療例 未到達、 既治療例 16.2ヵ月
【安全性】全体集団
主な有害事象 (カッコ内 Grade3~4)
- 浮腫 79.8% (21.4%)
- 低アルブミン血症 38.1% (0%)
- 頭痛 32.1% (2.4%)
- 食欲減少 32.1% (1.2%)
- 悪心 28.6% (1.2%)
- 血中ビリルビン上昇 27.4% (0%)
- ALT上昇 26.2% (1.2%)
- 嘔吐 23.8% (1.2%)
- AST上昇 21.4% (1.2%)
- 高血糖 17.9% (0%)
- 倦怠感 16.7% (3.6%)
- 貧血 16.7% (3.6%)
- 低カリウム血症 15.5% (3.6%)
- 白血球数減少 15.5% (1.2%)
- 好中球数減少 14.3% (4.8%)
- 低Na血症 14.3% (3.6%)
- 血小板数減少 14.3% (0%)
- 高尿酸血症 14.3% (0%)
- 便秘 13.1% (0%)
- 血清Cre上昇 13.1% (0%)
- 低Ca血症 11.9% (0%)
- 発疹 11.9% (2.4%)
- 手足の痛み 11.9% (0%)
- タンパク尿 10.7% (0%)
- 心電図QT延長 9.5% (3.6%)
- 背部痛 9.5% (2.4%)
- 胸水 9.5% (3.6%)
- 体重減少 8.3% (1.2%)
- ALP上昇 8.3% (1.2%)
- 不快 8.3% (1.2%)
- 呼吸困難 6.0% (1.2%)
EClinicalMedicine. 2023 Apr 6:59:101952²⁾より引用
各プロトコル
投与開始基準
GLORY試験²⁾のプロトコル
MET遺伝子エクソン14スキッピング変異陽性の局所進行または転移を有するNSCLC患者

EClinicalMedicine. 2023 Apr 6:59:101952²⁾より作図
減量・休薬・休薬基準

ハイイータン®電子添文 (2024年9月改訂 第2版)¹⁾より作図
初回基準量と減量レベル

ハイイータン®電子添文 (2024年9月改訂 第2版)¹⁾より作図
特徴と注意点
MET阻害薬3剤の比較
臨床試験成績から直接比較は難しいものの、 各薬剤の治療成績はほぼ同等と考えられている。
- Tepotinib (テプミトコ®︎ VISION試験)
- Capmatinib (タブレクタ®︎ GEKMETRY試験)
- Gumarontinib (ハイイータン® GLORY試験)

各臨床試験結果をもとにHOKUTO編集部で作表
コンパニオン診断薬
各MET阻害剤で適応となるCDxは異なる。

最新情報は日本肺癌学会の各種手引きや編集部まとめコンテンツを参照ください。
肺癌遺伝子パネル検査・コンパニオン診断薬一覧ページへ遷移
MET阻害薬の副作用マネジメント
MET阻害薬の特徴的な副作用としては、 末梢性浮腫、 肝機能障害、 消化器毒性 (嘔気、 嘔吐)、 クレアチニン上昇、 低アルブミン血症が挙げられる。 MET阻害薬の有害事象の管理としては、 原則として忍容不能なGrade2の有害事象が発症した際に休薬・減量を行っていくことである。
肺癌診療ガイドライン2024の推奨⁴⁾
1次治療として、 MET-TKI単剤療法 (テポチニブ、カプマチニブ、 グマロンチニブのいずれか) を行うよう強く推奨されている。 いずれも推奨とエビデンスの強さは横並びの1Cである。 なお、 グマロンチニブはGLORY試験の結果と承認に基づく2024年版からの記載である。

- Tepotinib (テプミトコ®︎)
- Capmatinib (タブレクタ®︎)
- Gumarontinib (ハイイータン®)
出典
1) 海和製薬株式会社. ハイイータン®電子添文 (2024年9月改訂 第2版) [最終閲覧 : 2025/04/10]
2) 海和製薬株式会社. ハイイータン®適正使用ガイド (2024年6月作成) [最終閲覧 : 2025/04/10]
*大鵬薬品工業株式会社の外部サイトへ遷移します
4) 日本肺癌学会. 肺癌診療ガイドライン-悪性胸膜中皮腫・ 胸腺腫瘍含む-2024年版
最終更新日 : 2025年4月10日
監修医師 : HOKUTO編集部監修医師
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
がん薬物療法における治療計画をまとめたものです。
主要論文や適正使用ガイドをもとにした用量調整プロトコール、 有害事象対応をご紹介します。
なお、 本ツールは医師向けの教育用資料であり、 実臨床での使用は想定しておりません。 最新の添付文書やガイドラインを必ずご確認下さい。
また、 一般の方への情報提供ではないことを予めご了承ください。