2021年9月27日、 尿路上皮がん3次治療以降に使用する新規ADC (Antibody Drug Conjugate : 抗体薬物複合体) として承認
本コンテンツは特定の治療法を推奨するものではありません。 個々の患者の病態や、 実際の薬剤情報やガイドラインを確認の上、 利用者の判断と責任でご利用ください。
薬剤情報
*アステラス製薬株式会社の外部サイトへ遷移します
投与スケジュール
電子添文¹⁾の用法および用量
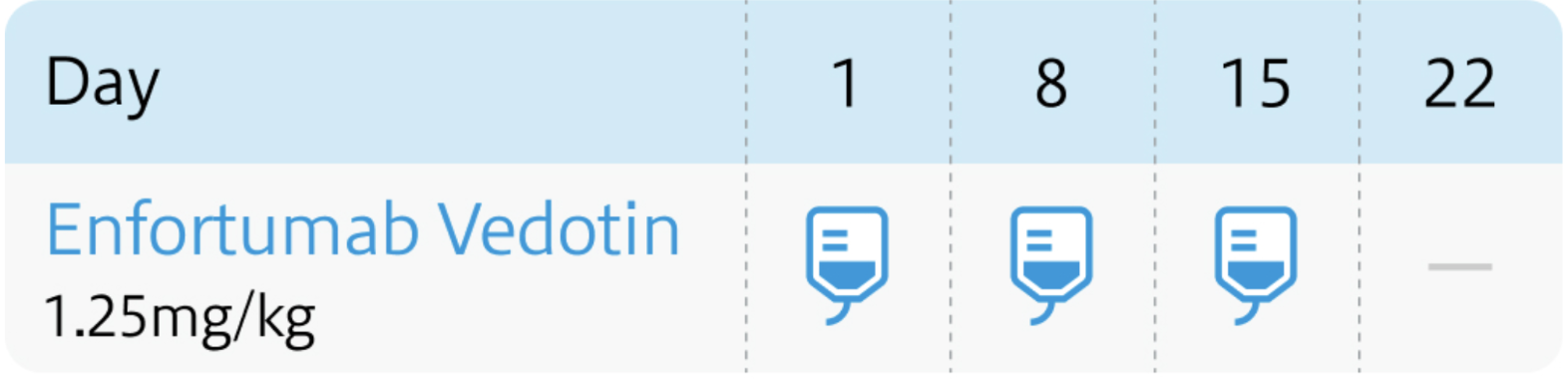
1回1.25mg/kgを30分以上かけて点滴静注し、 週1回投与を3週連続し、 4週目は休薬。 これを1サイクルとして投与を繰り返す。 ただし、 1回量として125mgを超えないこと。
パドセブ®電子添文 (2024年9月改訂 第8版)¹⁾より作図
初回基準量と減量レベル

パドセブ®電子添文 (2024年9月改訂 第8版)¹⁾より作図
KeyData|臨床試験結果
EV-301試験⁴⁾
白金製剤を含む化学療法およびPD-1またはPD-L1阻害剤による治療歴のある局所進行性または転移性尿路上皮癌患者において、 抗体薬物複合体 (ADC) エンホルツマブ ベドチン投与の効果を、 化学療法群を対照に検証した第Ⅲ相比較試験
有効性|エンホルツマブ ベドチン群
- ORR:40.6% (95%CI 34.9-46.5%)
- mPFS:5.55ヵ月 (95%CI 5.32-5.82)
- mOS: 12.88ヵ月 (95%CI 10.58-15.21)
- OS率 1年時:51.5% (95%CI 44.6-58.0)
主な有害事象 (カッコ内はGrade3~4)
- 貧血 11.5% (2.7%)
- 好中球数減少 10.1% (6.1%)
- 好中球減少症 6.8% (4.7%)
- 白血球数減少 5.4% (1.4%)
- 発熱性好中球減少症 0.7% (0.7%)
- 脱毛症 45.3% (0%)
- 末梢性感覚ニューロパチー 33.8% (3.0%)
- 倦怠感 31.1% (6.4%)
- 食欲低下 30.7% (3.0%)
- 下痢 24.3% (3.4%)
- 悪心 22.6% (1.0%)
N Engl J Med. 2021 Mar 25;384(12):1125-1135³⁾より引用
特徴と注意点
作用機序
エンホルツマブ ベドチンは癌細胞表面に発現するNectin-4を標的とする抗体薬物複合体である。 Nectin-4に結合後、 MMAEが細胞内で遊離し微小管阻害作用により効果を発揮する。
注意すべき有害事象
重症皮膚障害、 高血糖、 末梢性ニューロパチー、 眼障害など³⁾
監修 : 国立がん研究センター東病院 腫瘍内科 近藤 千紘先生
各プロトコル
投与開始基準
EV-301試験⁴⁾のプロトコル
尿路上皮癌 (膀胱、 腎盂、 尿管、 尿道の癌)の組織学的または細胞学的診断がある18歳以上の患者で以下を満たすもの

N Engl J Med. 2021 Mar 25;384(12):1125-1135⁴⁾より作図
減量・休薬・中止基準
電子添文¹⁾の基準
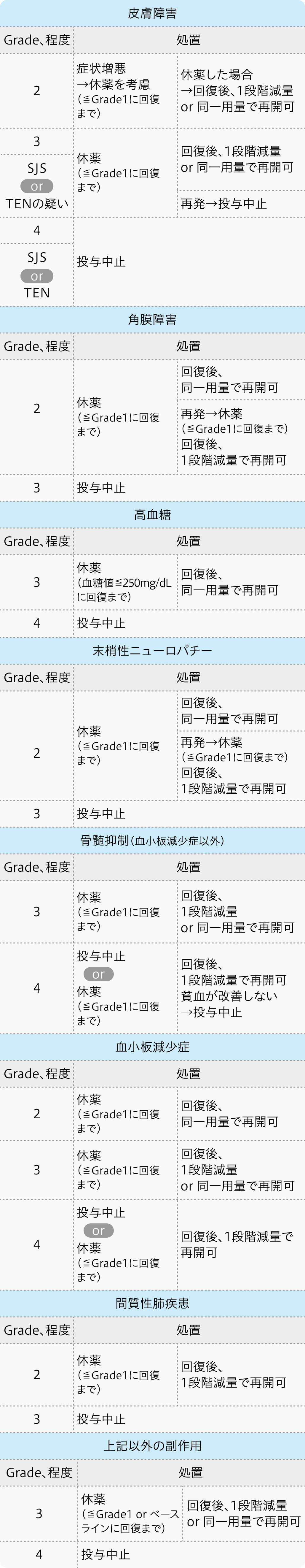
パドセブ®電子添文 (2024年9月改訂 第8版)¹⁾より作図
初回基準量と減量レベル

パドセブ®電子添文 (2024年9月改訂 第8版)¹⁾より作図
出典
1) アステラス製薬株式会社. パドセブ®電子添文 (2026年2月改訂 第10版)
2) アステラス製薬株式会社. パドセブ®適正使用ガイド (2024年9月作成)
3) アステラス製薬株式会社. パドセブ®副作用マネジメントガイド (2025年8月作成)
最終更新日 : 2026年2月2日
監修医師 : 国立がん研究センター東病院 腫瘍内科 近藤 千紘先生
EV (Enfortumab Vedotin)
2021年9月27日、 尿路上皮がん3次治療以降に使用する新規ADC (Antibody Drug Conjugate : 抗体薬物複合体) として承認
本コンテンツは特定の治療法を推奨するものではありません。 個々の患者の病態や、 実際の薬剤情報やガイドラインを確認の上、 利用者の判断と責任でご利用ください。
薬剤情報
*アステラス製薬株式会社の外部サイトへ遷移します
投与スケジュール
電子添文¹⁾の用法および用量

1回1.25mg/kgを30分以上かけて点滴静注し、 週1回投与を3週連続し、 4週目は休薬。 これを1サイクルとして投与を繰り返す。 ただし、 1回量として125mgを超えないこと。
パドセブ®電子添文 (2024年9月改訂 第8版)¹⁾より作図
初回基準量と減量レベル

パドセブ®電子添文 (2024年9月改訂 第8版)¹⁾より作図
KeyData|臨床試験結果
EV-301試験⁴⁾
白金製剤を含む化学療法およびPD-1またはPD-L1阻害剤による治療歴のある局所進行性または転移性尿路上皮癌患者において、 抗体薬物複合体 (ADC) エンホルツマブ ベドチン投与の効果を、 化学療法群を対照に検証した第Ⅲ相比較試験
有効性|エンホルツマブ ベドチン群
- ORR:40.6% (95%CI 34.9-46.5%)
- mPFS:5.55ヵ月 (95%CI 5.32-5.82)
- mOS: 12.88ヵ月 (95%CI 10.58-15.21)
- OS率 1年時:51.5% (95%CI 44.6-58.0)
主な有害事象 (カッコ内はGrade3~4)
- 貧血 11.5% (2.7%)
- 好中球数減少 10.1% (6.1%)
- 好中球減少症 6.8% (4.7%)
- 白血球数減少 5.4% (1.4%)
- 発熱性好中球減少症 0.7% (0.7%)
- 脱毛症 45.3% (0%)
- 末梢性感覚ニューロパチー 33.8% (3.0%)
- 倦怠感 31.1% (6.4%)
- 食欲低下 30.7% (3.0%)
- 下痢 24.3% (3.4%)
- 悪心 22.6% (1.0%)
N Engl J Med. 2021 Mar 25;384(12):1125-1135³⁾より引用
特徴と注意点
作用機序
エンホルツマブ ベドチンは癌細胞表面に発現するNectin-4を標的とする抗体薬物複合体である。 Nectin-4に結合後、 MMAEが細胞内で遊離し微小管阻害作用により効果を発揮する。
注意すべき有害事象
重症皮膚障害、 高血糖、 末梢性ニューロパチー、 眼障害など³⁾
監修 : 国立がん研究センター東病院 腫瘍内科 近藤 千紘先生
各プロトコル
投与開始基準
EV-301試験⁴⁾のプロトコル
尿路上皮癌 (膀胱、 腎盂、 尿管、 尿道の癌)の組織学的または細胞学的診断がある18歳以上の患者で以下を満たすもの

N Engl J Med. 2021 Mar 25;384(12):1125-1135⁴⁾より作図
減量・休薬・中止基準
電子添文¹⁾の基準

パドセブ®電子添文 (2024年9月改訂 第8版)¹⁾より作図
初回基準量と減量レベル

パドセブ®電子添文 (2024年9月改訂 第8版)¹⁾より作図
出典
1) アステラス製薬株式会社. パドセブ®電子添文 (2026年2月改訂 第10版)
2) アステラス製薬株式会社. パドセブ®適正使用ガイド (2024年9月作成)
3) アステラス製薬株式会社. パドセブ®副作用マネジメントガイド (2025年8月作成)
最終更新日 : 2026年2月2日
監修医師 : 国立がん研究センター東病院 腫瘍内科 近藤 千紘先生
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
がん薬物療法における治療計画をまとめたものです。
主要論文や適正使用ガイドをもとにした用量調整プロトコール、 有害事象対応をご紹介します。
なお、 本ツールは医師向けの教育用資料であり、 実臨床での使用は想定しておりません。 最新の添付文書やガイドラインを必ずご確認下さい。
また、 一般の方への情報提供ではないことを予めご了承ください。