VEN:ベネトクラクス(ベネクレクスタ®)
| 投与量 | コース | 投与日 |
|---|---|---|
| 100mg/body 経口 | 1 | Day 1 |
| 200mg/body 経口 | 1 | Day 2 |
| 400mg/body 経口 | 1 | Day 3~28 |
| 400mg/body 経口 | 2~ | Day 1~28 |
AZA:アザシチジン(ビダーザ®)
| 投与量 | コース | 投与日 |
|---|---|---|
| 75mg/m² 皮下注or点滴静注 | 1~ | Day 1~7 |
その他
| 1コースは28日間. |
本コンテンツは特定の治療法を推奨するものではありません。 個々の患者の病態や、 実際の薬剤情報やガイドラインを確認の上、 利用者の判断と責任でご利用ください。
薬剤情報
ベネクレクスタ® (ベネトクラクス)
*アッヴィ合同会社の外部サイトへ遷移します
ビダーザ® (アザシチジン)
添付文書³⁾
*日本新薬株式会社の外部サイトへ遷移します
投与スケジュール
【1コース】28日間
【催吐性】VEN : 軽度、 AZA : 中等度
【FN発症】高リスク*
*VIALE-A試験のFN発生率42%を基に編集部が分類
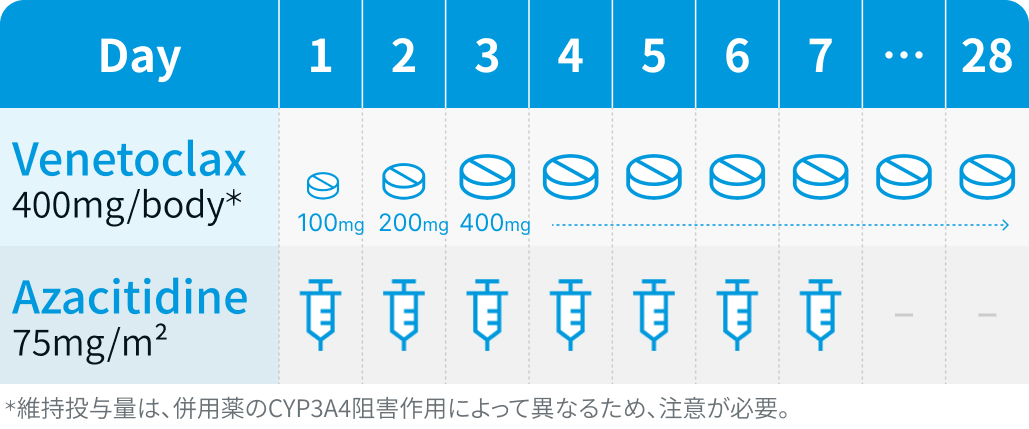
▼1コース目 (Day1~3が用量漸増期、 Day4~維持投与期)
▼2コース目以降
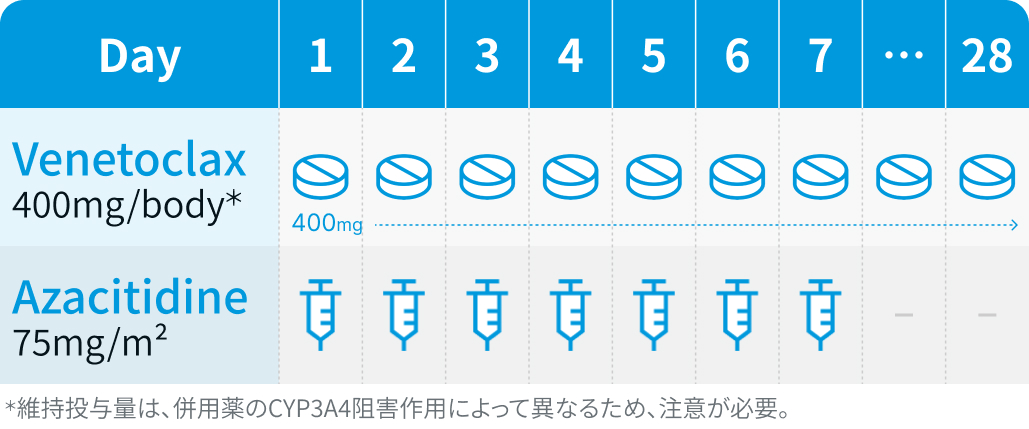
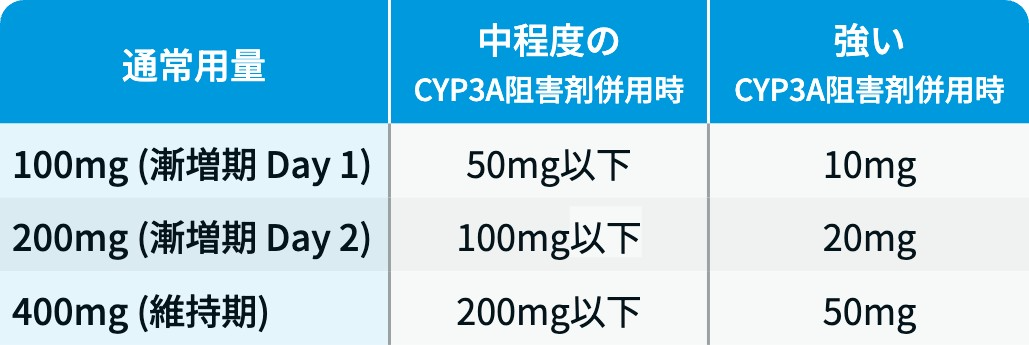
ベネトクラクス (VEN) : 用量漸増期は、 Day 1に100mg、 Day 2に200mg、 Day 3に400mgをそれぞれ1日1回、 食後に経口投与。 その後の維持投与期は、 400mgを1日1回、 食後に経口投与。 なお、 CYP3A4阻害薬併用時は、 下記を参考に維持投与量を減量。
アザシチジン (AZA) : 75mg/m²を4週間ごとにDay 1–7に皮下注射又は点滴静注。 原則として皮下投与を行い、 出血傾向などにより皮下投与が困難な場合は点滴静注を行う。
Key Data|臨床試験結果
📊 VIALE-A試験
N Engl J Med. 2020;383(7):617-29.
標準的寛解導入療法に適さない新規診断AML患者を対象とした第III相無作為化比較試験。 アザシチジン+ベネトクラクス群286例とアザシチジン+プラセボ群145例を2:1で割り付け、 主要評価項目はOSとした。
【有効性】VEN+AZA (vs プラセボ+AZA)
- OS中央値 14.7ヵ月 (vs 9.6ヵ月)
- HR 0.66 (95%CI 0.52–0.85、 p<0.001)
- CR 36.7% (vs 17.9%、 p<0.001)
- CR+CRi 66.4% (vs 28.3%、 p<0.001)
【安全性】主な有害事象 : 全Grade (Grade≧3)
- 血小板減少症 46% (45%)
- 好中球減少症 42% (42%)
- 発熱性好中球減少症 42% (42%)
- 貧血 28% (26%)
- 白血球減少症 21% (21%)
- 悪心 44% (2%)
- 便秘 43% (1%)
- 下痢 41% (5%)
- 嘔吐 30% (2%)
- 低カリウム血症 29% (11%)
- 末梢性浮腫 24% (<1%)
- 発熱 23% (2%)
- 食欲不振 25% (4%)
- 倦怠感 21% (3%)
- 感染症 84% (64%)
- 肺炎 23% (20%)
- 心房細動 5% (4%)
- 敗血症 6% (6%)
各プロトコル
適格基準
- 60歳以上
- 標準寛解導入療法に不適格
- 75歳以上
- 60–74歳で以下のいずれかを有する : ECOG PS 2–3、 うっ血性心不全 (治療要) またはEF≦50%または慢性安定狭心症、 DLCO≦65%またはFEV1≦65%、 CrCl 30–45 mL/min、 中等度肝機能障害
- ECOG PS : ≧75歳は0–2、 60–74歳は0–3
- CrCl≧30 mL/min
- AST/ALT≦3×ULN
- 総ビリルビン≦1.5×ULN
75歳未満は≦3.0×ULNも可
腎障害患者に対する用量調整
VEN : 腎機能低下患者 (CrCl<80mL/min) ではTLSリスクが高いため、 投与開始時は予防策およびモニタリングをより厳重に行う。 軽度~中等度の腎機能障害患者 (CrCl≧30mL/min) では用量調節は推奨されないが、 重度腎機能障害患者 (CrCl<30mL/min) または透析患者に対する推奨用量は確立していない。
Venclexta® [venetoclax] Prescribing Information, FDA, 2022. Section 8.6 / 12.3
AZA : 腎障害患者ではAZAの曝露量が増加するため注意する。 重度腎機能障害患者では、 75mg/m²/日の皮下投与時に単回投与後で約70%、 反復投与後で約41%曝露量の増加が認められたが、 有害事象の増加との相関は認められなかった。 なお、 このときの曝露量は、 腎機能正常患者に100mg/m²を投与した場合と同程度であった。
Azacitidine [Vidaza®] Prescribing Information, FDA, 2022. Section 8.6 / 12.3
有害事象発現時の減量・休薬・中止基準
VEN : 血液毒性
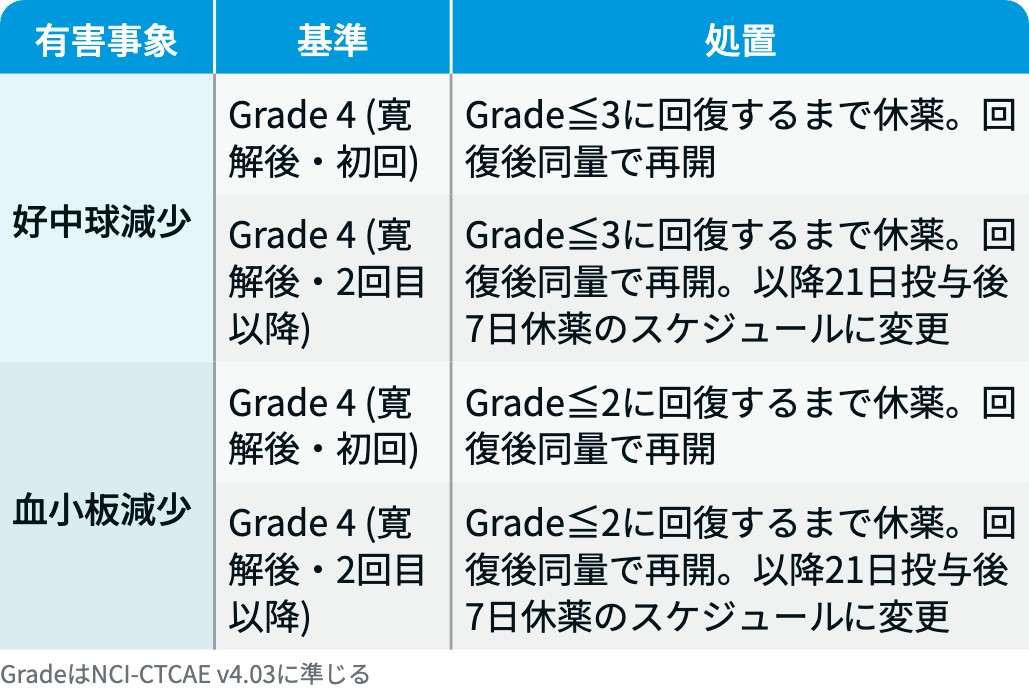
ベネクレクスタ®電子添文情報¹⁾を基に編集部作成
AZA : 血液毒性

AZA : 非血液毒性

ビダーザ®電子添文情報³⁾を基に編集部作成
VIALE-A試験⁴⁾のプロトコル (補足情報)
VEN :
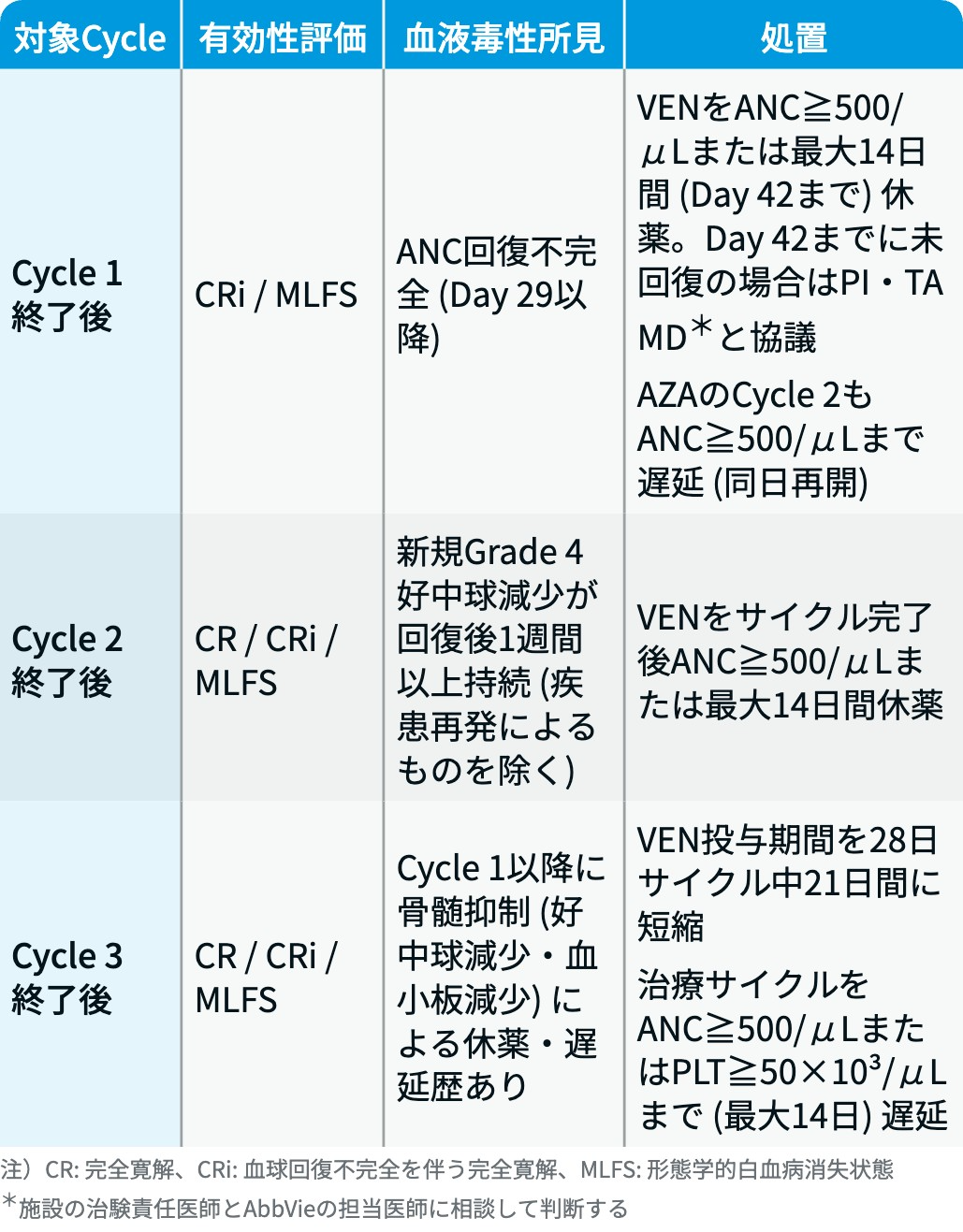
AZA :

レジメンの特徴と注意点
作用機序の特徴
VENはBcl-2に結合し、 抗アポトーシス作用を阻害することによりアポトーシスを誘導する。 AZAはDNAおよびRNAに取り込まれることで、 主にタンパク質合成を阻害し、 殺細胞作用を示す。 なお、 MDSでは、 がん抑制遺伝子プロモーター領域のDNA高メチル化および当該がん抑制遺伝子の発現抑制が報告されており、 DNAに取り込まれたアザシチジンは、 DNAメチル化を阻害することで細胞増殖抑制作用を示す可能性も報告されている。
レジメン適用時の注意事項
▼VEN
骨髄抑制 : 投与開始前および投与中は定期的に血液検査を行う。
腫瘍崩壊症候群 : 投与開始前に白血球数を2.5万/μL未満に調整し、 血液検査 (K・Ca・P・尿酸・Cr) を実施して電解質を補正する。 高尿酸血症治療薬を予防投与し、 用量漸増期は投与前・6–8時間後・漸増最終日±6–24時間後にモニタリングを行い、 維持投与期以降も定期的に血液検査を継続する。
▼AZA
血小板減少・好中球減少・貧血 : 投与前後に定期的な血液検査を行い観察する。
腎障害 : 定期的に血清重炭酸塩および腎機能の推移を確認する。
間質性肺疾患 : 咳嗽・呼吸困難・発熱等の臨床症状を十分に観察する。
腫瘍崩壊症候群 : 血清中電解質濃度および腎機能検査を行い患者の状態を十分に観察する。
RMP【重要な特定されたリスク】
ベネクレクスタ®RMP : 医薬品リスク管理計画書
- 腫瘍崩壊症候群
- 骨髄抑制
- 感染症
- CYP3A阻害剤との薬物相互作用
出典
1) アッヴィ合同会社. ベネクレクスタ®電子添文. 2025年11月改訂 第10版.
2) アッヴィ合同会社. ベネクレクスタ®適正使用ガイド. 2025年11月作成.
3) 日本新薬株式会社. ビダーザ®電子添文. 2025年4月改訂 第3版.
4) N Engl J Med. 2020;383(7):617-29.
最終更新 : 2026年3月12日
執筆 : HOKUTO編集部 がん専門・指導薬剤師
監修医師 : 東海大学血液腫瘍内科 扇屋大輔
VEN+AZA
VEN:ベネトクラクス(ベネクレクスタ®)
| 投与量 | コース | 投与日 |
|---|---|---|
| 100mg/body 経口 | 1 | Day 1 |
| 200mg/body 経口 | 1 | Day 2 |
| 400mg/body 経口 | 1 | Day 3~28 |
| 400mg/body 経口 | 2~ | Day 1~28 |
AZA:アザシチジン(ビダーザ®)
| 投与量 | コース | 投与日 |
|---|---|---|
| 75mg/m² 皮下注or点滴静注 | 1~ | Day 1~7 |
その他
| 1コースは28日間. |
概要
本コンテンツは特定の治療法を推奨するものではありません。 個々の患者の病態や、 実際の薬剤情報やガイドラインを確認の上、 利用者の判断と責任でご利用ください。
薬剤情報
ベネクレクスタ® (ベネトクラクス)
*アッヴィ合同会社の外部サイトへ遷移します
ビダーザ® (アザシチジン)
添付文書³⁾
*日本新薬株式会社の外部サイトへ遷移します
投与スケジュール
【1コース】28日間
【催吐性】VEN : 軽度、 AZA : 中等度
【FN発症】高リスク*
*VIALE-A試験のFN発生率42%を基に編集部が分類
▼1コース目 (Day1~3が用量漸増期、 Day4~維持投与期)

▼2コース目以降

ベネトクラクス (VEN) : 用量漸増期は、 Day 1に100mg、 Day 2に200mg、 Day 3に400mgをそれぞれ1日1回、 食後に経口投与。 その後の維持投与期は、 400mgを1日1回、 食後に経口投与。 なお、 CYP3A4阻害薬併用時は、 下記を参考に維持投与量を減量。

アザシチジン (AZA) : 75mg/m²を4週間ごとにDay 1–7に皮下注射又は点滴静注。 原則として皮下投与を行い、 出血傾向などにより皮下投与が困難な場合は点滴静注を行う。
Key Data|臨床試験結果
📊 VIALE-A試験
N Engl J Med. 2020;383(7):617-29.
標準的寛解導入療法に適さない新規診断AML患者を対象とした第III相無作為化比較試験。 アザシチジン+ベネトクラクス群286例とアザシチジン+プラセボ群145例を2:1で割り付け、 主要評価項目はOSとした。
【有効性】VEN+AZA (vs プラセボ+AZA)
- OS中央値 14.7ヵ月 (vs 9.6ヵ月)
- HR 0.66 (95%CI 0.52–0.85、 p<0.001)
- CR 36.7% (vs 17.9%、 p<0.001)
- CR+CRi 66.4% (vs 28.3%、 p<0.001)
【安全性】主な有害事象 : 全Grade (Grade≧3)
- 血小板減少症 46% (45%)
- 好中球減少症 42% (42%)
- 発熱性好中球減少症 42% (42%)
- 貧血 28% (26%)
- 白血球減少症 21% (21%)
- 悪心 44% (2%)
- 便秘 43% (1%)
- 下痢 41% (5%)
- 嘔吐 30% (2%)
- 低カリウム血症 29% (11%)
- 末梢性浮腫 24% (<1%)
- 発熱 23% (2%)
- 食欲不振 25% (4%)
- 倦怠感 21% (3%)
- 感染症 84% (64%)
- 肺炎 23% (20%)
- 心房細動 5% (4%)
- 敗血症 6% (6%)
各プロトコル
適格基準
- 60歳以上
- 標準寛解導入療法に不適格
- 75歳以上
- 60–74歳で以下のいずれかを有する : ECOG PS 2–3、 うっ血性心不全 (治療要) またはEF≦50%または慢性安定狭心症、 DLCO≦65%またはFEV1≦65%、 CrCl 30–45 mL/min、 中等度肝機能障害
- ECOG PS : ≧75歳は0–2、 60–74歳は0–3
- CrCl≧30 mL/min
- AST/ALT≦3×ULN
- 総ビリルビン≦1.5×ULN
75歳未満は≦3.0×ULNも可
腎障害患者に対する用量調整
VEN : 腎機能低下患者 (CrCl<80mL/min) ではTLSリスクが高いため、 投与開始時は予防策およびモニタリングをより厳重に行う。 軽度~中等度の腎機能障害患者 (CrCl≧30mL/min) では用量調節は推奨されないが、 重度腎機能障害患者 (CrCl<30mL/min) または透析患者に対する推奨用量は確立していない。
Venclexta® [venetoclax] Prescribing Information, FDA, 2022. Section 8.6 / 12.3
AZA : 腎障害患者ではAZAの曝露量が増加するため注意する。 重度腎機能障害患者では、 75mg/m²/日の皮下投与時に単回投与後で約70%、 反復投与後で約41%曝露量の増加が認められたが、 有害事象の増加との相関は認められなかった。 なお、 このときの曝露量は、 腎機能正常患者に100mg/m²を投与した場合と同程度であった。
Azacitidine [Vidaza®] Prescribing Information, FDA, 2022. Section 8.6 / 12.3
有害事象発現時の減量・休薬・中止基準
VEN : 血液毒性

ベネクレクスタ®電子添文情報¹⁾を基に編集部作成
AZA : 血液毒性

AZA : 非血液毒性

ビダーザ®電子添文情報³⁾を基に編集部作成
VIALE-A試験⁴⁾のプロトコル (補足情報)
VEN :

AZA :

レジメンの特徴と注意点
作用機序の特徴
VENはBcl-2に結合し、 抗アポトーシス作用を阻害することによりアポトーシスを誘導する。 AZAはDNAおよびRNAに取り込まれることで、 主にタンパク質合成を阻害し、 殺細胞作用を示す。 なお、 MDSでは、 がん抑制遺伝子プロモーター領域のDNA高メチル化および当該がん抑制遺伝子の発現抑制が報告されており、 DNAに取り込まれたアザシチジンは、 DNAメチル化を阻害することで細胞増殖抑制作用を示す可能性も報告されている。
レジメン適用時の注意事項
▼VEN
骨髄抑制 : 投与開始前および投与中は定期的に血液検査を行う。
腫瘍崩壊症候群 : 投与開始前に白血球数を2.5万/μL未満に調整し、 血液検査 (K・Ca・P・尿酸・Cr) を実施して電解質を補正する。 高尿酸血症治療薬を予防投与し、 用量漸増期は投与前・6–8時間後・漸増最終日±6–24時間後にモニタリングを行い、 維持投与期以降も定期的に血液検査を継続する。
▼AZA
血小板減少・好中球減少・貧血 : 投与前後に定期的な血液検査を行い観察する。
腎障害 : 定期的に血清重炭酸塩および腎機能の推移を確認する。
間質性肺疾患 : 咳嗽・呼吸困難・発熱等の臨床症状を十分に観察する。
腫瘍崩壊症候群 : 血清中電解質濃度および腎機能検査を行い患者の状態を十分に観察する。
RMP【重要な特定されたリスク】
ベネクレクスタ®RMP : 医薬品リスク管理計画書
- 腫瘍崩壊症候群
- 骨髄抑制
- 感染症
- CYP3A阻害剤との薬物相互作用
出典
1) アッヴィ合同会社. ベネクレクスタ®電子添文. 2025年11月改訂 第10版.
2) アッヴィ合同会社. ベネクレクスタ®適正使用ガイド. 2025年11月作成.
3) 日本新薬株式会社. ビダーザ®電子添文. 2025年4月改訂 第3版.
4) N Engl J Med. 2020;383(7):617-29.
最終更新 : 2026年3月12日
執筆 : HOKUTO編集部 がん専門・指導薬剤師
監修医師 : 東海大学血液腫瘍内科 扇屋大輔
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
がん薬物療法における治療計画をまとめたものです。
主要論文や適正使用ガイドをもとにした用量調整プロトコール、 有害事象対応をご紹介します。
なお、 本ツールは医師向けの教育用資料であり、 実臨床での使用は想定しておりません。 最新の添付文書やガイドラインを必ずご確認下さい。
また、 一般の方への情報提供ではないことを予めご了承ください。

