治療スケジュール
概要
監修医師
本コンテンツは特定の治療法を推奨するものではありません。 個々の患者の病態や、 実際の薬剤情報やガイドラインを確認の上、 利用者の判断と責任でご利用ください。
薬剤情報
PARP阻害薬 オラパリブ *MSD株式会社の外部サイトへ遷移
用法用量
投与開始基準
POLO試験:治療投与前28日以内に以下の基準を満たすこと

減量・休薬・中止基準
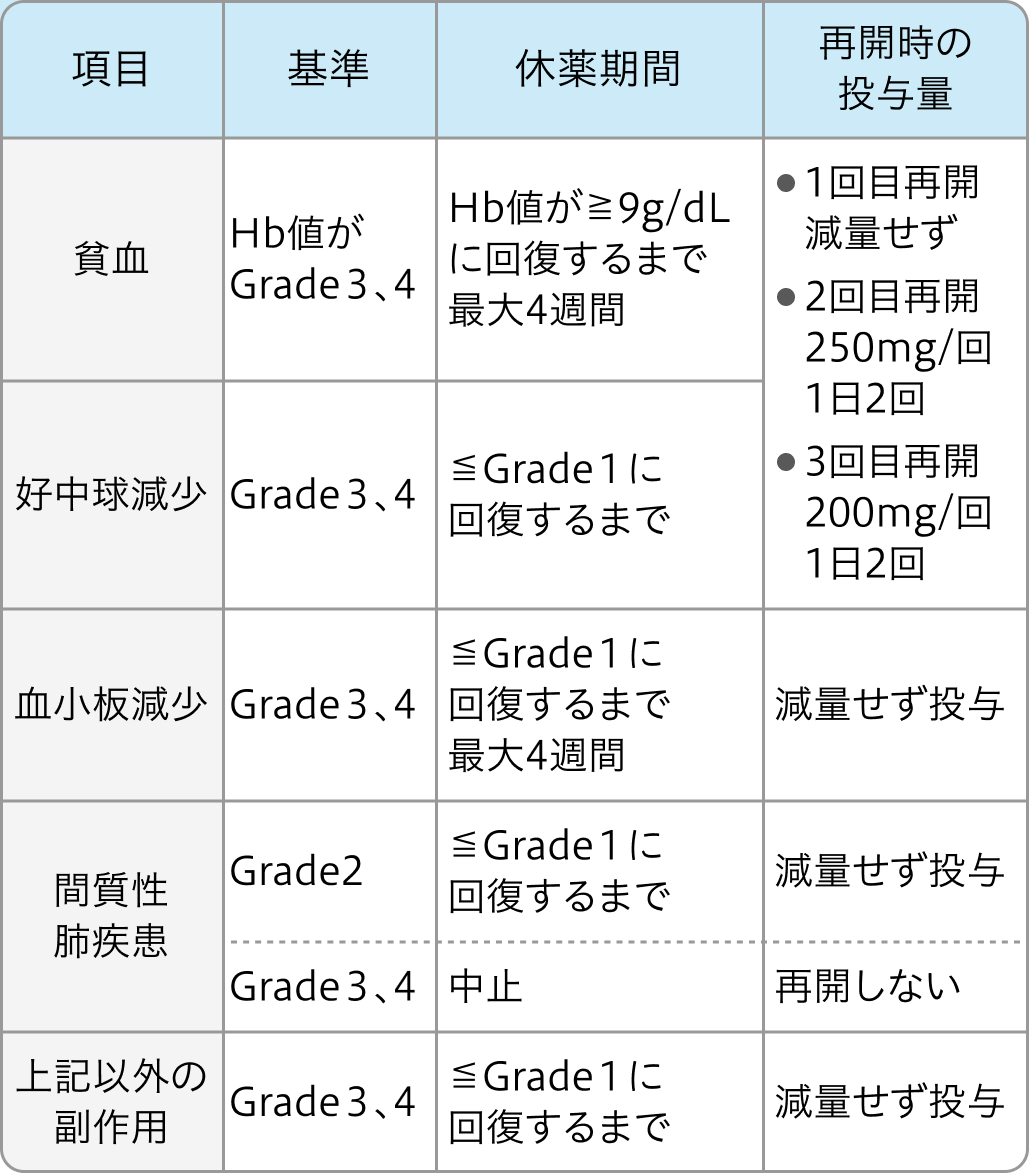
主な有害事象
POLO試験³⁾
国際的な試験の有害事象データを一部引用 (カッコ内はGrade3~4)
主な有害事象
- 倦怠感又は無力感 60% (5%)
- 嘔気 45% (0%)
- 腹痛 29% (2%)
- 下痢 29% (0%)
- 貧血 27% (11%)
- 食欲不振 25% (0%)
- 便秘 23% (0%)
- 嘔吐 20% (1%)
上手に使うためのワンポイント
- オラパリブ単剤療法は生殖細胞系列BRCA1/2遺伝子病的バリアントを有する切除不能膵癌に対するプラチナ系薬剤をベースとした化学療法後 (mFOLFIRINOX療法など) の維持療法としての標準治療である。
- 生殖細胞系列BRCA1/2遺伝子病的バリアントは膵癌全体の約5%に認められ、 投与開始にあたってはコンパニオン診断薬 (BRCAnalysis診断システム) や遺伝子パネル検査での同バリアントの確認が必要である。
- 維持療法としての実施にあたっては、 前治療としてプラチナ系薬剤をベースとした化学療法を病勢進行なく16週以上施行してることが条件である。
執筆医:慶應義塾大学医学部 腫瘍センター ゲノム医療ユニット統括マネージャー・特任講師 林秀幸先生
特徴と注意点
- 食事の影響は受けないので食後・空腹時のいずれでも内服可能であり、 1日2回12時間ごとを目安として内服する。
- 主に肝で代謝されることから肝機能障害を有する患者では血中濃度が上昇するおそれがあり、 注意が必要である。
- 軽度腎機能障害患者に投与する際は用量調整は不要だが、 中等度腎機能障害のある患者 (Ccr: 31~50mL/min) への投与や、 中程度 または強いCYP3A阻害薬を併用する場合は減量を考慮することが推奨されている。
- 妊娠する可能性のある患者およびパートナー が妊娠する可能性がある患者には、 服用中および服用終了後1ヵ月間は適切な避妊を行うよう指導する。
- 主な副作用として 骨髄抑制 (特に貧血) 、 疲労、 悪心・嘔吐があげられ、 骨髄抑制に関しては発現Gradeに応じて適宜休薬・減量を実施する。
執筆医:慶應義塾大学医学部 腫瘍センター ゲノム医療ユニット統括マネージャー・特任講師 林秀幸先生
関連する臨床試験|POLO試験³⁾
BRCA遺伝子変異を有し、 プラチナベースの化学療法中に病勢進行しなかった転移性膵腺癌患者において、 オラパリブの効果を、 プラセボを対照に検証した第Ⅲ相二重盲検ランダム化比較試験POLOの結果より、 無増悪生存期間 (PFS) における有効性が示された。
PFS中央値
- オラパリブ群:6.7ヵ月
- プラセボ群:3.7ヵ月
HR 0.49 (95%CI 0.33-0.73)、 p=0.0004
PFS率 (6ヵ月時、 12ヵ月時、 18ヵ月時、 24ヵ月時)
- オラパリブ群:53.0%、 33.7%、 27.6%、 22.1%
- プラセボ群:23.0%、 14.5%、 9.6%、 9.6%
OS中央値
- オラパリブ群:19.0ヵ月
- プラセボ群:19.2ヵ月
HR 0.83 (95%CI 0.56-1.22)、 p=0.3487
OS率 (24ヵ月時、 36ヵ月時)
- オラパリブ群:37.0%、 33.9%
- プラセボ群:27.4%、 17.8%
ORR
- オラパリブ群:23%
- プラセボ群:12%
オッズ比 2.30 (95%CI 0.89-6.76)
PFS2中央値
- オラパリブ群:16.9ヵ月
- プラセボ群:9.3ヵ月
HR 0.66 (95%CI 0.43-1.02)、 p=0.0613
PFS2率 (3年時)
- オラパリブ群:31.2%
- プラセボ群:13.1%
TFST中央値
- オラパリブ群:9.0ヵ月
- プラセボ群:5.4ヵ月
HR 0.44 (95%CI 0.30-0.66)、 p<0.0001
TSST
- オラパリブ群:14.9ヵ月
- プラセボ群:9.6ヵ月
HR 0.61 (95%CI 0.42-0.89)、 p=0.0111
TDT
- オラパリブ群:7.5ヵ月
- プラセボ群:3.8ヵ月
HR 0.43 (95%CI 0.29-0.63)、 p<0.0001
出典
- MSD株式会社. リムパーザ®電子添文 (2024年11月改訂第6版) [最終閲覧 : 2024/11/29]
- MSD株式会社. リムパーザ®適正使用ガイド 膵癌 (2023年8月作成) [最終閲覧 : 2024/11/29]
- Maintenance Olaparib for Germline BRCA-Mutated Metastatic Pancreatic Cancer. N Engl J Med. 2019 Jul 25;381(4):317-327. PMID: 31157963
最終更新日:2024年11月29日
執筆医:慶應義塾大学医学部 腫瘍センター ゲノム医療ユニット統括マネージャー・特任講師 林秀幸先生
監修医:神奈川県立がんセンター 消化器内科 上野 誠先生
Olaparib
オラパリブ (リムパーザ®)
膵癌 > 一次治療
2024年11月29日更新
オラパリブ:オラパリブ(リムパーザ®)
| 投与量 | コース | 投与日 |
|---|---|---|
| 600mg/日 分2経口 | 1~ | 連日投与 |
概要
本コンテンツは特定の治療法を推奨するものではありません。 個々の患者の病態や、 実際の薬剤情報やガイドラインを確認の上、 利用者の判断と責任でご利用ください。
薬剤情報
PARP阻害薬 オラパリブ *MSD株式会社の外部サイトへ遷移
用法用量

投与開始基準
POLO試験:治療投与前28日以内に以下の基準を満たすこと

減量・休薬・中止基準

主な有害事象
POLO試験³⁾
国際的な試験の有害事象データを一部引用 (カッコ内はGrade3~4)
主な有害事象
- 倦怠感又は無力感 60% (5%)
- 嘔気 45% (0%)
- 腹痛 29% (2%)
- 下痢 29% (0%)
- 貧血 27% (11%)
- 食欲不振 25% (0%)
- 便秘 23% (0%)
- 嘔吐 20% (1%)
上手に使うためのワンポイント
- オラパリブ単剤療法は生殖細胞系列BRCA1/2遺伝子病的バリアントを有する切除不能膵癌に対するプラチナ系薬剤をベースとした化学療法後 (mFOLFIRINOX療法など) の維持療法としての標準治療である。
- 生殖細胞系列BRCA1/2遺伝子病的バリアントは膵癌全体の約5%に認められ、 投与開始にあたってはコンパニオン診断薬 (BRCAnalysis診断システム) や遺伝子パネル検査での同バリアントの確認が必要である。
- 維持療法としての実施にあたっては、 前治療としてプラチナ系薬剤をベースとした化学療法を病勢進行なく16週以上施行してることが条件である。
執筆医:慶應義塾大学医学部 腫瘍センター ゲノム医療ユニット統括マネージャー・特任講師 林秀幸先生
特徴と注意点
- 食事の影響は受けないので食後・空腹時のいずれでも内服可能であり、 1日2回12時間ごとを目安として内服する。
- 主に肝で代謝されることから肝機能障害を有する患者では血中濃度が上昇するおそれがあり、 注意が必要である。
- 軽度腎機能障害患者に投与する際は用量調整は不要だが、 中等度腎機能障害のある患者 (Ccr: 31~50mL/min) への投与や、 中程度 または強いCYP3A阻害薬を併用する場合は減量を考慮することが推奨されている。
- 妊娠する可能性のある患者およびパートナー が妊娠する可能性がある患者には、 服用中および服用終了後1ヵ月間は適切な避妊を行うよう指導する。
- 主な副作用として 骨髄抑制 (特に貧血) 、 疲労、 悪心・嘔吐があげられ、 骨髄抑制に関しては発現Gradeに応じて適宜休薬・減量を実施する。
執筆医:慶應義塾大学医学部 腫瘍センター ゲノム医療ユニット統括マネージャー・特任講師 林秀幸先生
関連する臨床試験|POLO試験³⁾
BRCA遺伝子変異を有し、 プラチナベースの化学療法中に病勢進行しなかった転移性膵腺癌患者において、 オラパリブの効果を、 プラセボを対照に検証した第Ⅲ相二重盲検ランダム化比較試験POLOの結果より、 無増悪生存期間 (PFS) における有効性が示された。
PFS中央値
- オラパリブ群:6.7ヵ月
- プラセボ群:3.7ヵ月
HR 0.49 (95%CI 0.33-0.73)、 p=0.0004
PFS率 (6ヵ月時、 12ヵ月時、 18ヵ月時、 24ヵ月時)
- オラパリブ群:53.0%、 33.7%、 27.6%、 22.1%
- プラセボ群:23.0%、 14.5%、 9.6%、 9.6%
OS中央値
- オラパリブ群:19.0ヵ月
- プラセボ群:19.2ヵ月
HR 0.83 (95%CI 0.56-1.22)、 p=0.3487
OS率 (24ヵ月時、 36ヵ月時)
- オラパリブ群:37.0%、 33.9%
- プラセボ群:27.4%、 17.8%
ORR
- オラパリブ群:23%
- プラセボ群:12%
オッズ比 2.30 (95%CI 0.89-6.76)
PFS2中央値
- オラパリブ群:16.9ヵ月
- プラセボ群:9.3ヵ月
HR 0.66 (95%CI 0.43-1.02)、 p=0.0613
PFS2率 (3年時)
- オラパリブ群:31.2%
- プラセボ群:13.1%
TFST中央値
- オラパリブ群:9.0ヵ月
- プラセボ群:5.4ヵ月
HR 0.44 (95%CI 0.30-0.66)、 p<0.0001
TSST
- オラパリブ群:14.9ヵ月
- プラセボ群:9.6ヵ月
HR 0.61 (95%CI 0.42-0.89)、 p=0.0111
TDT
- オラパリブ群:7.5ヵ月
- プラセボ群:3.8ヵ月
HR 0.43 (95%CI 0.29-0.63)、 p<0.0001
出典
- MSD株式会社. リムパーザ®電子添文 (2024年11月改訂第6版) [最終閲覧 : 2024/11/29]
- MSD株式会社. リムパーザ®適正使用ガイド 膵癌 (2023年8月作成) [最終閲覧 : 2024/11/29]
- Maintenance Olaparib for Germline BRCA-Mutated Metastatic Pancreatic Cancer. N Engl J Med. 2019 Jul 25;381(4):317-327. PMID: 31157963
最終更新日:2024年11月29日
執筆医:慶應義塾大学医学部 腫瘍センター ゲノム医療ユニット統括マネージャー・特任講師 林秀幸先生
監修医:神奈川県立がんセンター 消化器内科 上野 誠先生
こちらの記事の監修医師
HOKUTO編集部
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
HOKUTO編集部
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
レジメン(消化器)
がん薬物療法における治療計画をまとめたものです。
主要論文や適正使用ガイドをもとにした用量調整プロトコール、 有害事象対応をご紹介します。
なお、 本ツールは医師向けの教育用資料であり、 実臨床での使用は想定しておりません。 最新の添付文書やガイドラインを必ずご確認下さい。
また、 一般の方への情報提供ではないことを予めご了承ください。
