本コンテンツは特定の治療法を推奨するものではございません. 個々の患者の病態や、 実際の薬剤情報やガイドラインを確認の上、 利用者の判断と責任でご利用ください.
薬剤情報
ヒト型抗ヒトCTLA-4モノクローナル抗体 (イピリムマブ)
*ブリストル・マイヤーズ スクイブ株式会社の外部サイトへ遷移します
ヒト型抗ヒトPD-1モノクローナル抗体 (ニボルマブ)
*小野薬品工業株式会社の外部サイトへ遷移します
投与スケジュール
【1コース】42日
【催吐性】 ともに最小度催吐性
【FN発症】低リスク
ニボルマブ2週間間隔の場合
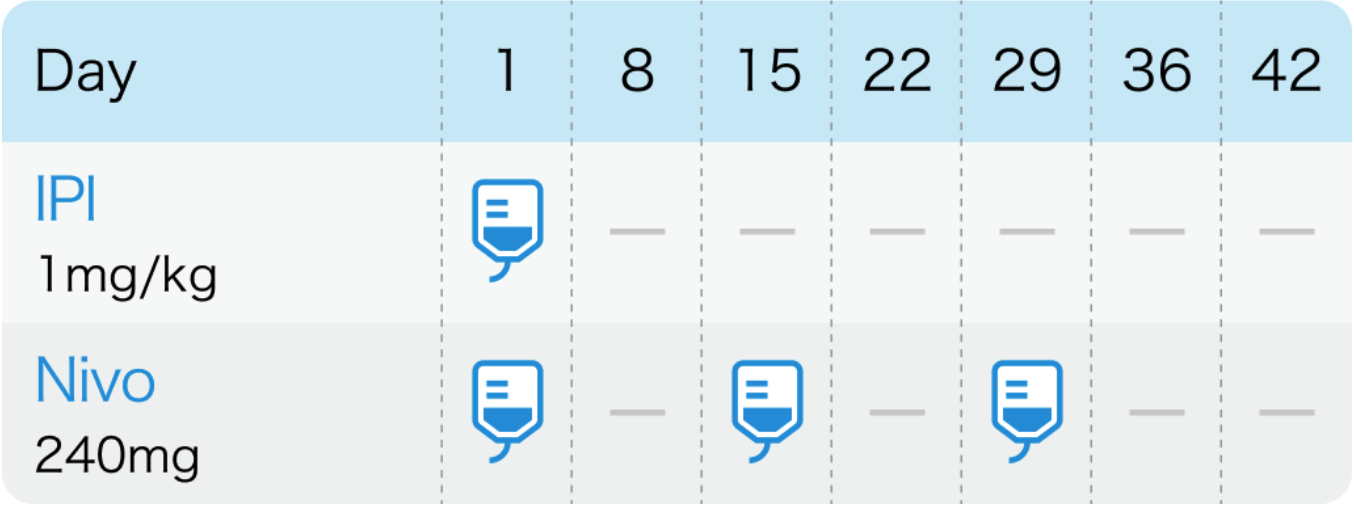
イピリムマブ1mg/kg 6週間毎、 ニボルマブ240mg 2週間毎投与
ニボルマブ3週間間隔の場合
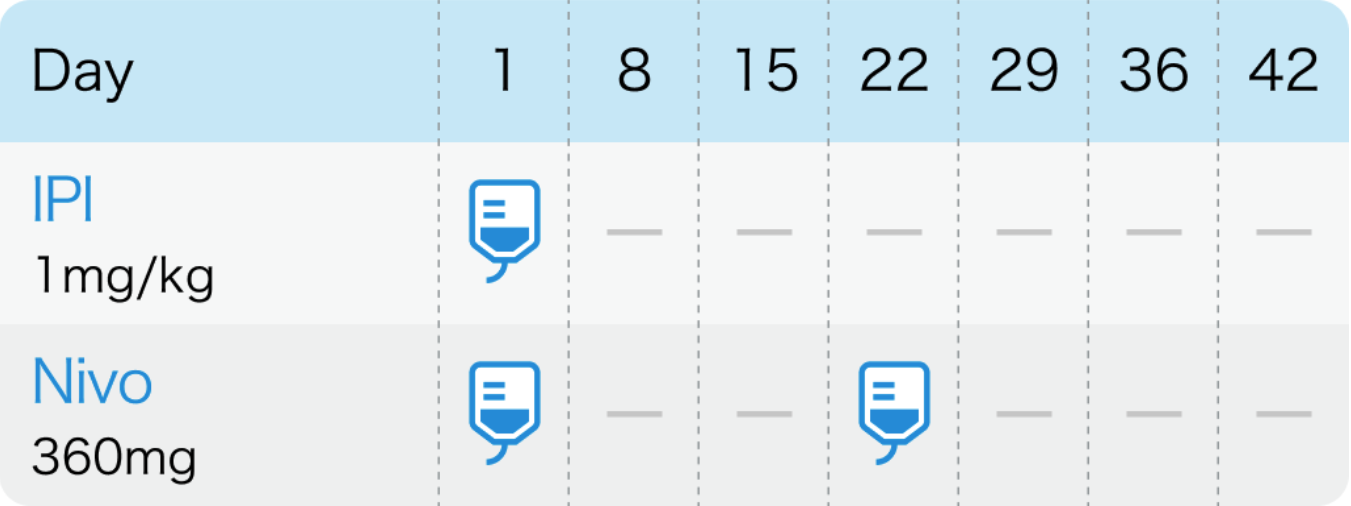
イピリムマブ1mg/kg 6週間毎、 ニボルマブ360mg 3週間毎投与
オプジーボ (ヤーボイ又は他の抗悪性腫瘍剤併用療法)・ヤーボイ適正使用ガイド²⁾より引用
※併用時の投与方法
Nivo 240mg又は360mgを30分以上かけて投与し、 投与完了後30分以上の間隔をおいて、 IPI 1mg/kgを30分かけて投与
オプジーボ (ヤーボイ又は他の抗悪性腫瘍剤併用療法)・ヤーボイ適正使用ガイド²⁾より引用
KeyData|臨床試験結果
📊CheckMate 227試験²⁾³⁾
N Engl J Med.2019 ;381(21):2020-31. [初回]
J Thorac Oncol.2025;20(10):1505-16. [6年追跡]
ファーストラインの転移性NSCLC患者を対象に、 非扁平上皮がんおよび扁平上皮がんの組織型にかかわらず、 ニボルマブを含むレジメンをプラチナ製剤を含む2剤併用化学療法と比較評価した複数のパートで構成された国際共同無作為化非盲検第Ⅲ相臨床試験
【有効性】Nivo + Ipi 併用療法群
Nivo 3mg/kgを2週間間隔+ Ipi 1mg/kg 6週間間隔
- mOS [PD-L1≧1%] : 17.1ヵ月
- mOS [PD-L1<1%] : 17.2ヵ月
【安全性】Nivo + Ipi 併用療法群
- 皮膚障害 (37.3%、 ≧Grade3 4.7%)
- 下痢 (17.0%、 ≧Grade3 1.7%
- 疲労 (14.4%、 ≧Grade3 1.7%)
- 甲状腺機能低下症 (12.5%、≧Grade3 0.3%)
- 食欲減退 (13.2%、 ≧Grade3 0.7%)
N Engl J Med. 2019 Nov 21;381(21):2020-31.より引用
レジメンの特徴と注意点
投与開始前の注意点
- EGFRおよびALK融合遺伝子陰性を確認。
- PSが0~1が治験時の患者登録基準である。
- 自己免疫疾患、 間質性肺疾患等の既往がある患者はirAEのリスク因子となるため投与前に事前に評価を行う。
副作用と対策
- PD-1阻害薬とCTLA-4阻害薬の併用は、 各単剤投与と比較して内分泌障害、 肺臓炎、 皮疹、 下痢等のirAEリスクがより高まるため毒性管理に注意。
irAE : 免疫関連副作用 (>>もっと見る)
- 内分泌機能検査 (TSH、 FT4、 ACTHなど) や血液検査など定期的に実施し、 注意深く観察する。
- その他尿検査や画像評価などの定期的なモニタリングも必要。
- 有害事象が疑われた場合には、 各専門医へのコンサルトも検討。
- 免疫チェックポイント阻害薬は投与を終了してから数か月後に副作用が認められることもあるため、 投与終了後のモニタリングにも注意が必要。
出典
1) オプジーボ (ヤーボイ又は他の抗悪性腫瘍剤併用療法)・ヤーボイ適正使用ガイド (2025年8月作成) [最終閲覧 2025/10/19]
最終更新日 : 2025年10月19日
監修・作図 : HOKUTO編集部専門医
Nivolumab+Ipilimumab
本コンテンツは特定の治療法を推奨するものではございません. 個々の患者の病態や、 実際の薬剤情報やガイドラインを確認の上、 利用者の判断と責任でご利用ください.
薬剤情報
ヒト型抗ヒトCTLA-4モノクローナル抗体 (イピリムマブ)
*ブリストル・マイヤーズ スクイブ株式会社の外部サイトへ遷移します
ヒト型抗ヒトPD-1モノクローナル抗体 (ニボルマブ)
*小野薬品工業株式会社の外部サイトへ遷移します
投与スケジュール
【1コース】42日
【催吐性】 ともに最小度催吐性
【FN発症】低リスク
ニボルマブ2週間間隔の場合

イピリムマブ1mg/kg 6週間毎、 ニボルマブ240mg 2週間毎投与
ニボルマブ3週間間隔の場合

イピリムマブ1mg/kg 6週間毎、 ニボルマブ360mg 3週間毎投与
オプジーボ (ヤーボイ又は他の抗悪性腫瘍剤併用療法)・ヤーボイ適正使用ガイド²⁾より引用
※併用時の投与方法
Nivo 240mg又は360mgを30分以上かけて投与し、 投与完了後30分以上の間隔をおいて、 IPI 1mg/kgを30分かけて投与
オプジーボ (ヤーボイ又は他の抗悪性腫瘍剤併用療法)・ヤーボイ適正使用ガイド²⁾より引用
KeyData|臨床試験結果
📊CheckMate 227試験²⁾³⁾
N Engl J Med.2019 ;381(21):2020-31. [初回]
J Thorac Oncol.2025;20(10):1505-16. [6年追跡]
ファーストラインの転移性NSCLC患者を対象に、 非扁平上皮がんおよび扁平上皮がんの組織型にかかわらず、 ニボルマブを含むレジメンをプラチナ製剤を含む2剤併用化学療法と比較評価した複数のパートで構成された国際共同無作為化非盲検第Ⅲ相臨床試験
【有効性】Nivo + Ipi 併用療法群
Nivo 3mg/kgを2週間間隔+ Ipi 1mg/kg 6週間間隔
- mOS [PD-L1≧1%] : 17.1ヵ月
- mOS [PD-L1<1%] : 17.2ヵ月
【安全性】Nivo + Ipi 併用療法群
- 皮膚障害 (37.3%、 ≧Grade3 4.7%)
- 下痢 (17.0%、 ≧Grade3 1.7%
- 疲労 (14.4%、 ≧Grade3 1.7%)
- 甲状腺機能低下症 (12.5%、≧Grade3 0.3%)
- 食欲減退 (13.2%、 ≧Grade3 0.7%)
N Engl J Med. 2019 Nov 21;381(21):2020-31.より引用
レジメンの特徴と注意点
投与開始前の注意点
- EGFRおよびALK融合遺伝子陰性を確認。
- PSが0~1が治験時の患者登録基準である。
- 自己免疫疾患、 間質性肺疾患等の既往がある患者はirAEのリスク因子となるため投与前に事前に評価を行う。
副作用と対策
- PD-1阻害薬とCTLA-4阻害薬の併用は、 各単剤投与と比較して内分泌障害、 肺臓炎、 皮疹、 下痢等のirAEリスクがより高まるため毒性管理に注意。
irAE : 免疫関連副作用 (>>もっと見る)
- 内分泌機能検査 (TSH、 FT4、 ACTHなど) や血液検査など定期的に実施し、 注意深く観察する。
- その他尿検査や画像評価などの定期的なモニタリングも必要。
- 有害事象が疑われた場合には、 各専門医へのコンサルトも検討。
- 免疫チェックポイント阻害薬は投与を終了してから数か月後に副作用が認められることもあるため、 投与終了後のモニタリングにも注意が必要。
出典
1) オプジーボ (ヤーボイ又は他の抗悪性腫瘍剤併用療法)・ヤーボイ適正使用ガイド (2025年8月作成) [最終閲覧 2025/10/19]
最終更新日 : 2025年10月19日
監修・作図 : HOKUTO編集部専門医
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
がん薬物療法における治療計画をまとめたものです。
主要論文や適正使用ガイドをもとにした用量調整プロトコール、 有害事象対応をご紹介します。
なお、 本ツールは医師向けの教育用資料であり、 実臨床での使用は想定しておりません。 最新の添付文書やガイドラインを必ずご確認下さい。
また、 一般の方への情報提供ではないことを予めご了承ください。