本コンテンツは特定の治療法を推奨するものではありません。 個々の患者の病態や、 実際の薬剤情報やガイドラインを確認の上、 利用者の判断と責任でご利用ください。
2025年5月19日、 切除不能な進行・再発の悪性胸膜中皮腫に対して適応拡大された。
薬剤情報
- キイトルーダ® (添付文書¹⁾ / 適正使用情報²⁾*)
*MSD製薬の外部サイトへ遷移します
- シスプラチン® (添付文書)
- カルボプラチン® (添付文書)
- ペメトレキセド® (添付文書³⁾)
投与スケジュール
切除不能な進行・再発の悪性胸膜中皮腫
【1コース】21日間
【催吐性】 高度
【FN発症】低リスク*
*KEYNOTE-483試験⁴⁾のFN発生率5%を基に編集部が分類
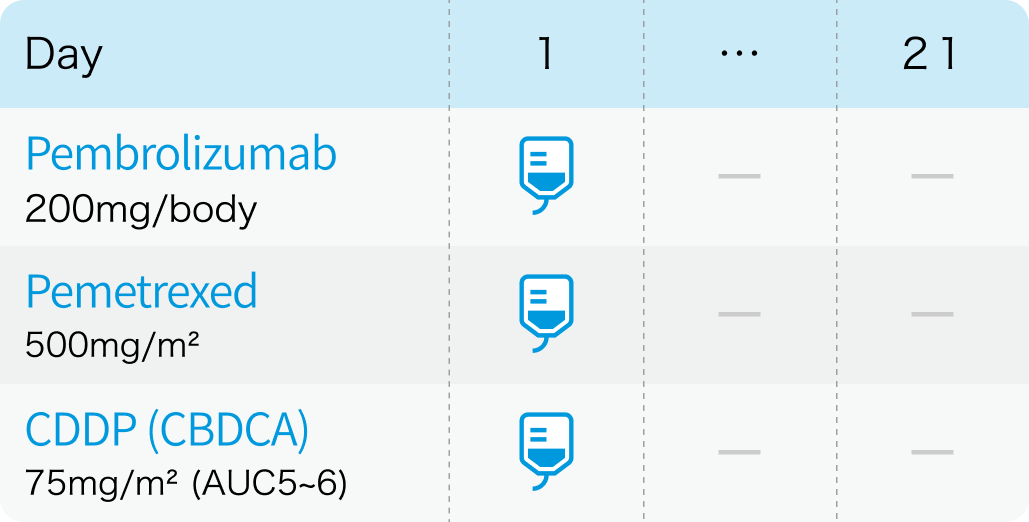
KEYNOTE-483試験⁴⁾のプロトコルを基に編集部作成
- 3週ごとに1サイクル
- Pembrolizumabは最大35サイクル (約2年間) まで投与
- CDDPは最大6サイクルまで投与、 禁忌または忍容性不良時のみCBDCAに代替可
国内第Ib相試験では、 化学療法との併用は最大4~6サイクルまでであり、 使用可能なプラチナ製剤はCDDPに限られていた。
- PemetrexedはCDDPまたはCBDCAと併用して最大6サイクルまで投与し、 その後はPembrolizumabとの併用により維持療法として継続可能
- KEYNOTE-483試験とは異なるが、 Pembrolizumab 400mg/bodyを6週ごとに投与する用法・用量も承認されている。
Key Data|臨床試験結果
📊 KEYNOTE-483試験⁴⁾
Lancet. 2023;402(10419):2295-2306.
未治療の進行性悪性胸膜中皮腫患者440例を対象とした国際共同 (カナダ、 イタリア、 フランス) 第III相非盲検ランダム化比較試験。 Pembrolizumab+化学療法 (CDDPまたはCBDCA+Pemetrexed) 群 (222例) と化学療法単独群 (218例) に1:1の比率で無作為に割り付け、 主要評価項目としてOSが設定された。
【有効性】 Pembrolizumab+化学療法群
- OS中央値: 17.3ヵ月 (HR 0.79、 p=0.03)
組織型やPD-L1発現状況にかかわらず、 Pembrolizumab群で有効性が認められた。
- PFS中央値: 7.1ヵ月 (HR 0.80、 p=0.04)
- 客観的奏効率: 62%
- 奏効期間中央値: 5.8ヵ月
【安全性】 主な有害事象 : 全Grade (Grade≧3)
試験薬の最終投与から30日以内に発現し、 いずれかの群で10%以上、 または≧Grade 3で2%以上の頻度で認められたもの
- 貧血: 2% (2%)
- 食欲不振: 17% (0%)
- 便秘: 16% (0%)
- 下痢: 23% (1%)
- 味覚異常: 12% (0%)
- 倦怠感: 51% (7%)
- 発熱性好中球減少症: 5% (5%)
- 口腔粘膜炎: 19% (0%)
- 悪心: 50% (5%)
- 末梢性感覚ニューロパチー: 11% (0%)
- そう痒症: 15% (0%)
- 発疹 (斑状丘疹状) : 14% (1%)
- 嘔吐: 19% (1%)
- 流涙増加: 12% (0%)
各プロトコル
適格基準
KEYNOTE-483試験⁴⁾の主な適格基準
- 年齢: 18歳以上
- PS: ECOG PS 0または1
- 好中球数: ≧1,500/μL
- 血小板数: ≧100,000/μL
- ヘモグロビン値: ≧9.0 g/dL
- 腎機能: CrCl ≧50mL/min、 または血清クレアチニン<1.25 × ULN
- 肝機能: 総ビリルビン ≦1.5 × ULN、 AST/ALT ≦2.5 × ULN
用量レベル
KEYNOTE-483試験⁴⁾では、 化学療法の具体的な減量ステップや用量レベルについて、 プロトコル上の詳細な規定は設けられておらず、 治験責任医師が各薬剤の添付文書や地域の標準的な診療ガイドラインに基づいて判断することとされていた。 なお、 ペムブロリズマブについては減量規定は設けられていない。
腎障害患者に対する用量調整
▼CDDP⁵⁾
- 重篤な腎障害例への投与は禁忌
- CrCl 46~60mL/minでは75%、 31~45mL/minでは50%に減量し、 CrCl≦30mL/minでは投与を推奨しない
- 別の報告 : CrCl 30~49mL/minでは75%、 10~29mL/minでは投与が必要な場合に75%、 CrCl<10mL/minでは投与が必要な場合に50%に減量
▼CBDCA⁵⁾
- Calvert式で投与量を算出する
▼Pemetrexed⁵⁾
- 重度の腎機能障害患者には投与しない。 なお、 CrCl<45mL/minの患者は臨床試験において除外されている
有害事象発現時の対応方法
▼Pembrolizumabの休薬・中止基準

キイトルーダ®電子添文¹⁾を基に編集部作図
▼CDDP/Pemetrexedの減量目安
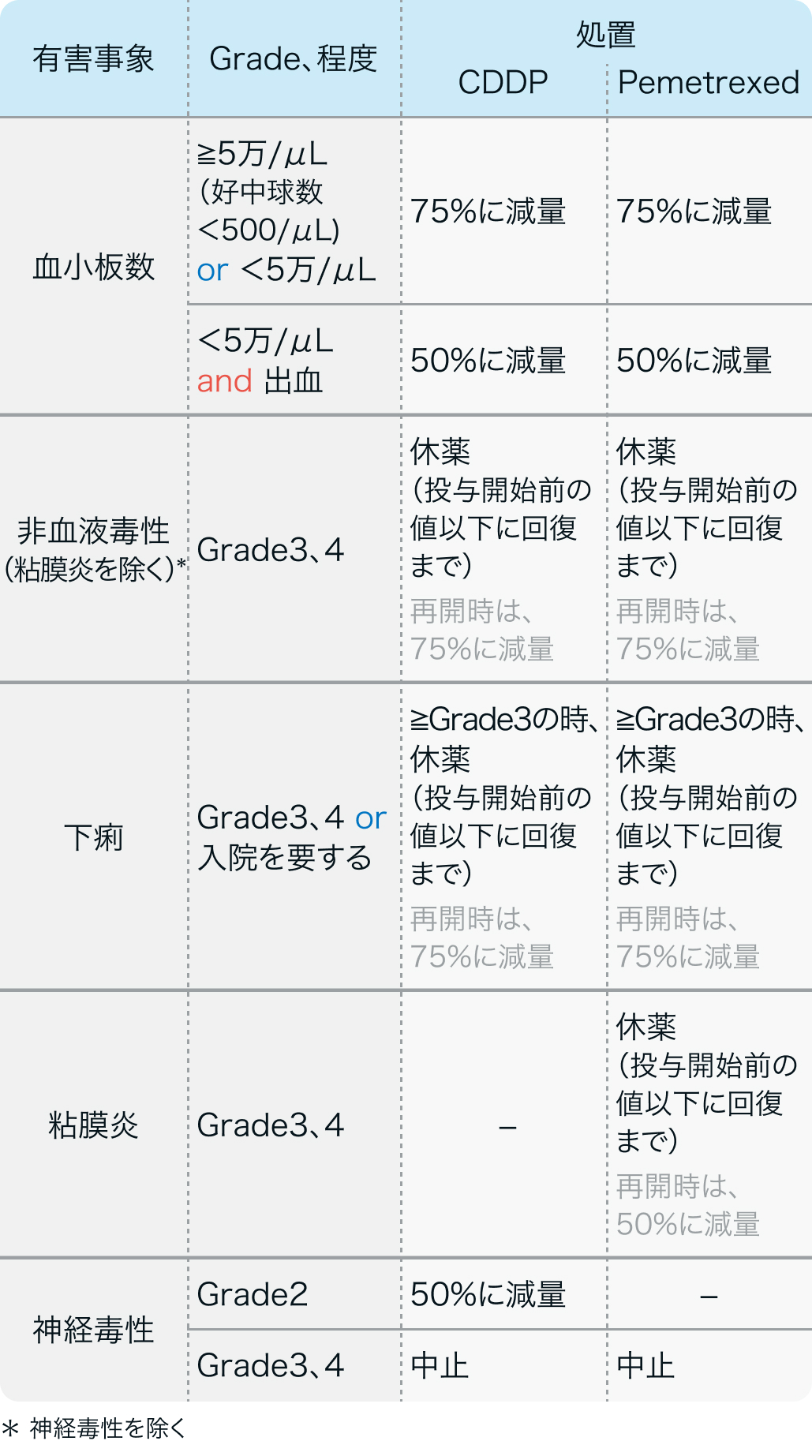
2回の減量後にGrade 3または4の血液毒性・非血液毒性、 あるいは神経毒性が認められた場合は、 直ちにPemetrexedの投与を中止すること。
アリムタ®添付文書³⁾を基に編集部作成
レジメンの特徴と注意点
本レジメンの位置づけ
- 本レジメンは、 未治療の進行性悪性胸膜中皮腫に対する1次治療である
- プラチナ製剤としてはCDDPを基本とし、 CBDCAへの代替は症例ごとに判断された
レジメン適用時の注意事項
- CDDPはPembrolizumab投与30分後に投与¹⁾
- CDDPによる腎障害予防のための十分な水分負荷と利尿管理を行う
- 水分負荷に対する心機能の耐容性を事前に確認する
- PEM関連の皮疹が認められた場合、 次コースより予防的ステロイド投与を検討する
FDA添付文書³⁾ : PEM投与前日から投与翌日までの3日間、 デキサメタゾン4mg 1日2回経口投与
RMP【重要な特定されたリスク】
キイトルーダ® 医薬品リスク管理計画書 (RMP)
- 間質性肺疾患
- 大腸炎・小腸炎・重度の下痢
- 劇症肝炎・肝不全・肝機能障害・肝炎・硬化性胆管炎
- 腎機能障害 (尿細管間質性腎炎、 糸球体腎炎等)
- 内分泌障害 (下垂体機能障害、 甲状腺機能障害、 副腎機能障害)
- 1型糖尿病
- ぶどう膜炎
- 筋炎・横紋筋融解症
- 膵炎・膵外分泌機能不全
- 神経障害 (ギラン・バレー症候群等)
- 重度の皮膚障害 (中毒性表皮壊死融解症、 皮膚粘膜眼症候群、 多形紅斑、 類天疱瘡等)
- 脳炎、 髄膜炎、 脊髄炎
- 重症筋無力症
- 心筋炎
- 重篤な血液障害 (免疫性血小板減少性紫斑病、 溶血性貧血、 赤芽球癆、 無顆粒球症等)
- 重度の胃炎
- 血球貪食症候群
- Infusion reaction
- 臓器移植歴 (造血幹細胞移植歴を含む) のある患者への使用
- 結核
出典
- キイトルーダ®点滴静注100mg 電子添文 (2025年5月改訂 第24版) [最終閲覧 : 2025/5/26]
- キイトルーダ®点滴静注100mg 適正使用ガイド (2025年5月作成) [最終閲覧 : 2025/5/26]
- アリムタ®注射用100mg/500mg 電子添文 (2024年8月改訂 第2版) [最終閲覧 : 2025/5/26]
- Lancet. 2023;402(10419):2295-2306.
- 日本腎臓学会、 日本癌治療学会、 日本臨床腫瘍学会、 日本腎臓病薬物療法学会編 : がん薬物療法時の腎障害診療ガイドライン2022. ライフサイエンス出版.
最終更新日 : 2025年6月4日
執筆 : HOKUTO編集部 がん専門・指導薬剤師
監修 : HOKUTO編集部監修医師
Pembrolizumab+CDDP (CBDCA) / PEM
本コンテンツは特定の治療法を推奨するものではありません。 個々の患者の病態や、 実際の薬剤情報やガイドラインを確認の上、 利用者の判断と責任でご利用ください。
2025年5月19日、 切除不能な進行・再発の悪性胸膜中皮腫に対して適応拡大された。
薬剤情報
- キイトルーダ® (添付文書¹⁾ / 適正使用情報²⁾*)
*MSD製薬の外部サイトへ遷移します
- シスプラチン® (添付文書)
- カルボプラチン® (添付文書)
- ペメトレキセド® (添付文書³⁾)
投与スケジュール
切除不能な進行・再発の悪性胸膜中皮腫
【1コース】21日間
【催吐性】 高度
【FN発症】低リスク*
*KEYNOTE-483試験⁴⁾のFN発生率5%を基に編集部が分類

KEYNOTE-483試験⁴⁾のプロトコルを基に編集部作成
- 3週ごとに1サイクル
- Pembrolizumabは最大35サイクル (約2年間) まで投与
- CDDPは最大6サイクルまで投与、 禁忌または忍容性不良時のみCBDCAに代替可
国内第Ib相試験では、 化学療法との併用は最大4~6サイクルまでであり、 使用可能なプラチナ製剤はCDDPに限られていた。
- PemetrexedはCDDPまたはCBDCAと併用して最大6サイクルまで投与し、 その後はPembrolizumabとの併用により維持療法として継続可能
- KEYNOTE-483試験とは異なるが、 Pembrolizumab 400mg/bodyを6週ごとに投与する用法・用量も承認されている。
Key Data|臨床試験結果
📊 KEYNOTE-483試験⁴⁾
Lancet. 2023;402(10419):2295-2306.
未治療の進行性悪性胸膜中皮腫患者440例を対象とした国際共同 (カナダ、 イタリア、 フランス) 第III相非盲検ランダム化比較試験。 Pembrolizumab+化学療法 (CDDPまたはCBDCA+Pemetrexed) 群 (222例) と化学療法単独群 (218例) に1:1の比率で無作為に割り付け、 主要評価項目としてOSが設定された。
【有効性】 Pembrolizumab+化学療法群
- OS中央値: 17.3ヵ月 (HR 0.79、 p=0.03)
組織型やPD-L1発現状況にかかわらず、 Pembrolizumab群で有効性が認められた。
- PFS中央値: 7.1ヵ月 (HR 0.80、 p=0.04)
- 客観的奏効率: 62%
- 奏効期間中央値: 5.8ヵ月
【安全性】 主な有害事象 : 全Grade (Grade≧3)
試験薬の最終投与から30日以内に発現し、 いずれかの群で10%以上、 または≧Grade 3で2%以上の頻度で認められたもの
- 貧血: 2% (2%)
- 食欲不振: 17% (0%)
- 便秘: 16% (0%)
- 下痢: 23% (1%)
- 味覚異常: 12% (0%)
- 倦怠感: 51% (7%)
- 発熱性好中球減少症: 5% (5%)
- 口腔粘膜炎: 19% (0%)
- 悪心: 50% (5%)
- 末梢性感覚ニューロパチー: 11% (0%)
- そう痒症: 15% (0%)
- 発疹 (斑状丘疹状) : 14% (1%)
- 嘔吐: 19% (1%)
- 流涙増加: 12% (0%)
各プロトコル
適格基準
KEYNOTE-483試験⁴⁾の主な適格基準
- 年齢: 18歳以上
- PS: ECOG PS 0または1
- 好中球数: ≧1,500/μL
- 血小板数: ≧100,000/μL
- ヘモグロビン値: ≧9.0 g/dL
- 腎機能: CrCl ≧50mL/min、 または血清クレアチニン<1.25 × ULN
- 肝機能: 総ビリルビン ≦1.5 × ULN、 AST/ALT ≦2.5 × ULN
用量レベル
KEYNOTE-483試験⁴⁾では、 化学療法の具体的な減量ステップや用量レベルについて、 プロトコル上の詳細な規定は設けられておらず、 治験責任医師が各薬剤の添付文書や地域の標準的な診療ガイドラインに基づいて判断することとされていた。 なお、 ペムブロリズマブについては減量規定は設けられていない。
腎障害患者に対する用量調整
▼CDDP⁵⁾
- 重篤な腎障害例への投与は禁忌
- CrCl 46~60mL/minでは75%、 31~45mL/minでは50%に減量し、 CrCl≦30mL/minでは投与を推奨しない
- 別の報告 : CrCl 30~49mL/minでは75%、 10~29mL/minでは投与が必要な場合に75%、 CrCl<10mL/minでは投与が必要な場合に50%に減量
▼CBDCA⁵⁾
- Calvert式で投与量を算出する
▼Pemetrexed⁵⁾
- 重度の腎機能障害患者には投与しない。 なお、 CrCl<45mL/minの患者は臨床試験において除外されている
有害事象発現時の対応方法
▼Pembrolizumabの休薬・中止基準

キイトルーダ®電子添文¹⁾を基に編集部作図
▼CDDP/Pemetrexedの減量目安

2回の減量後にGrade 3または4の血液毒性・非血液毒性、 あるいは神経毒性が認められた場合は、 直ちにPemetrexedの投与を中止すること。
アリムタ®添付文書³⁾を基に編集部作成
レジメンの特徴と注意点
本レジメンの位置づけ
- 本レジメンは、 未治療の進行性悪性胸膜中皮腫に対する1次治療である
- プラチナ製剤としてはCDDPを基本とし、 CBDCAへの代替は症例ごとに判断された
レジメン適用時の注意事項
- CDDPはPembrolizumab投与30分後に投与¹⁾
- CDDPによる腎障害予防のための十分な水分負荷と利尿管理を行う
- 水分負荷に対する心機能の耐容性を事前に確認する
- PEM関連の皮疹が認められた場合、 次コースより予防的ステロイド投与を検討する
FDA添付文書³⁾ : PEM投与前日から投与翌日までの3日間、 デキサメタゾン4mg 1日2回経口投与
RMP【重要な特定されたリスク】
キイトルーダ® 医薬品リスク管理計画書 (RMP)
- 間質性肺疾患
- 大腸炎・小腸炎・重度の下痢
- 劇症肝炎・肝不全・肝機能障害・肝炎・硬化性胆管炎
- 腎機能障害 (尿細管間質性腎炎、 糸球体腎炎等)
- 内分泌障害 (下垂体機能障害、 甲状腺機能障害、 副腎機能障害)
- 1型糖尿病
- ぶどう膜炎
- 筋炎・横紋筋融解症
- 膵炎・膵外分泌機能不全
- 神経障害 (ギラン・バレー症候群等)
- 重度の皮膚障害 (中毒性表皮壊死融解症、 皮膚粘膜眼症候群、 多形紅斑、 類天疱瘡等)
- 脳炎、 髄膜炎、 脊髄炎
- 重症筋無力症
- 心筋炎
- 重篤な血液障害 (免疫性血小板減少性紫斑病、 溶血性貧血、 赤芽球癆、 無顆粒球症等)
- 重度の胃炎
- 血球貪食症候群
- Infusion reaction
- 臓器移植歴 (造血幹細胞移植歴を含む) のある患者への使用
- 結核
出典
- キイトルーダ®点滴静注100mg 電子添文 (2025年5月改訂 第24版) [最終閲覧 : 2025/5/26]
- キイトルーダ®点滴静注100mg 適正使用ガイド (2025年5月作成) [最終閲覧 : 2025/5/26]
- アリムタ®注射用100mg/500mg 電子添文 (2024年8月改訂 第2版) [最終閲覧 : 2025/5/26]
- Lancet. 2023;402(10419):2295-2306.
- 日本腎臓学会、 日本癌治療学会、 日本臨床腫瘍学会、 日本腎臓病薬物療法学会編 : がん薬物療法時の腎障害診療ガイドライン2022. ライフサイエンス出版.
最終更新日 : 2025年6月4日
執筆 : HOKUTO編集部 がん専門・指導薬剤師
監修 : HOKUTO編集部監修医師
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
がん薬物療法における治療計画をまとめたものです。
主要論文や適正使用ガイドをもとにした用量調整プロトコール、 有害事象対応をご紹介します。
なお、 本ツールは医師向けの教育用資料であり、 実臨床での使用は想定しておりません。 最新の添付文書やガイドラインを必ずご確認下さい。
また、 一般の方への情報提供ではないことを予めご了承ください。