本コンテンツは特定の治療法を推奨するものではありません。 個々の患者の病態や、 実際の薬剤情報やガイドラインを確認の上、 利用者の判断と責任でご利用ください。
薬剤情報
タキソール® (添付文書¹⁾)
用法用量
電子添文¹⁾の用法および用量
血管肉腫にはB法を使用する。 B法では、 1日1回100mg/m²を1時間かけて点滴静注し、 週1回投与を6週連続し、 少なくとも2週間休薬
タキソール®電子添文 (2023年7月改訂 第2版)¹⁾より引用
ANGIOTAX試験²⁾のプロトコル
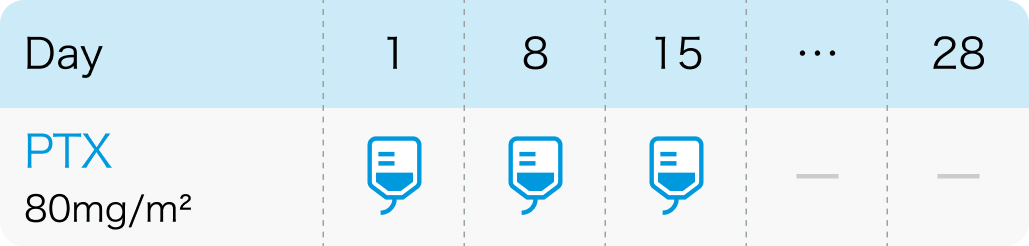
週1回投与を3週連続 (Day1、8、15)、1週間休薬
J Clin Oncol. 2008 Nov 10;26(32):5269-74.²⁾より作図
前投薬
電子添文¹⁾の前投薬
投与約30分前までに投与を終了するように、 デキサメタゾンリン酸エステルナトリウム注射液 (デキサメタゾンとして8mg)、 ラニチジン塩酸塩注射液 (ラニチジンとして50mg) または注射用ファモチジン (ファモチジンとして20mg) を静脈内投与、 ジフェンヒドラミン塩酸塩錠 (ジフェンヒドラミン塩酸塩として50mg) を経口投与
デキサメタゾンは初回投与時8mgとし、 次回投与時までに過敏症状の発現がみられなかった場合または臨床上特に問題のない過敏症状の場合は、 2週目の投与より半量 (4mg) に減量し投与してもよい。 以降の投与週においても同様の場合、 半量ずつ最低1mgまで減量し投与してもよい
タキソール®電子添文 (2023年7月改訂 第2版)¹⁾ より引用
投与開始基準
ANGIOTAX試験²⁾のプロトコル

J Clin Oncol. 2008 Nov 10;26(32):5269-74.²⁾より作図
主な有害事象
ANGIOTAX試験²⁾
主な有害事象 (カッコ内はGrade3~5)
- 貧血 80.0% (10.0%)
- 白血球数減少 50.0% (16.7%)
- 好中球数減少 43.3% (13.3%)
- 血小板数減少 16.7% (3.3%)
- 感染 23.3% (10.0%)
- 吐き気/嘔吐 26.7% (6.7%)
- 神経毒性 10.0% (0%)
- アレルギー反応 3.3% (0%)
- 筋肉痛/関節痛 30.0% (3.3%)
- 粘膜炎 16.7% (3.3%)
- 無力症 70.0% (10.0%)
- せん妄 6.7% (3.3%)
J Clin Oncol. 2008 Nov 10;26(32):5269-74.²⁾より引用
エキスパートによるワンポイント
1次治療の選択肢に
皮膚血管肉腫の大半を占める頭部原発症例では、 切除可能であれば広汎切除+術後放射線治療も選択肢となるものの、 本邦では原発巣が大きい症例が多く化学放射線治療が行われることが多い。
2012年にパクリタキセルが血管肉腫に対して保険適用となって以降は、 遠隔転移が無い症例に対して放射線と併用して使用されるとともに、 転移性血管肉腫に対する1次治療としても用いられる。 パクリタキセルは様々ながんに対して使用され投与量や投与間隔も様々だが、 血管肉腫にはweekly投与が保険適用となっている。
ANGIOTAX試験の投与法が多い
パクリタキセル1回100mg/m² (体表面積) を1時間かけて点滴静注する。 週1回投与を6週連続し、 2週休薬を1サイクルとして投与を繰り返す。 電子添文では上記B法となっているものの¹⁾、 後述のANGIOTAX試験の投与法である1回80mg/m² を週1回3週連続で投与し、 1週休薬を1サイクルとする投与法を用いることが多い。
高齢患者が多いことや放射線との併用で使用されることが多いことから、 減量や休薬を要することもある。 白血球数や好中球数の低下がある場合は電子添文の記載に従って減量する¹⁾。
血液毒性は減量や休薬により対処可能なことが多いが、 長期投与患者に生じる末梢神経障害は頻度が高く治療法が確立しておらず、 高齢者が多い本疾患においては転倒などのリスクにもなりうる。 事前に説明しておき症状が顕在化してきたら減量や休薬、 薬剤の変更など検討する。
臨床試験では奏効率18%
ANGIOTAX試験は転移性または切除不能血管肉腫30人に対して、 weeklyパクリタキセル1回80mg/m²の3週投与1週休薬を1サイクルとした第Ⅱ相試験であり、 奏効率18%、 2ヵ月時点での病勢制御率74%と報告された²⁾ 。 無増悪期間中央値は4ヵ月、 全生存期間中央値は8ヵ月であった。
Grade3以上の副作用で多く見られたのは白血球減少で、 血小板減少を誘因とした死亡が1例報告されている。 国内の後ろ向き観察研究では、 放射線と併用した55例において、 全生存期間中央値は624日、 Grade3以上の有害事象は23.6%であったと報告されている³⁾ 。
アナフィラキシーなどの重篤な過敏症状を起こすことがあるため、 ステロイド、 H1・H2ブロッカーの前投薬が必要である。 添加物にエタノールが含まれるためアルコール不耐患者に投与する際は注意する。
監修 : 国立がん研究センター中央病院 皮膚腫瘍科 中野英司先生
出典
- クリニジェン株式会社. タキソール®電子添文 (2023年7月改訂 第2版) [最終閲覧 : 2024/03/26]
- Phase II trial of weekly paclitaxel for unresectable angiosarcoma: the ANGIOTAX Study. J Clin Oncol. 2008 Nov 10;26(32):5269-74. PMID: 18809609
- Cutaneous angiosarcoma treated with taxane-based chemoradiotherapy: A multicenter study of 90 Japanese cases. Skin Health Dis. 2022 Nov 8;3(1):e180. PMID: 36751323
最終更新日 : 2024年5月14日
監修医師 : 国立がん研究センター中央病院 皮膚腫瘍科 中野英司先生
weekly PTX
本コンテンツは特定の治療法を推奨するものではありません。 個々の患者の病態や、 実際の薬剤情報やガイドラインを確認の上、 利用者の判断と責任でご利用ください。
薬剤情報
タキソール® (添付文書¹⁾)
用法用量
電子添文¹⁾の用法および用量
血管肉腫にはB法を使用する。 B法では、 1日1回100mg/m²を1時間かけて点滴静注し、 週1回投与を6週連続し、 少なくとも2週間休薬
タキソール®電子添文 (2023年7月改訂 第2版)¹⁾より引用
ANGIOTAX試験²⁾のプロトコル

週1回投与を3週連続 (Day1、8、15)、1週間休薬
J Clin Oncol. 2008 Nov 10;26(32):5269-74.²⁾より作図
前投薬
電子添文¹⁾の前投薬
投与約30分前までに投与を終了するように、 デキサメタゾンリン酸エステルナトリウム注射液 (デキサメタゾンとして8mg)、 ラニチジン塩酸塩注射液 (ラニチジンとして50mg) または注射用ファモチジン (ファモチジンとして20mg) を静脈内投与、 ジフェンヒドラミン塩酸塩錠 (ジフェンヒドラミン塩酸塩として50mg) を経口投与
デキサメタゾンは初回投与時8mgとし、 次回投与時までに過敏症状の発現がみられなかった場合または臨床上特に問題のない過敏症状の場合は、 2週目の投与より半量 (4mg) に減量し投与してもよい。 以降の投与週においても同様の場合、 半量ずつ最低1mgまで減量し投与してもよい
タキソール®電子添文 (2023年7月改訂 第2版)¹⁾ より引用
投与開始基準
ANGIOTAX試験²⁾のプロトコル

J Clin Oncol. 2008 Nov 10;26(32):5269-74.²⁾より作図
主な有害事象
ANGIOTAX試験²⁾
主な有害事象 (カッコ内はGrade3~5)
- 貧血 80.0% (10.0%)
- 白血球数減少 50.0% (16.7%)
- 好中球数減少 43.3% (13.3%)
- 血小板数減少 16.7% (3.3%)
- 感染 23.3% (10.0%)
- 吐き気/嘔吐 26.7% (6.7%)
- 神経毒性 10.0% (0%)
- アレルギー反応 3.3% (0%)
- 筋肉痛/関節痛 30.0% (3.3%)
- 粘膜炎 16.7% (3.3%)
- 無力症 70.0% (10.0%)
- せん妄 6.7% (3.3%)
J Clin Oncol. 2008 Nov 10;26(32):5269-74.²⁾より引用
エキスパートによるワンポイント
1次治療の選択肢に
皮膚血管肉腫の大半を占める頭部原発症例では、 切除可能であれば広汎切除+術後放射線治療も選択肢となるものの、 本邦では原発巣が大きい症例が多く化学放射線治療が行われることが多い。
2012年にパクリタキセルが血管肉腫に対して保険適用となって以降は、 遠隔転移が無い症例に対して放射線と併用して使用されるとともに、 転移性血管肉腫に対する1次治療としても用いられる。 パクリタキセルは様々ながんに対して使用され投与量や投与間隔も様々だが、 血管肉腫にはweekly投与が保険適用となっている。
ANGIOTAX試験の投与法が多い
パクリタキセル1回100mg/m² (体表面積) を1時間かけて点滴静注する。 週1回投与を6週連続し、 2週休薬を1サイクルとして投与を繰り返す。 電子添文では上記B法となっているものの¹⁾、 後述のANGIOTAX試験の投与法である1回80mg/m² を週1回3週連続で投与し、 1週休薬を1サイクルとする投与法を用いることが多い。
高齢患者が多いことや放射線との併用で使用されることが多いことから、 減量や休薬を要することもある。 白血球数や好中球数の低下がある場合は電子添文の記載に従って減量する¹⁾。
血液毒性は減量や休薬により対処可能なことが多いが、 長期投与患者に生じる末梢神経障害は頻度が高く治療法が確立しておらず、 高齢者が多い本疾患においては転倒などのリスクにもなりうる。 事前に説明しておき症状が顕在化してきたら減量や休薬、 薬剤の変更など検討する。
臨床試験では奏効率18%
ANGIOTAX試験は転移性または切除不能血管肉腫30人に対して、 weeklyパクリタキセル1回80mg/m²の3週投与1週休薬を1サイクルとした第Ⅱ相試験であり、 奏効率18%、 2ヵ月時点での病勢制御率74%と報告された²⁾ 。 無増悪期間中央値は4ヵ月、 全生存期間中央値は8ヵ月であった。
Grade3以上の副作用で多く見られたのは白血球減少で、 血小板減少を誘因とした死亡が1例報告されている。 国内の後ろ向き観察研究では、 放射線と併用した55例において、 全生存期間中央値は624日、 Grade3以上の有害事象は23.6%であったと報告されている³⁾ 。
アナフィラキシーなどの重篤な過敏症状を起こすことがあるため、 ステロイド、 H1・H2ブロッカーの前投薬が必要である。 添加物にエタノールが含まれるためアルコール不耐患者に投与する際は注意する。
監修 : 国立がん研究センター中央病院 皮膚腫瘍科 中野英司先生
出典
- クリニジェン株式会社. タキソール®電子添文 (2023年7月改訂 第2版) [最終閲覧 : 2024/03/26]
- Phase II trial of weekly paclitaxel for unresectable angiosarcoma: the ANGIOTAX Study. J Clin Oncol. 2008 Nov 10;26(32):5269-74. PMID: 18809609
- Cutaneous angiosarcoma treated with taxane-based chemoradiotherapy: A multicenter study of 90 Japanese cases. Skin Health Dis. 2022 Nov 8;3(1):e180. PMID: 36751323
最終更新日 : 2024年5月14日
監修医師 : 国立がん研究センター中央病院 皮膚腫瘍科 中野英司先生
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
がん薬物療法における治療計画をまとめたものです。
主要論文や適正使用ガイドをもとにした用量調整プロトコール、 有害事象対応をご紹介します。
なお、 本ツールは医師向けの教育用資料であり、 実臨床での使用は想定しておりません。 最新の添付文書やガイドラインを必ずご確認下さい。
また、 一般の方への情報提供ではないことを予めご了承ください。