本コンテンツは特定の治療法を推奨するものではありません。 個々の患者の病態や、 実際の薬剤情報やガイドラインを確認の上、 利用者の判断と責任でご利用ください。
薬剤情報
フリュザクラ®カプセル (フルキンチニブ)
武田薬品工業株式会社の外部サイトへ遷移します
投与スケジュール
【1コース】 28日間
【催吐性】最小度*
【FN発症】未報告**
*NCCN Guidelines Ver.2.2025 Antiemesis、 **FRESCO-2試験³⁾

1日1回5mgを3週間連日経口投与後に1週間休薬し、 これを1サイクルとして反復する。
飲み忘れは次回まで12時間以上なら気づいた時点で1回服用し、 12時間以内なら服用せず次回から再開し、 服用後に嘔吐しても追加服用しない。
レゴラフェニブ (REG) およびトリフルリジン・チピラシル (FTD/TPI) のいずれの治療歴もない患者では、 これらの薬剤による治療が困難な患者が投与対象
Key Data|臨床試験結果
📊 FRESCO-2試験
Lancet. 2023;402(10395):41-53.
標準治療 (フッ化ピリミジン系、 オキサリプラチン、 イリノテカン、 および抗VEGF/EGFR抗体) 歴を有し、 かつFTD/TPIまたはREG治療中に進行・不耐となった転移性結腸・直腸癌患者*を対象とした第III相無作為化比較試験。 フルキンチニブ群461例、 プラセボ群230例に2:1で割り付け、 主要評価項目はOSとした。
MSI-HまたはdMMR腫瘍を有する場合は免疫チェックポイント阻害剤治療歴があること、 またBRAF V600E変異腫瘍を有する場合はBRAF阻害剤による治療歴を有する患者が対象。
【有効性】フルキンチニブ群 (vs プラセボ群)
- OS中央値 7.4ヵ月 (vs 4.8ヵ月)
- HR 0.66 (95%CI 0.55–0.80、 p<0.001)
- PFS中央値 3.7ヵ月 (vs 1.8ヵ月)
- HR 0.32 (95%CI 0.27–0.39、 p<0.001)
- 客観的奏効率 2% (vs 0%)
- 病勢制御率 56% (vs 16%)
【安全性】主な有害事象 : 全Grade (Grade≧3)
- 高血圧 36.8% (13.6%)
- 無力症 34.0% (7.7%)
- 食欲減退 27.2% (2.4%)
- 下痢 24.1% (3.5%)
- 甲状腺機能低下症 20.6% (0.4%)
- 疲労 20.0% (3.9%)
- 手足症候群 19.3% (6.4%)
- 腹痛 18.2% (3.1%)
- 悪心 17.3% (0.7%)
- 蛋白尿 17.3% (1.8%)
- 便秘 17.1% (0.4%)
- 発声障害 16.2% (0%)
- 口内炎 14.7% (1.8%)
- 嘔吐 14.5% (1.5%)
- 粘膜炎症 13.6% (0.4%)
- 体重減少 12.3% (0.7%)
- 関節痛 11.0% (0.9%)
- AST増加 10.5% (2.2%)
- ALT増加 10.3% (3.1%)
- 背部痛 10.3% (1.3%)
- 発熱 10.1% (0.4%)
重点的評価 (AE of special interest) : 全Grade (Grade≧3)
- 高血圧 38.4% (14.0%)
- 皮膚毒性 34.4% (6.8%)
- 甲状腺機能障害 27.0% (0.4%)
- 肝機能異常 24.8% (0.8%)
- 感染症 21.1% (6.6%)
- 蛋白尿 17.5% (1.8%)
- 出血 14.3% (1.8%)
- 塞栓・血栓イベント 4.6% (3.1%)
- 消化管穿孔 3.5% (2.2%)
- 左室駆出率低下 1.1% (0.9%)
各プロトコル
適格基準
FRESCO-2試験³⁾の主な適格基準
- 18歳以上
- ECOG PS 0–1
- 好中球≧1500/mm³
- 血小板≧10万/mm³
- Hb≧9.0g/dL
- 肝機能 : T-Bil≦1.5×ULN、 AST/ALT≦2.5×ULN (肝転移は≦5.0×ULN)
- 腎機能 : Cre≦1.5×ULNまたはCrCl≧60mL/min
- 尿蛋白 : 尿定性試験<2+ または 24時間尿蛋白<1.0g
用量レベル
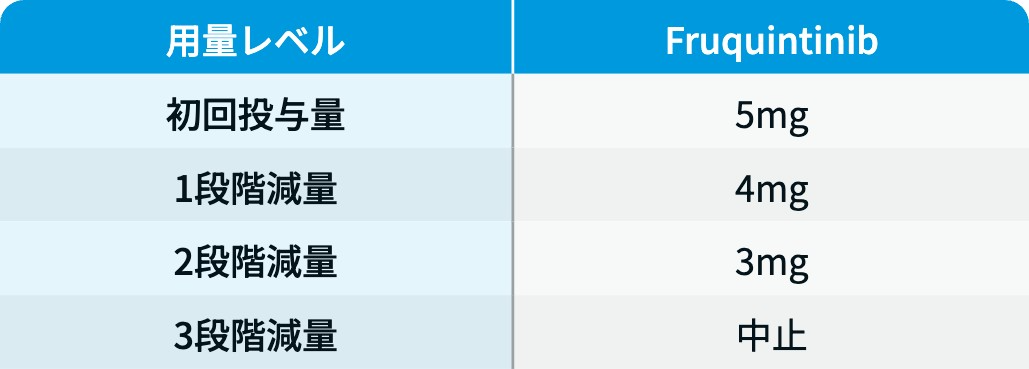
フリュザクラ®電子添文¹⁾を元に編集部作成
腎障害患者に対する用量調整
尿中未変化体排泄率は0.5%と低く、 腎クリアランスの寄与は小さいため、 腎障害時の用量調整は不要と考えられる。
フリュザクラ®電子添文¹⁾を元に編集部が評価
有害事象発現時の減量・休薬・中止基準
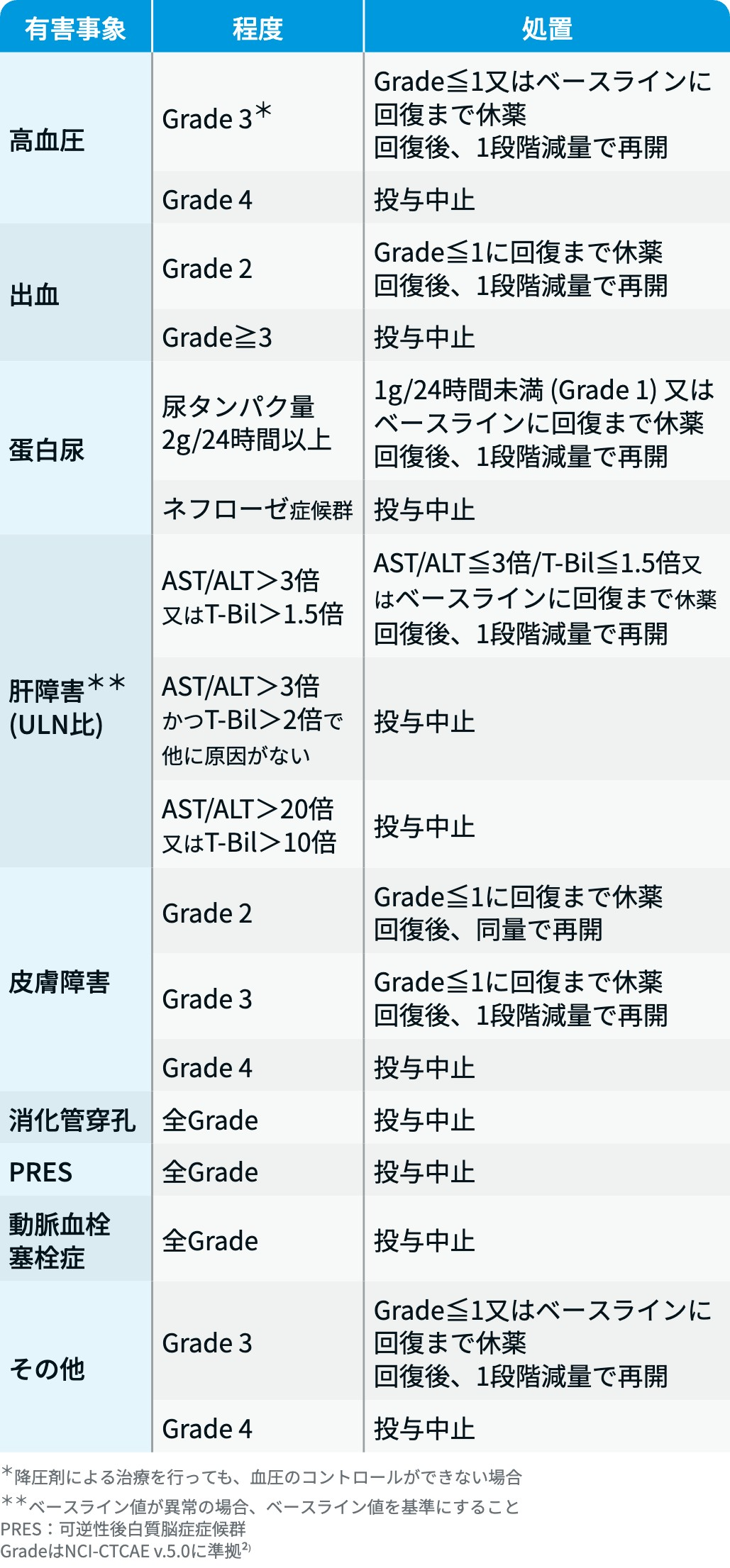
フリュザクラ®電子添文¹⁾を元に編集部作成
FRESCO-2試験³⁾では、 以下の有害事象に対する対応も規定されていた。

FRESCO-2試験³⁾のプロトコルを基に編集部作成
レジメンの特徴と注意点
🧑⚕️フルキンチニブは選択性の高い血管内皮増殖因子受容体 (VEGFR1–3) 阻害薬であり、 FRESCO-2試験でOSの有意な延長を示しました。 本邦のリアルワールドデータ*でも既報と同様の有効性に加え、 有害事象による中止率は2.9%と低く、 良好な忍容性が確認されています。 主な有害事象は蛋白尿、 高血圧、 手足症候群で、 46%に休薬・減量が必要とされ、 その7割以上が開始後4週以内に集中しています。 蛋白尿については、 前治療での蛋白尿の既往がある場合や、 血管新生阻害薬による前治療が長期間に及ぶ場合にとくに留意が必要であり、 早期の適切な用量管理 (休薬・減量) が治療継続の鍵となります。
神奈川県立がんセンター 大隅寛木先生
*石塚千紘ら. 切除不能・再発大腸癌に対するFruquintinibの安全性と有効性~多施設観察研究. 第104回大腸癌研究会 (O3-8).
作用機序の特徴
フルキンチニブは、 血管内皮増殖因子受容体 (VEGFR1、 2、 3) のキナーゼ活性を阻害して腫瘍血管新生を抑制し、 腫瘍増殖抑制作用を示すと考えられている。
レジメン適用時の注意事項
併用薬 : 本剤はCYP3A4で代謝されるため、 強いまたは中程度のCYP3A誘導薬 (リファンピシン、 フェニトイン、 カルバマゼピンなど) との併用で有効性が減弱するおそれがあり、 可能な限り併用を避けて代替薬を検討する。
高血圧 : 高血圧クリーゼを含む高血圧が現れることがあるため、 投与開始前および投与期間中は定期的に血圧を測定する。
蛋白尿 : 蛋白尿が現れることがあるため、 投与開始前および投与期間中は定期的に尿蛋白を観察する。
創傷治癒遅延 : 創傷治癒を遅らせる可能性があるため、 外科的処置が予定されている場合は処置前に投与を中断し、 処置後の投与再開は十分な創傷治癒を確認したうえで患者の状態に応じて判断する。
参考⁴⁾ : 大手術の2週間前から休薬し、 術後は少なくとも2週間は投与せず、 創部の十分な治癒を確認してから再開する (創傷治癒合併症が改善した後の再開安全性は未確立)。
RMP【重要な特定されたリスク】
フリュザクラ®医薬品リスク管理計画書 (RMP)
- 出血
- 高血圧
- 可逆性後白質脳症症候群
- 消化管穿孔
- 皮膚障害
- 静脈血栓塞栓症
- 動脈解離
出典
1) 武田薬品工業株式会社.フリュザクラカプセル1mg/5mg 電子添文 2026年2月改訂 第4版.
2) 武田薬品工業株式会社.フリュザクラカプセル1mg/5mg 適正使用の手引き. 2025年6月作成.
3) Lancet. 2023;402(10395):41-53.
4) Takeda Pharmaceuticals America, Inc. FRUZAQLA® (fruquintinib) capsules: Prescribing Information. Revised 2025年2月. (参照 2026年1月20日).
最終更新日 : 2026年2月12日
執筆 : 京都桂病院 薬剤科 塩飽英二
監修 : 神奈川県立がんセンター 消化器内科 (消化管) 部長 大隅寛木
Fruquintinib
本コンテンツは特定の治療法を推奨するものではありません。 個々の患者の病態や、 実際の薬剤情報やガイドラインを確認の上、 利用者の判断と責任でご利用ください。
薬剤情報
フリュザクラ®カプセル (フルキンチニブ)
武田薬品工業株式会社の外部サイトへ遷移します
投与スケジュール
【1コース】 28日間
【催吐性】最小度*
【FN発症】未報告**
*NCCN Guidelines Ver.2.2025 Antiemesis、 **FRESCO-2試験³⁾

1日1回5mgを3週間連日経口投与後に1週間休薬し、 これを1サイクルとして反復する。
飲み忘れは次回まで12時間以上なら気づいた時点で1回服用し、 12時間以内なら服用せず次回から再開し、 服用後に嘔吐しても追加服用しない。
レゴラフェニブ (REG) およびトリフルリジン・チピラシル (FTD/TPI) のいずれの治療歴もない患者では、 これらの薬剤による治療が困難な患者が投与対象
Key Data|臨床試験結果
📊 FRESCO-2試験
Lancet. 2023;402(10395):41-53.
標準治療 (フッ化ピリミジン系、 オキサリプラチン、 イリノテカン、 および抗VEGF/EGFR抗体) 歴を有し、 かつFTD/TPIまたはREG治療中に進行・不耐となった転移性結腸・直腸癌患者*を対象とした第III相無作為化比較試験。 フルキンチニブ群461例、 プラセボ群230例に2:1で割り付け、 主要評価項目はOSとした。
MSI-HまたはdMMR腫瘍を有する場合は免疫チェックポイント阻害剤治療歴があること、 またBRAF V600E変異腫瘍を有する場合はBRAF阻害剤による治療歴を有する患者が対象。
【有効性】フルキンチニブ群 (vs プラセボ群)
- OS中央値 7.4ヵ月 (vs 4.8ヵ月)
- HR 0.66 (95%CI 0.55–0.80、 p<0.001)
- PFS中央値 3.7ヵ月 (vs 1.8ヵ月)
- HR 0.32 (95%CI 0.27–0.39、 p<0.001)
- 客観的奏効率 2% (vs 0%)
- 病勢制御率 56% (vs 16%)
【安全性】主な有害事象 : 全Grade (Grade≧3)
- 高血圧 36.8% (13.6%)
- 無力症 34.0% (7.7%)
- 食欲減退 27.2% (2.4%)
- 下痢 24.1% (3.5%)
- 甲状腺機能低下症 20.6% (0.4%)
- 疲労 20.0% (3.9%)
- 手足症候群 19.3% (6.4%)
- 腹痛 18.2% (3.1%)
- 悪心 17.3% (0.7%)
- 蛋白尿 17.3% (1.8%)
- 便秘 17.1% (0.4%)
- 発声障害 16.2% (0%)
- 口内炎 14.7% (1.8%)
- 嘔吐 14.5% (1.5%)
- 粘膜炎症 13.6% (0.4%)
- 体重減少 12.3% (0.7%)
- 関節痛 11.0% (0.9%)
- AST増加 10.5% (2.2%)
- ALT増加 10.3% (3.1%)
- 背部痛 10.3% (1.3%)
- 発熱 10.1% (0.4%)
重点的評価 (AE of special interest) : 全Grade (Grade≧3)
- 高血圧 38.4% (14.0%)
- 皮膚毒性 34.4% (6.8%)
- 甲状腺機能障害 27.0% (0.4%)
- 肝機能異常 24.8% (0.8%)
- 感染症 21.1% (6.6%)
- 蛋白尿 17.5% (1.8%)
- 出血 14.3% (1.8%)
- 塞栓・血栓イベント 4.6% (3.1%)
- 消化管穿孔 3.5% (2.2%)
- 左室駆出率低下 1.1% (0.9%)
各プロトコル
適格基準
FRESCO-2試験³⁾の主な適格基準
- 18歳以上
- ECOG PS 0–1
- 好中球≧1500/mm³
- 血小板≧10万/mm³
- Hb≧9.0g/dL
- 肝機能 : T-Bil≦1.5×ULN、 AST/ALT≦2.5×ULN (肝転移は≦5.0×ULN)
- 腎機能 : Cre≦1.5×ULNまたはCrCl≧60mL/min
- 尿蛋白 : 尿定性試験<2+ または 24時間尿蛋白<1.0g
用量レベル

フリュザクラ®電子添文¹⁾を元に編集部作成
腎障害患者に対する用量調整
尿中未変化体排泄率は0.5%と低く、 腎クリアランスの寄与は小さいため、 腎障害時の用量調整は不要と考えられる。
フリュザクラ®電子添文¹⁾を元に編集部が評価
有害事象発現時の減量・休薬・中止基準

フリュザクラ®電子添文¹⁾を元に編集部作成
FRESCO-2試験³⁾では、 以下の有害事象に対する対応も規定されていた。

FRESCO-2試験³⁾のプロトコルを基に編集部作成
レジメンの特徴と注意点
🧑⚕️フルキンチニブは選択性の高い血管内皮増殖因子受容体 (VEGFR1–3) 阻害薬であり、 FRESCO-2試験でOSの有意な延長を示しました。 本邦のリアルワールドデータ*でも既報と同様の有効性に加え、 有害事象による中止率は2.9%と低く、 良好な忍容性が確認されています。 主な有害事象は蛋白尿、 高血圧、 手足症候群で、 46%に休薬・減量が必要とされ、 その7割以上が開始後4週以内に集中しています。 蛋白尿については、 前治療での蛋白尿の既往がある場合や、 血管新生阻害薬による前治療が長期間に及ぶ場合にとくに留意が必要であり、 早期の適切な用量管理 (休薬・減量) が治療継続の鍵となります。
神奈川県立がんセンター 大隅寛木先生
*石塚千紘ら. 切除不能・再発大腸癌に対するFruquintinibの安全性と有効性~多施設観察研究. 第104回大腸癌研究会 (O3-8).
作用機序の特徴
フルキンチニブは、 血管内皮増殖因子受容体 (VEGFR1、 2、 3) のキナーゼ活性を阻害して腫瘍血管新生を抑制し、 腫瘍増殖抑制作用を示すと考えられている。
レジメン適用時の注意事項
併用薬 : 本剤はCYP3A4で代謝されるため、 強いまたは中程度のCYP3A誘導薬 (リファンピシン、 フェニトイン、 カルバマゼピンなど) との併用で有効性が減弱するおそれがあり、 可能な限り併用を避けて代替薬を検討する。
高血圧 : 高血圧クリーゼを含む高血圧が現れることがあるため、 投与開始前および投与期間中は定期的に血圧を測定する。
蛋白尿 : 蛋白尿が現れることがあるため、 投与開始前および投与期間中は定期的に尿蛋白を観察する。
創傷治癒遅延 : 創傷治癒を遅らせる可能性があるため、 外科的処置が予定されている場合は処置前に投与を中断し、 処置後の投与再開は十分な創傷治癒を確認したうえで患者の状態に応じて判断する。
参考⁴⁾ : 大手術の2週間前から休薬し、 術後は少なくとも2週間は投与せず、 創部の十分な治癒を確認してから再開する (創傷治癒合併症が改善した後の再開安全性は未確立)。
RMP【重要な特定されたリスク】
フリュザクラ®医薬品リスク管理計画書 (RMP)
- 出血
- 高血圧
- 可逆性後白質脳症症候群
- 消化管穿孔
- 皮膚障害
- 静脈血栓塞栓症
- 動脈解離
出典
1) 武田薬品工業株式会社.フリュザクラカプセル1mg/5mg 電子添文 2026年2月改訂 第4版.
2) 武田薬品工業株式会社.フリュザクラカプセル1mg/5mg 適正使用の手引き. 2025年6月作成.
3) Lancet. 2023;402(10395):41-53.
4) Takeda Pharmaceuticals America, Inc. FRUZAQLA® (fruquintinib) capsules: Prescribing Information. Revised 2025年2月. (参照 2026年1月20日).
最終更新日 : 2026年2月12日
執筆 : 京都桂病院 薬剤科 塩飽英二
監修 : 神奈川県立がんセンター 消化器内科 (消化管) 部長 大隅寛木
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
がん薬物療法における治療計画をまとめたものです。
主要論文や適正使用ガイドをもとにした用量調整プロトコール、 有害事象対応をご紹介します。
なお、 本ツールは医師向けの教育用資料であり、 実臨床での使用は想定しておりません。 最新の添付文書やガイドラインを必ずご確認下さい。
また、 一般の方への情報提供ではないことを予めご了承ください。