本コンテンツは特定の治療法を推奨するものではありません。 個々の患者の病態や、 実際の薬剤情報やガイドラインを確認の上、 利用者の判断と責任でご利用ください。
薬剤情報
ハイカムチン®注射用 (ノギテカン)
*日本化薬株式会社の外部サイトへ遷移します
投与スケジュール
【1コース】3週間
【催吐性】 軽度催吐性
【FN発症】高リスク (>20%)
JCOG0605試験¹⁾のプロトコル
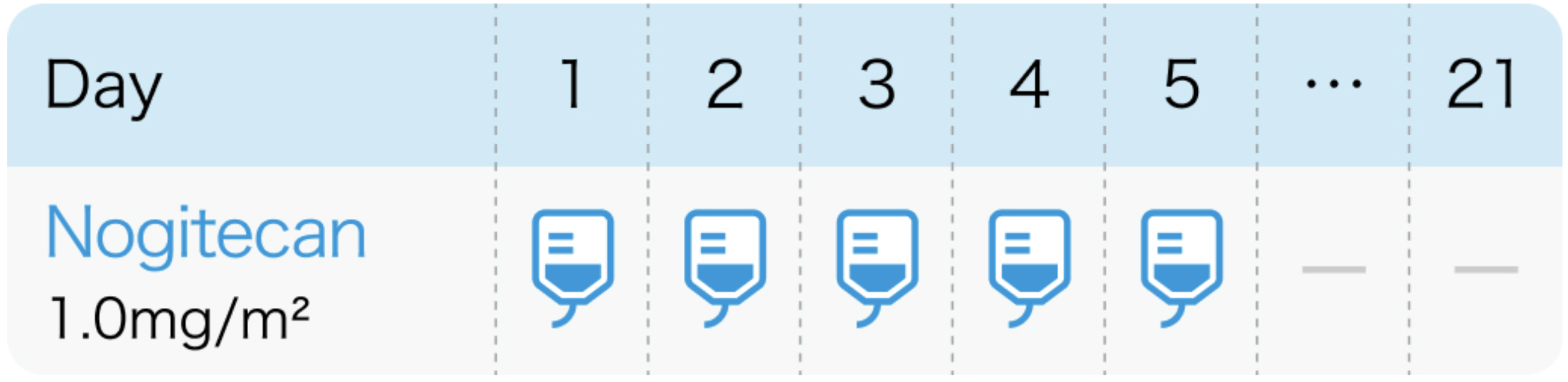
ノギテカン1日1回1.0mg/㎡ (体表面積) を5日間連日点滴静注し、 少なくとも16日間休薬する
Lancet Oncol. 2016 Aug;17(8):1147-1157. より引用
前投薬 : デキサメタゾン3.3~6.6mg 静注 (4~8mg経口) 単剤投与。 状況に応じてプロクロルペラジンもしくはメトクロプラミドの使用やロラゼパムやH2受容体拮抗薬あるいはプロトンポンプ阻害薬の併用も検討
KeyData|臨床試験結果
JCOG0605試験¹⁾ >>詳しくみる
初回化学療法もしくは初回化学放射線療法が奏効し、 治療終了後90日以降に再発 (sensitive relapse) した小細胞肺癌に対してノギテカン療法 (NGT療法)に対する、 シスプラチン+エトポシド+イリノテカン療法 (PEI療法) の優越性を検証する第Ⅲ相ランダム化比較試験
【有効性】NGT療法群の結果
- ORR 27%
- mPFS 3.6ヵ月
- mOS 12.5ヵ月
【安全性】主な有害事象 (括弧内はGrade3~4)
- 好中球数減少 100% (85.6%)
- 白血球数減少 98.9% (51.1%)
- 貧血 88.9% (27.8%)
- 血小板数減少 77.8% (27.8%)
- ALT上昇 36.7% (1.1%)
- AST上昇 25.6% (0%)
- 悪心 45.6% (2.2%)
- 便秘 41.1% (1.1%)
- 倦怠感 37.8% (1.1%)
- 発熱 15.6% (1.1%)
- 下痢 13.3% (0%)
- 嘔吐 8.9% (0%)
- 粘膜炎 (臨床検査) 7.8% (0%)
- 粘膜炎 (機能性または症候性) 6.7% (0%)
- 脱毛症 27.8% (0%)
👨⚕️監修医師コメント : 欧米における2次治療の標準レジメン (*投与量が国内外で異なる) だが、 国内ではAmrubicin (AMR) が主流である。
各プロトコル
以下はJCOG0605試験¹⁾より抜粋
投与開始基準
20~75歳で、 組織学的または細胞学的に小細胞肺癌が確認され、 プラチナ製剤をベースとした一次化学療法または放射線療法が奏効した以下に該当する患者
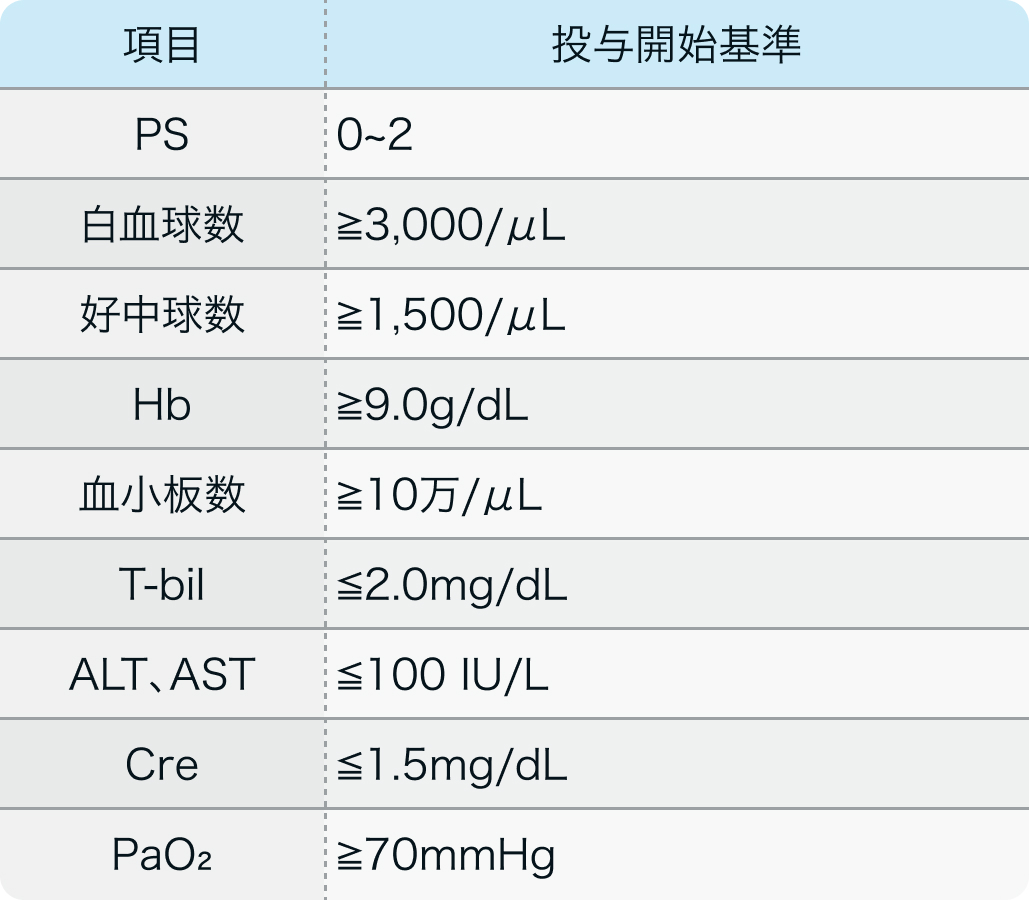
Lancet Oncol. 2016 Aug;17(8):1147-1157. より引用
増量・減量基準
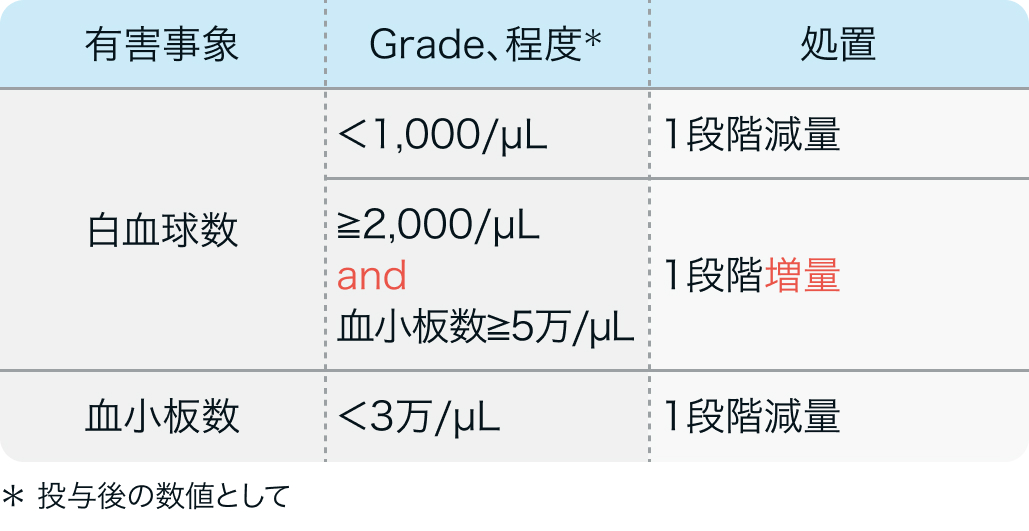
初回基準量と増減量レベル

Lancet Oncol. 2016 Aug;17(8):1147-1157. より引用
特徴と注意点
肺癌診療ガイドライン2025の推奨²⁾
PS 0–2の再発小細胞肺癌 (sensitive relapse*) に対しては、 本レジメン、 AMR単剤療法、 PEI療法 (CDDP+ETP+CPT-11)、 CE療法 (CBDCA+ETP) が強く推奨されている [1A]。
*「sensitive relapse」は初回薬物療法が奏効し、 かつ初回治療終了後から再発までの期間が長い場合 (60~90日以上が多い)、「refractory relapse」はそれ以外の場合と定義されることが多い。 前者の方が、 再発時の薬物療法の効果が高い。
👨⚕️監修医師コメント : 欧米における2次治療の標準レジメン (*投与量が国内外で異なる) だが、 国内ではAmrubicin (AMR) が主流である。
出典
2) 日本肺癌学会. 肺癌診療ガイドライン-胸膜中皮腫・ 胸腺腫瘍含む-2025年版
最終更新日 : 2025年11月14日
監修医師 : HOKUTO編集部医師監修
Nogitecan
本コンテンツは特定の治療法を推奨するものではありません。 個々の患者の病態や、 実際の薬剤情報やガイドラインを確認の上、 利用者の判断と責任でご利用ください。
薬剤情報
ハイカムチン®注射用 (ノギテカン)
*日本化薬株式会社の外部サイトへ遷移します
投与スケジュール
【1コース】3週間
【催吐性】 軽度催吐性
【FN発症】高リスク (>20%)
JCOG0605試験¹⁾のプロトコル

ノギテカン1日1回1.0mg/㎡ (体表面積) を5日間連日点滴静注し、 少なくとも16日間休薬する
Lancet Oncol. 2016 Aug;17(8):1147-1157. より引用
前投薬 : デキサメタゾン3.3~6.6mg 静注 (4~8mg経口) 単剤投与。 状況に応じてプロクロルペラジンもしくはメトクロプラミドの使用やロラゼパムやH2受容体拮抗薬あるいはプロトンポンプ阻害薬の併用も検討
KeyData|臨床試験結果
JCOG0605試験¹⁾ >>詳しくみる
初回化学療法もしくは初回化学放射線療法が奏効し、 治療終了後90日以降に再発 (sensitive relapse) した小細胞肺癌に対してノギテカン療法 (NGT療法)に対する、 シスプラチン+エトポシド+イリノテカン療法 (PEI療法) の優越性を検証する第Ⅲ相ランダム化比較試験
【有効性】NGT療法群の結果
- ORR 27%
- mPFS 3.6ヵ月
- mOS 12.5ヵ月
【安全性】主な有害事象 (括弧内はGrade3~4)
- 好中球数減少 100% (85.6%)
- 白血球数減少 98.9% (51.1%)
- 貧血 88.9% (27.8%)
- 血小板数減少 77.8% (27.8%)
- ALT上昇 36.7% (1.1%)
- AST上昇 25.6% (0%)
- 悪心 45.6% (2.2%)
- 便秘 41.1% (1.1%)
- 倦怠感 37.8% (1.1%)
- 発熱 15.6% (1.1%)
- 下痢 13.3% (0%)
- 嘔吐 8.9% (0%)
- 粘膜炎 (臨床検査) 7.8% (0%)
- 粘膜炎 (機能性または症候性) 6.7% (0%)
- 脱毛症 27.8% (0%)
👨⚕️監修医師コメント : 欧米における2次治療の標準レジメン (*投与量が国内外で異なる) だが、 国内ではAmrubicin (AMR) が主流である。
各プロトコル
以下はJCOG0605試験¹⁾より抜粋
投与開始基準
20~75歳で、 組織学的または細胞学的に小細胞肺癌が確認され、 プラチナ製剤をベースとした一次化学療法または放射線療法が奏効した以下に該当する患者

Lancet Oncol. 2016 Aug;17(8):1147-1157. より引用
増量・減量基準

初回基準量と増減量レベル

Lancet Oncol. 2016 Aug;17(8):1147-1157. より引用
特徴と注意点
肺癌診療ガイドライン2025の推奨²⁾
PS 0–2の再発小細胞肺癌 (sensitive relapse*) に対しては、 本レジメン、 AMR単剤療法、 PEI療法 (CDDP+ETP+CPT-11)、 CE療法 (CBDCA+ETP) が強く推奨されている [1A]。
*「sensitive relapse」は初回薬物療法が奏効し、 かつ初回治療終了後から再発までの期間が長い場合 (60~90日以上が多い)、「refractory relapse」はそれ以外の場合と定義されることが多い。 前者の方が、 再発時の薬物療法の効果が高い。
👨⚕️監修医師コメント : 欧米における2次治療の標準レジメン (*投与量が国内外で異なる) だが、 国内ではAmrubicin (AMR) が主流である。
出典
2) 日本肺癌学会. 肺癌診療ガイドライン-胸膜中皮腫・ 胸腺腫瘍含む-2025年版
最終更新日 : 2025年11月14日
監修医師 : HOKUTO編集部医師監修
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
がん薬物療法における治療計画をまとめたものです。
主要論文や適正使用ガイドをもとにした用量調整プロトコール、 有害事象対応をご紹介します。
なお、 本ツールは医師向けの教育用資料であり、 実臨床での使用は想定しておりません。 最新の添付文書やガイドラインを必ずご確認下さい。
また、 一般の方への情報提供ではないことを予めご了承ください。