本コンテンツは特定の治療法を推奨するものではありません。 個々の患者の病態や、 実際の薬剤情報やガイドラインを確認の上、 利用者の判断と責任でご利用ください。
薬剤情報
IL-2依存性ジフテリア毒素断片 デニロイキン ジフチトクス
*エーザイ株式会社の外部サイトへ遷移します
用法用量
電子添文¹⁾の用法および用量
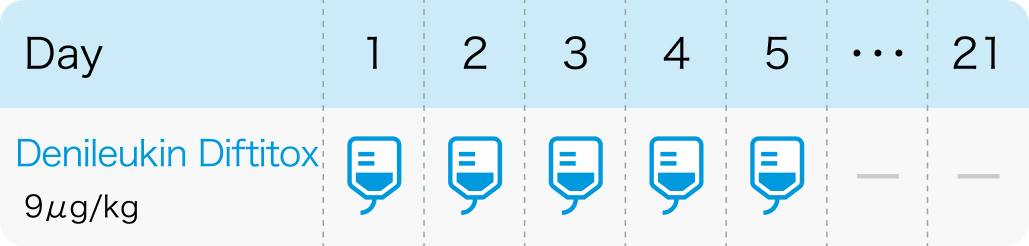
レミトロ®電子添文 (2023年7月改訂 第5版)¹⁾より作図
投与開始基準
E7777-J081-205試験³⁾のプロトコル
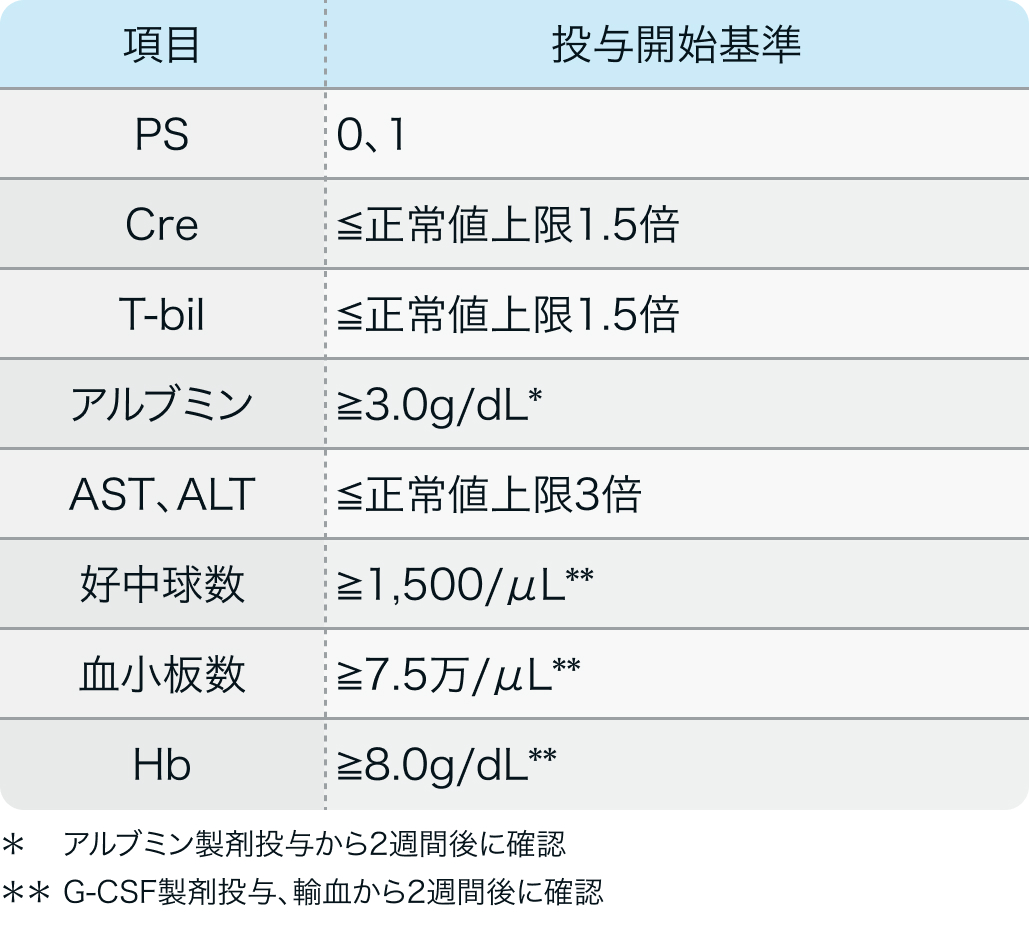
Cancer Sci. 2021 Jun;112(6):2426-2435³⁾より作図
減量・休薬・中止基準
適正使用ガイド²⁾の基準

レミトロ®適正使用ガイド (2022年4月作成)より作図
初回基準量と減量レベル
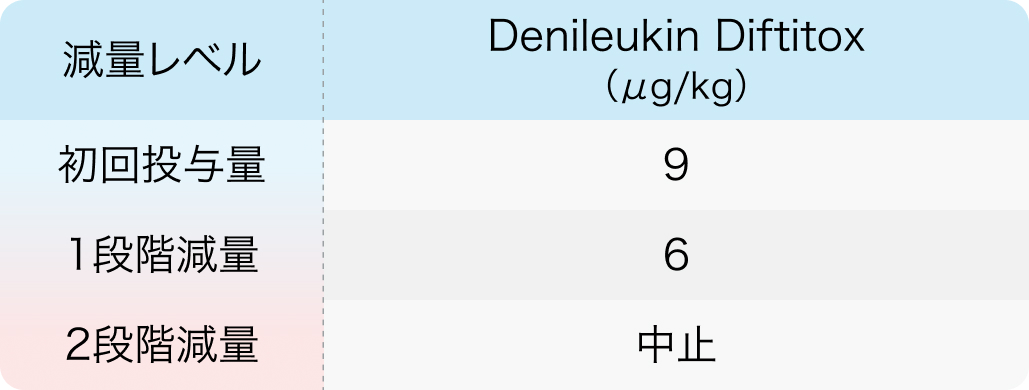
レミトロ®適正使用ガイド (2022年4月作成)より作図
エキスパートのワンポイント
どのような患者で選択されるレジメンか、同ライン薬剤との比較
承認が現時点での皮膚リンパ腫ガイドライン (2020年版) 作成後であったこともあり、 ガイドラインのアルゴリズムには入っていない。
保険適応は再発または難治性の末梢性T細胞リンパ腫/皮膚T細胞リンパ腫であるが、 皮膚科領域ではskin directed therapy抵抗性の進行期菌状息肉症においてsecond line以降 (一般的にはthird line以降) に用いられることが多い。
レジメンの用法および用量、減量・休薬・中止基準について実臨床での対応
1日1回9μg/kgを1時間かけて5日間点滴静注した後、 16日間休薬する。 この21日間を1サイクルとして、 最大8サイクル投与を繰り返す。
各サイクルの第2~5日目の投与開始前にGrade 3以上の副作用が認められた場合、 Grade 2以下 (低Alb血症はGrade 1以下) に回復するまで休薬する。 回復後は、 同一用量で再開することができる副作用等により、 2サイクル連続で次サイクルの投与を延期した場合、 6μg/kgに減量する。
生命を脅かす重篤な副作用が認められた場合、 次サイクル開始予定日より21日を超えて投与を再開できない場合、 6μg/kgに減量後、 さらに減量が必要な場合は投与を中止する。
過去の主要な臨床試験名と、その有効性および安全性の解釈について
国内第II相試験 (E7777-J081-205) では17例の末梢性T細胞リンパ腫と19例の皮膚T細胞リンパ腫の患者が登録された。 皮膚T細胞リンパ腫では奏効例は6例 (31.6%) であった。 菌状息肉症に限っては12例中5例 (41.7%) で奏効が得られた。 無増悪奏効期間は4.2ヵ月であった。 皮膚T細胞リンパ腫群における副作用は低Alb血症を73.7%(Grade3以上は5.3%)認め、 毛細血管漏出症候群も26.3% (Grade3以上は21.1%) 認めている。
因果関係は不明だが、 本試験で毛細血管漏出症候群を呈したのは全例皮膚T細胞リンパ腫群であった。 他の頻度の高い副作用としてAST/ALT高値、 リンパ球減少、 倦怠感、 発熱などであった。
RMP【重要な特定されたリスク】
RMP : 医薬品リスク管理計画書
- 毛細血管漏出症候群
- 横紋筋融解症
- 視力障害・色覚異常
- 肝機能障害
- 骨髄抑制
- 感染症
- Infusion reaction
- 虚血性心疾患・不整脈・心不全
- 重度の皮膚障害
特徴的な副作用について
本剤に特徴的な副作用として、 毛細血管漏出症候群、 横紋筋融解、 視力障害、 色覚異常がある。
毛細血管漏出症候群
本剤の投与開始前及び投与期間中は定期的に血清Alb値、 血圧、 脈拍、 体重の測定を行う必要がある。 特にAlb値に関してはサイクル開始前に3.0g/dL未満であった場合、 投与を延期する必要がある。
横紋筋融解症
本剤の投与開始前及び投与期間中は定期的にCK、 クレアチニン等の検査を行い、 筋力低下、 筋肉痛、 CK上昇、 血中及び尿中ミオグロビン上昇等の観察を十分に行う。
視力障害、 色覚異常
本剤の投与開始前及び投与期間中は定期的に眼科検査を実施し、 患者の状態を十分に観察する必要がある。
主な有害事象
E7777-J081-205試験³⁾
- リンパ球数減少 70.3% (56.8%)
- 血小板数減少 35.1% (16.2%)
- 貧血 13.5% (5.4%)
- 白血球数増加 10.8% (0%)
- 白血球数減少 10.8% (2.7%)
- 好中球数減少 5.4% (5.4%)
- 便秘 37.8% (0%)
- 悪心 29.7% (0%)
- 嘔吐 18.9% (0%)
- 発熱 51.4% (0%)
Cancer Sci. 2021 Jun;112(6):2426-2435³⁾より引用
出典
- エーザイ株式会社. レミトロ®電子添文 (2025年5月改訂 第7版) [最終閲覧 : 2025/6/13]
- エーザイ株式会社. レミトロ®適正使用ガイド (2025年4月作成) [最終閲覧 : 2025/6/13]
- Cancer Sci. 2021;112(6):2426-2435.
- 皮膚悪性腫瘍ガイドライン第3版 皮膚リンパ腫診療ガイドライン2020. 公益社団法人日本皮膚科学会 [最終閲覧 : 2024/5/20]
最終更新日 : 2025年6月13日
監修医師 : 近畿大学皮膚科 藤井 一恭先生
Denileukin Diftitox
本コンテンツは特定の治療法を推奨するものではありません。 個々の患者の病態や、 実際の薬剤情報やガイドラインを確認の上、 利用者の判断と責任でご利用ください。
薬剤情報
IL-2依存性ジフテリア毒素断片 デニロイキン ジフチトクス
*エーザイ株式会社の外部サイトへ遷移します
用法用量
電子添文¹⁾の用法および用量

レミトロ®電子添文 (2023年7月改訂 第5版)¹⁾より作図
投与開始基準
E7777-J081-205試験³⁾のプロトコル

Cancer Sci. 2021 Jun;112(6):2426-2435³⁾より作図
減量・休薬・中止基準
適正使用ガイド²⁾の基準

レミトロ®適正使用ガイド (2022年4月作成)より作図
初回基準量と減量レベル

レミトロ®適正使用ガイド (2022年4月作成)より作図
エキスパートのワンポイント
どのような患者で選択されるレジメンか、同ライン薬剤との比較
承認が現時点での皮膚リンパ腫ガイドライン (2020年版) 作成後であったこともあり、 ガイドラインのアルゴリズムには入っていない。
保険適応は再発または難治性の末梢性T細胞リンパ腫/皮膚T細胞リンパ腫であるが、 皮膚科領域ではskin directed therapy抵抗性の進行期菌状息肉症においてsecond line以降 (一般的にはthird line以降) に用いられることが多い。
レジメンの用法および用量、減量・休薬・中止基準について実臨床での対応
1日1回9μg/kgを1時間かけて5日間点滴静注した後、 16日間休薬する。 この21日間を1サイクルとして、 最大8サイクル投与を繰り返す。
各サイクルの第2~5日目の投与開始前にGrade 3以上の副作用が認められた場合、 Grade 2以下 (低Alb血症はGrade 1以下) に回復するまで休薬する。 回復後は、 同一用量で再開することができる副作用等により、 2サイクル連続で次サイクルの投与を延期した場合、 6μg/kgに減量する。
生命を脅かす重篤な副作用が認められた場合、 次サイクル開始予定日より21日を超えて投与を再開できない場合、 6μg/kgに減量後、 さらに減量が必要な場合は投与を中止する。
過去の主要な臨床試験名と、その有効性および安全性の解釈について
国内第II相試験 (E7777-J081-205) では17例の末梢性T細胞リンパ腫と19例の皮膚T細胞リンパ腫の患者が登録された。 皮膚T細胞リンパ腫では奏効例は6例 (31.6%) であった。 菌状息肉症に限っては12例中5例 (41.7%) で奏効が得られた。 無増悪奏効期間は4.2ヵ月であった。 皮膚T細胞リンパ腫群における副作用は低Alb血症を73.7%(Grade3以上は5.3%)認め、 毛細血管漏出症候群も26.3% (Grade3以上は21.1%) 認めている。
因果関係は不明だが、 本試験で毛細血管漏出症候群を呈したのは全例皮膚T細胞リンパ腫群であった。 他の頻度の高い副作用としてAST/ALT高値、 リンパ球減少、 倦怠感、 発熱などであった。
RMP【重要な特定されたリスク】
RMP : 医薬品リスク管理計画書
- 毛細血管漏出症候群
- 横紋筋融解症
- 視力障害・色覚異常
- 肝機能障害
- 骨髄抑制
- 感染症
- Infusion reaction
- 虚血性心疾患・不整脈・心不全
- 重度の皮膚障害
特徴的な副作用について
本剤に特徴的な副作用として、 毛細血管漏出症候群、 横紋筋融解、 視力障害、 色覚異常がある。
毛細血管漏出症候群
本剤の投与開始前及び投与期間中は定期的に血清Alb値、 血圧、 脈拍、 体重の測定を行う必要がある。 特にAlb値に関してはサイクル開始前に3.0g/dL未満であった場合、 投与を延期する必要がある。
横紋筋融解症
本剤の投与開始前及び投与期間中は定期的にCK、 クレアチニン等の検査を行い、 筋力低下、 筋肉痛、 CK上昇、 血中及び尿中ミオグロビン上昇等の観察を十分に行う。
視力障害、 色覚異常
本剤の投与開始前及び投与期間中は定期的に眼科検査を実施し、 患者の状態を十分に観察する必要がある。
主な有害事象
E7777-J081-205試験³⁾
- リンパ球数減少 70.3% (56.8%)
- 血小板数減少 35.1% (16.2%)
- 貧血 13.5% (5.4%)
- 白血球数増加 10.8% (0%)
- 白血球数減少 10.8% (2.7%)
- 好中球数減少 5.4% (5.4%)
- 便秘 37.8% (0%)
- 悪心 29.7% (0%)
- 嘔吐 18.9% (0%)
- 発熱 51.4% (0%)
Cancer Sci. 2021 Jun;112(6):2426-2435³⁾より引用
出典
- エーザイ株式会社. レミトロ®電子添文 (2025年5月改訂 第7版) [最終閲覧 : 2025/6/13]
- エーザイ株式会社. レミトロ®適正使用ガイド (2025年4月作成) [最終閲覧 : 2025/6/13]
- Cancer Sci. 2021;112(6):2426-2435.
- 皮膚悪性腫瘍ガイドライン第3版 皮膚リンパ腫診療ガイドライン2020. 公益社団法人日本皮膚科学会 [最終閲覧 : 2024/5/20]
最終更新日 : 2025年6月13日
監修医師 : 近畿大学皮膚科 藤井 一恭先生
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
がん薬物療法における治療計画をまとめたものです。
主要論文や適正使用ガイドをもとにした用量調整プロトコール、 有害事象対応をご紹介します。
なお、 本ツールは医師向けの教育用資料であり、 実臨床での使用は想定しておりません。 最新の添付文書やガイドラインを必ずご確認下さい。
また、 一般の方への情報提供ではないことを予めご了承ください。