本コンテンツは特定の治療法を推奨するものではありません。 個々の患者の病態や、 実際の薬剤情報やガイドラインを確認の上、 利用者の判断と責任でご利用ください。
薬剤情報
【催吐性】 中等度催吐性
*エーザイ株式会社の外部サイトへ遷移します
*MSD製薬の外部サイトへ遷移します
用法用量
電子添文¹⁾³⁾、 KEYNOTE-775試験⁵⁾プロトコル
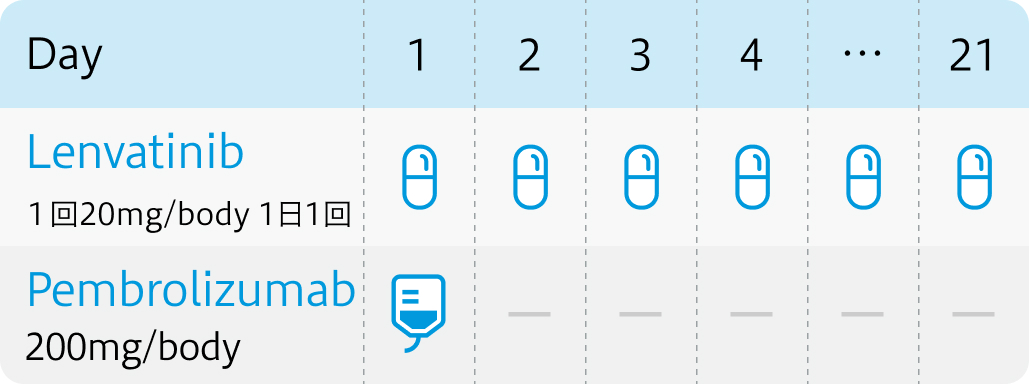
レンビマ®電子添文 (2024年2月改訂 第5版)¹⁾およびキイトルーダ®電子添文 (2024年1月改訂 第17版)³⁾より作図
※ペムブロリズマブ400mg 6週間ごと投与も可
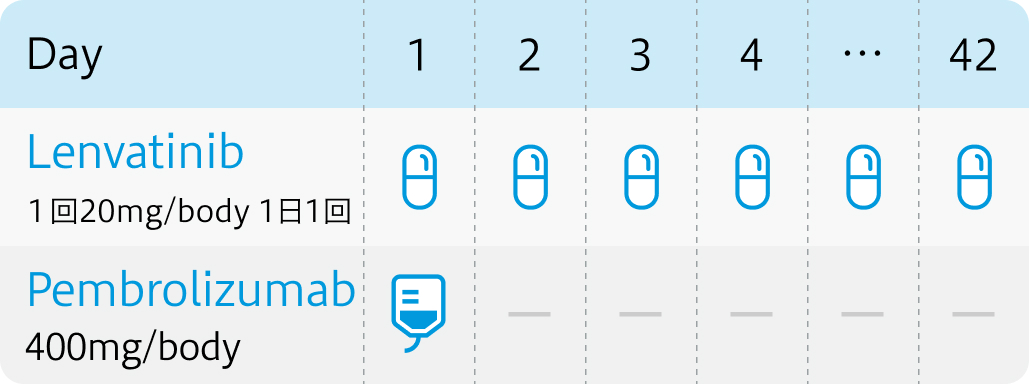
レンビマ®電子添文 (2024年2月改訂 第5版)¹⁾およびキイトルーダ®電子添文 (2024年1月改訂 第17版)³⁾より作図
前投薬・投与スケジュール例
前投薬は不要である
- ペムブロリズマブ+生食100ml (30分)
日本医科大学 武蔵小杉病院 腫瘍内科教授 勝俣 範之先生提供
投与開始基準
KEYNOTE-775試験⁵⁾のプロトコル
プラチナ製剤を含む化学療法歴のある切除不能な進行・再発の子宮体癌患者
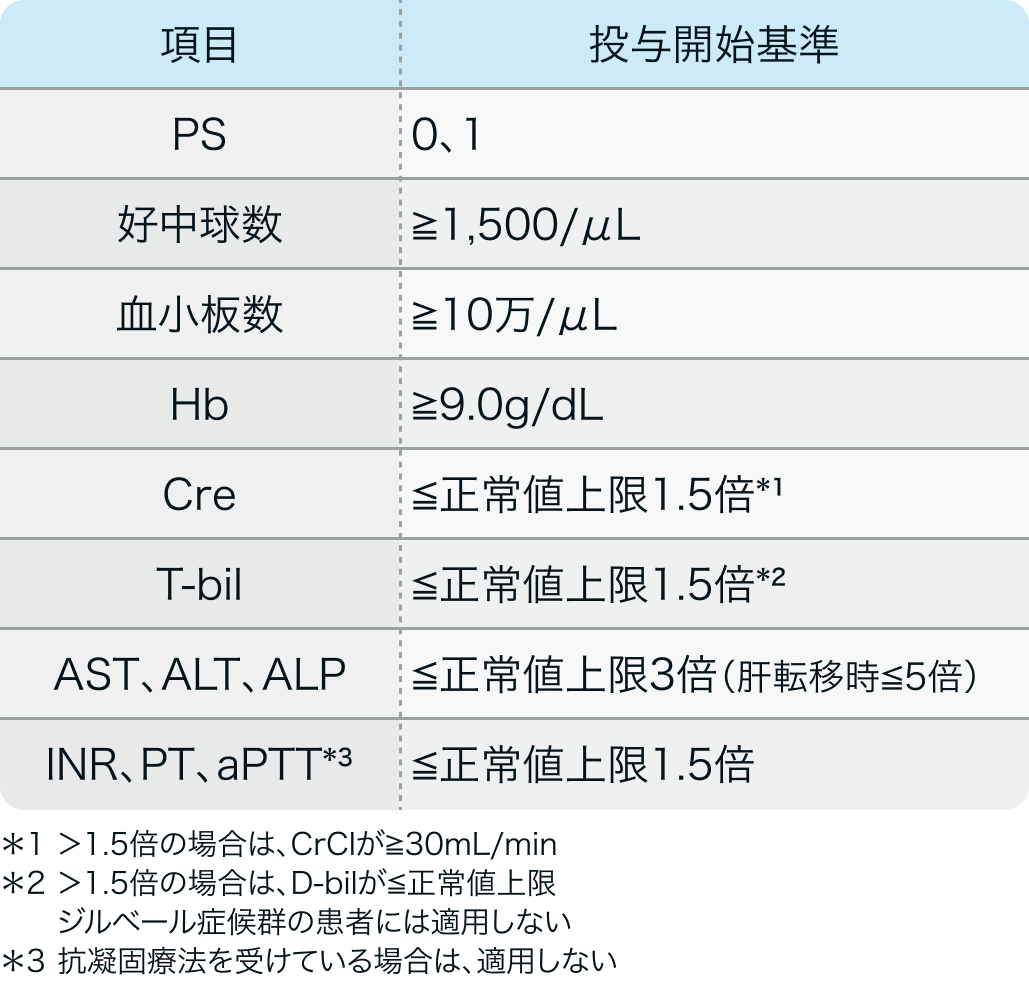
N Engl J Med. 2022 Feb 3;386(5):437-448⁵⁾より作図
減量・休薬・中止基準
レンバチニブ電子添文¹⁾の基準
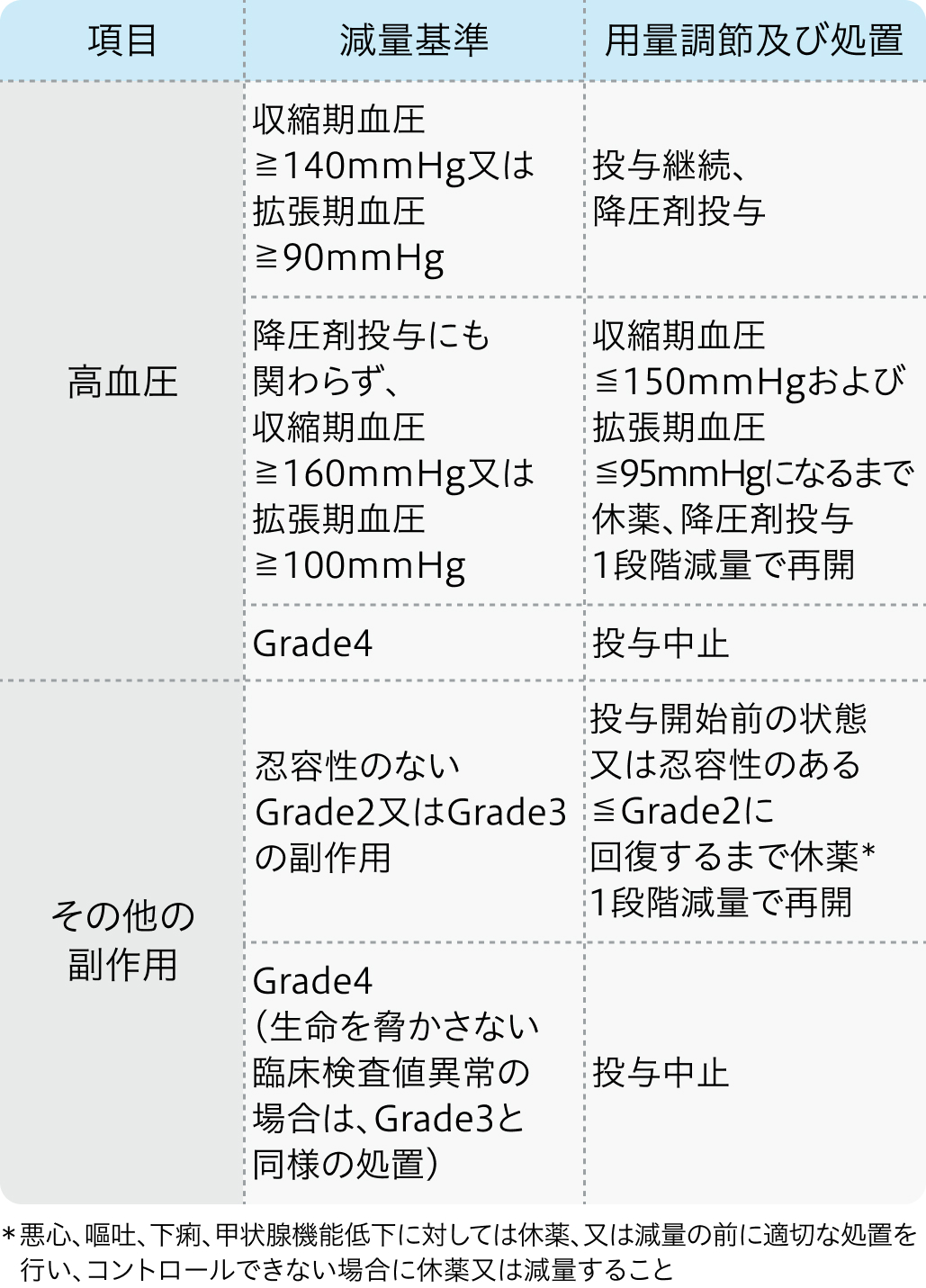
レンビマ®電子添文 (2024年2月改訂 第5版)¹⁾より作図
初回基準量と減量レベル
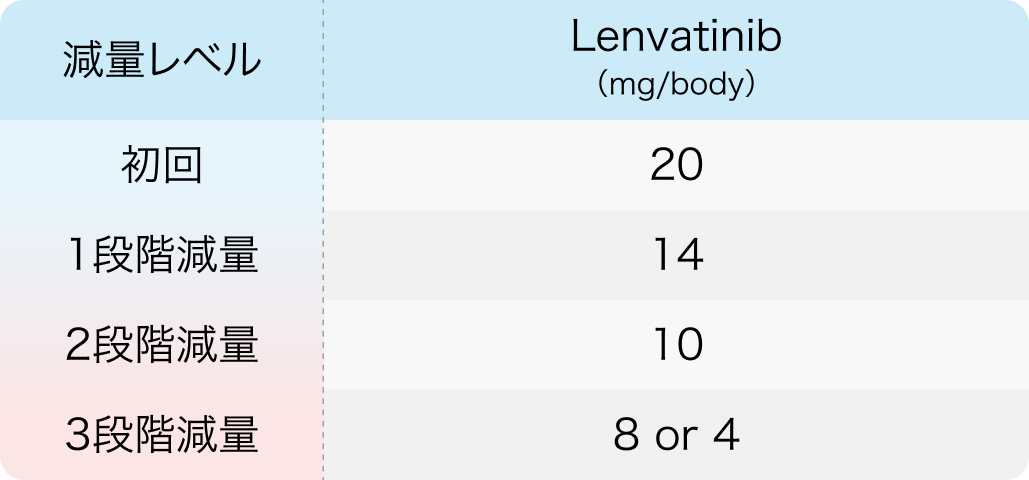
レンビマ®電子添文 (2024年2月改訂 第5版)¹⁾より作図
ペムブロリズマブ電子添文³⁾の基準

キイトルーダ®電子添文 (2024年1月改訂 第17版)³⁾より作図
KeyData|臨床試験結果
KEYNOTE-775試験⁵⁾
対象: プラチナ製剤を含む化学療法歴のある進行・再発の子宮体癌患者827例
方法: Lenvatinib + Pembrolizumab群 vs 化学療法群
【有効性】Lenvatinib + Pembrolizumab群
- ORR 31.9%
- mPFS 7.2ヵ月
- mOS 18.3ヵ月
【安全性】主な有害事象 (カッコ内 Grade3~4)
- 高血圧 64.0% (37.9%)
- 甲状腺機能低下症 57.4% (1.2%)
- 下痢 54.2% (7.6%)
- 悪心 49.5% (3.4%)
- 食欲低下 44.8% (7.9%)
- 嘔吐 36.7% (2.7%)
- 体重減少 34.0% (10.3%)
- 倦怠感 33.0% (5.2%)
- 蛋白尿 28.8% (5.4%)
- 貧血 26.1% (6.2%)
- 便秘 25.9% (0.7%)
- 好中球数減少 7.4% (1.7%)
- 脱毛症 5.4% (0%)
N Engl J Med. 2022 Feb 3;386(5):437-448⁵⁾より引用
エキスパートによるワンポイント
Lenvatinib+Pembrolizumabとは
進行子宮体癌の二次療法 (プラチナ前投与歴のある) で、 化学療法と比較して、 OS (全生存期間) で優り⁵⁾、 承認されたレジメンです [KEYNOTE-775試験]。 子宮体癌に対しては、 初めての免疫チェックポイント阻害剤の承認となりました。
KEYNOTE-775試験 OSのKaplan-Meier曲線
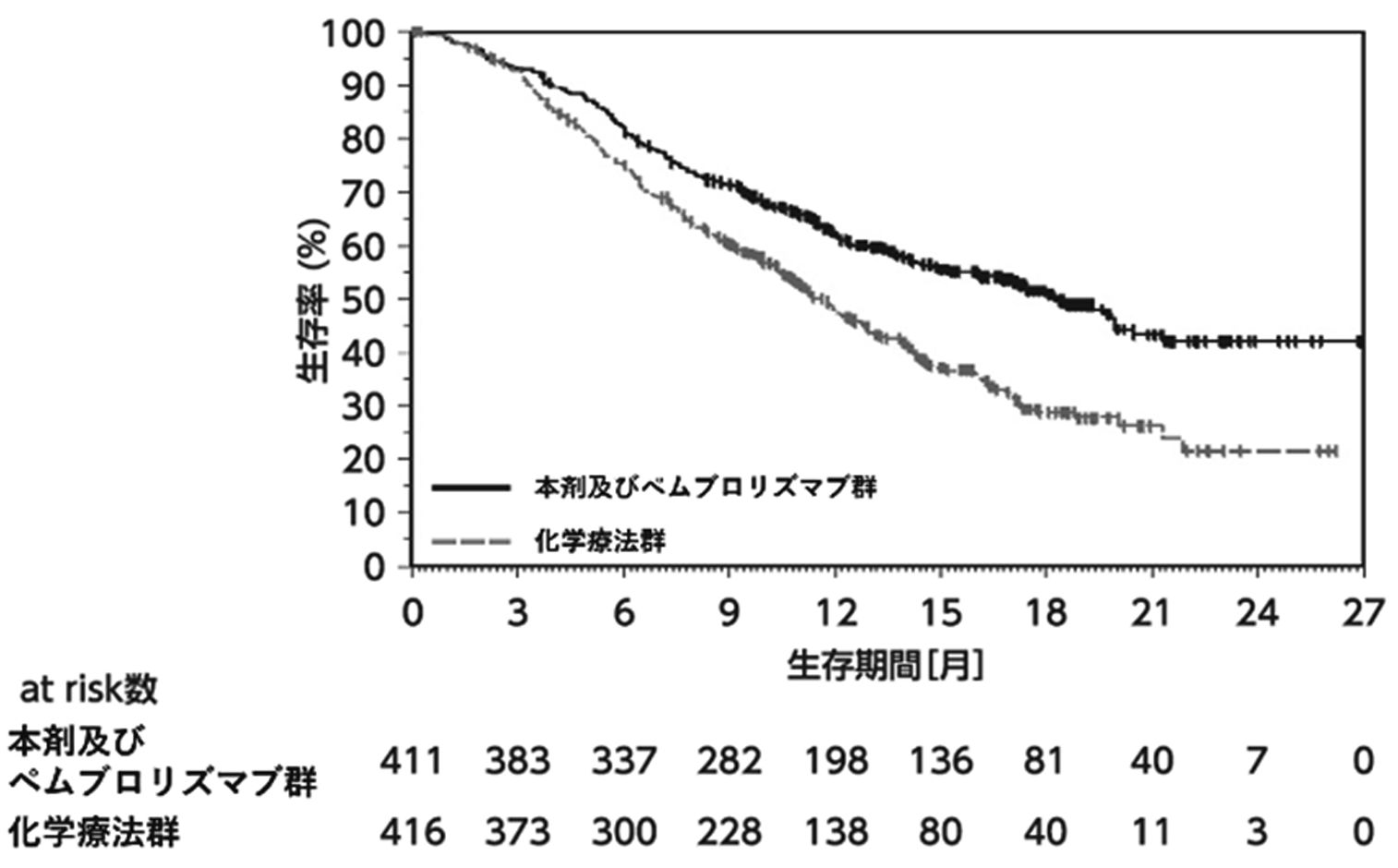
レンビマ®電子添文 (2024年2月改訂 第5版)¹⁾より引用
dMMR (MSI-high) に、 レンバチニブの追加が必要になるか
MSI-high腫瘍に対しては、 ペムブロリズマブ単剤でも高い奏効率(53%)が得られますが⁶⁾、 KEYNOTE-775試験⁵⁾では、 dMMR, pMMR (MSI-stable) の両者に奏効が認められています。
dMMRに、 ベネフィットが高い傾向がありました (HR=0.37、 95%CI 0.22-0.62) ので、 レンバチニブの投与のリスクが少ない患者 (血栓の既往、 重症脳、 心疾患の合併症などがない) の場合には、 レンバチニブ追加も考慮すべきだと思います。
監修 : 日本医科大学 武蔵小杉病院 腫瘍内科教授 勝俣 範之先生
出典
- エーザイ株式会社. レンビマ®電子添文 (2024年2月改訂 第5版) [最終閲覧 : 2024/03/14]
- エーザイ株式会社. レンビマ®適正使用ガイド (2024年2月作成) [最終閲覧 : 2024/03/14]
- MSD製薬. キイトルーダ®電子添文 (2024年1月改訂 第17版) [最終閲覧 : 2024/03/14]
- MSD製薬. キイトルーダ®適正使用ガイド (2023年12月作成) [最終閲覧 : 2024/03/14]
- Lenvatinib plus Pembrolizumab for Advanced Endometrial Cancer. N Engl J Med. 2022 Feb 3;386(5):437-448. PMID: 35045221
- Mismatch repair deficiency predicts response of solid tumors to PD-1 blockade. Science. 2017 Jul 28;357(6349):409-413. PMID: 28596308
最終更新日 : 2024年8月3日
監修医師 : 日本医科大学 武蔵小杉病院 腫瘍内科教授 勝俣 範之先生
Lenvatinib + Pembrolizumab
本コンテンツは特定の治療法を推奨するものではありません。 個々の患者の病態や、 実際の薬剤情報やガイドラインを確認の上、 利用者の判断と責任でご利用ください。
薬剤情報
【催吐性】 中等度催吐性
*エーザイ株式会社の外部サイトへ遷移します
*MSD製薬の外部サイトへ遷移します
用法用量
電子添文¹⁾³⁾、 KEYNOTE-775試験⁵⁾プロトコル

レンビマ®電子添文 (2024年2月改訂 第5版)¹⁾およびキイトルーダ®電子添文 (2024年1月改訂 第17版)³⁾より作図
※ペムブロリズマブ400mg 6週間ごと投与も可

レンビマ®電子添文 (2024年2月改訂 第5版)¹⁾およびキイトルーダ®電子添文 (2024年1月改訂 第17版)³⁾より作図
前投薬・投与スケジュール例
前投薬は不要である
- ペムブロリズマブ+生食100ml (30分)
日本医科大学 武蔵小杉病院 腫瘍内科教授 勝俣 範之先生提供
投与開始基準
KEYNOTE-775試験⁵⁾のプロトコル
プラチナ製剤を含む化学療法歴のある切除不能な進行・再発の子宮体癌患者

N Engl J Med. 2022 Feb 3;386(5):437-448⁵⁾より作図
減量・休薬・中止基準
レンバチニブ電子添文¹⁾の基準

レンビマ®電子添文 (2024年2月改訂 第5版)¹⁾より作図
初回基準量と減量レベル

レンビマ®電子添文 (2024年2月改訂 第5版)¹⁾より作図
ペムブロリズマブ電子添文³⁾の基準

キイトルーダ®電子添文 (2024年1月改訂 第17版)³⁾より作図
KeyData|臨床試験結果
KEYNOTE-775試験⁵⁾
対象: プラチナ製剤を含む化学療法歴のある進行・再発の子宮体癌患者827例
方法: Lenvatinib + Pembrolizumab群 vs 化学療法群
【有効性】Lenvatinib + Pembrolizumab群
- ORR 31.9%
- mPFS 7.2ヵ月
- mOS 18.3ヵ月
【安全性】主な有害事象 (カッコ内 Grade3~4)
- 高血圧 64.0% (37.9%)
- 甲状腺機能低下症 57.4% (1.2%)
- 下痢 54.2% (7.6%)
- 悪心 49.5% (3.4%)
- 食欲低下 44.8% (7.9%)
- 嘔吐 36.7% (2.7%)
- 体重減少 34.0% (10.3%)
- 倦怠感 33.0% (5.2%)
- 蛋白尿 28.8% (5.4%)
- 貧血 26.1% (6.2%)
- 便秘 25.9% (0.7%)
- 好中球数減少 7.4% (1.7%)
- 脱毛症 5.4% (0%)
N Engl J Med. 2022 Feb 3;386(5):437-448⁵⁾より引用
エキスパートによるワンポイント
Lenvatinib+Pembrolizumabとは
進行子宮体癌の二次療法 (プラチナ前投与歴のある) で、 化学療法と比較して、 OS (全生存期間) で優り⁵⁾、 承認されたレジメンです [KEYNOTE-775試験]。 子宮体癌に対しては、 初めての免疫チェックポイント阻害剤の承認となりました。
KEYNOTE-775試験 OSのKaplan-Meier曲線

レンビマ®電子添文 (2024年2月改訂 第5版)¹⁾より引用
dMMR (MSI-high) に、 レンバチニブの追加が必要になるか
MSI-high腫瘍に対しては、 ペムブロリズマブ単剤でも高い奏効率(53%)が得られますが⁶⁾、 KEYNOTE-775試験⁵⁾では、 dMMR, pMMR (MSI-stable) の両者に奏効が認められています。
dMMRに、 ベネフィットが高い傾向がありました (HR=0.37、 95%CI 0.22-0.62) ので、 レンバチニブの投与のリスクが少ない患者 (血栓の既往、 重症脳、 心疾患の合併症などがない) の場合には、 レンバチニブ追加も考慮すべきだと思います。
監修 : 日本医科大学 武蔵小杉病院 腫瘍内科教授 勝俣 範之先生
出典
- エーザイ株式会社. レンビマ®電子添文 (2024年2月改訂 第5版) [最終閲覧 : 2024/03/14]
- エーザイ株式会社. レンビマ®適正使用ガイド (2024年2月作成) [最終閲覧 : 2024/03/14]
- MSD製薬. キイトルーダ®電子添文 (2024年1月改訂 第17版) [最終閲覧 : 2024/03/14]
- MSD製薬. キイトルーダ®適正使用ガイド (2023年12月作成) [最終閲覧 : 2024/03/14]
- Lenvatinib plus Pembrolizumab for Advanced Endometrial Cancer. N Engl J Med. 2022 Feb 3;386(5):437-448. PMID: 35045221
- Mismatch repair deficiency predicts response of solid tumors to PD-1 blockade. Science. 2017 Jul 28;357(6349):409-413. PMID: 28596308
最終更新日 : 2024年8月3日
監修医師 : 日本医科大学 武蔵小杉病院 腫瘍内科教授 勝俣 範之先生
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
がん薬物療法における治療計画をまとめたものです。
主要論文や適正使用ガイドをもとにした用量調整プロトコール、 有害事象対応をご紹介します。
なお、 本ツールは医師向けの教育用資料であり、 実臨床での使用は想定しておりません。 最新の添付文書やガイドラインを必ずご確認下さい。
また、 一般の方への情報提供ではないことを予めご了承ください。