S-1:Tegafur/Gimeracil/Oteracil(ティーエスワン®)
| 投与量 | コース | 投与日 |
|---|---|---|
| 80~120mg/日 経口 分2 朝夕食後 | 1~ | Day1~28 |
その他
| 1コース42日間。 |
本コンテンツは特定の治療法を推奨するものではありません。 個々の患者の病態や、 実際の薬剤情報やガイドラインを確認の上、 利用者の判断と責任でご利用ください。
薬剤情報
*大鵬薬品工業株式会社の外部サイトへ遷移します
用法用量
JASPAC 01試験³⁾のプロトコル
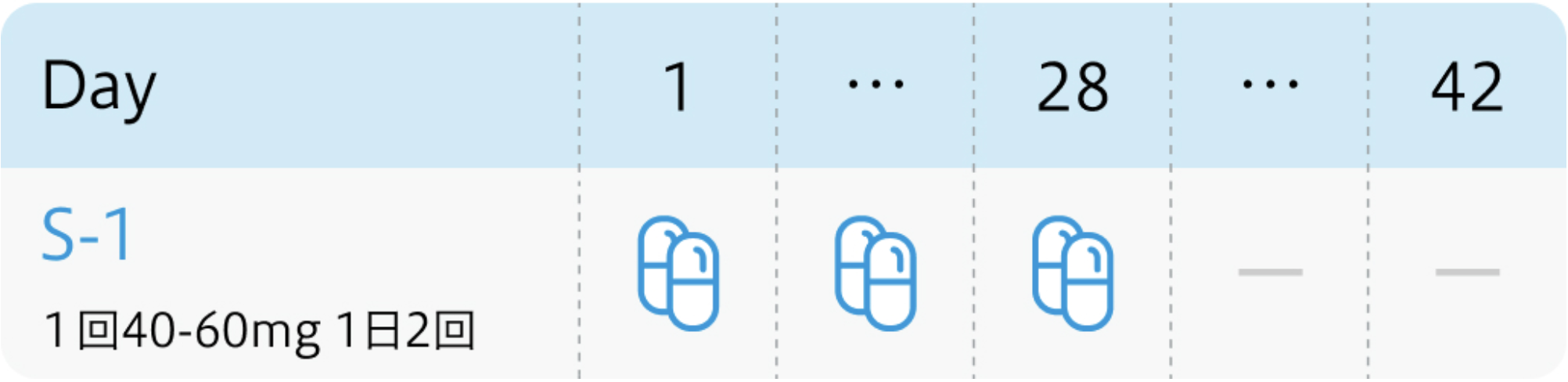
4週内服、2週間休薬を1コースとする。
Lancet. 2016 Jul 16;388(10041):248-57³⁾より作図
投与開始基準
適正使用ガイド²⁾の基準
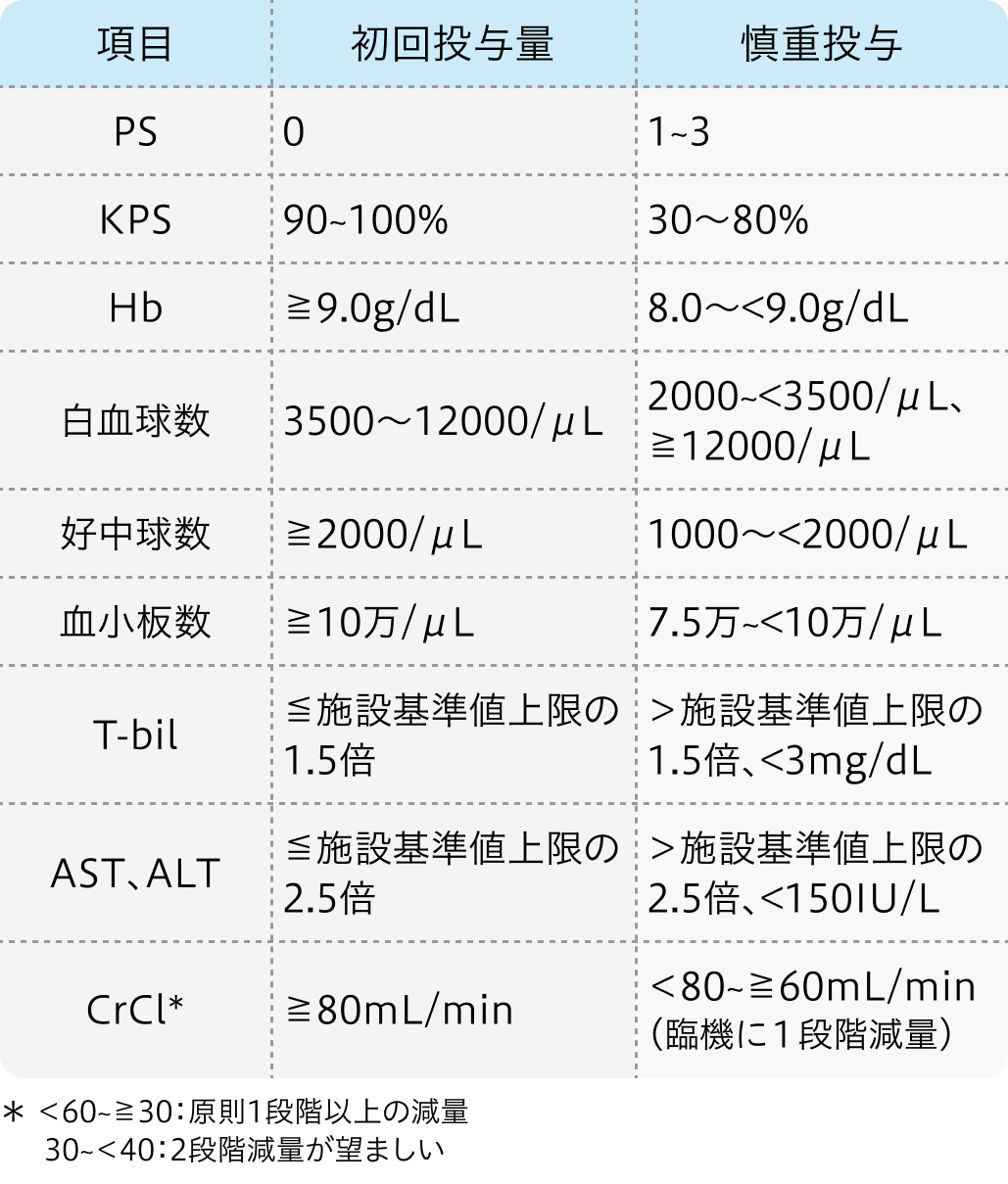
ティーエスワン®適正使用ガイド (2023年10月27日 更新)²⁾より引用
減量・休薬基準
適正使用ガイド²⁾の基準

ティーエスワン®適正使用ガイド (2023年10月27日 更新)²⁾より引用
再開方法の目安

ティーエスワン®適正使用ガイド (2023年10月27日 更新)²⁾より引用
主な有害事象
JASPAC 01試験³⁾
主な有害事象 (カッコ内はGrade3~4)
- ヘモグロビン減少 92.5% (13.9%)
- 好中球減少 74.9% (13.4%)
- AST増加 62.6% (1.1%)
- 白血球減少 55.6% (8.6%)
- ALT増加 55.6% (0.5%)
- 血小板減少 42.8% (4.8%)
- 発熱性好中球減少症 0.5% (0.5%)
- 倦怠感 66.3% (5.3%)
- 下痢 47.1% (4.8%)
- 吐き気 44.9% (3.7%)
- 発熱 24.6% (2.7%)
- 嘔吐 22.5% (1.6%)
Lancet. 2016 Jul 16;388(10041):248-57³⁾より引用
上手に使うためのワンポイント
患者説明のポイント
経口薬であるため、 簡便であるが、 口腔粘膜炎、 下痢、 食欲不振などの消化器毒性や血液毒性が発現する場合もあるため、 非血液毒性を中心とした有害事象が起こりうることを十分説明しておく。
2週投与1週休薬や隔日内服も選択肢
4週投与2週休薬が基本であるが、 2-3週目に有害事象が発現する患者では、 2週投与1週休薬や隔日内服も選択肢である。 ただし、 隔日内服の有用性は示されておらず³⁾、 全例で行うべきではない。
執筆:神奈川県立がんセンター 消化器内科 小林 智先生
特徴と注意点
ガイドラインにおける扱い
膵癌診療ガイドライン2022年版では、 遠隔転移を有する膵癌に対してFOLFIRINOX療法またはGEM+nab-PTX併用療法が適用とならない場合の治療として推奨されている。
腎機能低下例における対処
S-1の成分であるギメラシルは腎排泄性であるため、 腎機能低下例ではギメラシルの排泄が低下し、 5-FU血中濃度が上昇するため、 重篤な有害事象が発生しやすい。 クレアチニンクリアランス60-40ml/分では少なくとも一段階減量し、 30-40ml/分では少なくとも2段階減量が必要である。
執筆:神奈川県立がんセンター 消化器内科 小林 智先生
関連する臨床試験|JASPAC 01試験³⁾
浸潤性膵管癌の切除術後患者において、 S-1による術後化学療法の効果を、 ゲムシタビン(GEM) を対照に検証した第Ⅲ相ランダム化比較試験JASPAC 01の結果より、 全生存期間 (OS) および無再発生存期間 (RFS) に対する有効性が示された。
患者背景
両群間で手術術式以外は同様であった。
OS中央値
- S-1群:46.5ヵ月
(95%CI 37.8-63.7ヵ月)
- GEM群:25.5ヵ月
(95%CI 22.5-29.6ヵ月)
HR 0.57 (95%CI 0.44-0.72)、 非劣性p<0.0001、 優越性p<0.0001
OS率 (3年時、 5年時)
- S-1群:59.7%、 44.1%
- GEM群:38.8%、 24.4%
RFS中央値
- S-1群:22.9ヵ月
(95%CI 17.4-30.6ヵ月)
- GEM群:11.3ヵ月
(95%CI 9.7-13.6ヵ月)
HR 0.60 (95%CI 0.47-0.76)、 p<0.0001
RFS率 (3年時、 5年時)
- S-1群:39.2%、 33.3%
- GEM群:22.6%、 16.8%
HRQOL
6ヵ月以内のスコアの平均変化は両群間に有意差はなかったが、 12ヵ月から24ヵ月にかけてはS-1群の方がGEM群より有意に良好であった。
出典
- 大鵬薬品工業株式会社 . ティーエスワン®電子添文 (2023年9月改訂 第3版) [最終閲覧 : 2024/7/9]
- 大鵬薬品工業株式会社 . ティーエスワン®適正使用ガイド (2023年10月27日 更新) [最終閲覧 : 2024/7/9]
- Adjuvant chemotherapy of S-1 versus gemcitabine for resected pancreatic cancer: a phase 3, open-label, randomised, non-inferiority trial (JASPAC 01). Lancet. 2016 Jul 16;388(10041):248-57. PMID: 27265347
最終更新日:2024年8月21日
執筆医:神奈川県立がんセンター 消化器内科 小林 智先生
監修医:神奈川県立がんセンター 消化器内科 上野 誠先生
S-1
S-1:Tegafur/Gimeracil/Oteracil(ティーエスワン®)
| 投与量 | コース | 投与日 |
|---|---|---|
| 80~120mg/日 経口 分2 朝夕食後 | 1~ | Day1~28 |
その他
| 1コース42日間。 |
概要
本コンテンツは特定の治療法を推奨するものではありません。 個々の患者の病態や、 実際の薬剤情報やガイドラインを確認の上、 利用者の判断と責任でご利用ください。
薬剤情報
*大鵬薬品工業株式会社の外部サイトへ遷移します
用法用量
JASPAC 01試験³⁾のプロトコル

4週内服、2週間休薬を1コースとする。
Lancet. 2016 Jul 16;388(10041):248-57³⁾より作図
投与開始基準
適正使用ガイド²⁾の基準

ティーエスワン®適正使用ガイド (2023年10月27日 更新)²⁾より引用
減量・休薬基準
適正使用ガイド²⁾の基準

ティーエスワン®適正使用ガイド (2023年10月27日 更新)²⁾より引用
再開方法の目安

ティーエスワン®適正使用ガイド (2023年10月27日 更新)²⁾より引用
主な有害事象
JASPAC 01試験³⁾
主な有害事象 (カッコ内はGrade3~4)
- ヘモグロビン減少 92.5% (13.9%)
- 好中球減少 74.9% (13.4%)
- AST増加 62.6% (1.1%)
- 白血球減少 55.6% (8.6%)
- ALT増加 55.6% (0.5%)
- 血小板減少 42.8% (4.8%)
- 発熱性好中球減少症 0.5% (0.5%)
- 倦怠感 66.3% (5.3%)
- 下痢 47.1% (4.8%)
- 吐き気 44.9% (3.7%)
- 発熱 24.6% (2.7%)
- 嘔吐 22.5% (1.6%)
Lancet. 2016 Jul 16;388(10041):248-57³⁾より引用
上手に使うためのワンポイント
患者説明のポイント
経口薬であるため、 簡便であるが、 口腔粘膜炎、 下痢、 食欲不振などの消化器毒性や血液毒性が発現する場合もあるため、 非血液毒性を中心とした有害事象が起こりうることを十分説明しておく。
2週投与1週休薬や隔日内服も選択肢
4週投与2週休薬が基本であるが、 2-3週目に有害事象が発現する患者では、 2週投与1週休薬や隔日内服も選択肢である。 ただし、 隔日内服の有用性は示されておらず³⁾、 全例で行うべきではない。
執筆:神奈川県立がんセンター 消化器内科 小林 智先生
特徴と注意点
ガイドラインにおける扱い
膵癌診療ガイドライン2022年版では、 遠隔転移を有する膵癌に対してFOLFIRINOX療法またはGEM+nab-PTX併用療法が適用とならない場合の治療として推奨されている。
腎機能低下例における対処
S-1の成分であるギメラシルは腎排泄性であるため、 腎機能低下例ではギメラシルの排泄が低下し、 5-FU血中濃度が上昇するため、 重篤な有害事象が発生しやすい。 クレアチニンクリアランス60-40ml/分では少なくとも一段階減量し、 30-40ml/分では少なくとも2段階減量が必要である。
執筆:神奈川県立がんセンター 消化器内科 小林 智先生
関連する臨床試験|JASPAC 01試験³⁾
浸潤性膵管癌の切除術後患者において、 S-1による術後化学療法の効果を、 ゲムシタビン(GEM) を対照に検証した第Ⅲ相ランダム化比較試験JASPAC 01の結果より、 全生存期間 (OS) および無再発生存期間 (RFS) に対する有効性が示された。
患者背景
両群間で手術術式以外は同様であった。
OS中央値
- S-1群:46.5ヵ月
(95%CI 37.8-63.7ヵ月)
- GEM群:25.5ヵ月
(95%CI 22.5-29.6ヵ月)
HR 0.57 (95%CI 0.44-0.72)、 非劣性p<0.0001、 優越性p<0.0001
OS率 (3年時、 5年時)
- S-1群:59.7%、 44.1%
- GEM群:38.8%、 24.4%
RFS中央値
- S-1群:22.9ヵ月
(95%CI 17.4-30.6ヵ月)
- GEM群:11.3ヵ月
(95%CI 9.7-13.6ヵ月)
HR 0.60 (95%CI 0.47-0.76)、 p<0.0001
RFS率 (3年時、 5年時)
- S-1群:39.2%、 33.3%
- GEM群:22.6%、 16.8%
HRQOL
6ヵ月以内のスコアの平均変化は両群間に有意差はなかったが、 12ヵ月から24ヵ月にかけてはS-1群の方がGEM群より有意に良好であった。
出典
- 大鵬薬品工業株式会社 . ティーエスワン®電子添文 (2023年9月改訂 第3版) [最終閲覧 : 2024/7/9]
- 大鵬薬品工業株式会社 . ティーエスワン®適正使用ガイド (2023年10月27日 更新) [最終閲覧 : 2024/7/9]
- Adjuvant chemotherapy of S-1 versus gemcitabine for resected pancreatic cancer: a phase 3, open-label, randomised, non-inferiority trial (JASPAC 01). Lancet. 2016 Jul 16;388(10041):248-57. PMID: 27265347
最終更新日:2024年8月21日
執筆医:神奈川県立がんセンター 消化器内科 小林 智先生
監修医:神奈川県立がんセンター 消化器内科 上野 誠先生
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
がん薬物療法における治療計画をまとめたものです。
主要論文や適正使用ガイドをもとにした用量調整プロトコール、 有害事象対応をご紹介します。
なお、 本ツールは医師向けの教育用資料であり、 実臨床での使用は想定しておりません。 最新の添付文書やガイドラインを必ずご確認下さい。
また、 一般の方への情報提供ではないことを予めご了承ください。
