本コンテンツは特定の治療法を推奨するものではありません。 個々の患者の病態や、 実際の薬剤情報やガイドラインを確認の上、 利用者の判断と責任でご利用ください。
薬剤情報
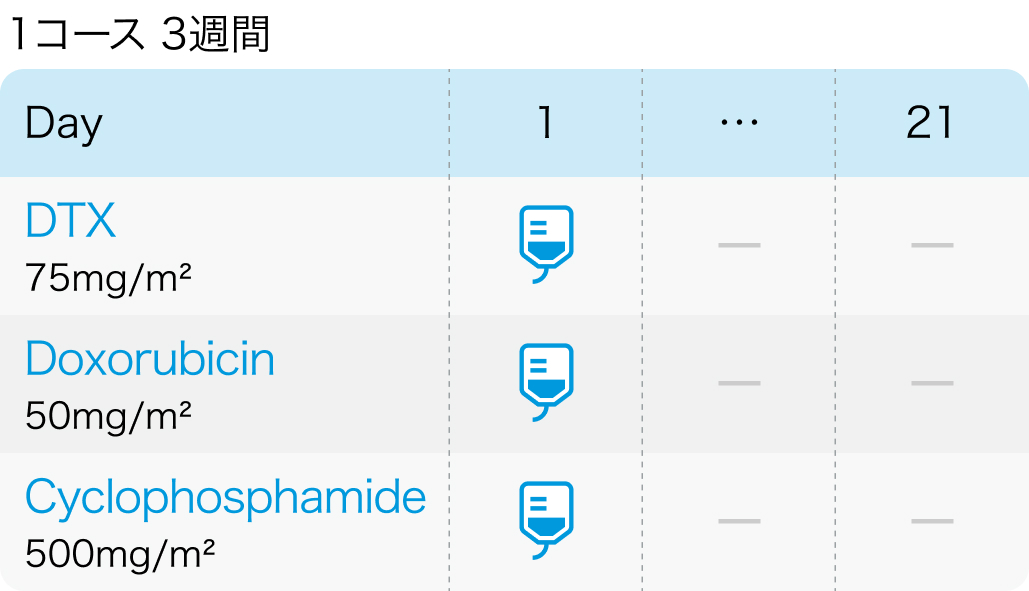
用法用量
BCIRG-001試験¹⁾、 BCIRG-005試験³⁾より抜粋
前投薬
高度催吐性リスクのため、 アプレピタント、 5HT3受容体拮抗薬、 デキサメタゾンを投与
投与開始基準
BCIRG-001試験¹⁾²⁾より抜粋
KPSが80%以上で、 手術可能な組織学的に確認された浸潤性乳腺癌の18~70歳の女性
BCIRG-005試験³⁾⁴⁾より抜粋
KPSが80%以上で、 腋窩リンパ節郭清を伴う初回手術 (乳房切除術、 または乳房温存術による腫瘍摘出) を受けた18~70歳の女性
主な有害事象
BCIRG-001試験¹⁾
主な有害事象 (カッコ内はGrade3、 4)
- 好中球数減少 71.4% (65.5%)
- 血小板数減少 39.4% (2.0%)
- 発熱性好中球減少症 28.8% (28.8%)
- 悪心 80.5% (5.1%)
- 口内炎 69.4% (7.1%)
- 嘔吐 44.5% (4.3%)
- 下痢 35.2% (3.8%)
注意すべき有害事象 (カッコ内はGrade3、 4)
- 脱毛症 97.8% (0%)
BCIRG-005試験³⁾
主な有害事象 (Grade3、 4)
- 好中球数減少 59.9%
- 発熱性好中球減少症 17.4%
- 貧血 2.9%
- 血小板数減少 2.5%
- 下痢 2.9%
- 倦怠感 5.1%
- 口内炎 2.6%
- 悪心 4.4%
- 嘔吐 4.1%
注意すべき有害事象 (Grade3、 4)
- 高血糖 1.3%
- 感覚性ニューロパチー 0.3%
特徴と注意点
- 周術期化学療法の一つ。
- ドセタキセルについては溶解剤にアルコールが含まれる、又はアルコール含有のプレミックス製剤を使用する場合は、 アルコール過敏症の確認が必要。必要に応じてアルコールを含有しない溶解剤を使用する。
- ドセタキセル総投与量が増えるにつれ浮腫の発現頻度が高くなるため、利尿剤を適宜使用する。 また、 浮腫予防として点滴翌日から2日間ステロイドを内服する。
- G-CSF製剤の1次予防投与を行わなかった場合、 FN発症率24.7%との報告あり。
- 発熱性好中球減少症の予防にペグフィルグラスチムを投与する。
- 皮疹に対して予防的に保湿剤を使用する。
- ドセタキセル、 ドキソルビシンは起壊死性抗がん薬のため、 血管外漏出に注意する。
- シクロホスファミドにより出血性膀胱炎が起こる可能性があるが、 ドキソルビシンの投与で尿が赤色に着色するため鑑別に注意が必要。
- アントラサイクリン系の心毒性に対して、 事前を含む定期的な左室駆出率の測定を行う。
関連する臨床試験①|BCIRG-001試験¹⁾
腋窩リンパ節転移陽性の乳癌患者において、 TACレジメン (ドセタキセル+ドキソルビシン+シクロホスファミド) の効果を、 FACレジメン (ドキソルビシン+フルオロウラシル+シクロホスファミド) を対照に検証した第Ⅲ相ランダム化比較試験BCIRG-001の結果より、 無病生存期間 (DFS) と全生存期間 (OS) を有意に改善させることが示された。
DFS率
5年時
- TAC群 : 75%
- FAC群 : 68%
HR 0.72、 (95%CI 0.59-0.88)、 p=0.001
10年時
- TAC群 : 62%
(95%CI 58-65%)
- FAC群 : 55%
(95%CI 51-59%)
HR 0.80、 (95%CI 0.68-0.93)、 p=0.0043
サブグループ解析
腋窩リンパ節転移の個数、 ホルモン受容体の状態、 HER2/neuの状態を含む、 すべてのサブグループにおいて、 TAC群のFAC群に対する優位性が一貫して認められた。
OS
イベント数
- TAC群 : 91例
- FAC群 : 130例
HR 0.70、 (95%CI 0.53-0.91)、 p=0.008
OS率 (5年時、 10年時)
- TAC群 : 87%、 76%
- FAC群 : 81%、 69%
10年時 : HR 0.74、 (95%CI 0.61-0.90)、 p=0.0020
関連する臨床試験②|BCIRG-005試験³⁾
HER2陰性かつリンパ節転移陽性の早期乳癌患者の術後療法において、 ドセタキセル+ドキソルビシン+シクロホスファミドの最適な投与スケジュールを評価するために、 逐次レジメン (AC→T療法) と併用レジメン (TAC療法) を比較した第Ⅲ相ランダム化比較試験BCIRG-005の結果より、 両レジメンの有効性が同等であることが示された。
DFS率 (1年時、 2年時、 5年時、 10年時)
- AC→T群 : 96.7%、 91.4%、 78.8%、 66.5%
- TAC群 : 97.2%、 91.3%、 79.3%、 66.3%
10年時 : p=0.749
サブグループ解析
どの集団においても有効性の差は示唆されなかった。
OS率 (1年時、 2年時、 5年時、 10年時)
- AC→T群 : 99.3%、 96.8%、 88.9%、 79.9%
- TAC群 : 99.1%、 96.5%、 88.1%、 78.9%
10年時 : p=0.506
サブグループ解析
どの集団においても有効性の差は示唆されなかった。
出典
- Adjuvant docetaxel for node-positive breast cancer. N Engl J Med. 2005 Jun 2;352(22):2302-13. PMID: 15930421
- Adjuvant docetaxel, doxorubicin, and cyclophosphamide in node-positive breast cancer: 10-year follow-up of the phase 3 randomised BCIRG 001 trial. Lancet Oncol. 2013 Jan;14(1):72-80. PMID: 23246022
- Phase III study of doxorubicin/cyclophosphamide with concomitant versus sequential docetaxel as adjuvant treatment in patients with human epidermal growth factor receptor 2-normal, node-positive breast cancer: BCIRG-005 trial. J Clin Oncol. 2011 Oct 10;29(29):3877-84. PMID: 21911726
- Long-term outcomes after adjuvant treatment of sequential versus combination docetaxel with doxorubicin and cyclophosphamide in node-positive breast cancer: BCIRG-005 randomized trial. Ann Oncol. 2016 Jun;27(6):1041-1047. PMID: 26940688
最終更新日:2024年7月16日
監修医師:HOKUTO編集部監修医師
執筆:公益財団法人 がん研究会 がん研有明病院 薬剤部 平岡 知子先生
TAC
本コンテンツは特定の治療法を推奨するものではありません。 個々の患者の病態や、 実際の薬剤情報やガイドラインを確認の上、 利用者の判断と責任でご利用ください。
薬剤情報
用法用量
BCIRG-001試験¹⁾、 BCIRG-005試験³⁾より抜粋

前投薬
高度催吐性リスクのため、 アプレピタント、 5HT3受容体拮抗薬、 デキサメタゾンを投与
投与開始基準
BCIRG-001試験¹⁾²⁾より抜粋
KPSが80%以上で、 手術可能な組織学的に確認された浸潤性乳腺癌の18~70歳の女性
BCIRG-005試験³⁾⁴⁾より抜粋
KPSが80%以上で、 腋窩リンパ節郭清を伴う初回手術 (乳房切除術、 または乳房温存術による腫瘍摘出) を受けた18~70歳の女性
主な有害事象
BCIRG-001試験¹⁾
主な有害事象 (カッコ内はGrade3、 4)
- 好中球数減少 71.4% (65.5%)
- 血小板数減少 39.4% (2.0%)
- 発熱性好中球減少症 28.8% (28.8%)
- 悪心 80.5% (5.1%)
- 口内炎 69.4% (7.1%)
- 嘔吐 44.5% (4.3%)
- 下痢 35.2% (3.8%)
注意すべき有害事象 (カッコ内はGrade3、 4)
- 脱毛症 97.8% (0%)
BCIRG-005試験³⁾
主な有害事象 (Grade3、 4)
- 好中球数減少 59.9%
- 発熱性好中球減少症 17.4%
- 貧血 2.9%
- 血小板数減少 2.5%
- 下痢 2.9%
- 倦怠感 5.1%
- 口内炎 2.6%
- 悪心 4.4%
- 嘔吐 4.1%
注意すべき有害事象 (Grade3、 4)
- 高血糖 1.3%
- 感覚性ニューロパチー 0.3%
特徴と注意点
- 周術期化学療法の一つ。
- ドセタキセルについては溶解剤にアルコールが含まれる、又はアルコール含有のプレミックス製剤を使用する場合は、 アルコール過敏症の確認が必要。必要に応じてアルコールを含有しない溶解剤を使用する。
- ドセタキセル総投与量が増えるにつれ浮腫の発現頻度が高くなるため、利尿剤を適宜使用する。 また、 浮腫予防として点滴翌日から2日間ステロイドを内服する。
- G-CSF製剤の1次予防投与を行わなかった場合、 FN発症率24.7%との報告あり。
- 発熱性好中球減少症の予防にペグフィルグラスチムを投与する。
- 皮疹に対して予防的に保湿剤を使用する。
- ドセタキセル、 ドキソルビシンは起壊死性抗がん薬のため、 血管外漏出に注意する。
- シクロホスファミドにより出血性膀胱炎が起こる可能性があるが、 ドキソルビシンの投与で尿が赤色に着色するため鑑別に注意が必要。
- アントラサイクリン系の心毒性に対して、 事前を含む定期的な左室駆出率の測定を行う。
関連する臨床試験①|BCIRG-001試験¹⁾
腋窩リンパ節転移陽性の乳癌患者において、 TACレジメン (ドセタキセル+ドキソルビシン+シクロホスファミド) の効果を、 FACレジメン (ドキソルビシン+フルオロウラシル+シクロホスファミド) を対照に検証した第Ⅲ相ランダム化比較試験BCIRG-001の結果より、 無病生存期間 (DFS) と全生存期間 (OS) を有意に改善させることが示された。
DFS率
5年時
- TAC群 : 75%
- FAC群 : 68%
HR 0.72、 (95%CI 0.59-0.88)、 p=0.001
10年時
- TAC群 : 62%
(95%CI 58-65%)
- FAC群 : 55%
(95%CI 51-59%)
HR 0.80、 (95%CI 0.68-0.93)、 p=0.0043
サブグループ解析
腋窩リンパ節転移の個数、 ホルモン受容体の状態、 HER2/neuの状態を含む、 すべてのサブグループにおいて、 TAC群のFAC群に対する優位性が一貫して認められた。
OS
イベント数
- TAC群 : 91例
- FAC群 : 130例
HR 0.70、 (95%CI 0.53-0.91)、 p=0.008
OS率 (5年時、 10年時)
- TAC群 : 87%、 76%
- FAC群 : 81%、 69%
10年時 : HR 0.74、 (95%CI 0.61-0.90)、 p=0.0020
関連する臨床試験②|BCIRG-005試験³⁾
HER2陰性かつリンパ節転移陽性の早期乳癌患者の術後療法において、 ドセタキセル+ドキソルビシン+シクロホスファミドの最適な投与スケジュールを評価するために、 逐次レジメン (AC→T療法) と併用レジメン (TAC療法) を比較した第Ⅲ相ランダム化比較試験BCIRG-005の結果より、 両レジメンの有効性が同等であることが示された。
DFS率 (1年時、 2年時、 5年時、 10年時)
- AC→T群 : 96.7%、 91.4%、 78.8%、 66.5%
- TAC群 : 97.2%、 91.3%、 79.3%、 66.3%
10年時 : p=0.749
サブグループ解析
どの集団においても有効性の差は示唆されなかった。
OS率 (1年時、 2年時、 5年時、 10年時)
- AC→T群 : 99.3%、 96.8%、 88.9%、 79.9%
- TAC群 : 99.1%、 96.5%、 88.1%、 78.9%
10年時 : p=0.506
サブグループ解析
どの集団においても有効性の差は示唆されなかった。
出典
- Adjuvant docetaxel for node-positive breast cancer. N Engl J Med. 2005 Jun 2;352(22):2302-13. PMID: 15930421
- Adjuvant docetaxel, doxorubicin, and cyclophosphamide in node-positive breast cancer: 10-year follow-up of the phase 3 randomised BCIRG 001 trial. Lancet Oncol. 2013 Jan;14(1):72-80. PMID: 23246022
- Phase III study of doxorubicin/cyclophosphamide with concomitant versus sequential docetaxel as adjuvant treatment in patients with human epidermal growth factor receptor 2-normal, node-positive breast cancer: BCIRG-005 trial. J Clin Oncol. 2011 Oct 10;29(29):3877-84. PMID: 21911726
- Long-term outcomes after adjuvant treatment of sequential versus combination docetaxel with doxorubicin and cyclophosphamide in node-positive breast cancer: BCIRG-005 randomized trial. Ann Oncol. 2016 Jun;27(6):1041-1047. PMID: 26940688
最終更新日:2024年7月16日
監修医師:HOKUTO編集部監修医師
執筆:公益財団法人 がん研究会 がん研有明病院 薬剤部 平岡 知子先生
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
がん薬物療法における治療計画をまとめたものです。
主要論文や適正使用ガイドをもとにした用量調整プロトコール、 有害事象対応をご紹介します。
なお、 本ツールは医師向けの教育用資料であり、 実臨床での使用は想定しておりません。 最新の添付文書やガイドラインを必ずご確認下さい。
また、 一般の方への情報提供ではないことを予めご了承ください。