本コンテンツは特定の治療法を推奨するものではありません。 個々の患者の病態や、 実際の薬剤情報やガイドラインを確認の上、 利用者の判断と責任でご利用ください。
薬剤情報
抗悪性腫瘍薬 > 代謝拮抗薬 ペメトレキセド
*日本イーライリリーの医療関係者向けサイトへ遷移します¹⁾
投与スケジュール
【1コース】21日
【催吐性】 軽度催吐性
【FN発症】低リスク
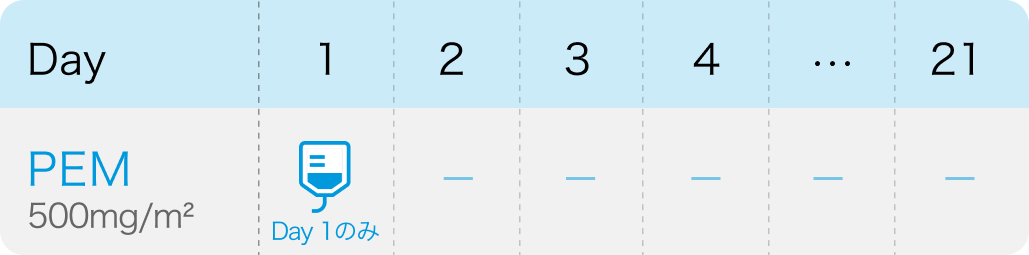
1日1回500mg/m² (体表面積) を10分間かけて点滴静注し、 少なくとも20日間休薬する。 これを1コースとし、 投与を繰り返す。
アリムタ®添付文書¹⁾より引用
KeyData|臨床試験結果
📊ランダム化比較非劣性第Ⅲ相試験³⁾
既治療NSCLCにおけるPEMのDTXに対するランダム化非劣性第Ⅲ相試験。 本試験の主要評価項目は全生存期間 (OS)、 副次評価項目は有害事象、 奏効割合 (RR)、 無増悪生存期間 (PFS)などであった。 結果、 有効性はほぼ同等で、 有害事象はDTXより著しく少なかった。
- ORR : 9.1%
DTX群 8.8% 奏効割合 P= .105
- mPFS : 2.9ヵ月
DTX群 2.9ヵ月 HR 0.97 (95%CI 0.82-1.16)
- mOS : 8.3ヵ月
DTX群 7.9ヵ月 HR 0.99 (95%CI 0.82-1.2; P=226)
レジメンの特徴と注意点
PEMとNSAIDs併用は控える
PEMの血中濃度が上昇し、 有害事象が増強する可能性があるため、 PEM投与5日前から投与2日後の8日間は併用を控えた方が良い。
投与に際しては葉酸とB12を併用
▼葉酸の投与
本剤初回投与の7日以上前から葉酸として1日1回0.5mgを連日経口投与する。 なお、 本剤の投与を中止又は終了する場合には、 本剤最終投与日から22日目まで可能な限り葉酸を投与する。
▼ビタミンB12の投与
本剤初回投与の少なくとも7日前に、 ビタミンB12として1回1mgを筋肉内投与する。 その後、 本剤投与期間中及び投与中止後22日目まで9週ごと (3コースごと) に1回投与する。
出典
1) 日本イーライリリー株式会社. アリムタ®添付文書 2025年7月改訂 (第3版) [最終閲覧: 2025/10/19]
2) 日本イーライリリー株式会社. アリムタ®︎適正使用ガイド 2025年7月作成 [最終閲覧: 2025/10/19]
最終更新日 : 2025年10月19日
監修・作図 : HOKUTO編集部専門医
Pemetrexed
本コンテンツは特定の治療法を推奨するものではありません。 個々の患者の病態や、 実際の薬剤情報やガイドラインを確認の上、 利用者の判断と責任でご利用ください。
薬剤情報
抗悪性腫瘍薬 > 代謝拮抗薬 ペメトレキセド
*日本イーライリリーの医療関係者向けサイトへ遷移します¹⁾
投与スケジュール
【1コース】21日
【催吐性】 軽度催吐性
【FN発症】低リスク

1日1回500mg/m² (体表面積) を10分間かけて点滴静注し、 少なくとも20日間休薬する。 これを1コースとし、 投与を繰り返す。
アリムタ®添付文書¹⁾より引用
KeyData|臨床試験結果
📊ランダム化比較非劣性第Ⅲ相試験³⁾
既治療NSCLCにおけるPEMのDTXに対するランダム化非劣性第Ⅲ相試験。 本試験の主要評価項目は全生存期間 (OS)、 副次評価項目は有害事象、 奏効割合 (RR)、 無増悪生存期間 (PFS)などであった。 結果、 有効性はほぼ同等で、 有害事象はDTXより著しく少なかった。
- ORR : 9.1%
DTX群 8.8% 奏効割合 P= .105
- mPFS : 2.9ヵ月
DTX群 2.9ヵ月 HR 0.97 (95%CI 0.82-1.16)
- mOS : 8.3ヵ月
DTX群 7.9ヵ月 HR 0.99 (95%CI 0.82-1.2; P=226)
レジメンの特徴と注意点
PEMとNSAIDs併用は控える
PEMの血中濃度が上昇し、 有害事象が増強する可能性があるため、 PEM投与5日前から投与2日後の8日間は併用を控えた方が良い。
投与に際しては葉酸とB12を併用
▼葉酸の投与
本剤初回投与の7日以上前から葉酸として1日1回0.5mgを連日経口投与する。 なお、 本剤の投与を中止又は終了する場合には、 本剤最終投与日から22日目まで可能な限り葉酸を投与する。
▼ビタミンB12の投与
本剤初回投与の少なくとも7日前に、 ビタミンB12として1回1mgを筋肉内投与する。 その後、 本剤投与期間中及び投与中止後22日目まで9週ごと (3コースごと) に1回投与する。
出典
1) 日本イーライリリー株式会社. アリムタ®添付文書 2025年7月改訂 (第3版) [最終閲覧: 2025/10/19]
2) 日本イーライリリー株式会社. アリムタ®︎適正使用ガイド 2025年7月作成 [最終閲覧: 2025/10/19]
最終更新日 : 2025年10月19日
監修・作図 : HOKUTO編集部専門医
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
がん薬物療法における治療計画をまとめたものです。
主要論文や適正使用ガイドをもとにした用量調整プロトコール、 有害事象対応をご紹介します。
なお、 本ツールは医師向けの教育用資料であり、 実臨床での使用は想定しておりません。 最新の添付文書やガイドラインを必ずご確認下さい。
また、 一般の方への情報提供ではないことを予めご了承ください。