Pola:ポラツズマブ ベドチン(ポライビー®)
| 投与量 | コース | 投与日 |
|---|---|---|
| 1.8mg/kg | 1-6 | Day 1 (または2) |
RIT:リツキシマブ(リツキサン®)
| 投与量 | コース | 投与日 |
|---|---|---|
| 375mg/m² | 1-8 | Day 1 |
CPA:シクロホスファミド(エンドキサン®)
| 投与量 | コース | 投与日 |
|---|---|---|
| 750mg/m² | 1-6 | Day 1 |
DXR:ドキソルビシン(アドリアシン®)
| 投与量 | コース | 投与日 |
|---|---|---|
| 50mg/m² | 1-6 | Day 1 |
PSL:プレドニゾロン(プレドニン®)
| 投与量 | コース | 投与日 |
|---|---|---|
| 100mg/body | 1-6 | Day 1~5 |
前投薬
| RIT投与開始の60分以上前にPSL100mg (又はmPSL80mg) を投与し、 RIT投与開始の30分以上前に解熱鎮痛薬、 抗ヒスタミン薬を投与. |
| RIT投与終了後にPola (PV)を投与する際、 infusion reaction症状があらわれていないことを確認するため経過観察の時間を設ける (初回投与時は90分間、 以降は忍容性が良好であれば30分間). |
| Polaの初回投与で前投与を行わずにinfusion reactionが認められた場合、 以降はPola前に前投与を行う. |
その他
| 1コース21日間、 Pola-R-CHPとして計6コース. |
| 臨床試験では、 Pola-R-CHP 6コース後に、 RIT単剤を7-8コース目に投与. |
| PolaはDay2に投与も可. |
| Polaは初回投与時は90分かけて投与し、忍容性が良好であれば2回目以降の投与時間は30分間まで短縮できる. |
| 実臨床では、「Polaも含めて1日目に投与」、「Polaのみ2日目に投与」以外に、「1日目にRITのみ投与し2日目にPola+CHP投与」も行われているが臨床試験のプロトコルに沿った投与法でないことに注意. |
本コンテンツは特定の治療法を推奨するものではありません。 個々の患者の病態や、 実際の薬剤情報やガイドラインを確認の上、 利用者の判断と責任でご利用ください。
薬剤情報
ポライビー® (ポラツズマブ ベドチン)
*中外製薬株式会社の外部サイトへ遷移します
投与スケジュール
【1コース】 21日間
【催吐性】高度
【FN発症】 中等度リスク*
*POLARIX試験のFN発生率14.3%を基に編集部作成
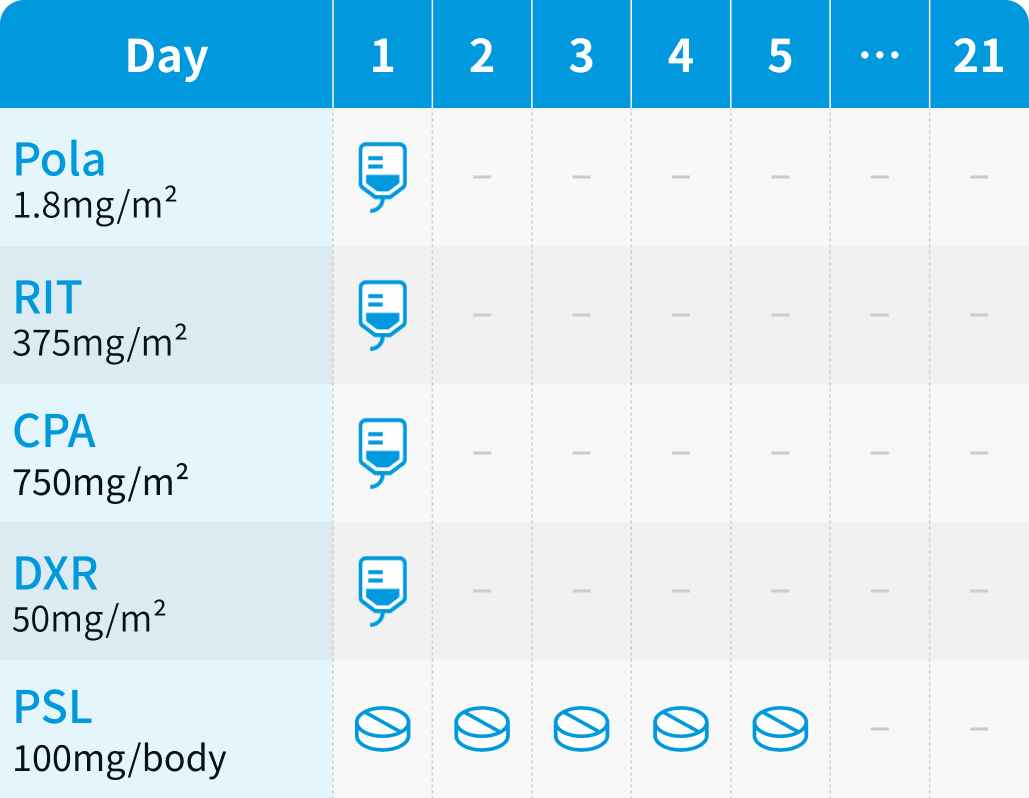
ポラツズマブ ベドチン (Pola) : 1.8mg/kgを1日1回点滴静注し、 3週ごと (Day 1) に投与
リツキシマブ (RIT) : 375mg/m²を点滴静注し、 3週ごと (Day 1) に投与
シクロホスファミド (CPA) : 750mg/m²を点滴静注し、 3週ごと (Day 1) に投与
ドキソルビシン (DXR) : 50mg/m²を点滴静注し、 3週ごと (Day 1) に投与
プレドニゾロン (PSL) : 100mg/bodyを1日1回経口投与し、 3週ごと (Day 1–5) に投与
Pola-R-CHP計6コース後、 RIT単剤療法を2コース行う。
Key Data|臨床試験結果
📊 POLARIX試験
N Engl J Med. 2022;386(4):351-363.
J Clin Oncol. 2025;43(35):3698-3705.
未治療のDLBCL患者 (IPIスコア2–5) を対象とした第III相無作為化化比較試験。 Pola-R-CHP群440例、 R-CHOP群439例を1:1に割り付け、 両群とも併用療法を6サイクル実施後、 RIT単剤を2サイクル投与した。 主要評価項目は治験担当医師評価によるPFSとした。
【有効性】Pola-R-CHP群 (vs R-CHOP群)
- PFS
- HR 0.77 (95%CI 0.62–0.97)
- 5年PFS率 64.9% (vs 59.1%)
- EFS
- HR 0.75 (95%CI 0.58–0.96、 p=0.02)
- 2年EFS率 75.6% (vs 69.4%)
- CR率 (治療終了時) 78.0% (vs 74.0%)
- OS
- HR 0.85 (95%CI 0.63–1.15)
- 5年OS率 82.3% (vs 79.5%)
【安全性】主な有害事象 : 全Grade (Grade≧3)
- 末梢神経障害 52.9% (1.6%)
- 悪心 41.6% (1.1%)
- 好中球減少 30.8% (28.3%)
- 下痢 30.8% (3.9%)
- 貧血 28.7% (12.0%)
- 便秘 28.7% (1.1%)
- 疲労 25.7% (0.9%)
- 脱毛症 24.4% (0%)
- 食欲減退 16.3% (1.1%)
- 発熱 15.6% (1.4%)
- 嘔吐 14.9% (1.1%)
- 発熱性好中球減少症 14.3% (13.8%)
- 頭痛 12.9% (0.2%)
- 咳嗽 12.9% (0%)
- 体重減少 12.6% (0.9%)
- 無力症 12.2% (1.6%)
- 味覚異常 11.3% (0%)
各プロトコル
適格基準
POLARIX試験³⁾⁴⁾の主な適格基準
- IPIスコア 2–5
- 18歳以上80歳以下
- ECOG PS 0–2
- 好中球≧1000/μL
- 血小板≧7.5万/μL
- Hb≧9.0g/dL
- 肝機能 : AST/ALT≦2.5×ULN、 T-Bil≦1.5×ULN
- 腎機能 : CrCl≧40mL/min
用量レベル
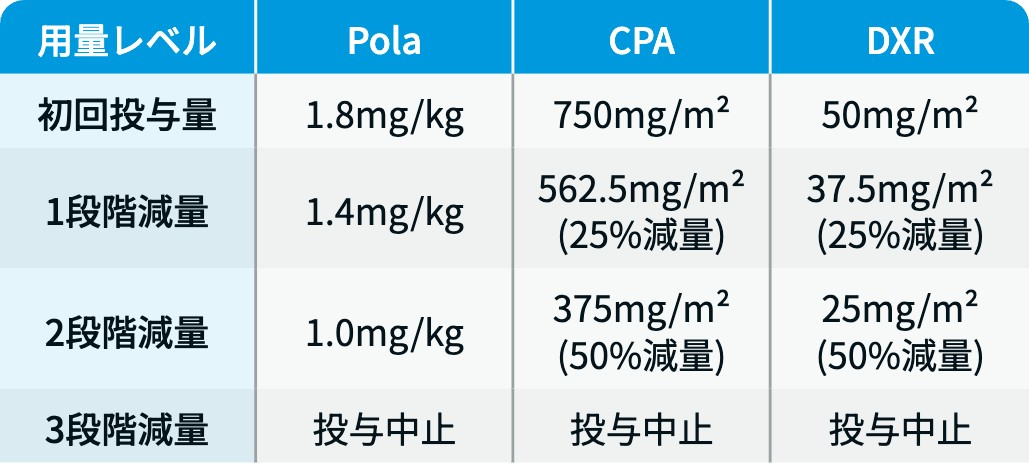
POLARIX試験³⁾⁴⁾のプロトコルを基に編集部作成
腎障害患者に対する用量調整
Pola : CrCl 30–89mL/minで抗体結合型MMAE/非抱合MMAEのPKに臨床的に有意な影響なし。 CrCl 15–29mL/minや末期腎不全 (透析有無) の影響は不明
U.S. Food and Drug Administration. POLIVY (polatuzumab vedotin-piiq) prescribing information. Genentech; 2019.
RIT : 抗体薬は多様な細胞でのエンドサイトーシスとリソソーム分解により消失するため、 一般に減量は不要と考えられる
編集部の見解
CPA : 重度腎機能障害 (とくにCrCl<10mL/min) では腎排泄低下でCPA/代謝物が上昇し、 毒性増加の可能性あり。 CPA/代謝物は透析性あり
U.S. Food and Drug Administration. CYCLOPHOSPHAMIDE injection prescribing information. Dr. Reddy’s Laboratories, Inc.; 2025.
DXR : 副作用が強くあらわれるおそれがあるが、 減量は不要
アドリアシン®インタビューフォーム
有害事象発現時の減量・休薬・中止基準
ポライビー®電子添文情報¹⁾ :
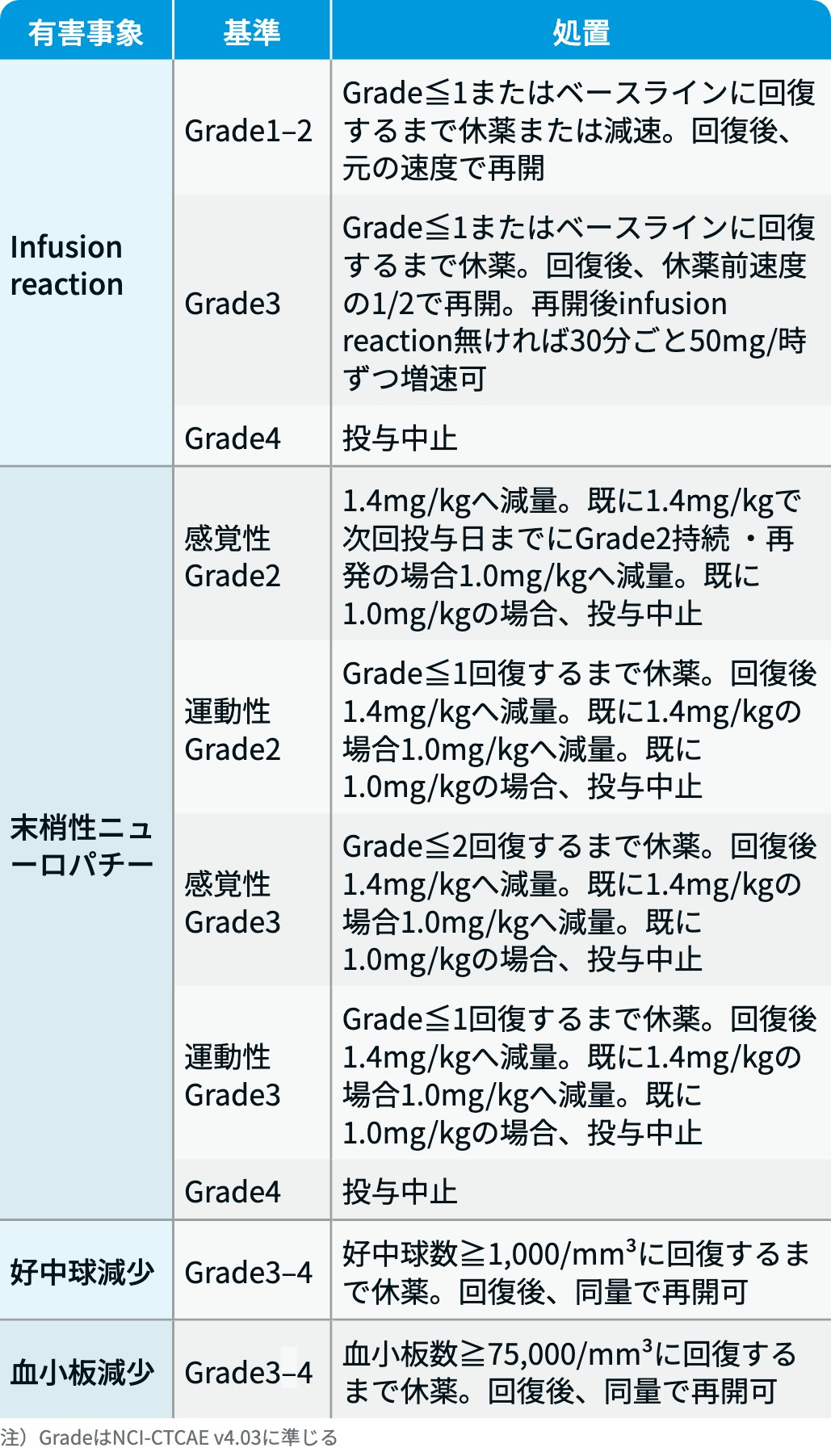
ポライビー®電子添文情報¹⁾を基に編集部作成
POLARIX試験³⁾⁴⁾のプロトコル (補足情報) :

レジメンの特徴と注意点
作用機序の特徴
Polaは、 抗CD79bヒト化IgG1モノクローナル抗体に微小管重合阻害作用を有するMMAEを結合させた抗体薬物複合体である。 細胞内に取り込まれた後、 遊離したMMAEが微小管重合を阻害し、 細胞分裂阻害やアポトーシス誘導を介して腫瘍増殖を抑制する。
レジメン適用時の注意事項
骨髄抑制 : 好中球減少、 発熱性好中球減少症、 貧血、 血小板減少、 白血球減少、 リンパ球減少等があらわれることがあるため、 定期的に血液検査を行い、 G-CSF製剤の適切な使用を考慮すること。
腫瘍崩壊症候群 : 血清中電解質濃度及び腎機能検査を行うなど、 患者の状態を十分に観察すること。
肝機能障害 : 定期的に肝機能検査を行うなど、 患者の状態を十分に観察すること。
RMP【重要な特定されたリスク】
ポライビー®RMP : 医薬品リスク管理計画書
- 骨髄抑制
- 末梢性ニューロパチー
- 感染症
- Infusion reaction
出典
1) 中外製薬株式会社. ポライビー®点滴静注用 電子添文. 2025年4月改訂 第9版.
2) 中外製薬株式会社. ポライビー®点滴静注用 適正使用ガイド. 2025年4月改訂.
3) N Engl J Med. 2022;386(4):351-363.
4) J Clin Oncol. 2025;43(35):3698-3705.
最終更新 : 2026年2月9日
執筆 : 京都桂病院薬剤科 冨士原あゆみ
監修 : 東海大学血液腫瘍内科 扇屋大輔
Pola-R-CHP
Pola:ポラツズマブ ベドチン(ポライビー®)
| 投与量 | コース | 投与日 |
|---|---|---|
| 1.8mg/kg | 1-6 | Day 1 (または2) |
RIT:リツキシマブ(リツキサン®)
| 投与量 | コース | 投与日 |
|---|---|---|
| 375mg/m² | 1-8 | Day 1 |
CPA:シクロホスファミド(エンドキサン®)
| 投与量 | コース | 投与日 |
|---|---|---|
| 750mg/m² | 1-6 | Day 1 |
DXR:ドキソルビシン(アドリアシン®)
| 投与量 | コース | 投与日 |
|---|---|---|
| 50mg/m² | 1-6 | Day 1 |
PSL:プレドニゾロン(プレドニン®)
| 投与量 | コース | 投与日 |
|---|---|---|
| 100mg/body | 1-6 | Day 1~5 |
前投薬
| RIT投与開始の60分以上前にPSL100mg (又はmPSL80mg) を投与し、 RIT投与開始の30分以上前に解熱鎮痛薬、 抗ヒスタミン薬を投与. |
| RIT投与終了後にPola (PV)を投与する際、 infusion reaction症状があらわれていないことを確認するため経過観察の時間を設ける (初回投与時は90分間、 以降は忍容性が良好であれば30分間). |
| Polaの初回投与で前投与を行わずにinfusion reactionが認められた場合、 以降はPola前に前投与を行う. |
その他
| 1コース21日間、 Pola-R-CHPとして計6コース. |
| 臨床試験では、 Pola-R-CHP 6コース後に、 RIT単剤を7-8コース目に投与. |
| PolaはDay2に投与も可. |
| Polaは初回投与時は90分かけて投与し、忍容性が良好であれば2回目以降の投与時間は30分間まで短縮できる. |
| 実臨床では、「Polaも含めて1日目に投与」、「Polaのみ2日目に投与」以外に、「1日目にRITのみ投与し2日目にPola+CHP投与」も行われているが臨床試験のプロトコルに沿った投与法でないことに注意. |
概要
本コンテンツは特定の治療法を推奨するものではありません。 個々の患者の病態や、 実際の薬剤情報やガイドラインを確認の上、 利用者の判断と責任でご利用ください。
薬剤情報
ポライビー® (ポラツズマブ ベドチン)
*中外製薬株式会社の外部サイトへ遷移します
投与スケジュール
【1コース】 21日間
【催吐性】高度
【FN発症】 中等度リスク*
*POLARIX試験のFN発生率14.3%を基に編集部作成

ポラツズマブ ベドチン (Pola) : 1.8mg/kgを1日1回点滴静注し、 3週ごと (Day 1) に投与
リツキシマブ (RIT) : 375mg/m²を点滴静注し、 3週ごと (Day 1) に投与
シクロホスファミド (CPA) : 750mg/m²を点滴静注し、 3週ごと (Day 1) に投与
ドキソルビシン (DXR) : 50mg/m²を点滴静注し、 3週ごと (Day 1) に投与
プレドニゾロン (PSL) : 100mg/bodyを1日1回経口投与し、 3週ごと (Day 1–5) に投与
Pola-R-CHP計6コース後、 RIT単剤療法を2コース行う。
Key Data|臨床試験結果
📊 POLARIX試験
N Engl J Med. 2022;386(4):351-363.
J Clin Oncol. 2025;43(35):3698-3705.
未治療のDLBCL患者 (IPIスコア2–5) を対象とした第III相無作為化化比較試験。 Pola-R-CHP群440例、 R-CHOP群439例を1:1に割り付け、 両群とも併用療法を6サイクル実施後、 RIT単剤を2サイクル投与した。 主要評価項目は治験担当医師評価によるPFSとした。
【有効性】Pola-R-CHP群 (vs R-CHOP群)
- PFS
- HR 0.77 (95%CI 0.62–0.97)
- 5年PFS率 64.9% (vs 59.1%)
- EFS
- HR 0.75 (95%CI 0.58–0.96、 p=0.02)
- 2年EFS率 75.6% (vs 69.4%)
- CR率 (治療終了時) 78.0% (vs 74.0%)
- OS
- HR 0.85 (95%CI 0.63–1.15)
- 5年OS率 82.3% (vs 79.5%)
【安全性】主な有害事象 : 全Grade (Grade≧3)
- 末梢神経障害 52.9% (1.6%)
- 悪心 41.6% (1.1%)
- 好中球減少 30.8% (28.3%)
- 下痢 30.8% (3.9%)
- 貧血 28.7% (12.0%)
- 便秘 28.7% (1.1%)
- 疲労 25.7% (0.9%)
- 脱毛症 24.4% (0%)
- 食欲減退 16.3% (1.1%)
- 発熱 15.6% (1.4%)
- 嘔吐 14.9% (1.1%)
- 発熱性好中球減少症 14.3% (13.8%)
- 頭痛 12.9% (0.2%)
- 咳嗽 12.9% (0%)
- 体重減少 12.6% (0.9%)
- 無力症 12.2% (1.6%)
- 味覚異常 11.3% (0%)
各プロトコル
適格基準
POLARIX試験³⁾⁴⁾の主な適格基準
- IPIスコア 2–5
- 18歳以上80歳以下
- ECOG PS 0–2
- 好中球≧1000/μL
- 血小板≧7.5万/μL
- Hb≧9.0g/dL
- 肝機能 : AST/ALT≦2.5×ULN、 T-Bil≦1.5×ULN
- 腎機能 : CrCl≧40mL/min
用量レベル

POLARIX試験³⁾⁴⁾のプロトコルを基に編集部作成
腎障害患者に対する用量調整
Pola : CrCl 30–89mL/minで抗体結合型MMAE/非抱合MMAEのPKに臨床的に有意な影響なし。 CrCl 15–29mL/minや末期腎不全 (透析有無) の影響は不明
U.S. Food and Drug Administration. POLIVY (polatuzumab vedotin-piiq) prescribing information. Genentech; 2019.
RIT : 抗体薬は多様な細胞でのエンドサイトーシスとリソソーム分解により消失するため、 一般に減量は不要と考えられる
編集部の見解
CPA : 重度腎機能障害 (とくにCrCl<10mL/min) では腎排泄低下でCPA/代謝物が上昇し、 毒性増加の可能性あり。 CPA/代謝物は透析性あり
U.S. Food and Drug Administration. CYCLOPHOSPHAMIDE injection prescribing information. Dr. Reddy’s Laboratories, Inc.; 2025.
DXR : 副作用が強くあらわれるおそれがあるが、 減量は不要
アドリアシン®インタビューフォーム
有害事象発現時の減量・休薬・中止基準
ポライビー®電子添文情報¹⁾ :

ポライビー®電子添文情報¹⁾を基に編集部作成
POLARIX試験³⁾⁴⁾のプロトコル (補足情報) :

レジメンの特徴と注意点
作用機序の特徴
Polaは、 抗CD79bヒト化IgG1モノクローナル抗体に微小管重合阻害作用を有するMMAEを結合させた抗体薬物複合体である。 細胞内に取り込まれた後、 遊離したMMAEが微小管重合を阻害し、 細胞分裂阻害やアポトーシス誘導を介して腫瘍増殖を抑制する。
レジメン適用時の注意事項
骨髄抑制 : 好中球減少、 発熱性好中球減少症、 貧血、 血小板減少、 白血球減少、 リンパ球減少等があらわれることがあるため、 定期的に血液検査を行い、 G-CSF製剤の適切な使用を考慮すること。
腫瘍崩壊症候群 : 血清中電解質濃度及び腎機能検査を行うなど、 患者の状態を十分に観察すること。
肝機能障害 : 定期的に肝機能検査を行うなど、 患者の状態を十分に観察すること。
RMP【重要な特定されたリスク】
ポライビー®RMP : 医薬品リスク管理計画書
- 骨髄抑制
- 末梢性ニューロパチー
- 感染症
- Infusion reaction
出典
1) 中外製薬株式会社. ポライビー®点滴静注用 電子添文. 2025年4月改訂 第9版.
2) 中外製薬株式会社. ポライビー®点滴静注用 適正使用ガイド. 2025年4月改訂.
3) N Engl J Med. 2022;386(4):351-363.
4) J Clin Oncol. 2025;43(35):3698-3705.
最終更新 : 2026年2月9日
執筆 : 京都桂病院薬剤科 冨士原あゆみ
監修 : 東海大学血液腫瘍内科 扇屋大輔
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
がん薬物療法における治療計画をまとめたものです。
主要論文や適正使用ガイドをもとにした用量調整プロトコール、 有害事象対応をご紹介します。
なお、 本ツールは医師向けの教育用資料であり、 実臨床での使用は想定しておりません。 最新の添付文書やガイドラインを必ずご確認下さい。
また、 一般の方への情報提供ではないことを予めご了承ください。
