治療スケジュール
概要
監修医師
L-OHP:Oxaliplatin(エルプラット®)
| 投与量 | コース | 投与日 |
|---|---|---|
| 130mg/m² 点滴 | 1~ | Day1 |
Cape:Capecitabine(ゼローダ®)
| 投与量 | コース | 投与日 |
|---|---|---|
| 2,000mg/m²/日 経口分2 朝夕食後 | 1~ | Day1~15 |
その他
| 1コース21日間。 |
| L-OHP+CapeをCAPOXと呼ぶ。 |
本コンテンツは特定の治療法を推奨するものではありません。 個々の患者の病態や、 実際の薬剤情報やガイドラインを確認の上、 利用者の判断と責任でご利用ください。
薬剤情報
*チェプラファームの外部サイトへ遷移します
用法用量
電子添文¹⁾²⁾の用法および用量
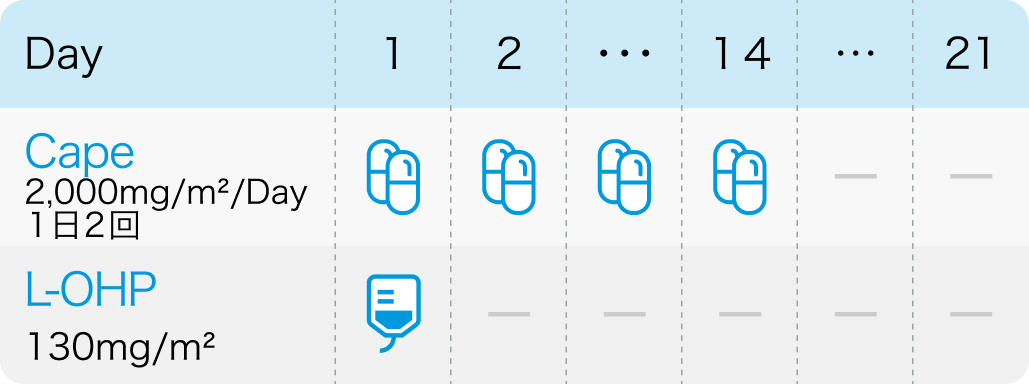
ゼローダ®電子添文 (2024年2月改訂 第3版)¹⁾ 、 エルプラット®電子添文 (2024年4月改訂 第4版)²⁾より作図
投与開始基準
国際第Ⅲ相試験⁴⁾のプロトコル
18歳以上の組織学的に証明された食道、 胃食道接合部、 または胃の腺癌、 扁平上皮癌、 または局所進行性 (手術不能) または転移性の未分化癌患者
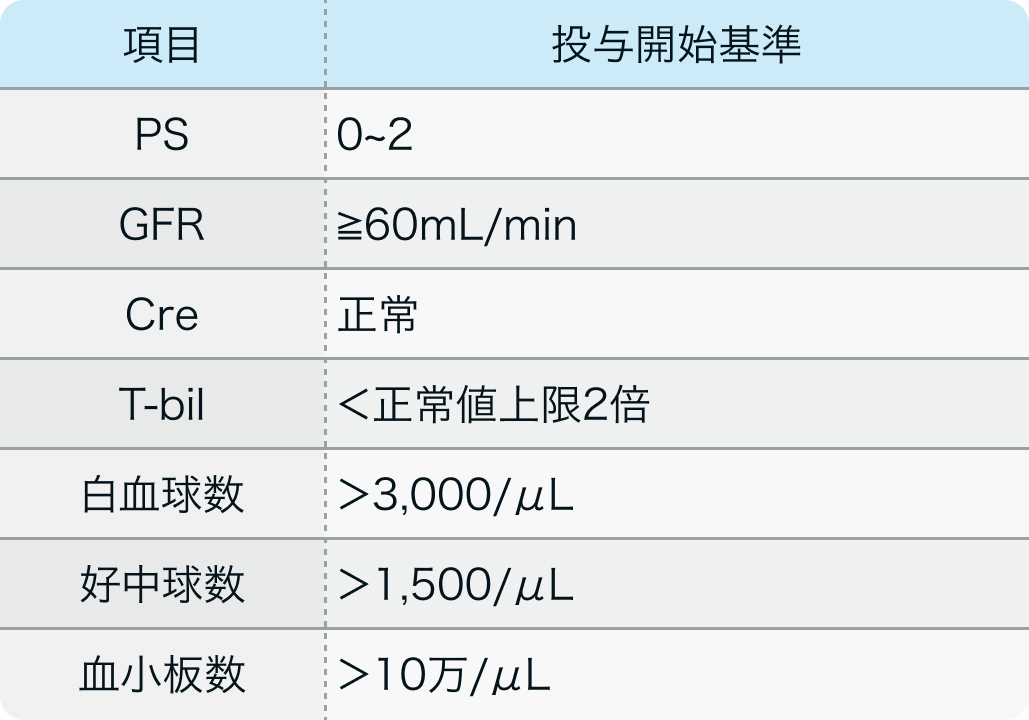
N Engl J Med. 2008 Jan 3;358(1):36-46⁴⁾より引用
主な有害事象
国際第Ⅲ相試験⁴⁾
主な有害事象 (括弧内は≧Grade3)
- 貧血 64.2% (8.6%)
- 血小板減少症 21.1% (5.2%)
- 好中球減少症 62.9% (27.6%)
- 発熱性好中球減少症 9.8% (7.8%)
- 下痢 61.7% (11.9%)
- 口内炎 38.1% (2.2%)
- 悪心/嘔吐 78.9% (11.4%)
注意すべき有害事象 (括弧内は≧Grade3)
- 手足症候群 39.3% (3.1%)
- 脱毛症 74.2% (28.8%)
N Engl J Med. 2008 Jan 3;358(1):36-46⁴⁾より引用
上手に使うためのワンポイント
- 胃癌は治療開始時にすでに体重減少を伴っていることが多いこと、 狭窄・腹膜播種など催吐リスクが高いことから、 オキサリプラチン130mg/m²で投与する場合には特に、 CINV予防として3剤併用 (NK1拮抗薬+5HT3拮抗薬+ステロイド) を考慮する。
- オキサリプラチンによるCIPNにより、 2次治療のPTX投与が困難になる時がある。 治療効果が十分と考えられ、 CIPN Grade2となった場合は、 オキサリプラチンの中止を考慮する。 上記を考慮しオキサリプラチンについては計画中止も治療選択肢と考えられる。
- カペシタビンによる手足症候群の症状と、 オキサリプラチンによるCIPNの症状がオーバーラップするため問診時には混同しないように注意する。
特徴と注意点
- ガイドラインでは、 HER2陰性胃癌1次治療において 「推奨される化学療法レジメン」 である。 通常の術後再発例はもちろん、 S-1レジメンとの使い分けとして術後補助療法S-1に不応となった早期再発例に対するXParTS試験の結果から、 早期再発例の第一選択とする医師もいる。
- オキサリプラチンの併用が必要なためvulnerableな高齢患者への適用には注意が必要である。 CAPOXは国内でも大腸癌の場合、 オキサリプラチンの初回投与量は130mg/m²だが、 70歳以上高齢者を対象としたTCOG GI-1601試験初期解析において毒性により両薬剤の1段階減量による継続を結論づけられた。 S-1におけるWJOG8315Gの結果と合わせて、 高齢者の初回投与量は100mg/m²が妥当かもしれない。
関連する臨床試験
国際第Ⅲ相試験⁴⁾
未治療の進行性食道胃がんに対する、 それぞれ注入フルオロウラシルとシスプラチンの代替品として、 カペシタビンとオキサリプラチンを評価するための試験。 主要評価項目はフルオロウラシルと比較したカペシタビンを含む三種療法と、 シスプラチンと比較したオキサリプラチンを含む三種療法の全生存期間における非劣性。
N Engl J Med. 2008 Jan 3;358(1):36-46.
出典
- チェプラファーム. ゼローダ®電子添文 (2024年2月改訂 第3版) [最終閲覧 : 2024/5/10]
- チェプラファーム. ゼローダ®適正使用ガイド (2024年2月改訂) [最終閲覧 : 2024/5/10]
- ヤクルト本社. エルプラット®電子添文 (2024年4月改訂 第4版) [最終閲覧 : 2024/04/17]
- Capecitabine and oxaliplatin for advanced esophagogastric cancer. N Engl J Med. 2008 Jan 3;358(1):36-46. PMID: 18172173
最終更新日 : 2024年8月21日
監修医師 : 神奈川県立がんセンター消化器内科部長 町田望先生
CAPOX
カペシタビン (ゼローダ®) + オキサリプラチン (エルプラット®)
胃癌 > 一次治療
2024年08月21日更新
L-OHP:Oxaliplatin(エルプラット®)
| 投与量 | コース | 投与日 |
|---|---|---|
| 130mg/m² 点滴 | 1~ | Day1 |
Cape:Capecitabine(ゼローダ®)
| 投与量 | コース | 投与日 |
|---|---|---|
| 2,000mg/m²/日 経口分2 朝夕食後 | 1~ | Day1~15 |
その他
| 1コース21日間。 |
| L-OHP+CapeをCAPOXと呼ぶ。 |
概要
本コンテンツは特定の治療法を推奨するものではありません。 個々の患者の病態や、 実際の薬剤情報やガイドラインを確認の上、 利用者の判断と責任でご利用ください。
薬剤情報
*チェプラファームの外部サイトへ遷移します
用法用量
電子添文¹⁾²⁾の用法および用量

ゼローダ®電子添文 (2024年2月改訂 第3版)¹⁾ 、 エルプラット®電子添文 (2024年4月改訂 第4版)²⁾より作図
投与開始基準
国際第Ⅲ相試験⁴⁾のプロトコル
18歳以上の組織学的に証明された食道、 胃食道接合部、 または胃の腺癌、 扁平上皮癌、 または局所進行性 (手術不能) または転移性の未分化癌患者

N Engl J Med. 2008 Jan 3;358(1):36-46⁴⁾より引用
主な有害事象
国際第Ⅲ相試験⁴⁾
主な有害事象 (括弧内は≧Grade3)
- 貧血 64.2% (8.6%)
- 血小板減少症 21.1% (5.2%)
- 好中球減少症 62.9% (27.6%)
- 発熱性好中球減少症 9.8% (7.8%)
- 下痢 61.7% (11.9%)
- 口内炎 38.1% (2.2%)
- 悪心/嘔吐 78.9% (11.4%)
注意すべき有害事象 (括弧内は≧Grade3)
- 手足症候群 39.3% (3.1%)
- 脱毛症 74.2% (28.8%)
N Engl J Med. 2008 Jan 3;358(1):36-46⁴⁾より引用
上手に使うためのワンポイント
- 胃癌は治療開始時にすでに体重減少を伴っていることが多いこと、 狭窄・腹膜播種など催吐リスクが高いことから、 オキサリプラチン130mg/m²で投与する場合には特に、 CINV予防として3剤併用 (NK1拮抗薬+5HT3拮抗薬+ステロイド) を考慮する。
- オキサリプラチンによるCIPNにより、 2次治療のPTX投与が困難になる時がある。 治療効果が十分と考えられ、 CIPN Grade2となった場合は、 オキサリプラチンの中止を考慮する。 上記を考慮しオキサリプラチンについては計画中止も治療選択肢と考えられる。
- カペシタビンによる手足症候群の症状と、 オキサリプラチンによるCIPNの症状がオーバーラップするため問診時には混同しないように注意する。
特徴と注意点
- ガイドラインでは、 HER2陰性胃癌1次治療において 「推奨される化学療法レジメン」 である。 通常の術後再発例はもちろん、 S-1レジメンとの使い分けとして術後補助療法S-1に不応となった早期再発例に対するXParTS試験の結果から、 早期再発例の第一選択とする医師もいる。
- オキサリプラチンの併用が必要なためvulnerableな高齢患者への適用には注意が必要である。 CAPOXは国内でも大腸癌の場合、 オキサリプラチンの初回投与量は130mg/m²だが、 70歳以上高齢者を対象としたTCOG GI-1601試験初期解析において毒性により両薬剤の1段階減量による継続を結論づけられた。 S-1におけるWJOG8315Gの結果と合わせて、 高齢者の初回投与量は100mg/m²が妥当かもしれない。
関連する臨床試験
国際第Ⅲ相試験⁴⁾
未治療の進行性食道胃がんに対する、 それぞれ注入フルオロウラシルとシスプラチンの代替品として、 カペシタビンとオキサリプラチンを評価するための試験。 主要評価項目はフルオロウラシルと比較したカペシタビンを含む三種療法と、 シスプラチンと比較したオキサリプラチンを含む三種療法の全生存期間における非劣性。
N Engl J Med. 2008 Jan 3;358(1):36-46.
出典
- チェプラファーム. ゼローダ®電子添文 (2024年2月改訂 第3版) [最終閲覧 : 2024/5/10]
- チェプラファーム. ゼローダ®適正使用ガイド (2024年2月改訂) [最終閲覧 : 2024/5/10]
- ヤクルト本社. エルプラット®電子添文 (2024年4月改訂 第4版) [最終閲覧 : 2024/04/17]
- Capecitabine and oxaliplatin for advanced esophagogastric cancer. N Engl J Med. 2008 Jan 3;358(1):36-46. PMID: 18172173
最終更新日 : 2024年8月21日
監修医師 : 神奈川県立がんセンター消化器内科部長 町田望先生
こちらの記事の監修医師
HOKUTO編集部
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
HOKUTO編集部
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
レジメン(消化器)
がん薬物療法における治療計画をまとめたものです。
主要論文や適正使用ガイドをもとにした用量調整プロトコール、 有害事象対応をご紹介します。
なお、 本ツールは医師向けの教育用資料であり、 実臨床での使用は想定しておりません。 最新の添付文書やガイドラインを必ずご確認下さい。
また、 一般の方への情報提供ではないことを予めご了承ください。
