Amivantamab:Amivantamab(ライブリバント®)
| 投与量 | コース | 投与日 |
|---|---|---|
| 350mg 点滴 | 1 | Day 1 |
| 1050mg 点滴 | 1 | Day 2 |
| 1400mg 点滴 | 1 | Day 8、 15 |
| 1400mg 点滴 | 2 | Day 1 |
| 1750mg 点滴 | 3~ | Day 1 |
Amivantamab:Amivantamab+rHuPH20(リブロファズ®)
| 投与量 | コース | 投与日 |
|---|---|---|
| 1600mg 皮下注 | 1 | Day 1 |
| 2400mg 皮下注 | 1 | Day 8、 15 |
| 2400mg 皮下注 | 2~ | Day 1 |
PEM:Pemetrexed(ペメトレキセド®)
| 投与量 | コース | 投与日 |
|---|---|---|
| 500mg/m² 点滴 | 1~ | Day 1 |
CBDCA:Carboplatin(カルボプラチン®)
| 投与量 | コース | 投与日 |
|---|---|---|
| AUC 5 | 1~4 | Day 1 |
前投薬
| リブロファズ®投与前は、サイクル1 Day1にステロイド+抗ヒスタミン剤+解熱鎮痛剤(必要時H2拮抗剤・制吐剤)を投与し、Day8以降は抗ヒスタミン剤+解熱鎮痛剤(必要時ステロイド・H2拮抗剤・制吐剤)を投与する。 |
| ライブリバント®投与前は、サイクル1 Day1・2にステロイド+抗ヒスタミン剤+解熱鎮痛剤(必要時H2拮抗剤・制吐剤)を投与し、Day8以降は抗ヒスタミン剤+解熱鎮痛剤(必要時ステロイド・H2拮抗剤・制吐剤)を投与する。 |
その他
| 1コース21日間。 |
| アミバンタマブは、体重に基づき投与。初回は1400mg (体重≥80kg: 1750mg) をDay1/2に分割投与、Day8, 15に同量投与。Cycle 2 Day 1に同量投与。Cycle 3 Day 1以降は1750mg (体重≥80kg: 2100mg) を3週間間隔(各サイクルのDay 1)で点滴静注。 |
| CBDCAは最大4サイクルまで。その後は病勢進行までアミバンタマブ+PEM維持療法として継続。 |
| PEMはビタミンB₁₂、葉酸の補充が必須。 |
2024年5月31日、 「EGFR遺伝子変異陽性の切除不能な進行・再発の非小細胞肺癌」 を対象として製造販売承認を申請し、 2025年5月19日に正式に承認された。
本コンテンツは特定の治療法を推奨するものではありません。 個々の患者の病態や、 実際の薬剤情報やガイドラインを確認の上、 利用者の判断と責任でご利用ください。
薬剤情報
リブロファズ® (アミバンタマブ+rHuPH20)
ライブリバント® (アミバンタマブ)
EGFR/MET二重特異性抗体
*ヤンセンファーマ株式会社の外部サイトへ遷移
投与スケジュール
【1コース】21日間
【催吐性】 中等度*
【FN発症】低リスク**
*Amivantamabは軽度、 CBDCA/PEMは中等度催吐性
**MARIPOSA-2試験⁵⁾のFN発症率2%に基づき編集部が分類。
▼1コース目

▼2コース目 : リブロファズ®は2コース目以降、 同量継続
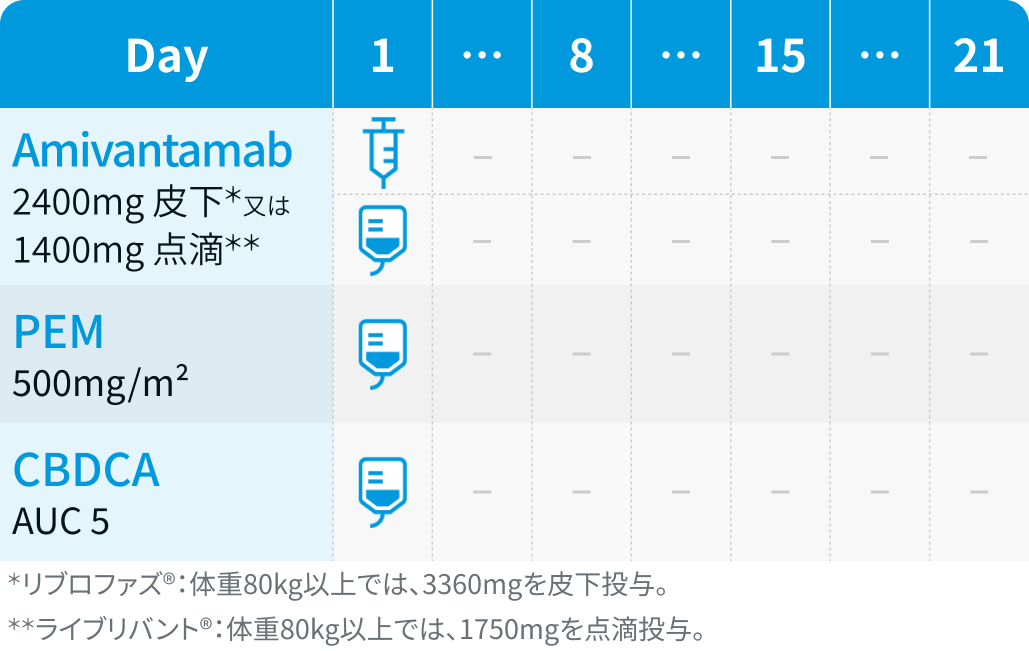
▼3–4コース目 : ライブリバント®は3コース目以降、 同量継続
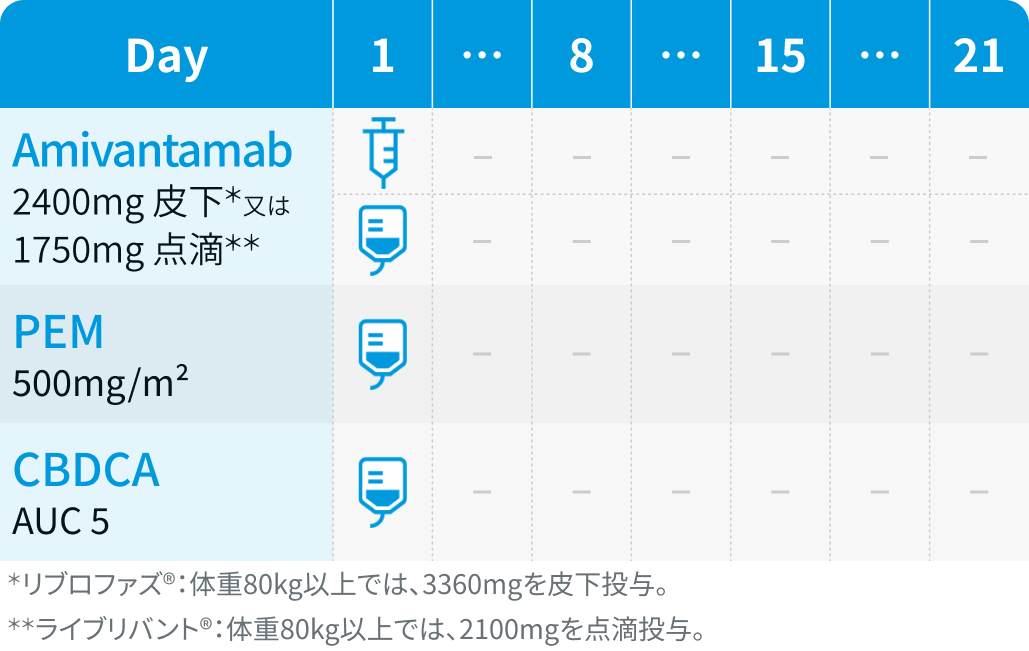
▼5コース目以降 : CBDCAは投与しない
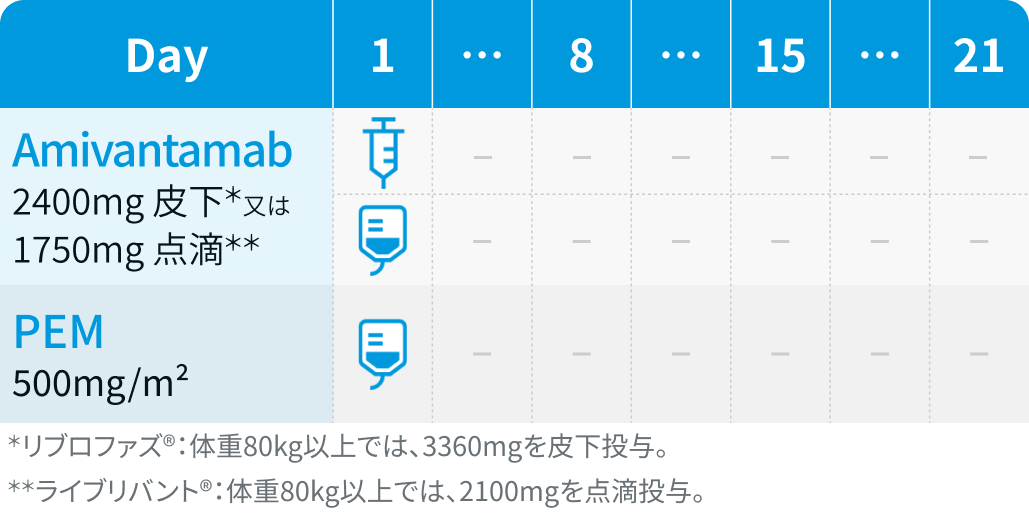
アミバンタマブ (Ami) : 3週間を1コースとし、 1コース目は週1回投与、 2コース目以降は3週ごとに病勢進行まで継続投与 (用量は製剤ごとに以下のとおり)
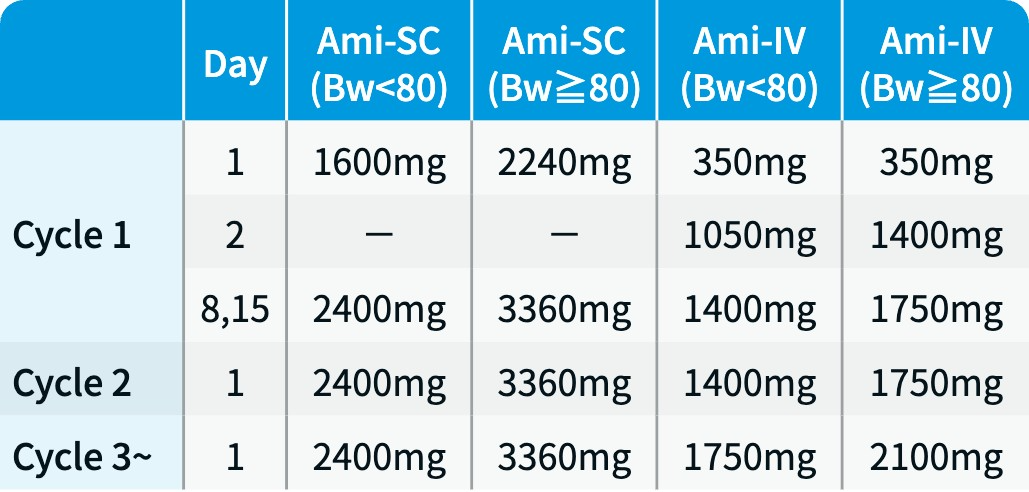
Ami-SC : リブロファズ®、 Ami-IV : ライブリバント®、 Bw (kg)
ペメトレキセド (PEM) : 500mg/m²を各コースDay1に静脈内投与し、 疾患進行まで維持投与
カルボプラチン (CBDCA) : AUC 5をDay1に静脈内投与 (最大4コースまで)
MARIPOSA-2試験⁵⁾では、 PEM、 CBDCA、 Amiの順に投与した。
Key Data|臨床試験結果
📊 MARIPOSA-2試験
オシメルチニブ治療中または治療後に病勢進行したEGFR遺伝子変異 (Ex19delまたはL858R) 陽性の局所進行または転移性NSCLC患者657例を対象とする第III相無作為化比較試験である。 Ami+化学療法 (CBDCA+PEM) 群、 化学療法単独群、 Ami+Lazertinib+化学療法群に2:1:2で割り付けた。 主要評価項目はPFSであり、 Ami+化学療法群 vs 化学療法群、 ならびにAmi+Lazertinib+化学療法群 vs 化学療法群で評価した。
【有効性】Ami+化学療法群 (vs 化学療法)
- PFS中央値 6.3ヵ月 (vs 4.2ヵ月)
- HR 0.48 (95%CI 0.36–0.64、 p<0.001)
- 6ヵ月PFS率 51% (vs 30%)
- 12ヵ月PFS率 22% (vs 13%)
- 頭蓋内PFS中央値 12.5ヵ月 (vs 8.3ヵ月)
- HR 0.55 (95%CI 0.38–0.79)
- 客観的奏効率 64%
- 奏効期間中央値 6.9ヵ月
- OS (中間解析)
- HR 0.77 (95%CI 0.49–1.21)
【安全性】主な有害事象 : 全Grade (Grade≧3)
IV製剤のデータであることに留意
- 好中球減少 57% (45%)
- 血小板減少 44% (19%)
- Infusion-related reaction (IRR) 58% (5%)
- 貧血 39% (12%)
- 爪囲炎 37% (2%)
- 悪心 45% (1%)
- 発疹 43% (6%)
- 口内炎 32% (1%)
- 白血球減少 28% (20%)
- 低アルブミン血症 22% (2%)
- 便秘 38% (1%)
- 食欲減退 31% (0%)
- 末梢性浮腫 32% (2%)
- 嘔吐 25% (1%)
- 疲労 28% (3%)
- 下痢 14% (1%)
- 無力症 26% (1%)
- ざ瘡様皮膚炎 20% (4%)
- ALT上昇 20% (5%)
- 低カリウム血症 18% (5%)
- COVID-19 21% (2%)
- 低カルシウム血症 12% (1%)
- AST上昇 15% (1%)
- 低ナトリウム血症 10% (4%)
- 掻痒症 15% (0%)
各プロトコル
適格基準
MARIPOSA-2試験⁵⁾の主な適格基準
- 18歳以上
- ECOG PS 0または1
- 好中球≧1500/μL
- 血小板≧10万/μL
- Hb≧10g/dL
- 腎機能 : CrCl>50mL/min
- 肝機能 : T-Bil≦1.5×ULN、 ALT/AST≦3×ULN
リブロファズ®の減量・休薬・中止基準
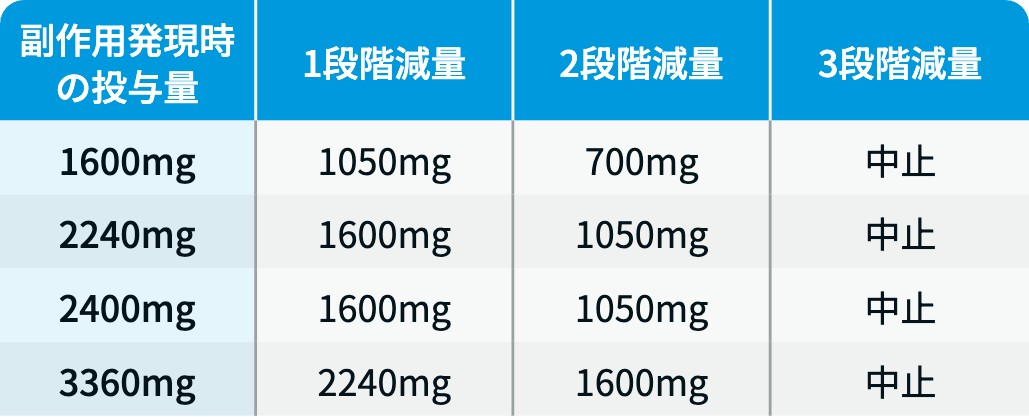
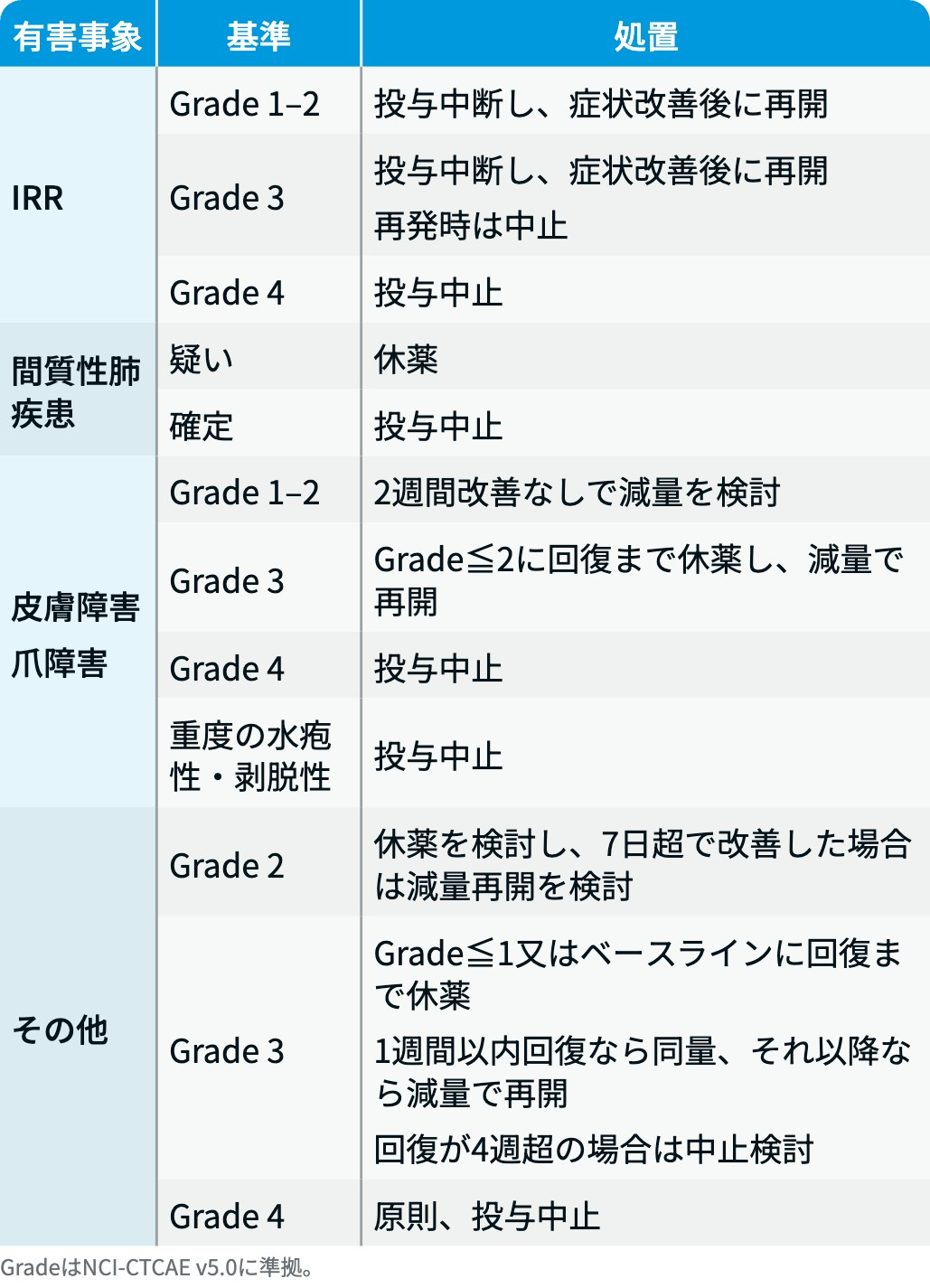
リブロファズ®電子添文情報¹⁾を基に編集部作成
MARIPOSA-2試験⁵⁾では、 以下の血液毒性Grade 4が発現した場合に限り、 Ami投与を延期することが規定されていた。
- Grade 4の血液毒性が7日超で持続
- 出血または入院を伴う血小板減少Grade 4
- FN Grade 4
ライブリバント®の減量・休薬・中止基準
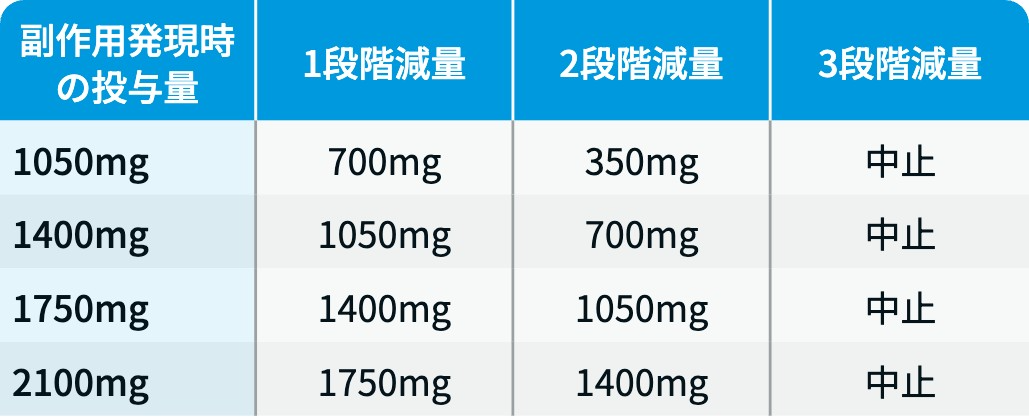
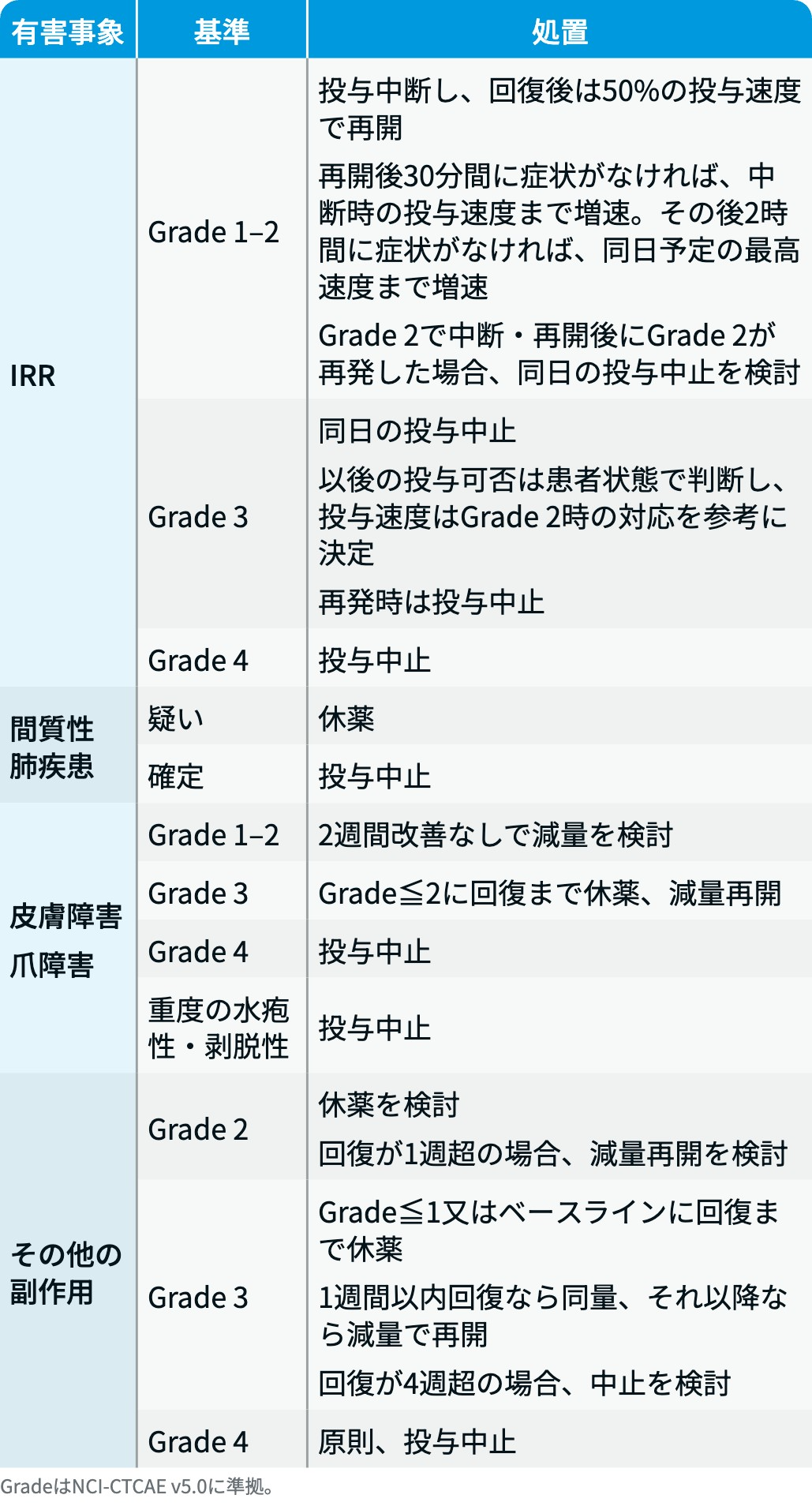
ライブリバント® 電子添文³⁾を基に編集部作成
MARIPOSA-2試験⁵⁾では、 以下の血液毒性Grade 4が発現した場合に限り、 Ami投与を延期することが規定されていた。
- Grade 4の血液毒性が7日超で持続
- 出血または入院を伴う血小板減少Grade 4
- FN Grade 4
CBDCA+PEMの減量・休薬・中止基準
以下に該当する場合は、 化学療法を延期する。
- 好中球<1500/µL
- 血小板<10万/µL
- 非血液毒性Grade≧3
MARIPOSA-2試験⁵⁾では、 CBDCA/PEMの再投与基準を満たさない場合は化学療法を1週ごとに延期し、 化学療法が予定日に実施できなくてもAmiの再投与基準を満たす場合はAmiを計画通り投与するとされた (化学療法がDay 8またはDay 15にずれた場合は、 次サイクルのAmiを±1週調整して化学療法と同日にそろえる)。
また、 有害事象発現時の用量調整は、 以下に基づき実施する。
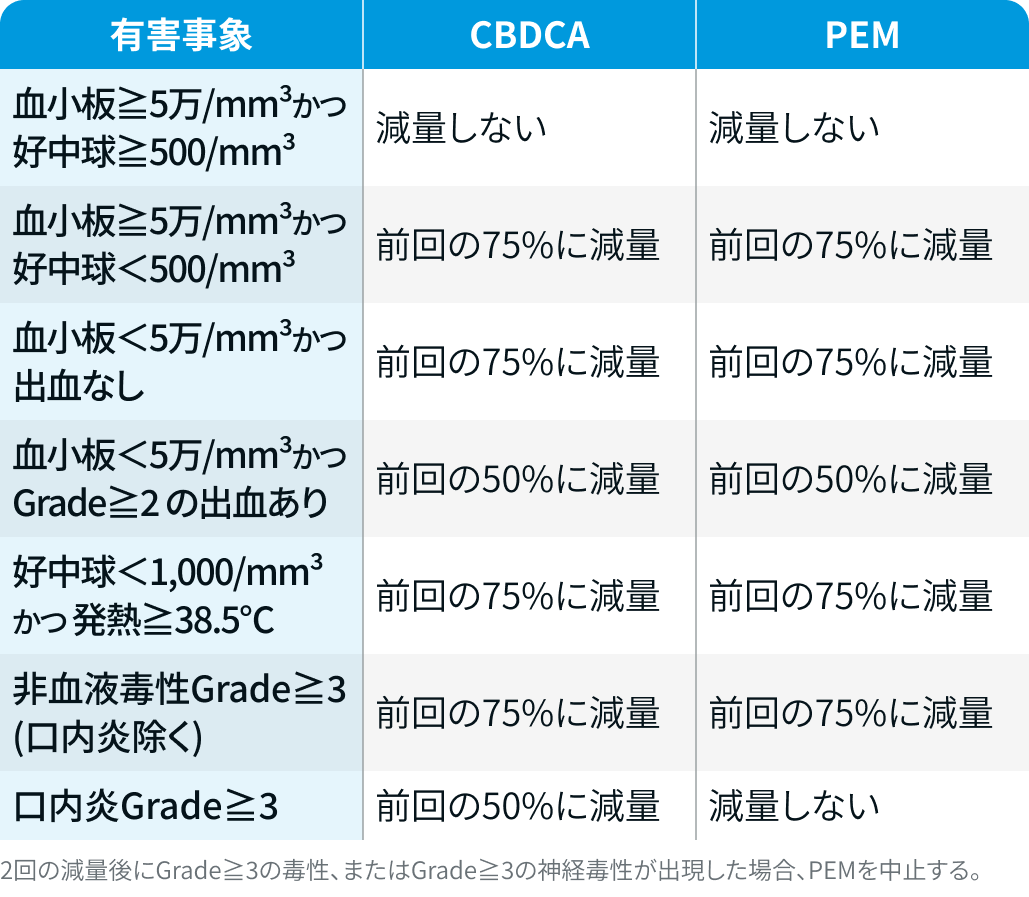
GradeはNCI-CTCAE v.5.0に準拠。 MARIPOSA-2試験⁵⁾のプロトコルを基に編集部作成
腎障害患者に対する用量調節
Ami : 抗体薬は多様な細胞でのエンドサイトーシスとリソソーム分解により消失するため、 一般に減量は不要と考えられる。
編集部の見解
CBDCA : Calvert式で投与量を算出する
PEM : 重度の腎機能障害患者には投与しない。 なお、 CrCl<45mL/minの患者は別の臨床試験で除外されている
FDA添付文書 : CrCl<45mL/minの患者には投与しない
レジメンの特徴と注意点
2025年12月22日、 アミバンタマブ (ライブリバント®点滴静注) と同一の効能・効果で、 リブロファズ®配合皮下注 (アミバンタマブ・ボルヒアルロニダーゼ アルファ) が承認された。
🧑⚕️本レジメンは、 MARIPOSA試験と比較して皮膚障害はやや軽度である一方、 IRR、 下痢、 浮腫、 骨髄抑制など多様な有害事象への対応が求められる。 Amiの皮下投与により、 IRRおよびVTEの低減が期待されるほか、 投与時間の短縮も見込まれる。
和歌山県立医科大学附属病院 赤松弘朗先生
作用機序の特徴
Amiは、 EGFRとMETに対する二重特異性モノクローナル抗体であり、 シグナル伝達の阻害とADCC活性などにより腫瘍増殖を抑制すると考えられている。
本レジメンの位置付け
本レジメンは、 EGFR遺伝子変異陽性NSCLCに対し、 オシメルチニブ治療後に病勢進行した症例における2次治療以降の選択肢である。
レジメン適用時の注意事項
Ami、 ラゼルチニブ、 CBDCA、 PEMの4剤併用投与は行わないこと。
IRR (ライブリバント®) : Day 1・Day 2の分割投与および必須の前投薬で予防し、 規定の投与速度で投与する。 以下に、 投与速度および前投薬を示す。
▼ライブリバント®調製後の希釈液 (投与量/250mL) 投与速度
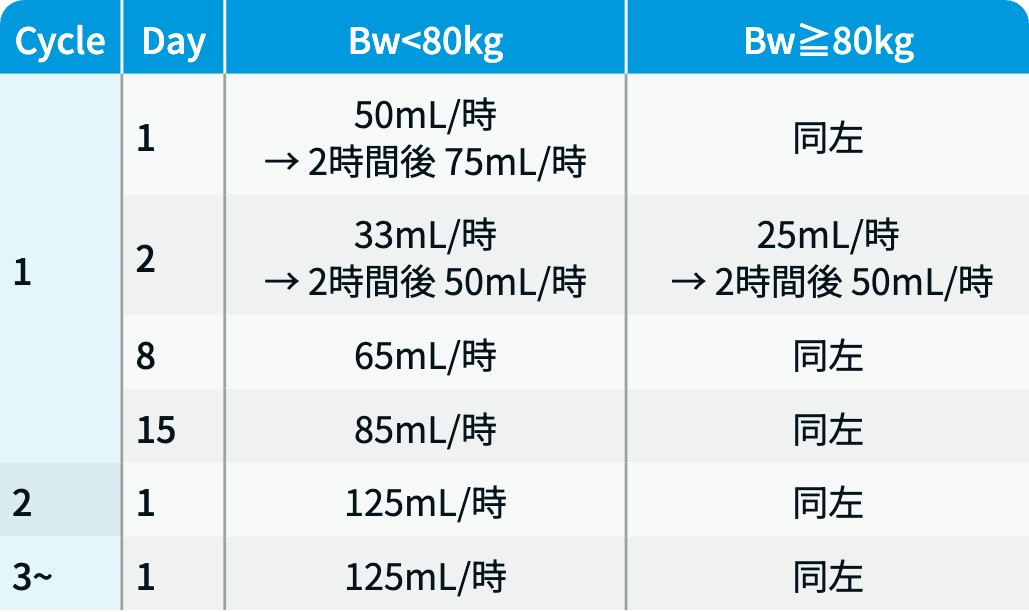
ライブリバント® 電子添文¹⁾を基に編集部作成
▼MARIPOSA-2試験⁵⁾で規定された必須の前投薬
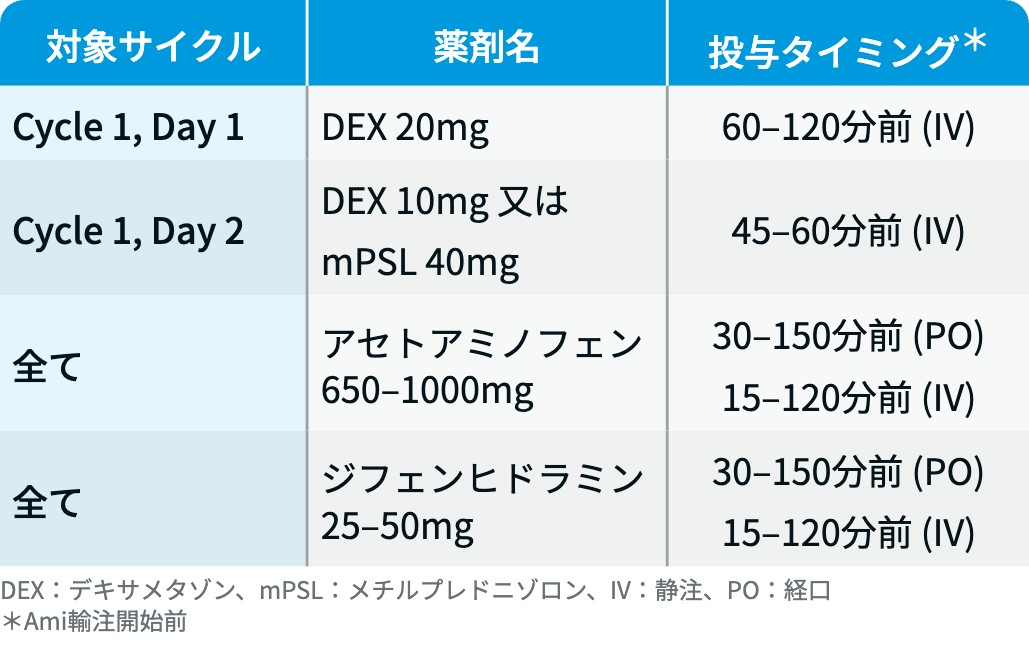
IRR (リブロファズ®) : 必須の前投薬で予防する。
▼リブロファズ®のピボタル試験で規定された必須の前投薬²⁾

皮膚・爪障害 : EGFR阻害薬に共通する症状であり、 保湿や日光防護に加え、 症状出現時はステロイド外用や抗生剤軟膏などで早期介入する。 重症例では休薬を検討する。
間質性肺疾患 : 呼吸困難、 咳嗽、 発熱などの初期症状を確認し、 定期的に胸部画像検査を行って十分に観察し、 必要に応じてPaO2、 SpO2、 A-aDO2、 DLco等を評価し、 症状出現時は速やかに受診するよう指導する。
皮下投与時の注意事項 (リブロファズ®) : 21~23G針または皮下投与セットを使用し、 1回量は15mL以内とする。 15mL超は複数シリンジに均等分割し、 腹部皮下に約5分で投与する。 複数回投与時は臍周囲5cmを避け、 腹部の異なる部位に連続投与し、 必要に応じて生食でフラッシュする。
RMP【重要な特定されたリスク】
リブロファズ®/ライブリバント® 医薬品リスク管理計画書 (RMP)
- Infusion reaction
- 間質性肺疾患
- 重度の皮膚障害
- 体液貯留
出典
1) ヤンセンファーマ株式会社. リブロファズ® 電子添文情報 2026年3月作成 第2版.
2) ヤンセンファーマ株式会社. リブロファズ® 適正使用ガイド 2026年3月作成.
3) ヤンセンファーマ株式会社. ライブリバント® 電子添文情報 2026年3月改訂 第6版.
4) ヤンセンファーマ株式会社. ライブリバント® 適正使用ガイド (カルボプラチン・ペメトレキセドの併用療法) 2025年5月改訂
5) Ann Oncol. 2024;35(1):77-90.
最終確認・更新日 : 2026年3月19日
執筆 : HOKUTO編集部がん専門・指導薬剤師
監修医師 : 和歌山県立医科大学附属病院 赤松弘
Amivantamab (IV/SC) +CBDCA+PEM
Amivantamab:Amivantamab(ライブリバント®)
| 投与量 | コース | 投与日 |
|---|---|---|
| 350mg 点滴 | 1 | Day 1 |
| 1050mg 点滴 | 1 | Day 2 |
| 1400mg 点滴 | 1 | Day 8、 15 |
| 1400mg 点滴 | 2 | Day 1 |
| 1750mg 点滴 | 3~ | Day 1 |
Amivantamab:Amivantamab+rHuPH20(リブロファズ®)
| 投与量 | コース | 投与日 |
|---|---|---|
| 1600mg 皮下注 | 1 | Day 1 |
| 2400mg 皮下注 | 1 | Day 8、 15 |
| 2400mg 皮下注 | 2~ | Day 1 |
PEM:Pemetrexed(ペメトレキセド®)
| 投与量 | コース | 投与日 |
|---|---|---|
| 500mg/m² 点滴 | 1~ | Day 1 |
CBDCA:Carboplatin(カルボプラチン®)
| 投与量 | コース | 投与日 |
|---|---|---|
| AUC 5 | 1~4 | Day 1 |
前投薬
| リブロファズ®投与前は、サイクル1 Day1にステロイド+抗ヒスタミン剤+解熱鎮痛剤(必要時H2拮抗剤・制吐剤)を投与し、Day8以降は抗ヒスタミン剤+解熱鎮痛剤(必要時ステロイド・H2拮抗剤・制吐剤)を投与する。 |
| ライブリバント®投与前は、サイクル1 Day1・2にステロイド+抗ヒスタミン剤+解熱鎮痛剤(必要時H2拮抗剤・制吐剤)を投与し、Day8以降は抗ヒスタミン剤+解熱鎮痛剤(必要時ステロイド・H2拮抗剤・制吐剤)を投与する。 |
その他
| 1コース21日間。 |
| アミバンタマブは、体重に基づき投与。初回は1400mg (体重≥80kg: 1750mg) をDay1/2に分割投与、Day8, 15に同量投与。Cycle 2 Day 1に同量投与。Cycle 3 Day 1以降は1750mg (体重≥80kg: 2100mg) を3週間間隔(各サイクルのDay 1)で点滴静注。 |
| CBDCAは最大4サイクルまで。その後は病勢進行までアミバンタマブ+PEM維持療法として継続。 |
| PEMはビタミンB₁₂、葉酸の補充が必須。 |
概要
2024年5月31日、 「EGFR遺伝子変異陽性の切除不能な進行・再発の非小細胞肺癌」 を対象として製造販売承認を申請し、 2025年5月19日に正式に承認された。
本コンテンツは特定の治療法を推奨するものではありません。 個々の患者の病態や、 実際の薬剤情報やガイドラインを確認の上、 利用者の判断と責任でご利用ください。
薬剤情報
リブロファズ® (アミバンタマブ+rHuPH20)
ライブリバント® (アミバンタマブ)
EGFR/MET二重特異性抗体
*ヤンセンファーマ株式会社の外部サイトへ遷移
投与スケジュール
【1コース】21日間
【催吐性】 中等度*
【FN発症】低リスク**
*Amivantamabは軽度、 CBDCA/PEMは中等度催吐性
**MARIPOSA-2試験⁵⁾のFN発症率2%に基づき編集部が分類。
▼1コース目

▼2コース目 : リブロファズ®は2コース目以降、 同量継続

▼3–4コース目 : ライブリバント®は3コース目以降、 同量継続

▼5コース目以降 : CBDCAは投与しない

アミバンタマブ (Ami) : 3週間を1コースとし、 1コース目は週1回投与、 2コース目以降は3週ごとに病勢進行まで継続投与 (用量は製剤ごとに以下のとおり)

Ami-SC : リブロファズ®、 Ami-IV : ライブリバント®、 Bw (kg)
ペメトレキセド (PEM) : 500mg/m²を各コースDay1に静脈内投与し、 疾患進行まで維持投与
カルボプラチン (CBDCA) : AUC 5をDay1に静脈内投与 (最大4コースまで)
MARIPOSA-2試験⁵⁾では、 PEM、 CBDCA、 Amiの順に投与した。
Key Data|臨床試験結果
📊 MARIPOSA-2試験
オシメルチニブ治療中または治療後に病勢進行したEGFR遺伝子変異 (Ex19delまたはL858R) 陽性の局所進行または転移性NSCLC患者657例を対象とする第III相無作為化比較試験である。 Ami+化学療法 (CBDCA+PEM) 群、 化学療法単独群、 Ami+Lazertinib+化学療法群に2:1:2で割り付けた。 主要評価項目はPFSであり、 Ami+化学療法群 vs 化学療法群、 ならびにAmi+Lazertinib+化学療法群 vs 化学療法群で評価した。
【有効性】Ami+化学療法群 (vs 化学療法)
- PFS中央値 6.3ヵ月 (vs 4.2ヵ月)
- HR 0.48 (95%CI 0.36–0.64、 p<0.001)
- 6ヵ月PFS率 51% (vs 30%)
- 12ヵ月PFS率 22% (vs 13%)
- 頭蓋内PFS中央値 12.5ヵ月 (vs 8.3ヵ月)
- HR 0.55 (95%CI 0.38–0.79)
- 客観的奏効率 64%
- 奏効期間中央値 6.9ヵ月
- OS (中間解析)
- HR 0.77 (95%CI 0.49–1.21)
【安全性】主な有害事象 : 全Grade (Grade≧3)
IV製剤のデータであることに留意
- 好中球減少 57% (45%)
- 血小板減少 44% (19%)
- Infusion-related reaction (IRR) 58% (5%)
- 貧血 39% (12%)
- 爪囲炎 37% (2%)
- 悪心 45% (1%)
- 発疹 43% (6%)
- 口内炎 32% (1%)
- 白血球減少 28% (20%)
- 低アルブミン血症 22% (2%)
- 便秘 38% (1%)
- 食欲減退 31% (0%)
- 末梢性浮腫 32% (2%)
- 嘔吐 25% (1%)
- 疲労 28% (3%)
- 下痢 14% (1%)
- 無力症 26% (1%)
- ざ瘡様皮膚炎 20% (4%)
- ALT上昇 20% (5%)
- 低カリウム血症 18% (5%)
- COVID-19 21% (2%)
- 低カルシウム血症 12% (1%)
- AST上昇 15% (1%)
- 低ナトリウム血症 10% (4%)
- 掻痒症 15% (0%)
各プロトコル
適格基準
MARIPOSA-2試験⁵⁾の主な適格基準
- 18歳以上
- ECOG PS 0または1
- 好中球≧1500/μL
- 血小板≧10万/μL
- Hb≧10g/dL
- 腎機能 : CrCl>50mL/min
- 肝機能 : T-Bil≦1.5×ULN、 ALT/AST≦3×ULN
リブロファズ®の減量・休薬・中止基準


リブロファズ®電子添文情報¹⁾を基に編集部作成
MARIPOSA-2試験⁵⁾では、 以下の血液毒性Grade 4が発現した場合に限り、 Ami投与を延期することが規定されていた。
- Grade 4の血液毒性が7日超で持続
- 出血または入院を伴う血小板減少Grade 4
- FN Grade 4
ライブリバント®の減量・休薬・中止基準


ライブリバント® 電子添文³⁾を基に編集部作成
MARIPOSA-2試験⁵⁾では、 以下の血液毒性Grade 4が発現した場合に限り、 Ami投与を延期することが規定されていた。
- Grade 4の血液毒性が7日超で持続
- 出血または入院を伴う血小板減少Grade 4
- FN Grade 4
CBDCA+PEMの減量・休薬・中止基準
以下に該当する場合は、 化学療法を延期する。
- 好中球<1500/µL
- 血小板<10万/µL
- 非血液毒性Grade≧3
MARIPOSA-2試験⁵⁾では、 CBDCA/PEMの再投与基準を満たさない場合は化学療法を1週ごとに延期し、 化学療法が予定日に実施できなくてもAmiの再投与基準を満たす場合はAmiを計画通り投与するとされた (化学療法がDay 8またはDay 15にずれた場合は、 次サイクルのAmiを±1週調整して化学療法と同日にそろえる)。
また、 有害事象発現時の用量調整は、 以下に基づき実施する。

GradeはNCI-CTCAE v.5.0に準拠。 MARIPOSA-2試験⁵⁾のプロトコルを基に編集部作成
腎障害患者に対する用量調節
Ami : 抗体薬は多様な細胞でのエンドサイトーシスとリソソーム分解により消失するため、 一般に減量は不要と考えられる。
編集部の見解
CBDCA : Calvert式で投与量を算出する
PEM : 重度の腎機能障害患者には投与しない。 なお、 CrCl<45mL/minの患者は別の臨床試験で除外されている
FDA添付文書 : CrCl<45mL/minの患者には投与しない
レジメンの特徴と注意点
2025年12月22日、 アミバンタマブ (ライブリバント®点滴静注) と同一の効能・効果で、 リブロファズ®配合皮下注 (アミバンタマブ・ボルヒアルロニダーゼ アルファ) が承認された。
🧑⚕️本レジメンは、 MARIPOSA試験と比較して皮膚障害はやや軽度である一方、 IRR、 下痢、 浮腫、 骨髄抑制など多様な有害事象への対応が求められる。 Amiの皮下投与により、 IRRおよびVTEの低減が期待されるほか、 投与時間の短縮も見込まれる。
和歌山県立医科大学附属病院 赤松弘朗先生
作用機序の特徴
Amiは、 EGFRとMETに対する二重特異性モノクローナル抗体であり、 シグナル伝達の阻害とADCC活性などにより腫瘍増殖を抑制すると考えられている。
本レジメンの位置付け
本レジメンは、 EGFR遺伝子変異陽性NSCLCに対し、 オシメルチニブ治療後に病勢進行した症例における2次治療以降の選択肢である。
レジメン適用時の注意事項
Ami、 ラゼルチニブ、 CBDCA、 PEMの4剤併用投与は行わないこと。
IRR (ライブリバント®) : Day 1・Day 2の分割投与および必須の前投薬で予防し、 規定の投与速度で投与する。 以下に、 投与速度および前投薬を示す。
▼ライブリバント®調製後の希釈液 (投与量/250mL) 投与速度

ライブリバント® 電子添文¹⁾を基に編集部作成
▼MARIPOSA-2試験⁵⁾で規定された必須の前投薬

IRR (リブロファズ®) : 必須の前投薬で予防する。
▼リブロファズ®のピボタル試験で規定された必須の前投薬²⁾

皮膚・爪障害 : EGFR阻害薬に共通する症状であり、 保湿や日光防護に加え、 症状出現時はステロイド外用や抗生剤軟膏などで早期介入する。 重症例では休薬を検討する。
間質性肺疾患 : 呼吸困難、 咳嗽、 発熱などの初期症状を確認し、 定期的に胸部画像検査を行って十分に観察し、 必要に応じてPaO2、 SpO2、 A-aDO2、 DLco等を評価し、 症状出現時は速やかに受診するよう指導する。
皮下投与時の注意事項 (リブロファズ®) : 21~23G針または皮下投与セットを使用し、 1回量は15mL以内とする。 15mL超は複数シリンジに均等分割し、 腹部皮下に約5分で投与する。 複数回投与時は臍周囲5cmを避け、 腹部の異なる部位に連続投与し、 必要に応じて生食でフラッシュする。
RMP【重要な特定されたリスク】
リブロファズ®/ライブリバント® 医薬品リスク管理計画書 (RMP)
- Infusion reaction
- 間質性肺疾患
- 重度の皮膚障害
- 体液貯留
出典
1) ヤンセンファーマ株式会社. リブロファズ® 電子添文情報 2026年3月作成 第2版.
2) ヤンセンファーマ株式会社. リブロファズ® 適正使用ガイド 2026年3月作成.
3) ヤンセンファーマ株式会社. ライブリバント® 電子添文情報 2026年3月改訂 第6版.
4) ヤンセンファーマ株式会社. ライブリバント® 適正使用ガイド (カルボプラチン・ペメトレキセドの併用療法) 2025年5月改訂
5) Ann Oncol. 2024;35(1):77-90.
最終確認・更新日 : 2026年3月19日
執筆 : HOKUTO編集部がん専門・指導薬剤師
監修医師 : 和歌山県立医科大学附属病院 赤松弘
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
がん薬物療法における治療計画をまとめたものです。
主要論文や適正使用ガイドをもとにした用量調整プロトコール、 有害事象対応をご紹介します。
なお、 本ツールは医師向けの教育用資料であり、 実臨床での使用は想定しておりません。 最新の添付文書やガイドラインを必ずご確認下さい。
また、 一般の方への情報提供ではないことを予めご了承ください。



