治療スケジュール
概要
監修医師
RAM:Ramucirumab(サイラムザ®)
| 投与量 | コース | 投与日 |
|---|---|---|
| 8mg/kg 点滴 | 1~ | Day1,15 |
nab-PTX:nab-Paclitaxel(アブラキサン®)
| 投与量 | コース | 投与日 |
|---|---|---|
| 100mg/m³ 点滴 | 1~ | Day1,8,15 |
その他
| 1コース28日間 |
本コンテンツは特定の治療法を推奨するものではありません。 個々の患者の病態や、 実際の薬剤情報やガイドラインを確認の上、 利用者の判断と責任でご利用ください。
薬剤情報
*大鵬薬品工業株式会社の外部サイトへ遷移します
*日本イーライリリー株式会社の外部サイトへ遷移します
用法用量
J-0202試験⁵⁾のプロトコル
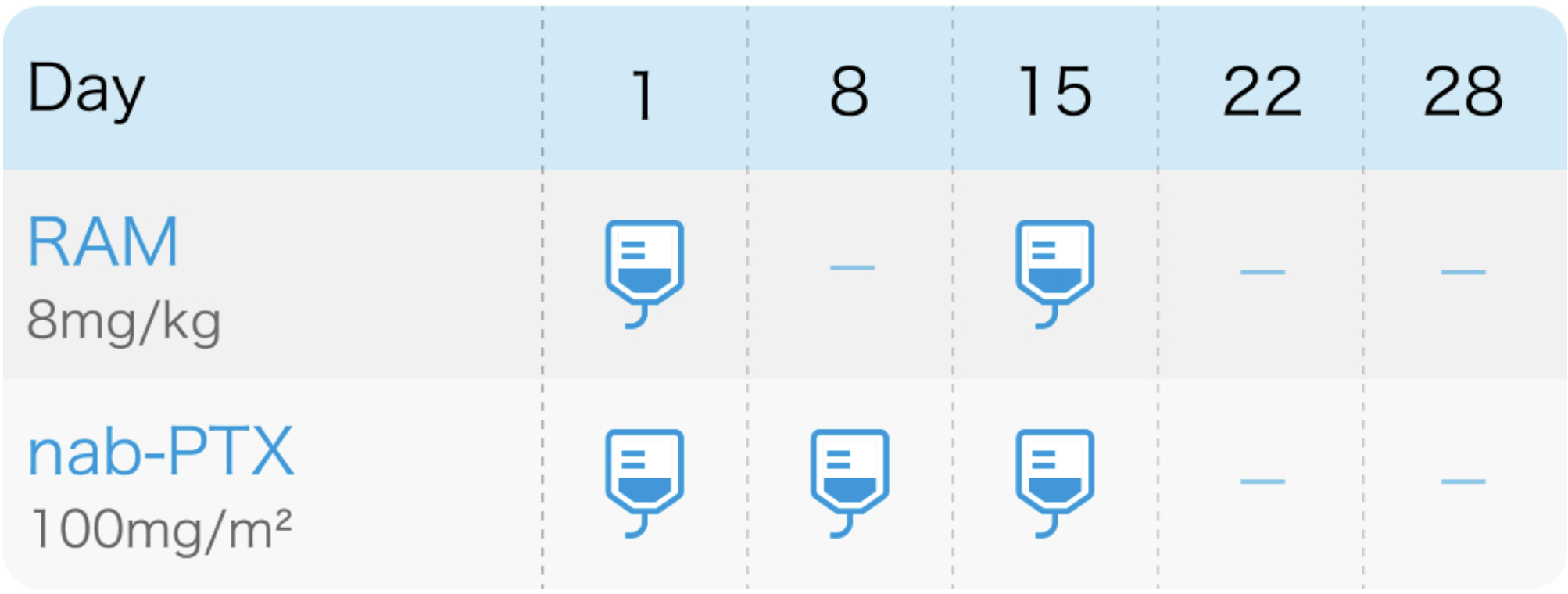
前投薬
Infusion reaction予防として
クロルフェニラミン5mg1A+NS 50mL div
執筆:静岡県立静岡がんセンター 消化器内科 川上 武志先生
投与開始基準
適正使用ガイド²⁾の基準

アブラキサン®適正使用ガイド (2022年11月改訂)²⁾より作図
減量・休薬・中止基準
ラムシルマブ電子添文³⁾の基準
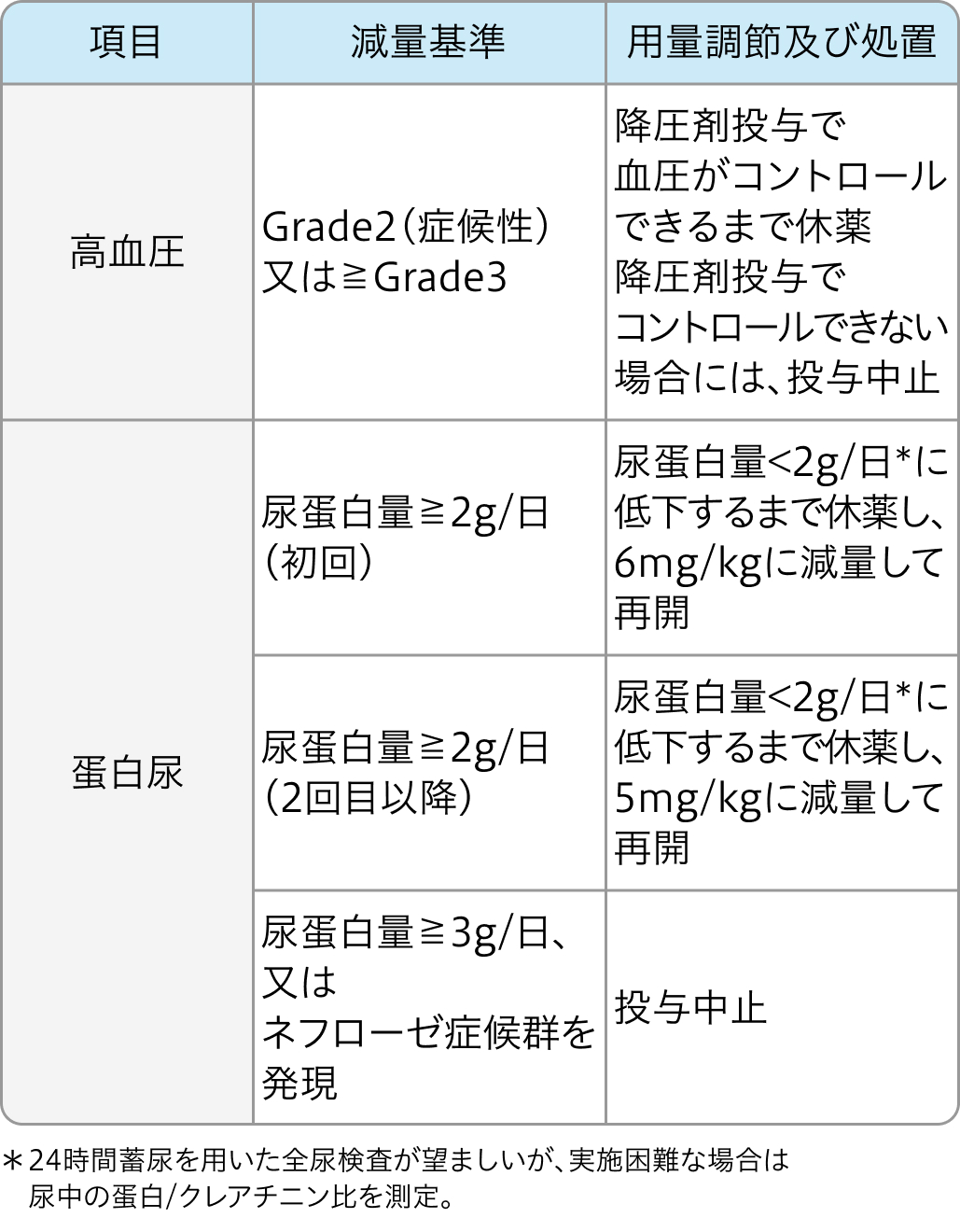
サイラムザ®電子添文 (2024年6月改訂第4版)³⁾より作図
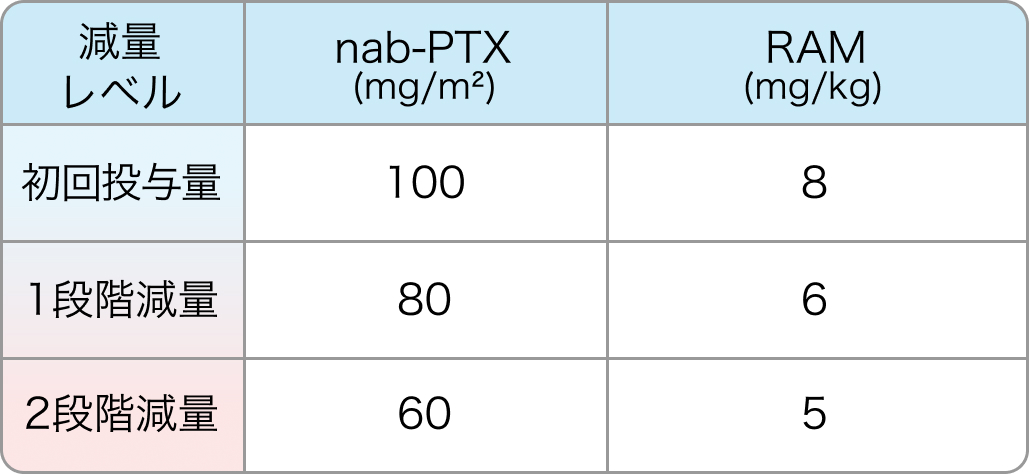
初回基準量と減量レベル
主な有害事象
J-0202試験⁵⁾
主な有害事象 (カッコ内はGrade3~4)
- 貧血 14.0% (9.3%)
- 白血球減少症 16.3% (14.0%)
- 下痢 23.3% (0%)
- 悪心 11.6% (2.3%)
- 口内炎 25.6% (0%)
- 疲労 16.3% (0%)
- 好中球数減少 90.7% (76.7%)
- 白血球数減少 20.9% (14.0%)
- 食欲減退 18.6% (7.0%)
注意すべき有害事象 (カッコ内はGrade3~4)
- 末梢性感覚ニューロパチー 58.1% (0%)
- 脱毛症 93.0% (0%)
- 高血圧 41.9% (4.7%)
Eur J Cancer. 2018 Mar;91:86-91⁵⁾より引用
上手に使うためのワンポイント
- RAMの血中濃度と有効性に相関が見られる報告があり⁶⁾、 nab-PTXが投与困難な場合でもRAMの禁忌が無い場合はRAMのみ投与する。
- 2次治療導入時、 末梢神経障害のため、 PTXまたはnab-PTXが導入できない場合、 RAM単剤で開始し、末梢神経障害が改善したタイミングでPTXまたはnab-PTXを開始する方法もある。
- 好中球数減少を繰り返す症例においては、 まずは減量を実施する。 減量後も血球減少を繰り返す症例は、 Biweekly投与も選択肢である⁷⁾。
- RAMで蛋白尿を生じることがあるが、 尿定性で2+以上でもUPCR<2であれば投与可能である。
執筆:静岡県立静岡がんセンター 消化器内科 川上 武志先生
特徴と注意点
- 胃癌治療ガイドラインでは、 条件付き推奨レジメンの1つである。
- RAMのinfusion reactionの頻度は低く⁸⁾⁹⁾、 適正使用ガイドにおいてもinfusion reaction予防の前投与は「考慮」となっている。 症例によっては前投薬のヒスタミン阻害剤は省略可能である。
- アルコール不耐や自家用車での通院を希望される症例に良い適応である。
- RAMはBmabと異なり、 蛋白尿Grade3を生じた場合は次回投与以降減量が必要である。
執筆:静岡県立静岡がんセンター 消化器内科 川上 武志先生
関連する臨床試験
J-0202試験⁵⁾
フッ化ピリミジン系抗悪性腫瘍剤を含む初回化学療法に不応となった切除不能進行・再発胃癌患者を対象として、 nab-PTX/RAM併用投与の有効性、安全性を評価した国内第Ⅱ相試験。 主要評価項目は全奏効率 (ORR)、 副次評価項目は無増悪生存期間 (PFS)、 安全性等に設定された。
Eur J Cancer. 2018 Mar;91:86-91.
出典
- 大鵬薬品工業株式会社. アブラキサン®電子添文 (2021年8月改訂 第1版) [最終閲覧 : 2024/7/18]
- 大鵬薬品工業株式会社. アブラキサン®適正使用ガイド (2022年11月改訂) [最終閲覧 : 2024/7/18]
- 日本イーライリリー株式会社. サイラムザ®電子添文 (2024年6月改訂第4版) [最終閲覧 : 2024/7/11]
- 日本イーライリリー株式会社. サイラムザ®適正使用ガイド (2024年6月作成) [最終閲覧 : 2024/7/18]
- A phase II study of nab-paclitaxel in combination with ramucirumab in patients with previously treated advanced gastric cancer. Eur J Cancer. 2018 Mar;91:86-91. PMID: 29353164
- Exposure-Response Analyses of Ramucirumab from Two Randomized, Phase III Trials of Second-line Treatment for Advanced Gastric or Gastroesophageal Junction Cancer. Mol Cancer Ther. 2017 Oct;16(10):2215-2222. PMID: 28716815
- A Multicenter, Phase II Trial of Schedule Modification for Nab-Paclitaxel in Combination with Ramucirumab for Patients with Previously Treated Advanced Gastric or Gastroesophageal Junction Cancer: The B-RAX Trial (JACCRO GC-09). Target Oncol. 2023 May;18(3):359-368. PMID: 37060430
- Safety of Ramucirumab Regimen Without H1-antihistamine Premedication in Patients With Solid Cancers. In Vivo. 2020 Nov-Dec;34(6):3489-3493. PMID: 33144458
- Infusion-related reaction to ramucirumab plus FOLFIRI in patients with advanced colorectal cancer. Int J Clin Oncol. 2021 Nov;26(11):2025-2028. PMID: 34476649
最終更新日:2024年8月27日
執筆医:静岡県立静岡がんセンター 消化器内科 川上 武志先生
監修医師:神奈川県立がんセンター消化器内科部長 町田望先生
nab-PTX + RAM
パクリタキセル (アルブミン懸濁型) (アブラキサン®) + ラムシルマブ(サイラムザ®)
胃癌 > 二次治療
2024年08月27日更新
RAM:Ramucirumab(サイラムザ®)
| 投与量 | コース | 投与日 |
|---|---|---|
| 8mg/kg 点滴 | 1~ | Day1,15 |
nab-PTX:nab-Paclitaxel(アブラキサン®)
| 投与量 | コース | 投与日 |
|---|---|---|
| 100mg/m³ 点滴 | 1~ | Day1,8,15 |
その他
| 1コース28日間 |
概要
本コンテンツは特定の治療法を推奨するものではありません。 個々の患者の病態や、 実際の薬剤情報やガイドラインを確認の上、 利用者の判断と責任でご利用ください。
薬剤情報
*大鵬薬品工業株式会社の外部サイトへ遷移します
*日本イーライリリー株式会社の外部サイトへ遷移します
用法用量
J-0202試験⁵⁾のプロトコル

前投薬
Infusion reaction予防として
クロルフェニラミン5mg1A+NS 50mL div
執筆:静岡県立静岡がんセンター 消化器内科 川上 武志先生
投与開始基準
適正使用ガイド²⁾の基準

アブラキサン®適正使用ガイド (2022年11月改訂)²⁾より作図
減量・休薬・中止基準
ラムシルマブ電子添文³⁾の基準

サイラムザ®電子添文 (2024年6月改訂第4版)³⁾より作図
初回基準量と減量レベル

主な有害事象
J-0202試験⁵⁾
主な有害事象 (カッコ内はGrade3~4)
- 貧血 14.0% (9.3%)
- 白血球減少症 16.3% (14.0%)
- 下痢 23.3% (0%)
- 悪心 11.6% (2.3%)
- 口内炎 25.6% (0%)
- 疲労 16.3% (0%)
- 好中球数減少 90.7% (76.7%)
- 白血球数減少 20.9% (14.0%)
- 食欲減退 18.6% (7.0%)
注意すべき有害事象 (カッコ内はGrade3~4)
- 末梢性感覚ニューロパチー 58.1% (0%)
- 脱毛症 93.0% (0%)
- 高血圧 41.9% (4.7%)
Eur J Cancer. 2018 Mar;91:86-91⁵⁾より引用
上手に使うためのワンポイント
- RAMの血中濃度と有効性に相関が見られる報告があり⁶⁾、 nab-PTXが投与困難な場合でもRAMの禁忌が無い場合はRAMのみ投与する。
- 2次治療導入時、 末梢神経障害のため、 PTXまたはnab-PTXが導入できない場合、 RAM単剤で開始し、末梢神経障害が改善したタイミングでPTXまたはnab-PTXを開始する方法もある。
- 好中球数減少を繰り返す症例においては、 まずは減量を実施する。 減量後も血球減少を繰り返す症例は、 Biweekly投与も選択肢である⁷⁾。
- RAMで蛋白尿を生じることがあるが、 尿定性で2+以上でもUPCR<2であれば投与可能である。
執筆:静岡県立静岡がんセンター 消化器内科 川上 武志先生
特徴と注意点
- 胃癌治療ガイドラインでは、 条件付き推奨レジメンの1つである。
- RAMのinfusion reactionの頻度は低く⁸⁾⁹⁾、 適正使用ガイドにおいてもinfusion reaction予防の前投与は「考慮」となっている。 症例によっては前投薬のヒスタミン阻害剤は省略可能である。
- アルコール不耐や自家用車での通院を希望される症例に良い適応である。
- RAMはBmabと異なり、 蛋白尿Grade3を生じた場合は次回投与以降減量が必要である。
執筆:静岡県立静岡がんセンター 消化器内科 川上 武志先生
関連する臨床試験
J-0202試験⁵⁾
フッ化ピリミジン系抗悪性腫瘍剤を含む初回化学療法に不応となった切除不能進行・再発胃癌患者を対象として、 nab-PTX/RAM併用投与の有効性、安全性を評価した国内第Ⅱ相試験。 主要評価項目は全奏効率 (ORR)、 副次評価項目は無増悪生存期間 (PFS)、 安全性等に設定された。
Eur J Cancer. 2018 Mar;91:86-91.
出典
- 大鵬薬品工業株式会社. アブラキサン®電子添文 (2021年8月改訂 第1版) [最終閲覧 : 2024/7/18]
- 大鵬薬品工業株式会社. アブラキサン®適正使用ガイド (2022年11月改訂) [最終閲覧 : 2024/7/18]
- 日本イーライリリー株式会社. サイラムザ®電子添文 (2024年6月改訂第4版) [最終閲覧 : 2024/7/11]
- 日本イーライリリー株式会社. サイラムザ®適正使用ガイド (2024年6月作成) [最終閲覧 : 2024/7/18]
- A phase II study of nab-paclitaxel in combination with ramucirumab in patients with previously treated advanced gastric cancer. Eur J Cancer. 2018 Mar;91:86-91. PMID: 29353164
- Exposure-Response Analyses of Ramucirumab from Two Randomized, Phase III Trials of Second-line Treatment for Advanced Gastric or Gastroesophageal Junction Cancer. Mol Cancer Ther. 2017 Oct;16(10):2215-2222. PMID: 28716815
- A Multicenter, Phase II Trial of Schedule Modification for Nab-Paclitaxel in Combination with Ramucirumab for Patients with Previously Treated Advanced Gastric or Gastroesophageal Junction Cancer: The B-RAX Trial (JACCRO GC-09). Target Oncol. 2023 May;18(3):359-368. PMID: 37060430
- Safety of Ramucirumab Regimen Without H1-antihistamine Premedication in Patients With Solid Cancers. In Vivo. 2020 Nov-Dec;34(6):3489-3493. PMID: 33144458
- Infusion-related reaction to ramucirumab plus FOLFIRI in patients with advanced colorectal cancer. Int J Clin Oncol. 2021 Nov;26(11):2025-2028. PMID: 34476649
最終更新日:2024年8月27日
執筆医:静岡県立静岡がんセンター 消化器内科 川上 武志先生
監修医師:神奈川県立がんセンター消化器内科部長 町田望先生
こちらの記事の監修医師
HOKUTO編集部
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
HOKUTO編集部
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
レジメン(消化器)
がん薬物療法における治療計画をまとめたものです。
主要論文や適正使用ガイドをもとにした用量調整プロトコール、 有害事象対応をご紹介します。
なお、 本ツールは医師向けの教育用資料であり、 実臨床での使用は想定しておりません。 最新の添付文書やガイドラインを必ずご確認下さい。
また、 一般の方への情報提供ではないことを予めご了承ください。

