「進行再発の子宮体癌」 「ミスマッチ修復機能正常 (pMMR) の進行・再発の子宮体癌におけるデュルバルマブ (遺伝子組換え) を含む化学療法後の維持療法」 に対して、2024年10月30日に二部会の報告品目、 2024年11月22日に追加承認取得
本コンテンツは特定の治療法を推奨するものではありません。 個々の患者の病態や、 実際の薬剤情報やガイドラインを確認の上、 利用者の判断と責任でご利用ください。
薬剤情報
抗PD-L1抗体 デュルバルマブ
*アストラゼネカ株式会社の外部サイトへ遷移します
PARP阻害薬 オラパリブ
*アストラゼネカ株式会社の外部サイトへ遷移します
用法用量
DUO-E試験³⁾のプロトコル
白金製剤ベースの化学療法 (カルボプラチン AUC 5または6およびパクリタキセル 175mg/m²を3週間ごと) に加え、 デュルバルマブ 1,120mgを3週間ごと6サイクル投与

その後、 病勢が進行しなかった患者に維持療法として、 イミフィンジ1,500mgを4週間ごと ± オラパリブ 300mgを1日2回病勢進行まで投与
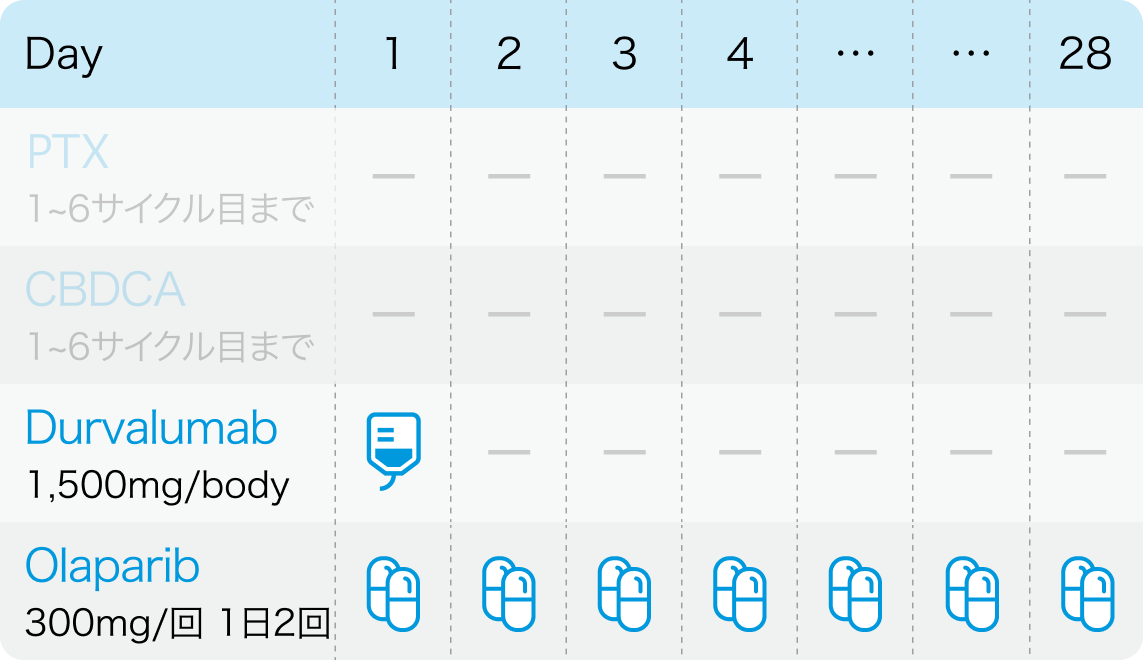
J Clin Oncol. 2024;42(3):283-99.より引用
添付文書の用法・用量 (一部引用改変)
DUO-E試験³⁾のプロトコルと同様である
イミフィンジ® : カルボプラチン及びタキサン系抗悪性腫瘍剤との併用で通常、 成人にはデュルバルマブ 1回1,120mgを3週間間隔で、 60分間以上かけて点滴静注。 その後の維持療法において、 デュルバルマブとして、 1回1500mgを4週間間隔で60分間以上かけて点滴静注。 ただし、 体重30kg以下の場合、 維持療法における1回投与量は、 20mg/kg (体重) とする。
リムパーザ® : デュルバルマブとの併用で通常、 成人にはオラパリブ 1回300mgを1日2回、 経口投与。 なお、 患者の状態により適宜減量する。
エキスパートによるワンポイント
DUO-E試験でPFS延長
進行再発子宮体癌に対し、 標準治療であるTC療法 (PTX + CBDCA) に、 PD-L1阻害剤であるDurvalmab単剤を上乗せする効果、 Durvalmabに加えPARP阻害剤であるOlaparibを上乗せする効果、 を検証した3群のランダム化比較試験。
無増悪生存期間 (PFS) は、 Durvalmab、 Durvalmab+Olaparibの両群ともPFS延長効果をもたらした。 しかし、 中間解析の結果であるが、 OS (全生存期間) は、 Durvalmab+Olaprib群のみOS延長効果があったということである。
監修 : 日本医科大学 武蔵小杉病院 腫瘍内科教授 勝俣 範之先生
Pembrolizumab併用との比較
進行子宮体癌に対しては、 Pembrolizumab、 Durvalmab+Olaparibの2剤が承認、 保険適用となる予定だが、 現時点ではPembrolizumabと Durvalmab+Olaparibのどちらが有用であるかどうかのエビデンスは不明である。
Durvalmab+Olaparibは、 有害事象がやや増えること、 費用負担が問題となる可能性がある。
監修 : 日本医科大学 武蔵小杉病院 腫瘍内科教授 勝俣 範之先生
KeyData|臨床試験結果
DUO-E試験³⁾
J Clin Oncol. 2024;42(3):283-99.
新たに診断された進行上皮性子宮体癌または再発子宮体癌の患者699人を対象に、 初回治療として デュルバルマブ+化学療法併用療法後に、 デュルバルマブ±オラパリブ併用による維持療法と、 化学療法を比較した第Ⅲ相試験。 主要評価項目はPFSであった。
【有効性】ITT集団
- mPFS
- TCのみ : 7.0ヵ月
- D併用 : 未到達
- D+O併用 : 31.8ヵ月
- ORR
- TCのみ : 55.1%
- D併用 : 61.9%
- D+O併用 : 63.6%
- mDOR
- TCのみ : 7.7ヵ月
- D併用 : 13.1ヵ月
- D+O併用 : 21.3ヵ月
【有効性】dMMR集団
- mPFS
- TCのみ : 7.0ヵ月
- D併用 : 10.2ヵ月
- D+O併用 : 15.1ヵ月
- ORR
- TCのみ : 50.5%
- D併用 : 40.5%
- D+O併用 : 71.4%
- mDOR
- TCのみ : 10.5ヵ月
- D併用 : 未到達
- D+O併用 : 29.9ヵ月
【有効性】pMMR集団
- mPFS
- TCのみ : 9.7ヵ月
- D併用 : 9.9ヵ月
- D+O併用 : 15.0ヵ月
- ORR
- TCのみ : 59.0%
- D併用 : 59.4%
- D+O併用 : 62.1%
- mDOR
- TCのみ : 7.6ヵ月
- D併用 : 10.6ヵ月
- D+O併用 : 18.7ヵ月
出典
1) アストラゼネカ株式会社. イミフィンジ®電子添文 (2026年1月改訂 第10版)
2) アストラゼネカ株式会社. リムパーザ®電子添文 (2026年3月改訂第7版)
最終更新日 : 2026年3月18日
監修医師 : 日本医科大学 武蔵小杉病院 腫瘍内科教授 勝俣 範之先生
TC + Durvalumab ± Olaparib
「進行再発の子宮体癌」 「ミスマッチ修復機能正常 (pMMR) の進行・再発の子宮体癌におけるデュルバルマブ (遺伝子組換え) を含む化学療法後の維持療法」 に対して、2024年10月30日に二部会の報告品目、 2024年11月22日に追加承認取得
本コンテンツは特定の治療法を推奨するものではありません。 個々の患者の病態や、 実際の薬剤情報やガイドラインを確認の上、 利用者の判断と責任でご利用ください。
薬剤情報
抗PD-L1抗体 デュルバルマブ
*アストラゼネカ株式会社の外部サイトへ遷移します
PARP阻害薬 オラパリブ
*アストラゼネカ株式会社の外部サイトへ遷移します
用法用量
DUO-E試験³⁾のプロトコル
白金製剤ベースの化学療法 (カルボプラチン AUC 5または6およびパクリタキセル 175mg/m²を3週間ごと) に加え、 デュルバルマブ 1,120mgを3週間ごと6サイクル投与

その後、 病勢が進行しなかった患者に維持療法として、 イミフィンジ1,500mgを4週間ごと ± オラパリブ 300mgを1日2回病勢進行まで投与

J Clin Oncol. 2024;42(3):283-99.より引用
添付文書の用法・用量 (一部引用改変)
DUO-E試験³⁾のプロトコルと同様である
イミフィンジ® : カルボプラチン及びタキサン系抗悪性腫瘍剤との併用で通常、 成人にはデュルバルマブ 1回1,120mgを3週間間隔で、 60分間以上かけて点滴静注。 その後の維持療法において、 デュルバルマブとして、 1回1500mgを4週間間隔で60分間以上かけて点滴静注。 ただし、 体重30kg以下の場合、 維持療法における1回投与量は、 20mg/kg (体重) とする。
リムパーザ® : デュルバルマブとの併用で通常、 成人にはオラパリブ 1回300mgを1日2回、 経口投与。 なお、 患者の状態により適宜減量する。
エキスパートによるワンポイント
DUO-E試験でPFS延長
進行再発子宮体癌に対し、 標準治療であるTC療法 (PTX + CBDCA) に、 PD-L1阻害剤であるDurvalmab単剤を上乗せする効果、 Durvalmabに加えPARP阻害剤であるOlaparibを上乗せする効果、 を検証した3群のランダム化比較試験。
無増悪生存期間 (PFS) は、 Durvalmab、 Durvalmab+Olaparibの両群ともPFS延長効果をもたらした。 しかし、 中間解析の結果であるが、 OS (全生存期間) は、 Durvalmab+Olaprib群のみOS延長効果があったということである。
監修 : 日本医科大学 武蔵小杉病院 腫瘍内科教授 勝俣 範之先生
Pembrolizumab併用との比較
進行子宮体癌に対しては、 Pembrolizumab、 Durvalmab+Olaparibの2剤が承認、 保険適用となる予定だが、 現時点ではPembrolizumabと Durvalmab+Olaparibのどちらが有用であるかどうかのエビデンスは不明である。
Durvalmab+Olaparibは、 有害事象がやや増えること、 費用負担が問題となる可能性がある。
監修 : 日本医科大学 武蔵小杉病院 腫瘍内科教授 勝俣 範之先生
KeyData|臨床試験結果
DUO-E試験³⁾
J Clin Oncol. 2024;42(3):283-99.
新たに診断された進行上皮性子宮体癌または再発子宮体癌の患者699人を対象に、 初回治療として デュルバルマブ+化学療法併用療法後に、 デュルバルマブ±オラパリブ併用による維持療法と、 化学療法を比較した第Ⅲ相試験。 主要評価項目はPFSであった。
【有効性】ITT集団
- mPFS
- TCのみ : 7.0ヵ月
- D併用 : 未到達
- D+O併用 : 31.8ヵ月
- ORR
- TCのみ : 55.1%
- D併用 : 61.9%
- D+O併用 : 63.6%
- mDOR
- TCのみ : 7.7ヵ月
- D併用 : 13.1ヵ月
- D+O併用 : 21.3ヵ月
【有効性】dMMR集団
- mPFS
- TCのみ : 7.0ヵ月
- D併用 : 10.2ヵ月
- D+O併用 : 15.1ヵ月
- ORR
- TCのみ : 50.5%
- D併用 : 40.5%
- D+O併用 : 71.4%
- mDOR
- TCのみ : 10.5ヵ月
- D併用 : 未到達
- D+O併用 : 29.9ヵ月
【有効性】pMMR集団
- mPFS
- TCのみ : 9.7ヵ月
- D併用 : 9.9ヵ月
- D+O併用 : 15.0ヵ月
- ORR
- TCのみ : 59.0%
- D併用 : 59.4%
- D+O併用 : 62.1%
- mDOR
- TCのみ : 7.6ヵ月
- D併用 : 10.6ヵ月
- D+O併用 : 18.7ヵ月
出典
1) アストラゼネカ株式会社. イミフィンジ®電子添文 (2026年1月改訂 第10版)
2) アストラゼネカ株式会社. リムパーザ®電子添文 (2026年3月改訂第7版)
最終更新日 : 2026年3月18日
監修医師 : 日本医科大学 武蔵小杉病院 腫瘍内科教授 勝俣 範之先生
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
がん薬物療法における治療計画をまとめたものです。
主要論文や適正使用ガイドをもとにした用量調整プロトコール、 有害事象対応をご紹介します。
なお、 本ツールは医師向けの教育用資料であり、 実臨床での使用は想定しておりません。 最新の添付文書やガイドラインを必ずご確認下さい。
また、 一般の方への情報提供ではないことを予めご了承ください。