本コンテンツは特定の治療法を推奨するものではありません。 個々の患者の病態や、 実際の薬剤情報やガイドラインを確認の上、 利用者の判断と責任でご利用ください。
薬剤情報
アドリアシン® (添付文書¹⁾)
抗腫瘍性抗生物質 ドキソルビシン塩酸塩注射用
投与スケジュール
GeDDis試験²⁾のプロトコル
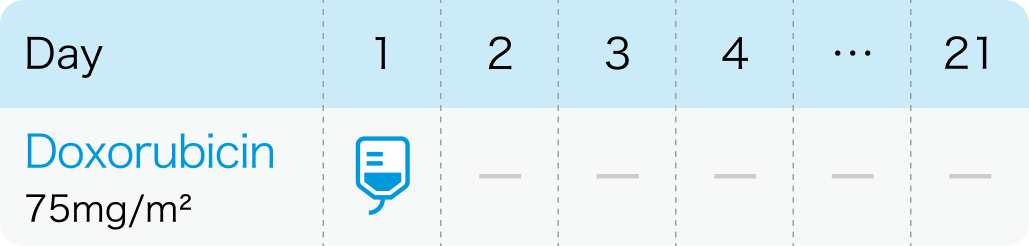
ドキソルビシン75mg/m²を21日サイクルで1日目に投与。 最大で6サイクルまで実施。
エキスパートによるワンポイント
進行・再発悪性軟部肉腫の標準治療
進行・再発悪性軟部肉腫に対しては、 DG療法 (DTX+GEM) は、 第Ⅱ相試験で良好な腫瘍縮小率があり、 期待された療法であったが、 第Ⅲ相試験GeDDis試験で、 従来からのアドリアマイシン単剤療法と比較した結果、 無増悪生存期間 (PFS)、 全生存期間 (OS) に差はなかった。
結果、 進行・再発悪性軟部肉腫に対する標準治療は、 引き続きアドリアマイシン単剤となった。
監修 : 日本医科大学 武蔵小杉病院 腫瘍内科教授 勝俣 範之先生
KeyData|臨床試験結果
GeDDis試験²⁾
英国の24の病院とスイス臨床癌研究グループ (SAKK) の1つの病院で実施された悪性軟部腫瘍進行例にドキソルビシン単剤とDG療法の有効性と安全性を比較したランダム化比較第Ⅲ相試験。 子宮平滑筋肉腫の患者は257例中71例含まれていた (ドキソルビシン129例中36例とDG療法128例中35例)。
有効性|ドキソルビシン群 全129例*
*子宮肉腫36例以外に悪性軟部肉腫93例を含む
- ORR : 20% (DG療法 20%)
- mPFS : 23.3週 (DG療法 23.7週)
- mOS : 76.3週 (DG療法 67.3週)
いずれもDG療法と有意差なし。 子宮肉腫患者のサブグループ解析も同様であった。
出典
1) 日本化薬株式会社. アドリアシン®電子添文 (2022年11月改訂 第1版) [最終閲覧 : 2024/12/29]
その他情報は随時更新予定です
最終更新日 : 2024年12月29日
監修医師 : 日本医科大学 武蔵小杉病院 腫瘍内科教授 勝俣 範之先生
Doxorubicin
本コンテンツは特定の治療法を推奨するものではありません。 個々の患者の病態や、 実際の薬剤情報やガイドラインを確認の上、 利用者の判断と責任でご利用ください。
薬剤情報
アドリアシン® (添付文書¹⁾)
抗腫瘍性抗生物質 ドキソルビシン塩酸塩注射用
投与スケジュール
GeDDis試験²⁾のプロトコル

ドキソルビシン75mg/m²を21日サイクルで1日目に投与。 最大で6サイクルまで実施。
エキスパートによるワンポイント
進行・再発悪性軟部肉腫の標準治療
進行・再発悪性軟部肉腫に対しては、 DG療法 (DTX+GEM) は、 第Ⅱ相試験で良好な腫瘍縮小率があり、 期待された療法であったが、 第Ⅲ相試験GeDDis試験で、 従来からのアドリアマイシン単剤療法と比較した結果、 無増悪生存期間 (PFS)、 全生存期間 (OS) に差はなかった。
結果、 進行・再発悪性軟部肉腫に対する標準治療は、 引き続きアドリアマイシン単剤となった。
監修 : 日本医科大学 武蔵小杉病院 腫瘍内科教授 勝俣 範之先生
KeyData|臨床試験結果
GeDDis試験²⁾
英国の24の病院とスイス臨床癌研究グループ (SAKK) の1つの病院で実施された悪性軟部腫瘍進行例にドキソルビシン単剤とDG療法の有効性と安全性を比較したランダム化比較第Ⅲ相試験。 子宮平滑筋肉腫の患者は257例中71例含まれていた (ドキソルビシン129例中36例とDG療法128例中35例)。
有効性|ドキソルビシン群 全129例*
*子宮肉腫36例以外に悪性軟部肉腫93例を含む
- ORR : 20% (DG療法 20%)
- mPFS : 23.3週 (DG療法 23.7週)
- mOS : 76.3週 (DG療法 67.3週)
いずれもDG療法と有意差なし。 子宮肉腫患者のサブグループ解析も同様であった。
出典
1) 日本化薬株式会社. アドリアシン®電子添文 (2022年11月改訂 第1版) [最終閲覧 : 2024/12/29]
その他情報は随時更新予定です
最終更新日 : 2024年12月29日
監修医師 : 日本医科大学 武蔵小杉病院 腫瘍内科教授 勝俣 範之先生
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
がん薬物療法における治療計画をまとめたものです。
主要論文や適正使用ガイドをもとにした用量調整プロトコール、 有害事象対応をご紹介します。
なお、 本ツールは医師向けの教育用資料であり、 実臨床での使用は想定しておりません。 最新の添付文書やガイドラインを必ずご確認下さい。
また、 一般の方への情報提供ではないことを予めご了承ください。