本コンテンツは特定の治療法を推奨するものではありません。 個々の患者の病態や、 実際の薬剤情報やガイドラインを確認の上、 利用者の判断と責任でご利用ください。
薬剤情報
PARP阻害薬 オラパリブ *MSD株式会社の外部サイトへ遷移
投与スケジュール
電子添文¹⁾の用法および用量
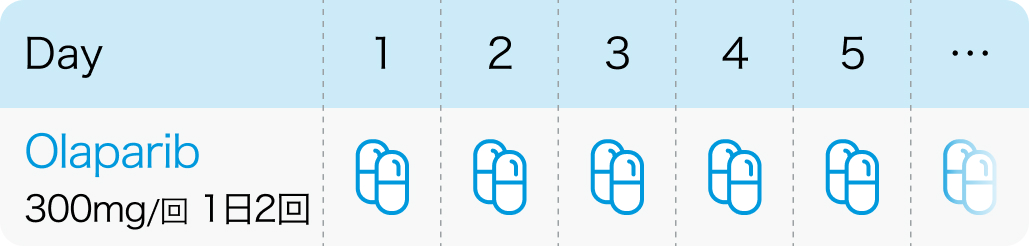
1回300mgを1日2回、 経口投与
*100mg錠と150mg錠の生物学的同等性は示されていないため、 300mgを投与する際には100mg錠を使用しないこと
リムパーザ®電子添文 (2024年11月改訂第6版)¹⁾より作図
各プロトコル
投与開始基準
SOLO1試験³⁾のプロトコル例
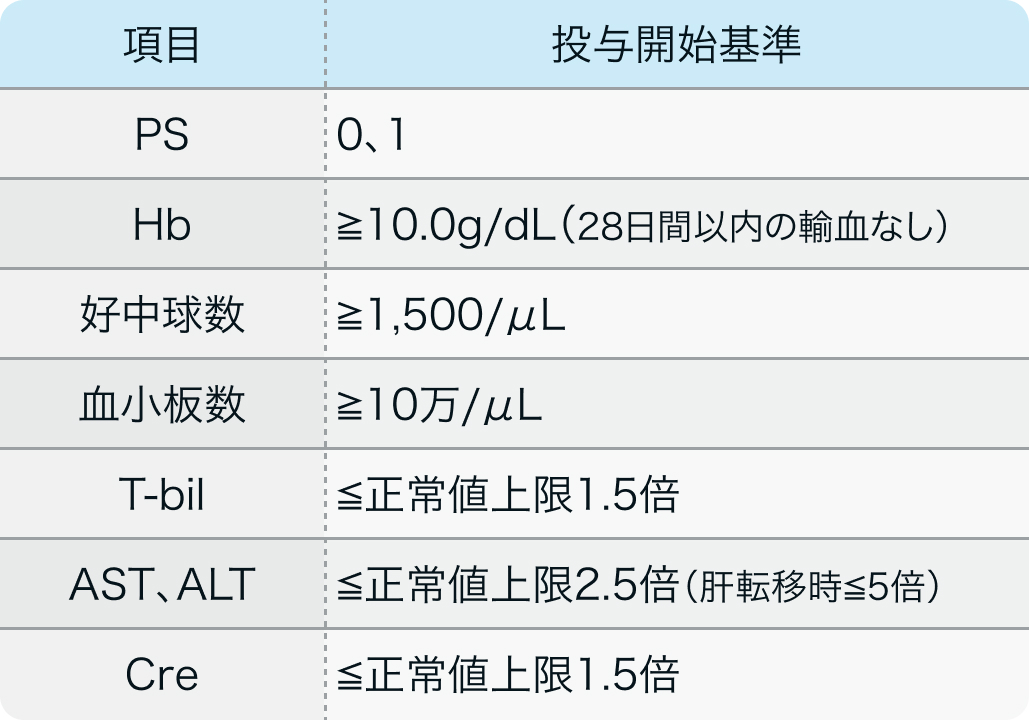
N Engl J Med. 2018 Dec 27;379(26):2495-2505³⁾より作図
電子添文¹⁾の効能または効果
白金系抗悪性腫瘍剤感受性の再発卵巣癌における維持療法 : 再発時の白金系抗悪性腫瘍剤を含む化学療法で奏効が維持されている患者
BRCA遺伝子変異陽性の卵巣癌における初回化学療法後の維持療法 : 国際産婦人科連合 (FIGO) 進行期分類III期またはIV期の卵巣癌と診断され、 白金系抗悪性腫瘍剤を含む初回化学療法で奏効が維持されている患者。 承認された体外診断用医薬品または医療機器を用いた検査により、 BRCA遺伝子変異を有することが確認された患者
リムパーザ®電子添文 (2024年11月改訂第6版)¹⁾より引用
減量・休薬・中止基準
電子添文¹⁾の基準

リムパーザ®電子添文 (2024年11月改訂第6版)¹⁾より作図
KeyData|臨床試験結果
SOLO2試験³⁾
対象: gBRCA遺伝子変異陽性プラチナ製剤感受性再発卵巣患者295例
方法: Olaparib群 vs プラセボ群
【有効性】Olaparib群
mPFS 19.1ヵ月
【安全性】主な有害事象(カッコ内はGrade3~4)
- 貧血 43.6% (19.5%)
- 好中球数減少 19.5% (5.1%)
- 血小板数減少 13.8% (1.0%)
- クレアチニン上昇 10.8% (0%)
- 白血球数減少 10.3% (1.5%)
- 悪心 75.9% (2.6%)
- 倦怠感/無力症 65.6% (4.1%)
- 嘔吐 37.4% (2.6%)
- 下痢 32.8% (1.0%)
- 食欲減退 22.1% (0%)
- 便秘 20.5% (0%)
- 発熱 13.3% (0%)
Lancet Oncol. 2017 Sep;18(9):1274-1284³⁾より引用
エキスパートによるワンポイント
SOLO-1試験の有効性
BRCA変異陽性卵巣癌患者に対して、 初回化学療法後の維持療法として、 Olaparib内服は、 プラセボ群と比較した第Ⅲ相SOLO-1試験でプライマリーエンドポイントの無増悪生存期間 (PFS) を有意に延長させました⁴⁾。
しかし、 その後報告された全生存期間 (OS) は、 Olaparib群に、 良好な結果 (HR=0.55、 95%CI 0.40-0.76, p=0.0004) であったものの⁵⁾、 αエラーを防ぐため多重性の調整をしたp<0.0001を満たさず、 OSに関しては、 有意差はなしと判定されています。
この理由として、 SOLO2試験の探索的解析結果⁶⁾からは、 「Olaparib使用後プラチナ耐性になってしまい予後が不良になる」 ことが示唆されています⁶⁾。
注意すべき有害事象とその対応
注意すべき有害事象として、 貧血は38.8% (うちGrade3 21.5%) に発生しました。 MDS/AMLの発生率は1.5% (プラセボ群0.8%) でした⁵⁾。 特にMDS/AMLに関しては重大な合併症であり、 発症した場合は血液内科医へのコンサルテーションが必要となります。
Re-challaengeについて
初回化学療法後にPARP阻害剤を投与された患者に対して、 再発後化学療法後の維持療法としてオラパリブを再使用すること (Re-challenge) については、 有効性を示すエビデンスが不足しているため、 現時点では再使用は控えるべきと考えられます⁶⁾。
監修 : 日本医科大学 武蔵小杉病院 腫瘍内科教授 勝俣 範之先生
出典
- アストラゼネカ株式会社. リムパーザ®電子添文 (2026年3月改訂第7版).
- アストラゼネカ株式会社. リムパーザ®適正使用ガイド (2024年12月作成).
- Olaparib tablets as maintenance therapy in patients with platinum-sensitive, relapsed ovarian cancer and a BRCA1/2 mutation (SOLO2/ENGOT-Ov21): a double-blind, randomised, placebo-controlled, phase 3 trial. Lancet Oncol. 2017 Sep;18(9):1274-1284. PMID: 2875448
- Maintenance Olaparib in Patients with Newly Diagnosed Advanced Ovarian Cancer. N Engl J Med. 2018 Dec 27;379(26):2495-2505. PMID: 30345884
- Overall Survival With Maintenance Olaparib at a 7-Year Follow-Up in Patients With Newly Diagnosed Advanced Ovarian Cancer and a BRCA Mutation: The SOLO1/GOG 3004 Trial. J Clin Oncol. 2022 Sep 9;JCO2201549.PMID: 36082969
- Efficacy of subsequent chemotherapy for patients with BRCA1/2-mutated recurrent epithelial ovarian cancer progressing on olaparib versus placebo maintenance: post-hoc analyses of the SOLO2/ENGOT Ov-21 trial. Ann Oncol. 2022 Oct;33(10):1021-1028. PMID: 35772665
最終更新日 : 2026年3月18日
監修医師 : 日本医科大学 武蔵小杉病院 腫瘍内科教授 勝俣 範之先生
Olaparib
本コンテンツは特定の治療法を推奨するものではありません。 個々の患者の病態や、 実際の薬剤情報やガイドラインを確認の上、 利用者の判断と責任でご利用ください。
薬剤情報
PARP阻害薬 オラパリブ *MSD株式会社の外部サイトへ遷移
投与スケジュール
電子添文¹⁾の用法および用量

1回300mgを1日2回、 経口投与
*100mg錠と150mg錠の生物学的同等性は示されていないため、 300mgを投与する際には100mg錠を使用しないこと
リムパーザ®電子添文 (2024年11月改訂第6版)¹⁾より作図
各プロトコル
投与開始基準
SOLO1試験³⁾のプロトコル例

N Engl J Med. 2018 Dec 27;379(26):2495-2505³⁾より作図
電子添文¹⁾の効能または効果
白金系抗悪性腫瘍剤感受性の再発卵巣癌における維持療法 : 再発時の白金系抗悪性腫瘍剤を含む化学療法で奏効が維持されている患者
BRCA遺伝子変異陽性の卵巣癌における初回化学療法後の維持療法 : 国際産婦人科連合 (FIGO) 進行期分類III期またはIV期の卵巣癌と診断され、 白金系抗悪性腫瘍剤を含む初回化学療法で奏効が維持されている患者。 承認された体外診断用医薬品または医療機器を用いた検査により、 BRCA遺伝子変異を有することが確認された患者
リムパーザ®電子添文 (2024年11月改訂第6版)¹⁾より引用
減量・休薬・中止基準
電子添文¹⁾の基準

リムパーザ®電子添文 (2024年11月改訂第6版)¹⁾より作図
KeyData|臨床試験結果
SOLO2試験³⁾
対象: gBRCA遺伝子変異陽性プラチナ製剤感受性再発卵巣患者295例
方法: Olaparib群 vs プラセボ群
【有効性】Olaparib群
mPFS 19.1ヵ月
【安全性】主な有害事象(カッコ内はGrade3~4)
- 貧血 43.6% (19.5%)
- 好中球数減少 19.5% (5.1%)
- 血小板数減少 13.8% (1.0%)
- クレアチニン上昇 10.8% (0%)
- 白血球数減少 10.3% (1.5%)
- 悪心 75.9% (2.6%)
- 倦怠感/無力症 65.6% (4.1%)
- 嘔吐 37.4% (2.6%)
- 下痢 32.8% (1.0%)
- 食欲減退 22.1% (0%)
- 便秘 20.5% (0%)
- 発熱 13.3% (0%)
Lancet Oncol. 2017 Sep;18(9):1274-1284³⁾より引用
エキスパートによるワンポイント
SOLO-1試験の有効性
BRCA変異陽性卵巣癌患者に対して、 初回化学療法後の維持療法として、 Olaparib内服は、 プラセボ群と比較した第Ⅲ相SOLO-1試験でプライマリーエンドポイントの無増悪生存期間 (PFS) を有意に延長させました⁴⁾。
しかし、 その後報告された全生存期間 (OS) は、 Olaparib群に、 良好な結果 (HR=0.55、 95%CI 0.40-0.76, p=0.0004) であったものの⁵⁾、 αエラーを防ぐため多重性の調整をしたp<0.0001を満たさず、 OSに関しては、 有意差はなしと判定されています。
この理由として、 SOLO2試験の探索的解析結果⁶⁾からは、 「Olaparib使用後プラチナ耐性になってしまい予後が不良になる」 ことが示唆されています⁶⁾。
注意すべき有害事象とその対応
注意すべき有害事象として、 貧血は38.8% (うちGrade3 21.5%) に発生しました。 MDS/AMLの発生率は1.5% (プラセボ群0.8%) でした⁵⁾。 特にMDS/AMLに関しては重大な合併症であり、 発症した場合は血液内科医へのコンサルテーションが必要となります。
Re-challaengeについて
初回化学療法後にPARP阻害剤を投与された患者に対して、 再発後化学療法後の維持療法としてオラパリブを再使用すること (Re-challenge) については、 有効性を示すエビデンスが不足しているため、 現時点では再使用は控えるべきと考えられます⁶⁾。
監修 : 日本医科大学 武蔵小杉病院 腫瘍内科教授 勝俣 範之先生
出典
- アストラゼネカ株式会社. リムパーザ®電子添文 (2026年3月改訂第7版).
- アストラゼネカ株式会社. リムパーザ®適正使用ガイド (2024年12月作成).
- Olaparib tablets as maintenance therapy in patients with platinum-sensitive, relapsed ovarian cancer and a BRCA1/2 mutation (SOLO2/ENGOT-Ov21): a double-blind, randomised, placebo-controlled, phase 3 trial. Lancet Oncol. 2017 Sep;18(9):1274-1284. PMID: 2875448
- Maintenance Olaparib in Patients with Newly Diagnosed Advanced Ovarian Cancer. N Engl J Med. 2018 Dec 27;379(26):2495-2505. PMID: 30345884
- Overall Survival With Maintenance Olaparib at a 7-Year Follow-Up in Patients With Newly Diagnosed Advanced Ovarian Cancer and a BRCA Mutation: The SOLO1/GOG 3004 Trial. J Clin Oncol. 2022 Sep 9;JCO2201549.PMID: 36082969
- Efficacy of subsequent chemotherapy for patients with BRCA1/2-mutated recurrent epithelial ovarian cancer progressing on olaparib versus placebo maintenance: post-hoc analyses of the SOLO2/ENGOT Ov-21 trial. Ann Oncol. 2022 Oct;33(10):1021-1028. PMID: 35772665
最終更新日 : 2026年3月18日
監修医師 : 日本医科大学 武蔵小杉病院 腫瘍内科教授 勝俣 範之先生
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
がん薬物療法における治療計画をまとめたものです。
主要論文や適正使用ガイドをもとにした用量調整プロトコール、 有害事象対応をご紹介します。
なお、 本ツールは医師向けの教育用資料であり、 実臨床での使用は想定しておりません。 最新の添付文書やガイドラインを必ずご確認下さい。
また、 一般の方への情報提供ではないことを予めご了承ください。