本コンテンツは特定の治療法を推奨するものではありません。 個々の患者の病態や、 実際の薬剤情報やガイドラインを確認の上、 利用者の判断と責任でご利用ください。
薬剤情報
ROS1/TRK選択的阻害薬 エヌトレクチニブ
*中外製薬株式会社の外部サイトへ遷移します
投与スケジュール
電子添文¹⁾の用法および用量

成人には1日1回600mgを経口投与。 小児には1日1回300mg/m² (最大600mgまで)
[小児患者の用量 (300mg/u1日1回経口投与)]
1) 体表面積0.43~0.50m² : 1日1回100mg
2) 体表面積0.51~0.80m² : 1日1回200mg
3) 体表面積0.81~1.10m² : 1日1回300mg
4) 体表面積1.11~1.50m² : 1日1回400mg
5) 体表面積≧1.51m² : 1日1回600mg
ロズリートレク®電子添文 (2023年11月改訂 第10版)¹⁾より作図
特徴と注意点
執筆 : 静岡県立静岡がんセンター 消化器内科 川上 武志先生
NTRK融合遺伝子陽性大腸癌について
全大腸癌の0.2%であり、 NTRK阻害薬の対象となる症例のスクリーニングが重要である。
大腸癌において、 NTRK融合遺伝子陽性例は、 MSS (0–23.1%) よりもMSI-H (11–76.9%) に多いことが報告されており³⁾⁴⁾、 特にMSI-H例ではがん遺伝子プロファイル検査を検討する。
ガイドラインの記載
大腸癌治療ガイドラインで、EntrectinibとLarotrectinibは、 NTRK融合遺伝子陽性大腸癌既治療例の標準治療である⁵⁾。
コンパニオン診断薬
ENTRはFoundationOneCDx®およびFounadtionOneLiquidCDx®、 LAROは、 FoundationOneCDx®のみとなっている。
EntrectinibとLarotrectinibの比較
稀少な対象であり、 両薬剤の有効性の差について検討した報告はない。 Larotrectinibはカプセルと液剤の剤型がある。
各プロトコル
投与開始基準
適正使用ガイド²⁾の基準

ロズリートレク®適正使用ガイド (2023年6月改訂)²⁾より作図
減量・休薬・中止基準
電子添文¹⁾の基準
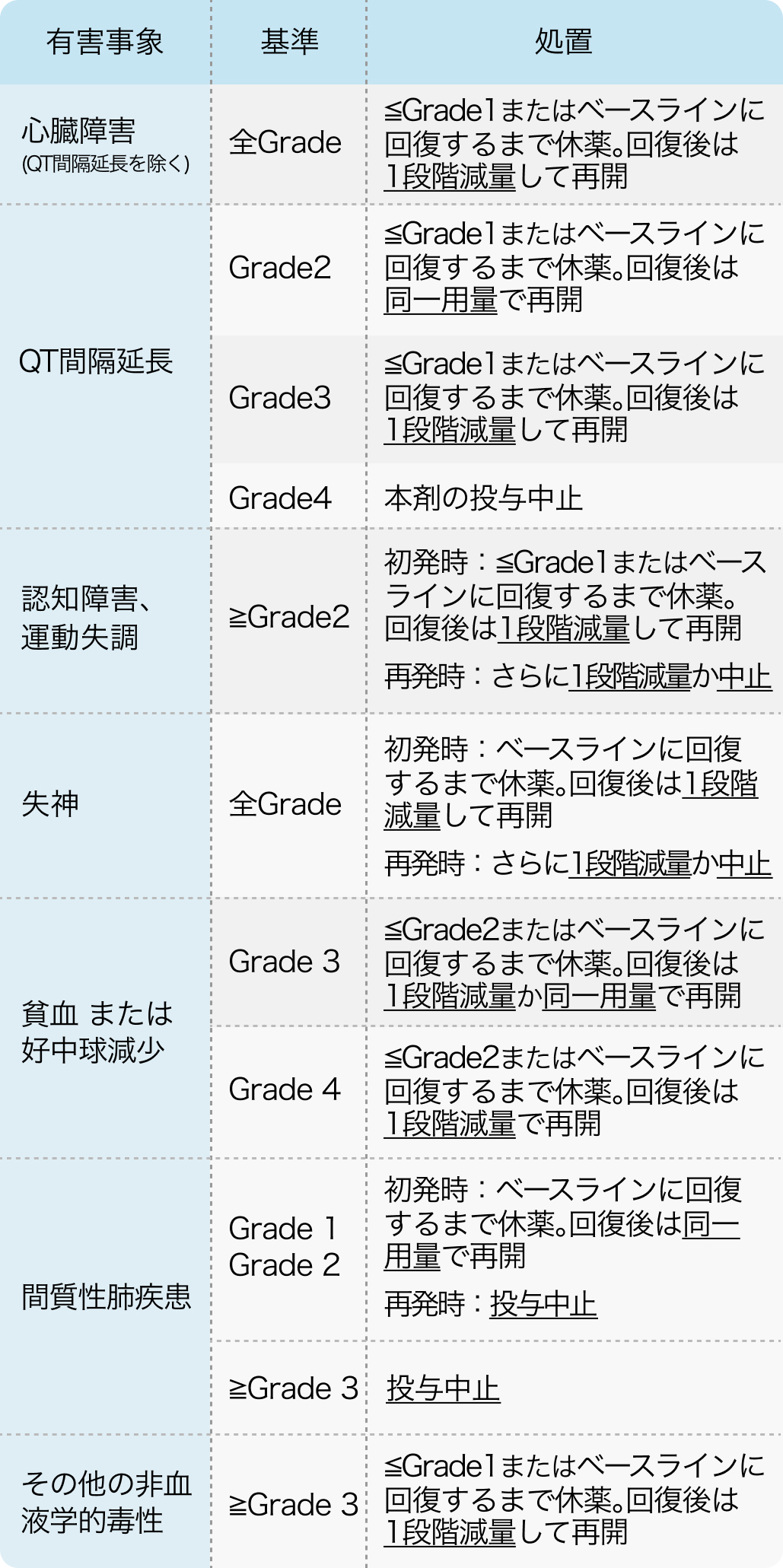
ロズリートレク®電子添文 (2023年11月改訂 第10版)¹⁾より作図
初回基準量と減量レベル

ロズリートレク®電子添文 (2023年11月改訂 第10版)¹⁾より作図
KeyData|臨床試験結果
第Ⅰ-Ⅱ相試験³⁾
Lancet Oncol. 2020 Feb;21(2):271-282.
発がん性NTRK1、 NTRK2、 およびNTRK3遺伝子融合を有する転移性または局所進行固形腫瘍患者の統合的な有効性と安全性の分析。 第Ⅰ相または第Ⅱ相臨床試験 (ALKA-372-001、 STARTRK-1、 および STARTRK-2) の極めて重要なデータセットで構成された。 主要評価項目は客観的奏効割合 (ORR) および奏効期間 (DoR) とされた。
Lancet Oncol. 2020 Feb;21(2):271-282.
NTRK陽性の安全性評価対象集団
主な有害事象 (カッコ内はGrade3~4)
- 便秘 27.9% (0%)
- 倦怠感 35.3% (7.4%)
- 下痢 27.9% (1.5%)
- 悪心 14.7% (0%)
- 嘔吐 13.2% (0%)
- 体重増加 22.1% (10.3%)
- AST増加 11.8% (1.5%)
- ALT増加 10.3% (1.5%)
- 貧血 19.1% (11.8%)
- 好中球数減少 5.9% (0%)
- 好中球減少症 7.4% (2.9%)
- 血小板数減少 2.9% (0%)
- 発熱 1.5% (0%)
- リンパ球数の減少 1.5% (0%)
全体的な安全性評価対象集団
主な有害事象 (カッコ内はGrade3~4)
- 便秘 23.7% (0.3%)
- 倦怠感 27.9% (2.8%)
- 下痢 22.8% (1.4%)
- 悪心 20.8% (0%)
- 嘔吐 13.5% (0%)
- 体重増加 19.4% (5.1%)
- AST増加 11.0% (1.1%)
- ALT増加 9.6% (1.1%)
- 貧血 12.1% (4.5%)
- 好中球数減少 5.9% (2.3%)
- 好中球減少症 5.1% (2.5%)
- 血小板数減少 1.4% (0.3%)
- 発熱 2.3% (0.3%)
- リンパ球数減少 1.4% (0.3%)
注意すべき有害事象 (カッコ内はGrade3~4)
- 高血圧 0.3% (0.3%)
Lancet Oncol. 2020 Feb;21(2):271-282³⁾より引用
出典
- 中外製薬株式会社 「ロズリートレク®カプセル 添付文書 2025年8月改訂 第12版
- 中外製薬株式会社 「ロズリートレク®適正使用ガイド (2023年6月改訂)」
- Entrectinib in patients with advanced or metastatic NTRK fusion-positive solid tumours: integrated analysis of three phase 1-2 trials. Lancet Oncol. 2020 Feb;21(2):271-282. PMID: 31838007
- ALK, ROS1, and NTRK Rearrangements in Metastatic Colorectal Cancer. J Natl Cancer Inst. 2017 Dec 1;109(12). PMID: 29370427
- Clinical Sequencing Defines the Genomic Landscape of Metastatic Colorectal Cancer. Cancer Cell. 2018 Jan 8;33(1):125-136.e3. PMID: 29316426
- 金原出版株式会社. 大腸癌治療ガイドライン医師用2024年版. 大腸癌研究会編
最終更新日 : 2025年9月11日
執筆医 : 静岡県立静岡がんセンター 消化器内科 川上 武志先生
監修医師 : HOKUTO編集部 医師
Entrectinib
本コンテンツは特定の治療法を推奨するものではありません。 個々の患者の病態や、 実際の薬剤情報やガイドラインを確認の上、 利用者の判断と責任でご利用ください。
薬剤情報
ROS1/TRK選択的阻害薬 エヌトレクチニブ
*中外製薬株式会社の外部サイトへ遷移します
投与スケジュール
電子添文¹⁾の用法および用量

成人には1日1回600mgを経口投与。 小児には1日1回300mg/m² (最大600mgまで)
[小児患者の用量 (300mg/u1日1回経口投与)]
1) 体表面積0.43~0.50m² : 1日1回100mg
2) 体表面積0.51~0.80m² : 1日1回200mg
3) 体表面積0.81~1.10m² : 1日1回300mg
4) 体表面積1.11~1.50m² : 1日1回400mg
5) 体表面積≧1.51m² : 1日1回600mg
ロズリートレク®電子添文 (2023年11月改訂 第10版)¹⁾より作図
特徴と注意点
執筆 : 静岡県立静岡がんセンター 消化器内科 川上 武志先生
NTRK融合遺伝子陽性大腸癌について
全大腸癌の0.2%であり、 NTRK阻害薬の対象となる症例のスクリーニングが重要である。
大腸癌において、 NTRK融合遺伝子陽性例は、 MSS (0–23.1%) よりもMSI-H (11–76.9%) に多いことが報告されており³⁾⁴⁾、 特にMSI-H例ではがん遺伝子プロファイル検査を検討する。
ガイドラインの記載
大腸癌治療ガイドラインで、EntrectinibとLarotrectinibは、 NTRK融合遺伝子陽性大腸癌既治療例の標準治療である⁵⁾。
コンパニオン診断薬
ENTRはFoundationOneCDx®およびFounadtionOneLiquidCDx®、 LAROは、 FoundationOneCDx®のみとなっている。
EntrectinibとLarotrectinibの比較
稀少な対象であり、 両薬剤の有効性の差について検討した報告はない。 Larotrectinibはカプセルと液剤の剤型がある。
各プロトコル
投与開始基準
適正使用ガイド²⁾の基準

ロズリートレク®適正使用ガイド (2023年6月改訂)²⁾より作図
減量・休薬・中止基準
電子添文¹⁾の基準

ロズリートレク®電子添文 (2023年11月改訂 第10版)¹⁾より作図
初回基準量と減量レベル

ロズリートレク®電子添文 (2023年11月改訂 第10版)¹⁾より作図
KeyData|臨床試験結果
第Ⅰ-Ⅱ相試験³⁾
Lancet Oncol. 2020 Feb;21(2):271-282.
発がん性NTRK1、 NTRK2、 およびNTRK3遺伝子融合を有する転移性または局所進行固形腫瘍患者の統合的な有効性と安全性の分析。 第Ⅰ相または第Ⅱ相臨床試験 (ALKA-372-001、 STARTRK-1、 および STARTRK-2) の極めて重要なデータセットで構成された。 主要評価項目は客観的奏効割合 (ORR) および奏効期間 (DoR) とされた。
Lancet Oncol. 2020 Feb;21(2):271-282.
NTRK陽性の安全性評価対象集団
主な有害事象 (カッコ内はGrade3~4)
- 便秘 27.9% (0%)
- 倦怠感 35.3% (7.4%)
- 下痢 27.9% (1.5%)
- 悪心 14.7% (0%)
- 嘔吐 13.2% (0%)
- 体重増加 22.1% (10.3%)
- AST増加 11.8% (1.5%)
- ALT増加 10.3% (1.5%)
- 貧血 19.1% (11.8%)
- 好中球数減少 5.9% (0%)
- 好中球減少症 7.4% (2.9%)
- 血小板数減少 2.9% (0%)
- 発熱 1.5% (0%)
- リンパ球数の減少 1.5% (0%)
全体的な安全性評価対象集団
主な有害事象 (カッコ内はGrade3~4)
- 便秘 23.7% (0.3%)
- 倦怠感 27.9% (2.8%)
- 下痢 22.8% (1.4%)
- 悪心 20.8% (0%)
- 嘔吐 13.5% (0%)
- 体重増加 19.4% (5.1%)
- AST増加 11.0% (1.1%)
- ALT増加 9.6% (1.1%)
- 貧血 12.1% (4.5%)
- 好中球数減少 5.9% (2.3%)
- 好中球減少症 5.1% (2.5%)
- 血小板数減少 1.4% (0.3%)
- 発熱 2.3% (0.3%)
- リンパ球数減少 1.4% (0.3%)
注意すべき有害事象 (カッコ内はGrade3~4)
- 高血圧 0.3% (0.3%)
Lancet Oncol. 2020 Feb;21(2):271-282³⁾より引用
出典
- 中外製薬株式会社 「ロズリートレク®カプセル 添付文書 2025年8月改訂 第12版
- 中外製薬株式会社 「ロズリートレク®適正使用ガイド (2023年6月改訂)」
- Entrectinib in patients with advanced or metastatic NTRK fusion-positive solid tumours: integrated analysis of three phase 1-2 trials. Lancet Oncol. 2020 Feb;21(2):271-282. PMID: 31838007
- ALK, ROS1, and NTRK Rearrangements in Metastatic Colorectal Cancer. J Natl Cancer Inst. 2017 Dec 1;109(12). PMID: 29370427
- Clinical Sequencing Defines the Genomic Landscape of Metastatic Colorectal Cancer. Cancer Cell. 2018 Jan 8;33(1):125-136.e3. PMID: 29316426
- 金原出版株式会社. 大腸癌治療ガイドライン医師用2024年版. 大腸癌研究会編
最終更新日 : 2025年9月11日
執筆医 : 静岡県立静岡がんセンター 消化器内科 川上 武志先生
監修医師 : HOKUTO編集部 医師
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
がん薬物療法における治療計画をまとめたものです。
主要論文や適正使用ガイドをもとにした用量調整プロトコール、 有害事象対応をご紹介します。
なお、 本ツールは医師向けの教育用資料であり、 実臨床での使用は想定しておりません。 最新の添付文書やガイドラインを必ずご確認下さい。
また、 一般の方への情報提供ではないことを予めご了承ください。