本コンテンツは特定の治療法を推奨するものではありません。 個々の患者の病態や、 実際の薬剤情報やガイドラインを確認の上、 利用者の判断と責任でご利用ください。
薬剤情報
*ファイザー株式会社の外部サイトへ遷移します
用法用量
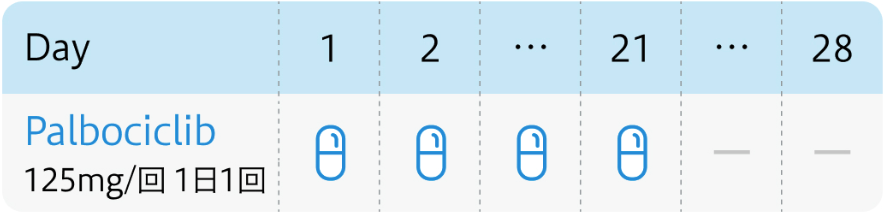
内分泌療法剤との併用において、 パルボシクリブ125mg/日を3週間連続経口投与し、1週間休薬
パルボシクリブ電子添文¹⁾ より引用
タモキシフェンとの併用の場合
タモキシフェン20mgを1日1回経口投与併用
PATHWAY試験³⁾の設定を踏まえたもの
レトロゾールとの併用の場合
レトロゾール2.5mgを1日1回経口投与併用
PALOMA-2試験⁴⁾の設定を踏まえたもの
フルベストラントとの併用の場合
フルベストラント500mgを1日目、 15日目及び29日目並びにその後は4週毎に筋注投与併用
PALOMA-3試験⁶⁾の設定を踏まえたもの
投与開始基準
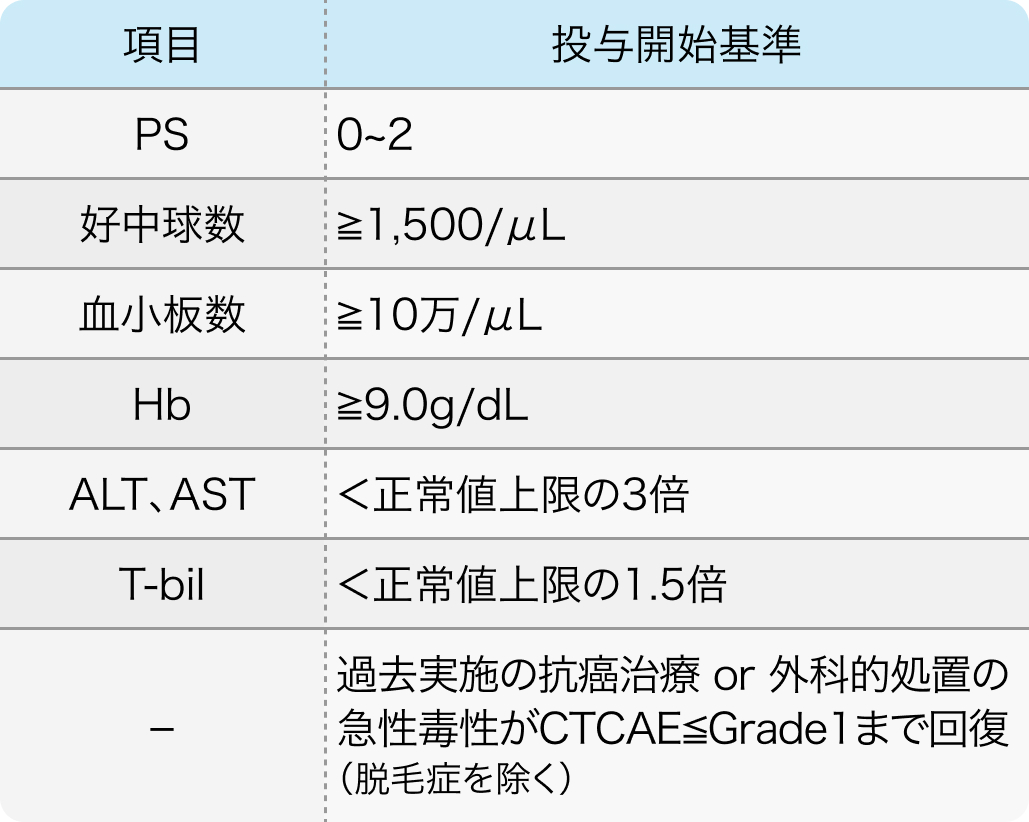
減量・休薬・中止基準
初回基準量と減量レベル
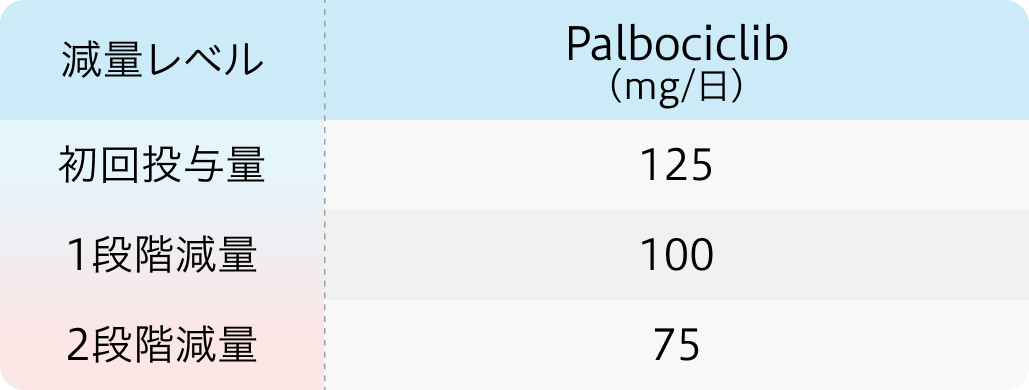
主な有害事象
PALOMA-2試験⁴⁾
アジア人の有害事象データを一部引用 (カッコ内はGrade3~4)
主な有害事象
- 好中球減少 95.4% (89.2%)
- 白血球減少 43.1% (32.2%)
- 貧血 24.6% (6.2%)
- 血小板減少 27.7% (4.6%)
- 倦怠感 24.6% (0%)
- 悪心 27.7% (0%)
- 口内炎 49.2% (0%)
- 下痢 6.2% (0%)
- 便秘 16.9% (0%)
- 嘔吐 9.2% (0%)
注意すべき有害事象
- 脱毛症 35.4% (0%)
PALOMA-2試験⁵⁾
有害事象データを一部引用 (カッコ内はGrade3~4)
主な有害事象
- 好中球減少 79.5% (66.4%)
- 白血球減少 39.0% (24.8%)
- 貧血 24.1% (5.4%)
- 血小板減少 15.5% (1.6%)
- 倦怠感 37.4% (1.8%)
- 悪心 35.1% (0.2%)
- 口内炎 15.3% (0.2%)
- 下痢 26.1% (1.4%)
- 便秘 19.4% (0.5%)
- 嘔吐 15.5% (0.5%)
注意すべき有害事象
- 脱毛症 32.9% (0%)
PALOMA-3試験⁶⁾
全体集団の有害事象データを一部引用 (カッコ内はGrade3~4)
主な有害事象
- 好中球減少 78.8% (62.0%)
- 白血球減少 45.5% (25.2%)
- 貧血 26.1% (2.6%)
- 血小板減少 19.4% (2.3%)
- 倦怠感 38.0% (2.0%)
- 悪心 29.0% (0%)
- 口内炎 11.6% (0.6%)
- 下痢 19.1% (0%)
- 便秘 16.8% (0%)
- 嘔吐 14.5% (0.3%)
注意すべき有害事象
- 脱毛症 14.8% (0%)
特徴と注意点
- ホルモン受容体陽性かつHER2陰性の手術不能又は再発乳がんに対して使用される。
- パルボシクリブは1日1回を3週服用後1週休薬を1サイクルとして繰り返す。 カプセル製剤は食後に服用する必要があるが、 錠剤製剤は食事の影響を受けない。
- 併用するホルモン療法はレトロゾールまたはフルベストラントが推奨されており、 他の抗エストロゲン薬 (タモキシフェン、 トレミフェン) やアロマターゼ阻害剤 (エキセメスタン、 アナストロゾール) 等と併用した場合のデータは乏しい。
- 血液毒性の頻度が高く、 Grade 3/4の好中球減少症が50%以上の頻度で発現する。 好中球減少症は投与初期 (初回発現までの中央値 : 15日) に好発するため、 1、 2サイクル目は投与開始2週目後に血液検査を行うことが望ましい。
- 間質性肺炎に注意が必要であり、 息切れ、 咳症状などの症状を確認し、 定期的な画像評価を行う。
- 脱毛は約10~30%の頻度で出現し、 臨床試験ではGrade1 (遠くからではわからない程度) が11~22%、 Grade2 (50%以上の脱毛) が0~3%で認められた。
関連する臨床試験|PALOMA-2試験⁴⁾⁵⁾
進行病変に対する治療歴のないER陽性/HER2陰性進行乳癌の閉経後女性患者において、 パルボシクリブ+レトロゾールの効果を、 プラセボ+レトロゾールを対照に検証した第Ⅲ相無作為化比較試験PALOMA-2の結果より、 無増悪生存期間 (PFS) に対する有効性が示された。
PFS中央値
- パルボシクリブ群 : 24.8ヵ月
(95%CI 22.1ヵ月-推定不能)
- プラセボ群 : 14.5ヵ月
(95%CI 12.9-17.1ヵ月)
HR 0.58 (95%CI 0.46-0.72)、 p<0.001
PFSのサブグループ解析
内臓疾患の有無やホルモン療法歴の有無に関わらず、 パルボシクリブ群で有効性が認められた。
ORR
- パルボシクリブ群 : 42.1%
(95%CI 37.5-46.9%)
- プラセボ群 : 34.7%
(95%CI 28.4-41.3%)
オッズ比 1.40 (95%CI 0.98-2.01)、 p=0.06
OS
データ不十分のため未報告
関連する臨床試験|PALOMA-3試験⁶⁾
ホルモン受容体陽性、 HER2陰性の進行乳癌患者において、 パルボシクリブ+フルベストラントの効果を、 プラセボ+フルベストラントを対照に検証した第Ⅲ相二重盲検無作為化比較試験PALOMA-3の結果より、 無増悪生存期間 (PFS) に対する有効性が示された。
PFS中央値
全患者
- パルボシクリブ群 : 9.5ヵ月
(95%CI 9.2-11.0ヵ月)
- プラセボ群 : 4.6ヵ月
(95%CI 3.5-5.6ヵ月)
HR 0.46 (95%CI 0.36-0.59)、 p<0.0001
過去の内分泌療法に対する感受性あり (410例)
- パルボシクリブ群 : 12.0ヵ月
(95%CI 11.1-13.9ヵ月)
- プラセボ群 : 4.2ヵ月
(95%CI 3.5-5.6ヵ月)
HR 0.46 (95%CI 0.36-0.59)
過去の内分泌療法に対する感受性なし (111例)
- パルボシクリブ群 : 7.4ヵ月
(95%CI 5.5-11.1ヵ月)
- プラセボ群 : 5.1ヵ月
(95%CI 1.9-7.4ヵ月)
HR 0.69 (95%CI 0.43-1.09)
OS中央値
- パルボシクリブ群 : 34.9ヵ月
(95%CI 28.8-40.0ヵ月)
- プラセボ群 : 28.0ヵ月
(95%CI 23.6-34.6ヵ月)
HR 0.81 (95%CI 0.64-1.03)、p=0.09
OS率 : 全患者 (3年時)
- パルボシクリブ群 : 50%
(95%CI 44-55%)
- プラセボ群 : 41%
(95%CI 33-48%)
OS (サブグループ解析)
過去の内分泌療法に対する感受性あり (410例)
- パルボシクリブ群 : 39.7ヵ月
(95%CI 34.8-45.7ヵ月)
- プラセボ群 : 29.7ヵ月
(95%CI 23.8-37.9ヵ月)
HR 0.72 (95%CI 0.55-0.94)
過去の内分泌療法に対する感受性なし (111例)
- パルボシクリブ群 : 20.2ヵ月
(95%CI 17.2-26.4ヵ月)
- プラセボ群 : 26.2ヵ月
(95%CI 17.5-31.8ヵ月)
HR 1.14 (95%CI 0.71-1.84)、p=0.12
内臓転移あり (311例)
- パルボシクリブ群 : 27.6ヵ月
(95%CI 24.4-31.2ヵ月)
- プラセボ群 : 24.7ヵ月
(95%CI 20.8-31.8ヵ月)
HR 0.85 (95%CI 0.64-1.13)
内臓転移なし (210例)
- パルボシクリブ群 : 46.9ヵ月
(95%CI 39.3ヵ月-NE)
- プラセボ群 : 35.4ヵ月
(95%CI 24.6ヵ月-NE)
HR 0.69 (95%CI 0.46-1.04)、p=0.44
閉経後患者 (413例)
- パルボシクリブ群 : 34.8ヵ月
(95%CI 28.8-40.1ヵ月)
- プラセボ群 : 27.1ヵ月
(95%CI 22.8-32.1ヵ月)
HR 0.73 (95%CI 0.57-0.95)
閉経前もしくは閉経前後の患者 (108例)
- パルボシクリブ群 : 38.0ヵ月
(95%CI 24.4ヵ月-NE)
- プラセボ群 : 38.0ヵ月
(95%CI 22.2ヵ月-NE)
HR 1.07 (95%CI 0.61-1.86)、p=0.25
奏効率
全患者
- パルボシクリブ群 : 19%
(95%CI 15.0-23.6%)
- プラセボ群 : 9%
(95%CI 4.9-13.8%)
オッズ比 2.47 (95%CI 1.36-4.91)、p=0.0019
ベースライン時に測定可能な病変を有する患者
- パルボシクリブ群 : 24.6%
(95%CI 19.6-30.2%)
- プラセボ群 : 10.9%
(95%CI 6.2-17.3%)
オッズ比 2.69 (95%CI 1.43-5.26)、p=0.0012
奏効までの期間 (中央値)
- パルボシクリブ群 : 112日
- プラセボ群 : 57日
患者報告アウトカム
QLQ-C30スコアのベースラインからの変化は、 パルボシクリブ群 (-0.9ポイント) よりプラセボ群 (-4.0ポイント) で有意に悪化した (p=0.03)。
出展
- ファイザー株式会社. イブランス®電子添文 (2024年1月改訂 第3版) [最終閲覧 : 2024/9/3]
- ファイザー株式会社. イブランス®適正使用ガイド (2024年3月改訂) [最終閲覧 : 2024/9/3]
- A phase 3 study (PATHWAY) of palbociclib plus tamoxifen in patients with HR-positive/HER2-negative advanced breast cancer. NPJ Breast Cancer. 2024 Aug 22;10(1):76. NPJ Breast Cancer . 2024 Aug 22;10(1):76. PMID: 39174547
- Palbociclib Plus Letrozole as First-Line Therapy in Postmenopausal Asian Women With Metastatic Breast Cancer: Results From the Phase III, Randomized PALOMA-2 Study. J Glob Oncol. 2019 May;5:1-19. PMID: 31125276
- Palbociclib and Letrozole in Advanced Breast Cancer. N Engl J Med. 2016 Nov 17;375(20):1925-1936. PMID: 27959613
- PALOMA-3: Phase III Trial of Fulvestrant With or Without Palbociclib in Premenopausal and Postmenopausal Women With Hormone Receptor-Positive, Human Epidermal Growth Factor Receptor 2-Negative Metastatic Breast Cancer That Progressed on Prior Endocrine Therapy-Safety and Efficacy in Asian Patients. J Glob Oncol. 2017 Apr 11;3(4):289-303. PMID: 28831437
- Palbociclib in Hormone-Receptor-Positive Advanced Breast Cancer. N Engl J Med. 2015 Jul 16;373(3):209-19. PMID: 26030518
最終更新日 : 2024年9月3日
監修医師 : HOKUTO編集部監修医師
執筆 : NTT東日本関東病院 薬剤部 兼平 暖先生
Palbociclib + ホルモン療法
本コンテンツは特定の治療法を推奨するものではありません。 個々の患者の病態や、 実際の薬剤情報やガイドラインを確認の上、 利用者の判断と責任でご利用ください。
薬剤情報
*ファイザー株式会社の外部サイトへ遷移します
用法用量

内分泌療法剤との併用において、 パルボシクリブ125mg/日を3週間連続経口投与し、1週間休薬
パルボシクリブ電子添文¹⁾ より引用
タモキシフェンとの併用の場合
タモキシフェン20mgを1日1回経口投与併用
PATHWAY試験³⁾の設定を踏まえたもの
レトロゾールとの併用の場合
レトロゾール2.5mgを1日1回経口投与併用
PALOMA-2試験⁴⁾の設定を踏まえたもの
フルベストラントとの併用の場合
フルベストラント500mgを1日目、 15日目及び29日目並びにその後は4週毎に筋注投与併用
PALOMA-3試験⁶⁾の設定を踏まえたもの
投与開始基準

減量・休薬・中止基準
初回基準量と減量レベル

主な有害事象
PALOMA-2試験⁴⁾
アジア人の有害事象データを一部引用 (カッコ内はGrade3~4)
主な有害事象
- 好中球減少 95.4% (89.2%)
- 白血球減少 43.1% (32.2%)
- 貧血 24.6% (6.2%)
- 血小板減少 27.7% (4.6%)
- 倦怠感 24.6% (0%)
- 悪心 27.7% (0%)
- 口内炎 49.2% (0%)
- 下痢 6.2% (0%)
- 便秘 16.9% (0%)
- 嘔吐 9.2% (0%)
注意すべき有害事象
- 脱毛症 35.4% (0%)
PALOMA-2試験⁵⁾
有害事象データを一部引用 (カッコ内はGrade3~4)
主な有害事象
- 好中球減少 79.5% (66.4%)
- 白血球減少 39.0% (24.8%)
- 貧血 24.1% (5.4%)
- 血小板減少 15.5% (1.6%)
- 倦怠感 37.4% (1.8%)
- 悪心 35.1% (0.2%)
- 口内炎 15.3% (0.2%)
- 下痢 26.1% (1.4%)
- 便秘 19.4% (0.5%)
- 嘔吐 15.5% (0.5%)
注意すべき有害事象
- 脱毛症 32.9% (0%)
PALOMA-3試験⁶⁾
全体集団の有害事象データを一部引用 (カッコ内はGrade3~4)
主な有害事象
- 好中球減少 78.8% (62.0%)
- 白血球減少 45.5% (25.2%)
- 貧血 26.1% (2.6%)
- 血小板減少 19.4% (2.3%)
- 倦怠感 38.0% (2.0%)
- 悪心 29.0% (0%)
- 口内炎 11.6% (0.6%)
- 下痢 19.1% (0%)
- 便秘 16.8% (0%)
- 嘔吐 14.5% (0.3%)
注意すべき有害事象
- 脱毛症 14.8% (0%)
特徴と注意点
- ホルモン受容体陽性かつHER2陰性の手術不能又は再発乳がんに対して使用される。
- パルボシクリブは1日1回を3週服用後1週休薬を1サイクルとして繰り返す。 カプセル製剤は食後に服用する必要があるが、 錠剤製剤は食事の影響を受けない。
- 併用するホルモン療法はレトロゾールまたはフルベストラントが推奨されており、 他の抗エストロゲン薬 (タモキシフェン、 トレミフェン) やアロマターゼ阻害剤 (エキセメスタン、 アナストロゾール) 等と併用した場合のデータは乏しい。
- 血液毒性の頻度が高く、 Grade 3/4の好中球減少症が50%以上の頻度で発現する。 好中球減少症は投与初期 (初回発現までの中央値 : 15日) に好発するため、 1、 2サイクル目は投与開始2週目後に血液検査を行うことが望ましい。
- 間質性肺炎に注意が必要であり、 息切れ、 咳症状などの症状を確認し、 定期的な画像評価を行う。
- 脱毛は約10~30%の頻度で出現し、 臨床試験ではGrade1 (遠くからではわからない程度) が11~22%、 Grade2 (50%以上の脱毛) が0~3%で認められた。
関連する臨床試験|PALOMA-2試験⁴⁾⁵⁾
進行病変に対する治療歴のないER陽性/HER2陰性進行乳癌の閉経後女性患者において、 パルボシクリブ+レトロゾールの効果を、 プラセボ+レトロゾールを対照に検証した第Ⅲ相無作為化比較試験PALOMA-2の結果より、 無増悪生存期間 (PFS) に対する有効性が示された。
PFS中央値
- パルボシクリブ群 : 24.8ヵ月
(95%CI 22.1ヵ月-推定不能)
- プラセボ群 : 14.5ヵ月
(95%CI 12.9-17.1ヵ月)
HR 0.58 (95%CI 0.46-0.72)、 p<0.001
PFSのサブグループ解析
内臓疾患の有無やホルモン療法歴の有無に関わらず、 パルボシクリブ群で有効性が認められた。
ORR
- パルボシクリブ群 : 42.1%
(95%CI 37.5-46.9%)
- プラセボ群 : 34.7%
(95%CI 28.4-41.3%)
オッズ比 1.40 (95%CI 0.98-2.01)、 p=0.06
OS
データ不十分のため未報告
関連する臨床試験|PALOMA-3試験⁶⁾
ホルモン受容体陽性、 HER2陰性の進行乳癌患者において、 パルボシクリブ+フルベストラントの効果を、 プラセボ+フルベストラントを対照に検証した第Ⅲ相二重盲検無作為化比較試験PALOMA-3の結果より、 無増悪生存期間 (PFS) に対する有効性が示された。
PFS中央値
全患者
- パルボシクリブ群 : 9.5ヵ月
(95%CI 9.2-11.0ヵ月)
- プラセボ群 : 4.6ヵ月
(95%CI 3.5-5.6ヵ月)
HR 0.46 (95%CI 0.36-0.59)、 p<0.0001
過去の内分泌療法に対する感受性あり (410例)
- パルボシクリブ群 : 12.0ヵ月
(95%CI 11.1-13.9ヵ月)
- プラセボ群 : 4.2ヵ月
(95%CI 3.5-5.6ヵ月)
HR 0.46 (95%CI 0.36-0.59)
過去の内分泌療法に対する感受性なし (111例)
- パルボシクリブ群 : 7.4ヵ月
(95%CI 5.5-11.1ヵ月)
- プラセボ群 : 5.1ヵ月
(95%CI 1.9-7.4ヵ月)
HR 0.69 (95%CI 0.43-1.09)
OS中央値
- パルボシクリブ群 : 34.9ヵ月
(95%CI 28.8-40.0ヵ月)
- プラセボ群 : 28.0ヵ月
(95%CI 23.6-34.6ヵ月)
HR 0.81 (95%CI 0.64-1.03)、p=0.09
OS率 : 全患者 (3年時)
- パルボシクリブ群 : 50%
(95%CI 44-55%)
- プラセボ群 : 41%
(95%CI 33-48%)
OS (サブグループ解析)
過去の内分泌療法に対する感受性あり (410例)
- パルボシクリブ群 : 39.7ヵ月
(95%CI 34.8-45.7ヵ月)
- プラセボ群 : 29.7ヵ月
(95%CI 23.8-37.9ヵ月)
HR 0.72 (95%CI 0.55-0.94)
過去の内分泌療法に対する感受性なし (111例)
- パルボシクリブ群 : 20.2ヵ月
(95%CI 17.2-26.4ヵ月)
- プラセボ群 : 26.2ヵ月
(95%CI 17.5-31.8ヵ月)
HR 1.14 (95%CI 0.71-1.84)、p=0.12
内臓転移あり (311例)
- パルボシクリブ群 : 27.6ヵ月
(95%CI 24.4-31.2ヵ月)
- プラセボ群 : 24.7ヵ月
(95%CI 20.8-31.8ヵ月)
HR 0.85 (95%CI 0.64-1.13)
内臓転移なし (210例)
- パルボシクリブ群 : 46.9ヵ月
(95%CI 39.3ヵ月-NE)
- プラセボ群 : 35.4ヵ月
(95%CI 24.6ヵ月-NE)
HR 0.69 (95%CI 0.46-1.04)、p=0.44
閉経後患者 (413例)
- パルボシクリブ群 : 34.8ヵ月
(95%CI 28.8-40.1ヵ月)
- プラセボ群 : 27.1ヵ月
(95%CI 22.8-32.1ヵ月)
HR 0.73 (95%CI 0.57-0.95)
閉経前もしくは閉経前後の患者 (108例)
- パルボシクリブ群 : 38.0ヵ月
(95%CI 24.4ヵ月-NE)
- プラセボ群 : 38.0ヵ月
(95%CI 22.2ヵ月-NE)
HR 1.07 (95%CI 0.61-1.86)、p=0.25
奏効率
全患者
- パルボシクリブ群 : 19%
(95%CI 15.0-23.6%)
- プラセボ群 : 9%
(95%CI 4.9-13.8%)
オッズ比 2.47 (95%CI 1.36-4.91)、p=0.0019
ベースライン時に測定可能な病変を有する患者
- パルボシクリブ群 : 24.6%
(95%CI 19.6-30.2%)
- プラセボ群 : 10.9%
(95%CI 6.2-17.3%)
オッズ比 2.69 (95%CI 1.43-5.26)、p=0.0012
奏効までの期間 (中央値)
- パルボシクリブ群 : 112日
- プラセボ群 : 57日
患者報告アウトカム
QLQ-C30スコアのベースラインからの変化は、 パルボシクリブ群 (-0.9ポイント) よりプラセボ群 (-4.0ポイント) で有意に悪化した (p=0.03)。
出展
- ファイザー株式会社. イブランス®電子添文 (2024年1月改訂 第3版) [最終閲覧 : 2024/9/3]
- ファイザー株式会社. イブランス®適正使用ガイド (2024年3月改訂) [最終閲覧 : 2024/9/3]
- A phase 3 study (PATHWAY) of palbociclib plus tamoxifen in patients with HR-positive/HER2-negative advanced breast cancer. NPJ Breast Cancer. 2024 Aug 22;10(1):76. NPJ Breast Cancer . 2024 Aug 22;10(1):76. PMID: 39174547
- Palbociclib Plus Letrozole as First-Line Therapy in Postmenopausal Asian Women With Metastatic Breast Cancer: Results From the Phase III, Randomized PALOMA-2 Study. J Glob Oncol. 2019 May;5:1-19. PMID: 31125276
- Palbociclib and Letrozole in Advanced Breast Cancer. N Engl J Med. 2016 Nov 17;375(20):1925-1936. PMID: 27959613
- PALOMA-3: Phase III Trial of Fulvestrant With or Without Palbociclib in Premenopausal and Postmenopausal Women With Hormone Receptor-Positive, Human Epidermal Growth Factor Receptor 2-Negative Metastatic Breast Cancer That Progressed on Prior Endocrine Therapy-Safety and Efficacy in Asian Patients. J Glob Oncol. 2017 Apr 11;3(4):289-303. PMID: 28831437
- Palbociclib in Hormone-Receptor-Positive Advanced Breast Cancer. N Engl J Med. 2015 Jul 16;373(3):209-19. PMID: 26030518
最終更新日 : 2024年9月3日
監修医師 : HOKUTO編集部監修医師
執筆 : NTT東日本関東病院 薬剤部 兼平 暖先生
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
がん薬物療法における治療計画をまとめたものです。
主要論文や適正使用ガイドをもとにした用量調整プロトコール、 有害事象対応をご紹介します。
なお、 本ツールは医師向けの教育用資料であり、 実臨床での使用は想定しておりません。 最新の添付文書やガイドラインを必ずご確認下さい。
また、 一般の方への情報提供ではないことを予めご了承ください。