2025年12月5日、 従来のカプセルよりも約3分の1に小型化した錠剤が新発売となった。
本コンテンツは特定の治療法を推奨するものではありません。 個々の患者の病態や、 実際の薬剤情報やガイドラインを確認の上、 利用者の判断と責任でご利用ください。
薬剤情報
レットヴィモ®カプセル/錠 (セルペルカチニブ)
*日本イーライリリー株式会社の外部サイトへ遷移します
投与スケジュール
【1コース】28日間 (連日内服)
【催吐性】最小度
【FN発症】低リスク*
*LIBRETTO-001試験³⁾⁴⁾でFN発現は未報告
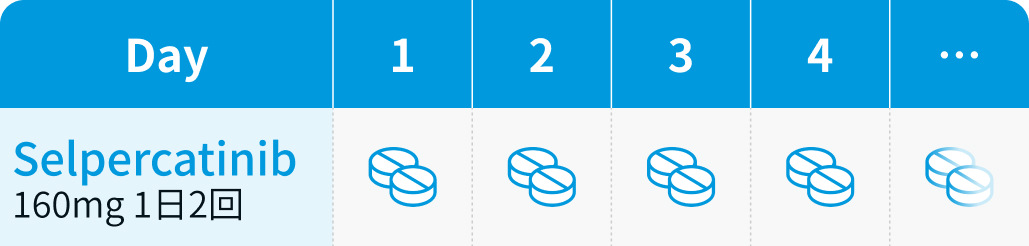
セルペルカチニブ : 1回160mg 1日2回経口投与
小児用量の記載
通常、 12歳以上の小児には体表面積に合わせて次の投与量 (セルペルカチニブとして1回約92mg/m²) を1日2回経口投与。
- 体表面積 1.2m²未満 : 80mg/回
- 体表面積 1.2m²以上1.6m²未満 : 120mg/回
- 体表面積 1.6m²以上 : 160mg/回
レットヴィモ®電子添文情報¹⁾を基に編集部作成
Key Data|臨床試験結果
📊 LIBRETTO-001試験
N Engl J Med. 2020;383:813-24 ³⁾
J Clin Oncol. 2023;41:385-394 ⁴⁾
RET融合遺伝子陽性の進行・再発NSCLCを対象に、 セルペルカチニブの有効性を評価した国際共同単群第I/II相試験。 治療歴なし69例、 化学療法既治療247例の計316例を対象とし、 独立評価委員会によるORRを主要評価項目とした。
出典⁴⁾では、 初回報告の144例³⁾から2倍超の316例へ拡大した更新データを提示し、 長期有効性と安全性をより詳細に評価した。
【有効性】
未治療例 (69例)
- ORR 84% (95%CI 73–92) / CR 6%
- PFS中央値 22.0ヵ月 (95%CI 13.8–NE)
- DoR中央値 20.2ヵ月 (95%CI 13.0–NE)
- 1年OS 92.7% (95%CI 83.3–96.9)
既治療例 (247例)
- ORR 61% (95%CI 55–67) / CR 7%
- PFS中央値 24.9ヵ月 (95%CI 19.3–NE)
- DoR中央値 28.6ヵ月 (95%CI 20.4–NE)
- 1年OS 87.9% (95%CI 83.0–91.4)
測定可能CNS転移例 (26例)
- 頭蓋内ORR 85% (95%CI 65–96) / CR 27%
【安全性】主な有害事象 : 全Grade (Grade≧3)
全安全性集団 (796例)
- 浮腫 48.5% (0.7%)
- 下痢 47.0% (5.0%)
- 倦怠感 45.9% (3.1%)
- 口内乾燥 43.2% (0%)
- 高血圧 41.0% (19.7%)
- AST上昇 36.7% (8.8%)
- ALT上昇 35.7% (11.4%)
- 腹痛 33.7% (2.5%)
- 便秘 32.8% (0.8%)
- 発疹 32.8% (0.6%)
- 悪心 31.2% (1.1%)
- Cre上昇 28.5% (1.9%)
- 頭痛 27.6% (1.4%)
- 咳嗽 23.1% (0%)
- 呼吸困難 22.5% (3.1%)
- 嘔吐 22.4% (1.8%)
- QTc延長 21.1% (4.8%)
- 関節痛 20.7% (0.3%)
📊 LIBRETTO-431試験
N Engl J Med. 2023;389:1839-50.⁵⁾
RET融合遺伝子陽性の未治療進行NSCLCを対象に、 1次治療としてセルペルカチニブ単独療法とプラチナ系化学療法±ペムブロリズマブを比較した国際共同第III相無作為化比較試験。 主要評価項目は独立評価委員会によるPFSとした。
【有効性】
主要解析集団 : セルペルカチニブ群129例 (vs 化学療法+ペムブロリズマブ群83例)
- PFS中央値 24.8ヵ月 (vs 11.2ヵ月)
- HR 0.46 (95%CI 0.31–0.70、 p<0.001)
- ORR 84% (vs 65%)
- CR 7% (vs 6%)
- DoR中央値 24.2ヵ月 (vs 11.5ヵ月)
全ITT集団 : セルペルカチニブ群159例 (vs 化学療法±ペムブロリズマブ群102例)
- PFS中央値 24.8ヵ月 (vs 11.2ヵ月)
- HR 0.48 (95%CI 0.33–0.70、 p<0.001)
- ORR 84% (vs 63%)
- CR 8% (vs 5%)
- DoR中央値 24.2ヵ月 (vs 12.0ヵ月)
各プロトコル
適格基準
LIBRETTO-001試験³⁾⁴⁾の主な適格基準
- 18歳以上
- ECOG PS 0–2
- 好中球数≧1,500/μL
- 血小板≧10万/μL
- Hb≧10g/dL
- 肝機能 : ALT/AST≦2.5×ULN、 T-Bil≦1.5×ULN
- 腎機能 : eGFR≧30mL/min
- QTcF≦470msec
EGFR変異、ALK転座、ROS1転座陽性例は除外
用量レベル
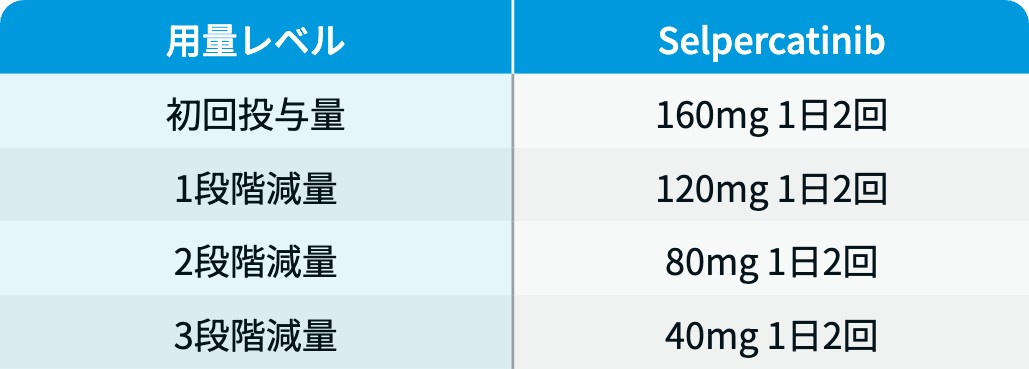
レットヴィモ®電子添文情報¹⁾を基に編集部作成
腎障害患者に対する用量調整
セルペルカチニブ : 軽度~高度の腎障害患者 (eGFR 15~89mL/分) では、 用量調整は不要。 末期腎不全患者に対する推奨用量は未確立。
Eli Lilly and Company. RETEVMO (selpercatinib) prescribing information. Revised: 11/2025.
有害事象発現時の減量・休薬・中止基準

レジメンの特徴と注意点
作用機序の特徴
セルペルカチニブは、 RET、 血管内皮増殖因子受容体 (VEGFR)、 線維芽細胞増殖因子受容体 (FGFR) などのキナーゼ活性を阻害する。 RET融合タンパクなどのリン酸化と、 その下流シグナル伝達分子のリン酸化を抑制することで、 腫瘍増殖抑制作用を示すと考えられている¹⁾。
肺癌診療ガイドライン2025の推奨⁶⁾
RET融合遺伝子陽性NSCLCの一次治療では、 セルペルカチニブ単剤療法が強く推奨されている [1B]。 2023年版では推奨度1Cであったが、 LIBRETTO-431試験⁵⁾の結果を踏まえ、 2024年版から1Bに改訂された。
レジメン適用時の注意事項
レットヴィモ®錠電子添文¹⁾ 「重要な基本的注意」 の要約
肝機能障害 : 投与開始前及び投与期間中は定期的に肝機能検査を行い、 患者の状態を十分に観察すること。
QT間隔延長 : 投与開始前にQTc≦470msecを確認し血清電解質検査を行うこと。 投与開始後1週間及び6ヵ月間は毎月1回、 心電図・電解質検査を実施すること。
LIBRETTO-001試験では、 QTcはFridericia式により補正された。
高血圧 : 投与開始前に血圧が適切に管理されていることを確認し、 投与中は定期的に血圧を測定すること。
間質性肺疾患 : 初期症状 (呼吸困難、 咳嗽、 発熱等) の確認及び胸部画像検査を実施し、 患者の状態を十分に観察すること。
RMP【重要な特定されたリスク】
レットヴィモ®RMP : 医薬品リスク管理計画書
- 肝機能障害
- QT間隔延長
- 過敏症
- 高血圧
- 間質性肺疾患
- 骨端離開
出典
1) 日本イーライリリー株式会社. レットヴィモ®錠電子添文. 2026年2月改訂 第3版.
2) 日本イーライリリー株式会社. レットヴィモ®適正使用ガイド. 2025年12月作成.
3) N Engl J Med. 2020;383:813-24.
4) J Clin Oncol. 2023;41:385-394.
5) N Engl J Med. 2023;389(20):1839-1850.
6) 日本肺癌学会. 肺癌診療ガイドライン-胸膜中皮腫・ 胸腺腫瘍含む-2025年版.
最終更新 : 2026年4月8日
執筆 : HOKUTO編集部 がん専門・指導薬剤師
監修医師 : HOKUTO編集部 医師
Selpercatinib
2025年12月5日、 従来のカプセルよりも約3分の1に小型化した錠剤が新発売となった。
本コンテンツは特定の治療法を推奨するものではありません。 個々の患者の病態や、 実際の薬剤情報やガイドラインを確認の上、 利用者の判断と責任でご利用ください。
薬剤情報
レットヴィモ®カプセル/錠 (セルペルカチニブ)
*日本イーライリリー株式会社の外部サイトへ遷移します
投与スケジュール
【1コース】28日間 (連日内服)
【催吐性】最小度
【FN発症】低リスク*
*LIBRETTO-001試験³⁾⁴⁾でFN発現は未報告

セルペルカチニブ : 1回160mg 1日2回経口投与
小児用量の記載
通常、 12歳以上の小児には体表面積に合わせて次の投与量 (セルペルカチニブとして1回約92mg/m²) を1日2回経口投与。
- 体表面積 1.2m²未満 : 80mg/回
- 体表面積 1.2m²以上1.6m²未満 : 120mg/回
- 体表面積 1.6m²以上 : 160mg/回
レットヴィモ®電子添文情報¹⁾を基に編集部作成
Key Data|臨床試験結果
📊 LIBRETTO-001試験
N Engl J Med. 2020;383:813-24 ³⁾
J Clin Oncol. 2023;41:385-394 ⁴⁾
RET融合遺伝子陽性の進行・再発NSCLCを対象に、 セルペルカチニブの有効性を評価した国際共同単群第I/II相試験。 治療歴なし69例、 化学療法既治療247例の計316例を対象とし、 独立評価委員会によるORRを主要評価項目とした。
出典⁴⁾では、 初回報告の144例³⁾から2倍超の316例へ拡大した更新データを提示し、 長期有効性と安全性をより詳細に評価した。
【有効性】
未治療例 (69例)
- ORR 84% (95%CI 73–92) / CR 6%
- PFS中央値 22.0ヵ月 (95%CI 13.8–NE)
- DoR中央値 20.2ヵ月 (95%CI 13.0–NE)
- 1年OS 92.7% (95%CI 83.3–96.9)
既治療例 (247例)
- ORR 61% (95%CI 55–67) / CR 7%
- PFS中央値 24.9ヵ月 (95%CI 19.3–NE)
- DoR中央値 28.6ヵ月 (95%CI 20.4–NE)
- 1年OS 87.9% (95%CI 83.0–91.4)
測定可能CNS転移例 (26例)
- 頭蓋内ORR 85% (95%CI 65–96) / CR 27%
【安全性】主な有害事象 : 全Grade (Grade≧3)
全安全性集団 (796例)
- 浮腫 48.5% (0.7%)
- 下痢 47.0% (5.0%)
- 倦怠感 45.9% (3.1%)
- 口内乾燥 43.2% (0%)
- 高血圧 41.0% (19.7%)
- AST上昇 36.7% (8.8%)
- ALT上昇 35.7% (11.4%)
- 腹痛 33.7% (2.5%)
- 便秘 32.8% (0.8%)
- 発疹 32.8% (0.6%)
- 悪心 31.2% (1.1%)
- Cre上昇 28.5% (1.9%)
- 頭痛 27.6% (1.4%)
- 咳嗽 23.1% (0%)
- 呼吸困難 22.5% (3.1%)
- 嘔吐 22.4% (1.8%)
- QTc延長 21.1% (4.8%)
- 関節痛 20.7% (0.3%)
📊 LIBRETTO-431試験
N Engl J Med. 2023;389:1839-50.⁵⁾
RET融合遺伝子陽性の未治療進行NSCLCを対象に、 1次治療としてセルペルカチニブ単独療法とプラチナ系化学療法±ペムブロリズマブを比較した国際共同第III相無作為化比較試験。 主要評価項目は独立評価委員会によるPFSとした。
【有効性】
主要解析集団 : セルペルカチニブ群129例 (vs 化学療法+ペムブロリズマブ群83例)
- PFS中央値 24.8ヵ月 (vs 11.2ヵ月)
- HR 0.46 (95%CI 0.31–0.70、 p<0.001)
- ORR 84% (vs 65%)
- CR 7% (vs 6%)
- DoR中央値 24.2ヵ月 (vs 11.5ヵ月)
全ITT集団 : セルペルカチニブ群159例 (vs 化学療法±ペムブロリズマブ群102例)
- PFS中央値 24.8ヵ月 (vs 11.2ヵ月)
- HR 0.48 (95%CI 0.33–0.70、 p<0.001)
- ORR 84% (vs 63%)
- CR 8% (vs 5%)
- DoR中央値 24.2ヵ月 (vs 12.0ヵ月)
各プロトコル
適格基準
LIBRETTO-001試験³⁾⁴⁾の主な適格基準
- 18歳以上
- ECOG PS 0–2
- 好中球数≧1,500/μL
- 血小板≧10万/μL
- Hb≧10g/dL
- 肝機能 : ALT/AST≦2.5×ULN、 T-Bil≦1.5×ULN
- 腎機能 : eGFR≧30mL/min
- QTcF≦470msec
EGFR変異、ALK転座、ROS1転座陽性例は除外
用量レベル

レットヴィモ®電子添文情報¹⁾を基に編集部作成
腎障害患者に対する用量調整
セルペルカチニブ : 軽度~高度の腎障害患者 (eGFR 15~89mL/分) では、 用量調整は不要。 末期腎不全患者に対する推奨用量は未確立。
Eli Lilly and Company. RETEVMO (selpercatinib) prescribing information. Revised: 11/2025.
有害事象発現時の減量・休薬・中止基準

レジメンの特徴と注意点
作用機序の特徴
セルペルカチニブは、 RET、 血管内皮増殖因子受容体 (VEGFR)、 線維芽細胞増殖因子受容体 (FGFR) などのキナーゼ活性を阻害する。 RET融合タンパクなどのリン酸化と、 その下流シグナル伝達分子のリン酸化を抑制することで、 腫瘍増殖抑制作用を示すと考えられている¹⁾。
肺癌診療ガイドライン2025の推奨⁶⁾
RET融合遺伝子陽性NSCLCの一次治療では、 セルペルカチニブ単剤療法が強く推奨されている [1B]。 2023年版では推奨度1Cであったが、 LIBRETTO-431試験⁵⁾の結果を踏まえ、 2024年版から1Bに改訂された。
レジメン適用時の注意事項
レットヴィモ®錠電子添文¹⁾ 「重要な基本的注意」 の要約
肝機能障害 : 投与開始前及び投与期間中は定期的に肝機能検査を行い、 患者の状態を十分に観察すること。
QT間隔延長 : 投与開始前にQTc≦470msecを確認し血清電解質検査を行うこと。 投与開始後1週間及び6ヵ月間は毎月1回、 心電図・電解質検査を実施すること。
LIBRETTO-001試験では、 QTcはFridericia式により補正された。
高血圧 : 投与開始前に血圧が適切に管理されていることを確認し、 投与中は定期的に血圧を測定すること。
間質性肺疾患 : 初期症状 (呼吸困難、 咳嗽、 発熱等) の確認及び胸部画像検査を実施し、 患者の状態を十分に観察すること。
RMP【重要な特定されたリスク】
レットヴィモ®RMP : 医薬品リスク管理計画書
- 肝機能障害
- QT間隔延長
- 過敏症
- 高血圧
- 間質性肺疾患
- 骨端離開
出典
1) 日本イーライリリー株式会社. レットヴィモ®錠電子添文. 2026年2月改訂 第3版.
2) 日本イーライリリー株式会社. レットヴィモ®適正使用ガイド. 2025年12月作成.
3) N Engl J Med. 2020;383:813-24.
4) J Clin Oncol. 2023;41:385-394.
5) N Engl J Med. 2023;389(20):1839-1850.
6) 日本肺癌学会. 肺癌診療ガイドライン-胸膜中皮腫・ 胸腺腫瘍含む-2025年版.
最終更新 : 2026年4月8日
執筆 : HOKUTO編集部 がん専門・指導薬剤師
監修医師 : HOKUTO編集部 医師
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
がん薬物療法における治療計画をまとめたものです。
主要論文や適正使用ガイドをもとにした用量調整プロトコール、 有害事象対応をご紹介します。
なお、 本ツールは医師向けの教育用資料であり、 実臨床での使用は想定しておりません。 最新の添付文書やガイドラインを必ずご確認下さい。
また、 一般の方への情報提供ではないことを予めご了承ください。