本コンテンツは特定の治療法を推奨するものではありません。 個々の患者の病態や、 実際の薬剤情報やガイドラインを確認の上、 利用者の判断と責任でご利用ください。
薬剤情報
ヒト型抗ヒトPD-1モノクローナル抗体 ニボルマブ
*小野薬品工業の外部サイトへ遷移します
投与スケジュール
電子添文¹⁾の用法および用量
2週間間隔の場合
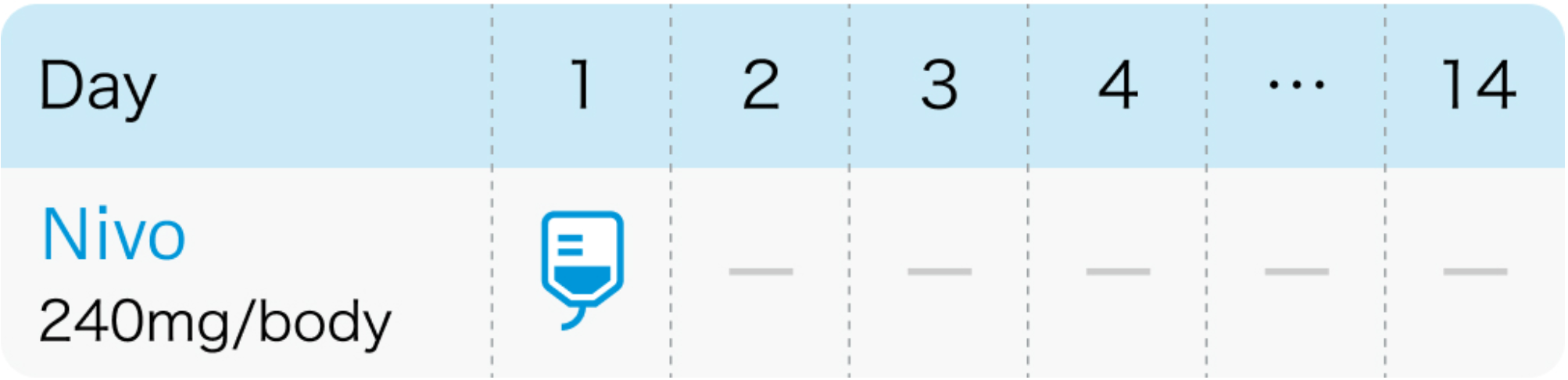
4週間間隔の場合
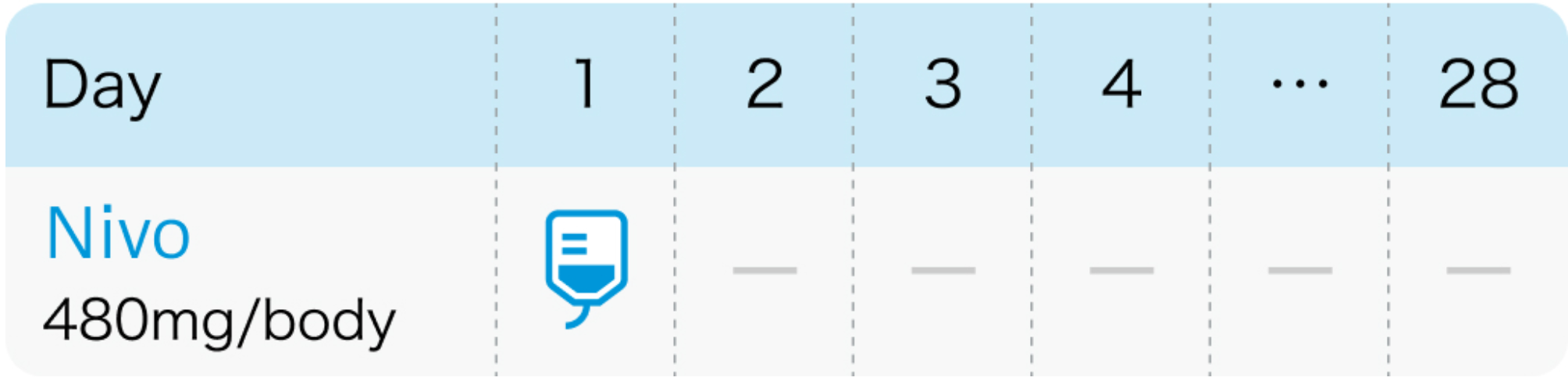
いずれの場合も投与期間は12ヵ月間までとする
オプジーボ®電子添文 (2024年7月改訂第21版)より引用
特徴と注意点
保険適応の範囲は術後補助療法のみ
監修 : 国立がん研究センター東病院 腫瘍内科 近藤 千紘先生
KeyData|臨床試験結果
CheckMate 274試験²⁾³⁾
²⁾ N Engl J Med . 2021;384(22):2102-14.
筋層浸潤性尿路上皮癌の術後患者において、 抗PD-1抗体ニボルマブ投与の効果を、 プラセボを対照に検証した第Ⅲ相比較試験
有効性|ニボルマブ群
- mDFS : 22.0ヵ月²⁾ (PD-L1≧1% 52.6ヵ月)
プラセボ群 10.9ヵ月、 HR 0.71 (95%CI 0.58-0.86)、 PD-L1≧1%プラセボ群 8.4ヵ月、 HR 0.52 (95%CI 0.37-0.72)
- mOS : 69.5ヵ月 (PD-L1≧1% NR)
プラセボ群 50.1ヵ月、 HR 0.76 (95%CI 0.61-0.96)、 PD-L1≧1%プラセボ群 NR、 HR 0.56 (95%CI 0.36-0.86)
主な有害事象 (カッコ内はGrade3~4)
- ALT上昇 4.3% (0.6%)
- AST上昇 3.7% (0.3%)
- 下痢 16.8% (0.9%)
注意すべき有害事象
- 甲状腺機能低下症 9.7% (0%)
- 甲状腺機能亢進症 9.4% (0%)
- 血尿 0.6% (0%)
各プロトコル
投与開始基準
CheckMate 274試験²⁾のプロトコル
病理学的に再発リスクの高い尿路上皮癌と診断され、 以下の基準を満たす18歳以上の患者
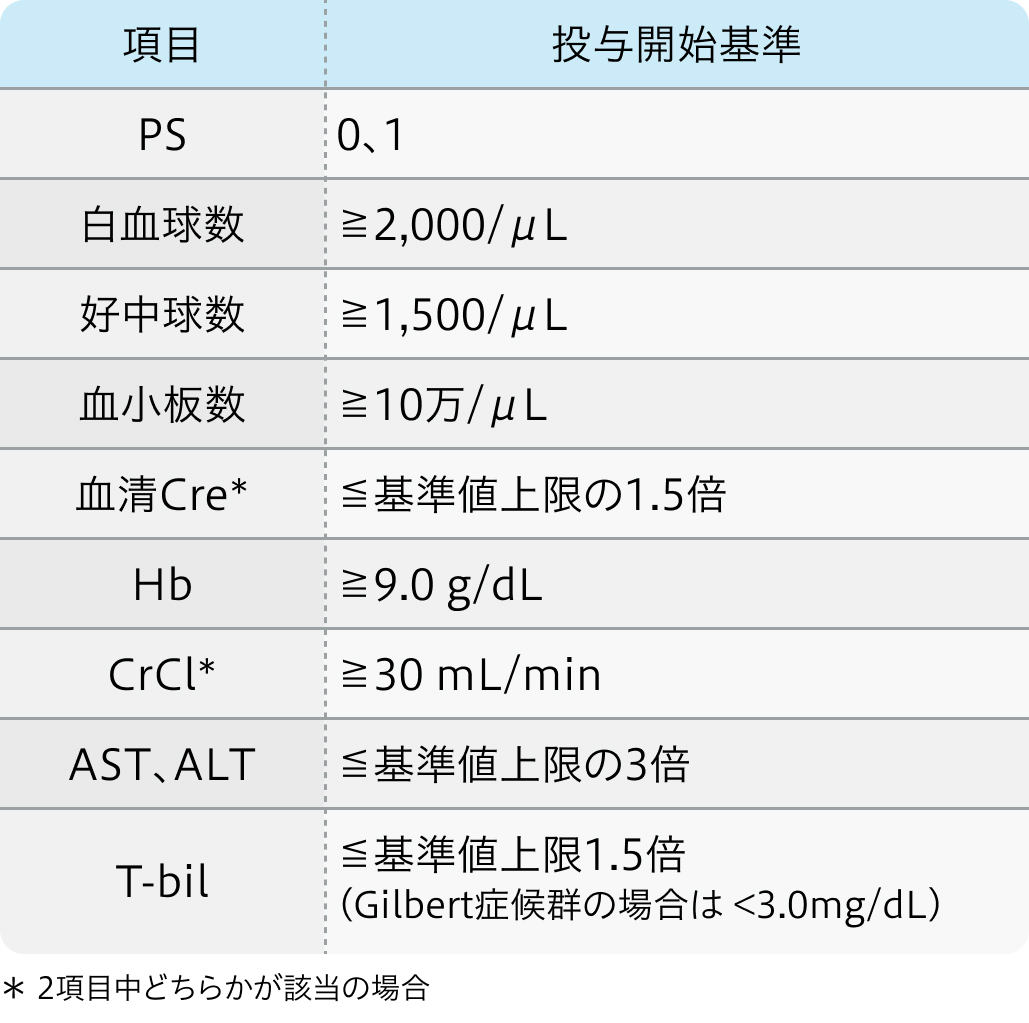
中止基準
CheckMate 274試験²⁾のプロトコル
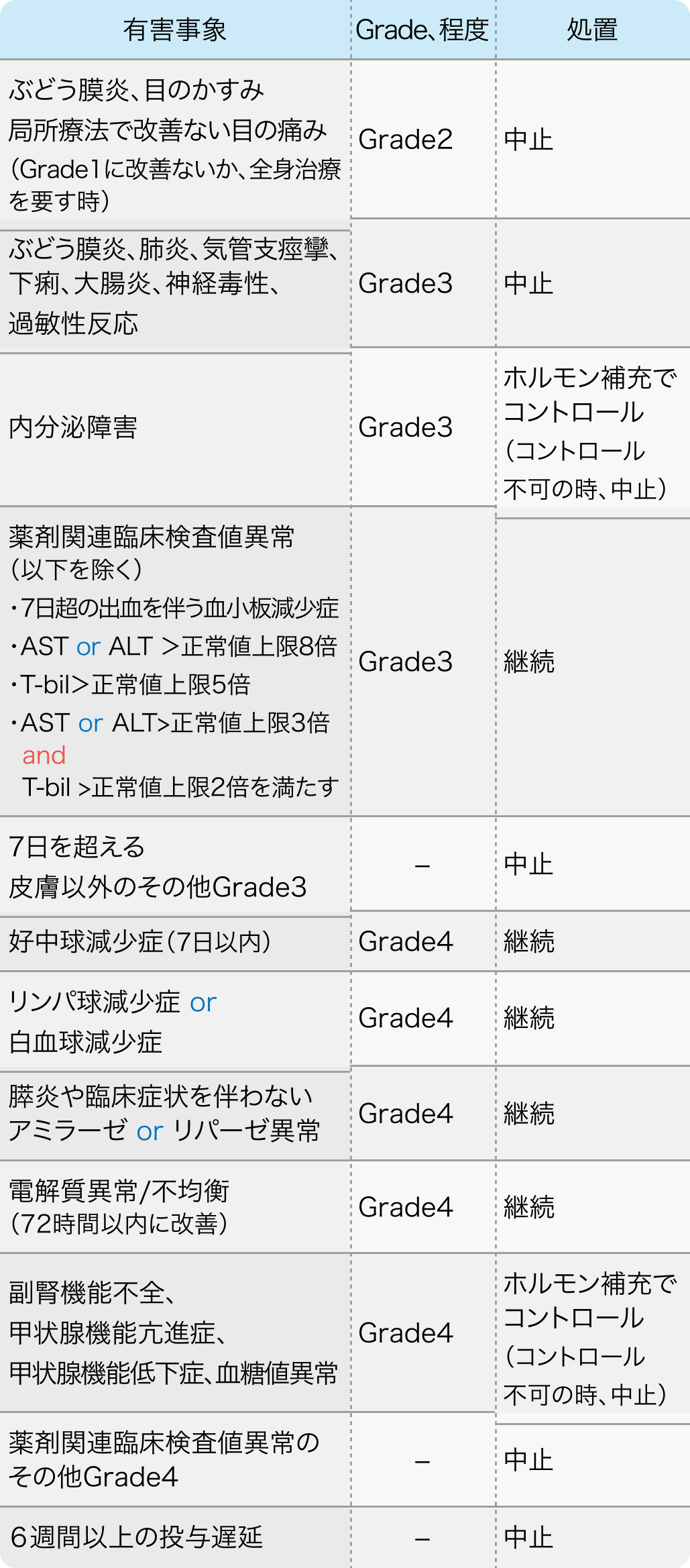
出典
1) オプジーボ®電子添文 (2024年7月改訂第21版) [最終閲覧 2024/11/27]
最終更新日 : 2024年11月27日
監修医師 : 国立がん研究センター東病院 腫瘍内科 近藤 千紘先生
Nivolumab
本コンテンツは特定の治療法を推奨するものではありません。 個々の患者の病態や、 実際の薬剤情報やガイドラインを確認の上、 利用者の判断と責任でご利用ください。
薬剤情報
ヒト型抗ヒトPD-1モノクローナル抗体 ニボルマブ
*小野薬品工業の外部サイトへ遷移します
投与スケジュール
電子添文¹⁾の用法および用量
2週間間隔の場合

4週間間隔の場合

いずれの場合も投与期間は12ヵ月間までとする
オプジーボ®電子添文 (2024年7月改訂第21版)より引用
特徴と注意点
保険適応の範囲は術後補助療法のみ
監修 : 国立がん研究センター東病院 腫瘍内科 近藤 千紘先生
KeyData|臨床試験結果
CheckMate 274試験²⁾³⁾
²⁾ N Engl J Med . 2021;384(22):2102-14.
筋層浸潤性尿路上皮癌の術後患者において、 抗PD-1抗体ニボルマブ投与の効果を、 プラセボを対照に検証した第Ⅲ相比較試験
有効性|ニボルマブ群
- mDFS : 22.0ヵ月²⁾ (PD-L1≧1% 52.6ヵ月)
プラセボ群 10.9ヵ月、 HR 0.71 (95%CI 0.58-0.86)、 PD-L1≧1%プラセボ群 8.4ヵ月、 HR 0.52 (95%CI 0.37-0.72)
- mOS : 69.5ヵ月 (PD-L1≧1% NR)
プラセボ群 50.1ヵ月、 HR 0.76 (95%CI 0.61-0.96)、 PD-L1≧1%プラセボ群 NR、 HR 0.56 (95%CI 0.36-0.86)
主な有害事象 (カッコ内はGrade3~4)
- ALT上昇 4.3% (0.6%)
- AST上昇 3.7% (0.3%)
- 下痢 16.8% (0.9%)
注意すべき有害事象
- 甲状腺機能低下症 9.7% (0%)
- 甲状腺機能亢進症 9.4% (0%)
- 血尿 0.6% (0%)
各プロトコル
投与開始基準
CheckMate 274試験²⁾のプロトコル
病理学的に再発リスクの高い尿路上皮癌と診断され、 以下の基準を満たす18歳以上の患者

中止基準
CheckMate 274試験²⁾のプロトコル

出典
1) オプジーボ®電子添文 (2024年7月改訂第21版) [最終閲覧 2024/11/27]
最終更新日 : 2024年11月27日
監修医師 : 国立がん研究センター東病院 腫瘍内科 近藤 千紘先生
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
がん薬物療法における治療計画をまとめたものです。
主要論文や適正使用ガイドをもとにした用量調整プロトコール、 有害事象対応をご紹介します。
なお、 本ツールは医師向けの教育用資料であり、 実臨床での使用は想定しておりません。 最新の添付文書やガイドラインを必ずご確認下さい。
また、 一般の方への情報提供ではないことを予めご了承ください。