「アンドロゲン受容体陽性の根治切除不能な進行・再発の唾液腺癌」 を対象として、 2026年3月23日に正式承認された。
本コンテンツは特定の治療法を推奨するものではありません。 個々の患者の病態や、 実際の薬剤情報やガイドラインを確認の上、 利用者の判断と責任でご利用ください。
薬剤情報
ニュベクオ® (ダロルタミド)
*バイエル薬品株式会社の外部サイトへ遷移します
投与スケジュール
【1コース】28日間
【催吐性】最小度~軽度*
【FN発症】低リスク**
*NCCN Guidelines Version 2.2025. Antiemesis
**DISCOVARY試験³⁾でFN発現は未報告
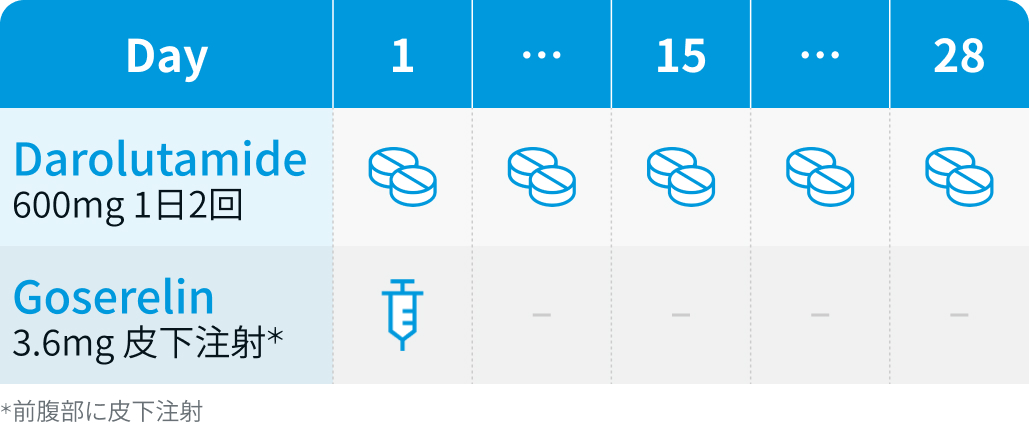
ダロルタミド : 600mgを1日2回食後*経口投与
*食後投与では空腹時投与より曝露量が高くなる
ゴセレリン : 3.6mgを4週間ごとに皮下注射
Key Data|臨床試験結果
📊 DISCOVARY試験³⁾
AR陽性の根治切除不能な進行・再発唾液腺癌 (97.0%が唾液腺導管癌) を対象とした、 多施設共同非盲検・第II相単群試験 (医師主導治験)。 ECOG PS 0–2かつ測定可能病変を有する33例が登録され、 ダロルタミド+ゴセレリンが投与された (有効性解析対象集団 [mFAS] 31例)。 主要評価項目は独立中央判定によるORRで、 閾値奏効率15%に対する正確な二項検定 (片側有意水準0.05) で評価した。
【有効性】
- ORR 45.2% (90%CI 29.7–61.3、 p<0.001)
- CR 3.2%
- PR 41.9%
- 奏効期間中央値 18.2ヵ月 (95%CI 11.3–NR)
- 臨床的有用率 51.6% (95%CI 33.1–69.8)
- 病勢制御率 64.5% (95%CI 45.4–80.8)
- PFS中央値 13.1ヵ月 (95%CI 2.0–NR)
- OS中央値 未到達 (95%CI 20.0ヵ月–NR)
NR : 未到達
【安全性】主な副作用 : 全Grade (Grade≧3)
- ALT上昇 18.2% (0%)
- AST上昇 18.2% (0%)
- 肝機能異常 9.1% (0%)
- 倦怠感 9.1% (0%)
- 体重減少 9.1% (0%)
- 貧血 6.1% (0%)
- 食欲減退 6.1% (0%)
- ほてり 6.1% (0%)
- そう痒症 6.1% (0%)
- 発熱 6.1% (0%)
- 好中球減少 6.1% (3.0%)
各プロトコル
適格基準
DISCOVARY試験³⁾の主な適格基準
- AR陽性 (IHC法による施設判定) の根治切除不能な進行・再発唾液腺癌
- 根治不能かつ手術及び放射線療法の適応とならない局所進行又は再発・転移
- ECOG PS 0–2
用量レベル
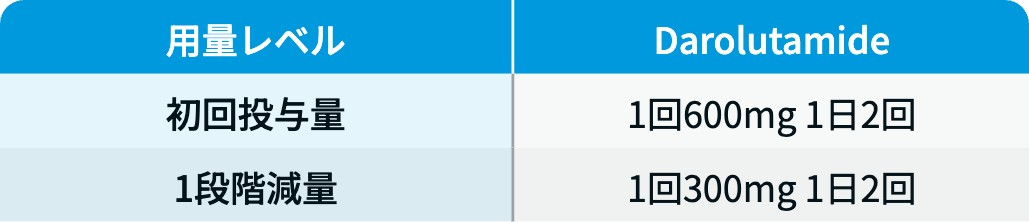
ニュベクオ®電子添文情報¹⁾を基に編集部作成
腎障害患者に対する用量調整
軽度~中等度腎機能障害 (eGFR 30–89mL/min/1.73m²) では減量不要である。 一方、 重度腎機能障害 (eGFR 15–29mL/min/1.73m²) で血液透析を受けていない患者では、 曝露量が増加するため、 1回300mgを1日2回に減量する。 末期腎不全 (eGFR≦15 mL/min/1.73m²) における薬物動態への影響は不明である。
Bayer HealthCare Pharmaceuticals Inc. NUBEQA® (darolutamide) prescribing information. Revised June 2025. U.S. Food and Drug Administration.
有害事象発現時の減量・休薬・中止基準
グレード≧3または忍容できない副作用が現れた場合は、 回復まで休薬し、 回復後は1回300mgを1日2回に減量して再開を考慮する。 ただし、 患者の状態に応じて通常用量への増量は可能。
DISCOVARY試験の対応方法 (補足情報)
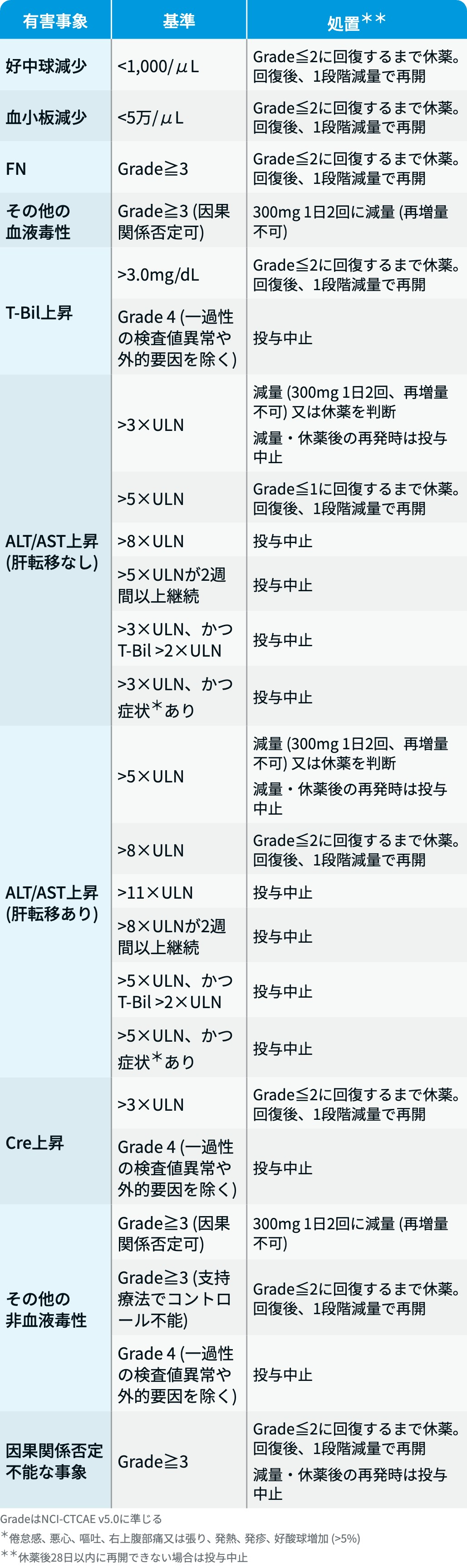
ニュベクオ®適正使用ガイド²⁾を基に編集部作成
レジメンの特徴と注意点
🧑⚕️これまで、 AR陽性唾液腺癌に対する標準的な抗アンドロゲン療法は、 GnRHアゴニストであるリュープロレリンと第一世代AR阻害薬ビカルタミドの併用療法に限られていた。 前立腺癌における治療体系に倣い、 本疾患においても第二世代AR阻害薬 (エンザルタミド、 アパルタミド、 ダロルタミド) を用いた臨床開発が進められてきた。 エンザルタミド単剤、 およびアパルタミドとゴセレリンの併用による前向き試験では期待された成果は得られなかったものの、 今般のDISCOVERY試験において 「ダロルタミド+ゴセレリン併用療法」 の優れた治療成績が示され、 AR陽性唾液腺癌を適応症として世界で初めて承認を得るに至った。 既報の各試験結果を概観すると、 奏効例の大半は、 AR陽性を特徴とする 「唾液腺導管癌 (SDC)」、 とりわけ腫瘍細胞の70%以上が陽性を示す 「AR強陽性」 例が占めている。 DISCOVERY試験の登録例の大部分がAR強陽性のSDCであった点は、 本治療法を適用する際に 「組織型」 および 「AR発現強度」 の精査が重要であることを示している。 また、 AR強陽性のSDCであっても奏効に至らない症例が散見されることから、 治療のさらなる最適化に向けて、 バイオマーカー研究による症例選別 (層別化) の確立が切望される。
国立がん研究センター中央病院 本間義崇先生
作用機序の特徴
ダロルタミドは、 アンドロゲン受容体 (AR) のリガンド結合部位に競合的に結合してARシグナル伝達を阻害する。 AR活性化の核内移行を阻害し、 AR依存性の転写活性を抑制することで腫瘍増殖を抑制する。
患者選択におけるAR検査⁴⁾
AR検査は、 十分な経験を有する病理医または検査施設で実施する。 ダロルタミド投与には、 IHC法によるAR陽性の確認が必要である。 DISCOVARY試験の中央判定ではSP107抗体 (ロシュ・ダイアグノスティックス) を用い、 腫瘍細胞核の1%以上にAR発現を認めた場合をAR陽性と判定した。
レジメン適用時の注意事項
心臓障害 : 不整脈等の心臓障害が報告されている。 投与開始前及び投与中は心機能を十分に観察する。
間質性肺疾患 : ダロルタミドとの因果関係は明らかでないが、 ILDが報告されている。 咳嗽や呼吸困難などの呼吸器症状に注意し、 異常を認めた場合は適切な検査を行う。
薬物相互作用 : 強いCYP3A誘導薬との併用ではダロルタミドの曝露量が低下し、 有効性が減弱するおそれがあるため、 代替薬を考慮する。 また、 ダロルタミドはBCRP、 OATP1B1、 OATP1B3を阻害するため、 これらの基質薬の血中濃度を上昇させ、 副作用を増強するおそれがある。
RMP【重要な特定されたリスク】
ニュベクオ®RMP : 医薬品リスク管理計画書
該当なし
出典
1) バイエル薬品株式会社. ニュベクオ®錠300mg 電子添文. 2026年3月改訂 第7版.
2) バイエル薬品株式会社. ニュベクオ®錠300mg 適正使用ガイド 唾液腺癌編. 2026年3月作成.
3) バイエル薬品株式会社. DISCOVARY試験について (PP-NUB-JP-2207-24-03).
4) 厚生労働省医薬局医薬品審査管理課. ダロルタミド製剤の使用にあたっての留意事項について (令和8年3月23日).
最終更新日 : 2026年4月1日
執筆 : HOKUTO編集部 がん専門・指導薬剤師
執筆協力 : 国立がん研究センター中央病院 頭頸部・食道内科 本間義崇
監修 : 国立がん研究センター中央病院 頭頸部・食道内科 加藤健
Darolutamide+Goserelin
「アンドロゲン受容体陽性の根治切除不能な進行・再発の唾液腺癌」 を対象として、 2026年3月23日に正式承認された。
本コンテンツは特定の治療法を推奨するものではありません。 個々の患者の病態や、 実際の薬剤情報やガイドラインを確認の上、 利用者の判断と責任でご利用ください。
薬剤情報
ニュベクオ® (ダロルタミド)
*バイエル薬品株式会社の外部サイトへ遷移します
投与スケジュール
【1コース】28日間
【催吐性】最小度~軽度*
【FN発症】低リスク**
*NCCN Guidelines Version 2.2025. Antiemesis
**DISCOVARY試験³⁾でFN発現は未報告

ダロルタミド : 600mgを1日2回食後*経口投与
*食後投与では空腹時投与より曝露量が高くなる
ゴセレリン : 3.6mgを4週間ごとに皮下注射
Key Data|臨床試験結果
📊 DISCOVARY試験³⁾
AR陽性の根治切除不能な進行・再発唾液腺癌 (97.0%が唾液腺導管癌) を対象とした、 多施設共同非盲検・第II相単群試験 (医師主導治験)。 ECOG PS 0–2かつ測定可能病変を有する33例が登録され、 ダロルタミド+ゴセレリンが投与された (有効性解析対象集団 [mFAS] 31例)。 主要評価項目は独立中央判定によるORRで、 閾値奏効率15%に対する正確な二項検定 (片側有意水準0.05) で評価した。
【有効性】
- ORR 45.2% (90%CI 29.7–61.3、 p<0.001)
- CR 3.2%
- PR 41.9%
- 奏効期間中央値 18.2ヵ月 (95%CI 11.3–NR)
- 臨床的有用率 51.6% (95%CI 33.1–69.8)
- 病勢制御率 64.5% (95%CI 45.4–80.8)
- PFS中央値 13.1ヵ月 (95%CI 2.0–NR)
- OS中央値 未到達 (95%CI 20.0ヵ月–NR)
NR : 未到達
【安全性】主な副作用 : 全Grade (Grade≧3)
- ALT上昇 18.2% (0%)
- AST上昇 18.2% (0%)
- 肝機能異常 9.1% (0%)
- 倦怠感 9.1% (0%)
- 体重減少 9.1% (0%)
- 貧血 6.1% (0%)
- 食欲減退 6.1% (0%)
- ほてり 6.1% (0%)
- そう痒症 6.1% (0%)
- 発熱 6.1% (0%)
- 好中球減少 6.1% (3.0%)
各プロトコル
適格基準
DISCOVARY試験³⁾の主な適格基準
- AR陽性 (IHC法による施設判定) の根治切除不能な進行・再発唾液腺癌
- 根治不能かつ手術及び放射線療法の適応とならない局所進行又は再発・転移
- ECOG PS 0–2
用量レベル

ニュベクオ®電子添文情報¹⁾を基に編集部作成
腎障害患者に対する用量調整
軽度~中等度腎機能障害 (eGFR 30–89mL/min/1.73m²) では減量不要である。 一方、 重度腎機能障害 (eGFR 15–29mL/min/1.73m²) で血液透析を受けていない患者では、 曝露量が増加するため、 1回300mgを1日2回に減量する。 末期腎不全 (eGFR≦15 mL/min/1.73m²) における薬物動態への影響は不明である。
Bayer HealthCare Pharmaceuticals Inc. NUBEQA® (darolutamide) prescribing information. Revised June 2025. U.S. Food and Drug Administration.
有害事象発現時の減量・休薬・中止基準
グレード≧3または忍容できない副作用が現れた場合は、 回復まで休薬し、 回復後は1回300mgを1日2回に減量して再開を考慮する。 ただし、 患者の状態に応じて通常用量への増量は可能。
DISCOVARY試験の対応方法 (補足情報)

ニュベクオ®適正使用ガイド²⁾を基に編集部作成
レジメンの特徴と注意点
🧑⚕️これまで、 AR陽性唾液腺癌に対する標準的な抗アンドロゲン療法は、 GnRHアゴニストであるリュープロレリンと第一世代AR阻害薬ビカルタミドの併用療法に限られていた。 前立腺癌における治療体系に倣い、 本疾患においても第二世代AR阻害薬 (エンザルタミド、 アパルタミド、 ダロルタミド) を用いた臨床開発が進められてきた。 エンザルタミド単剤、 およびアパルタミドとゴセレリンの併用による前向き試験では期待された成果は得られなかったものの、 今般のDISCOVERY試験において 「ダロルタミド+ゴセレリン併用療法」 の優れた治療成績が示され、 AR陽性唾液腺癌を適応症として世界で初めて承認を得るに至った。 既報の各試験結果を概観すると、 奏効例の大半は、 AR陽性を特徴とする 「唾液腺導管癌 (SDC)」、 とりわけ腫瘍細胞の70%以上が陽性を示す 「AR強陽性」 例が占めている。 DISCOVERY試験の登録例の大部分がAR強陽性のSDCであった点は、 本治療法を適用する際に 「組織型」 および 「AR発現強度」 の精査が重要であることを示している。 また、 AR強陽性のSDCであっても奏効に至らない症例が散見されることから、 治療のさらなる最適化に向けて、 バイオマーカー研究による症例選別 (層別化) の確立が切望される。
国立がん研究センター中央病院 本間義崇先生
作用機序の特徴
ダロルタミドは、 アンドロゲン受容体 (AR) のリガンド結合部位に競合的に結合してARシグナル伝達を阻害する。 AR活性化の核内移行を阻害し、 AR依存性の転写活性を抑制することで腫瘍増殖を抑制する。
患者選択におけるAR検査⁴⁾
AR検査は、 十分な経験を有する病理医または検査施設で実施する。 ダロルタミド投与には、 IHC法によるAR陽性の確認が必要である。 DISCOVARY試験の中央判定ではSP107抗体 (ロシュ・ダイアグノスティックス) を用い、 腫瘍細胞核の1%以上にAR発現を認めた場合をAR陽性と判定した。
レジメン適用時の注意事項
心臓障害 : 不整脈等の心臓障害が報告されている。 投与開始前及び投与中は心機能を十分に観察する。
間質性肺疾患 : ダロルタミドとの因果関係は明らかでないが、 ILDが報告されている。 咳嗽や呼吸困難などの呼吸器症状に注意し、 異常を認めた場合は適切な検査を行う。
薬物相互作用 : 強いCYP3A誘導薬との併用ではダロルタミドの曝露量が低下し、 有効性が減弱するおそれがあるため、 代替薬を考慮する。 また、 ダロルタミドはBCRP、 OATP1B1、 OATP1B3を阻害するため、 これらの基質薬の血中濃度を上昇させ、 副作用を増強するおそれがある。
RMP【重要な特定されたリスク】
ニュベクオ®RMP : 医薬品リスク管理計画書
該当なし
出典
1) バイエル薬品株式会社. ニュベクオ®錠300mg 電子添文. 2026年3月改訂 第7版.
2) バイエル薬品株式会社. ニュベクオ®錠300mg 適正使用ガイド 唾液腺癌編. 2026年3月作成.
3) バイエル薬品株式会社. DISCOVARY試験について (PP-NUB-JP-2207-24-03).
4) 厚生労働省医薬局医薬品審査管理課. ダロルタミド製剤の使用にあたっての留意事項について (令和8年3月23日).
最終更新日 : 2026年4月1日
執筆 : HOKUTO編集部 がん専門・指導薬剤師
執筆協力 : 国立がん研究センター中央病院 頭頸部・食道内科 本間義崇
監修 : 国立がん研究センター中央病院 頭頸部・食道内科 加藤健
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
がん薬物療法における治療計画をまとめたものです。
主要論文や適正使用ガイドをもとにした用量調整プロトコール、 有害事象対応をご紹介します。
なお、 本ツールは医師向けの教育用資料であり、 実臨床での使用は想定しておりません。 最新の添付文書やガイドラインを必ずご確認下さい。
また、 一般の方への情報提供ではないことを予めご了承ください。