2026年2月19日、 「がん化学療法後に増悪した低異型度漿液性卵巣癌」 について承認を取得した。
本コンテンツは特定の治療法を推奨するものではありません。 個々の患者の病態や、 実際の薬剤情報やガイドラインを確認の上、 利用者の判断と責任でご利用ください。
薬剤情報
メキニスト® (トラメチニブ)
添付文書¹⁾ / 適正使用情報 (準備中)²⁾
ノバルティスファーマ株式会社の外部サイトへ遷移します
投与スケジュール
【1コース】連日内服投与
【催吐性】最小度
【FN発症】未報告*
*GOG 281/LOGS試験ではFN発生率は未報告
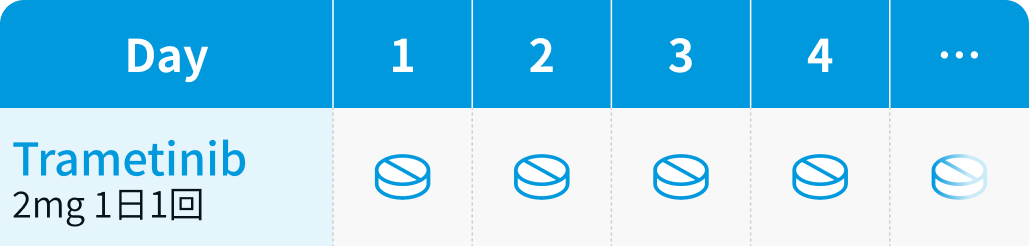
通常、 成人にはトラメチニブとして2mgを1日1回、 食事の1時間以上前又は食後2時間以降に経口投与する。 なお、 患者の状態により適宜減量する。
Key Data|臨床試験結果
📊 GOG 281/LOGS試験
Lancet. 2022;399(10324):541-553.
再発・進行の低異型度漿液性卵巣癌患者を対象に、 トラメチニブの有効性と安全性を標準治療 (医師選択治療*) と比較した国際共同第II/III相無作為化比較試験である。 トラメチニブ群130例、 標準治療群130例に1 : 1で割り付け、 主要評価項目はPFSに設定された。
*パクリタキセル、 PEG化リポソームドキソルビシン (PLD)、 トポテカン、 レトロゾール、 タモキシフェンのいずれか
【有効性】トラメチニブ群 (vs 標準治療群)
- PFS中央値 13.0ヵ月 (vs 7.2ヵ月)
- HR 0.48 (95%CI 0.36–0.64、 p<0.0001)
- ORR 26% (vs 6%)
- OS中央値 37.6ヵ月 (vs 29.2ヵ月)
- HR 0.76 (95%CI 0.51–1.12、 p=0.156)
【安全性】主な有害事象 : 全Grade (Grade≧3)
- 倦怠感 73% (8%)
- 末梢性浮腫 49% (0%)
- 腹痛 45% (6%)
- 便秘 42% (2%)
- 下痢 73% (10%)
- 口腔粘膜炎 35% (2%)
- 悪心 61% (9%)
- 嘔吐 46% (7%)
- 皮膚乾燥 44% (1%)
- 痤瘡様皮疹 63% (6%)
- 斑状丘疹状皮疹 42% (7%)
- 貧血 52% (13%)
- 白血球数減少 22% (1%)
- ALP増加 25% (2%)
- AST増加 37% (1%)
- ALT増加 22% (2%)
- クレアチニン増加 20% (1%)
- 食欲不振 27% (2%)
- 高血糖 25% (0%)
- 低カリウム血症 20% (4%)
- 低マグネシウム血症 32% (1%)
- 低アルブミン血症 34% (3%)
- 頭痛 21% (0%)
- 末梢性感覚ニューロパチー 28% (1%)
- 高血圧 39% (12%)
- 呼吸困難 35% (3%)
- 尿路感染 23% (7%)
各プロトコル
適格基準
GOG 281/LOGS試験³⁾の主な適格基準
- 18歳以上
- 組織学的に確認された低異型度漿液性卵巣癌
- 少なくとも1つの白金併用化学療法歴あり
- ECOG PS 0–1
- 好中球数≧1500/μL
- 血小板数≧10万/μL
- Hb≧9.0g/dL
- 肝機能 : T-Bil≦1.5×ULN、 AST/ALT≦2.5×ULN
用量レベル
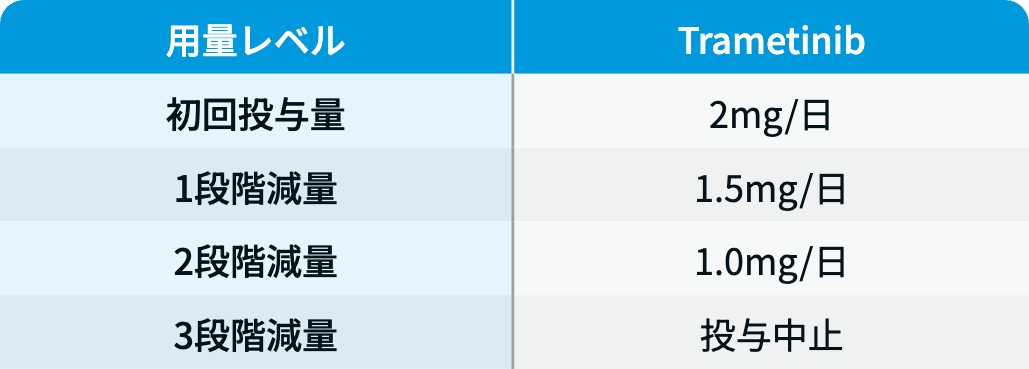
0.5mg錠と2mg錠の生物学的同等性は示されていないため、 2mgを投与する際は0.5mg錠を使用しないこと¹⁾。
腎障害患者に対する用量調整
腎機能障害 (eGFR 15~89mL/min/1.73m²) は、 トラメチニブの曝露量に臨床的に重要な影響を及ぼさない。
U.S. Food and Drug Administration. MEKINIST® (trametinib) tablets: Full Prescribing Information. Revised June 2022. Reference ID: 5002951.
有害事象発現時の減量・休薬・中止基準
電子添文情報¹⁾ :

GOG 281/LOGS試験のプロトコル³⁾ :

GOG 281/LOGS試験³⁾のプロトコルを基に編集部作成
レジメンの特徴と注意点
本レジメンの位置付け
遺伝子変異型によらず、 がん化学療法後に増悪した低異型度漿液性卵巣癌 (腹膜癌、 卵管癌及び卵巣癌) に対して有効性が期待できる⁴⁾。
他の抗悪性腫瘍剤との併用及び手術の補助療法における本剤の有効性及び安全性は確立していない。
作用機序の特徴
トラメチニブは、 MEK1及びMEK2の活性化並びにキナーゼ活性を阻害し、 A375P F11細胞株を皮下移植したマウスの腫瘍組織において、 MEKの基質であるERKのリン酸化を阻害した。
レジメン適用時の注意事項
心臓障害 : LVEF低下、 心不全等があらわれることがあるため、 本剤投与開始前及び投与中は、 心機能検査 (心エコー等) を定期的に実施する。
眼障害 : 網膜静脈閉塞症、 網膜剥離等の眼障害があらわれることがあるため、 視力異常等の異常が認められた場合には速やかに眼科医による検査を受けるよう患者に指導する。
肝機能障害 : 肝機能障害があらわれることがあるため、 定期的に肝機能検査を行う。
発熱 : 高頻度に認められ、 重度の脱水や低血圧を伴う例も報告されている。 患者の状態を十分に観察し、 異常が認められた場合は減量、 休薬、 解熱剤投与など適切に対応し、 感染症等の有無を評価する。 解熱剤で効果不十分な場合は、 経口ステロイド剤の投与を検討する。
横紋筋融解症 : 筋肉痛、 脱力感、 CK上昇等に注意し、 異常が認められた場合には適切な処置を行う。
好中球減少症、 白血球減少症 : 定期的に血液検査を実施するなど十分に観察する。
RMP【重要な特定されたリスク】
メキニスト®RMP : 医薬品リスク管理計画書
- 心臓障害
- 眼障害
- 肝機能障害
- 横紋筋融解症
- 発熱
- 好中球減少症・白血球減少症
監修医からのコメント
日本医科大学 武蔵小杉病院 腫瘍内科 勝俣 範之先生
低異形度漿液性腺癌は、 上皮性卵巣癌の約5%を占める希少疾患である。 増殖が比較的緩徐である一方、 化学療法の奏効率は高くなく、 長らく標準治療が確立していなかった。 加えて、 これまで再発した低異形度漿液性腺癌に承認された薬剤は存在しなかった。 こうした背景から、 MAPK経路異常を特徴とする本腫瘍に対して、 MEK阻害薬トラメチニブが期待されていた。
米国GOGを主体とする医師主導治験として実施されたGOG281/LOGS試験では、 前述のとおりトラメチニブ群でPFSの有意な延長が示され、 OSも良好な傾向を示した。 この結果を受け、 米国NCCNガイドラインにも記載された。
日本では、 日本臨床腫瘍学会、 日本婦人科腫瘍学会、 卵巣がん体験者の会スマイリーの3者からの要望を受け、 公知申請 (日本での治験成績がなくても、 海外の有力なエビデンスに基づいて承認する制度) により、 2026年2月19日に承認された。 要望書提出から3年を経ての承認であり、 低異形度漿液性腺癌の患者にとって朗報といえる。
出典
1) ノバルティスファーマ株式会社. メキニスト®電子添文情報 2026年2月改訂 第8版.
2) 準備中
3) Lancet. 2022;399(10324):541-553.
4) 公知申請への該当性に係る報告書. トラメチニブ ジメチルスルホキシド付加物. 再発した低異型度漿液性卵巣癌または腹膜癌
最終更新 : 2026年3月13日
執筆 : HOKUTO編集部 がん専門・指導薬剤師
監修医師 : 日本医科大学 武蔵小杉病院 腫瘍内科 勝俣 範之
Trametinib
2026年2月19日、 「がん化学療法後に増悪した低異型度漿液性卵巣癌」 について承認を取得した。
本コンテンツは特定の治療法を推奨するものではありません。 個々の患者の病態や、 実際の薬剤情報やガイドラインを確認の上、 利用者の判断と責任でご利用ください。
薬剤情報
メキニスト® (トラメチニブ)
添付文書¹⁾ / 適正使用情報 (準備中)²⁾
ノバルティスファーマ株式会社の外部サイトへ遷移します
投与スケジュール
【1コース】連日内服投与
【催吐性】最小度
【FN発症】未報告*
*GOG 281/LOGS試験ではFN発生率は未報告

通常、 成人にはトラメチニブとして2mgを1日1回、 食事の1時間以上前又は食後2時間以降に経口投与する。 なお、 患者の状態により適宜減量する。
Key Data|臨床試験結果
📊 GOG 281/LOGS試験
Lancet. 2022;399(10324):541-553.
再発・進行の低異型度漿液性卵巣癌患者を対象に、 トラメチニブの有効性と安全性を標準治療 (医師選択治療*) と比較した国際共同第II/III相無作為化比較試験である。 トラメチニブ群130例、 標準治療群130例に1 : 1で割り付け、 主要評価項目はPFSに設定された。
*パクリタキセル、 PEG化リポソームドキソルビシン (PLD)、 トポテカン、 レトロゾール、 タモキシフェンのいずれか
【有効性】トラメチニブ群 (vs 標準治療群)
- PFS中央値 13.0ヵ月 (vs 7.2ヵ月)
- HR 0.48 (95%CI 0.36–0.64、 p<0.0001)
- ORR 26% (vs 6%)
- OS中央値 37.6ヵ月 (vs 29.2ヵ月)
- HR 0.76 (95%CI 0.51–1.12、 p=0.156)
【安全性】主な有害事象 : 全Grade (Grade≧3)
- 倦怠感 73% (8%)
- 末梢性浮腫 49% (0%)
- 腹痛 45% (6%)
- 便秘 42% (2%)
- 下痢 73% (10%)
- 口腔粘膜炎 35% (2%)
- 悪心 61% (9%)
- 嘔吐 46% (7%)
- 皮膚乾燥 44% (1%)
- 痤瘡様皮疹 63% (6%)
- 斑状丘疹状皮疹 42% (7%)
- 貧血 52% (13%)
- 白血球数減少 22% (1%)
- ALP増加 25% (2%)
- AST増加 37% (1%)
- ALT増加 22% (2%)
- クレアチニン増加 20% (1%)
- 食欲不振 27% (2%)
- 高血糖 25% (0%)
- 低カリウム血症 20% (4%)
- 低マグネシウム血症 32% (1%)
- 低アルブミン血症 34% (3%)
- 頭痛 21% (0%)
- 末梢性感覚ニューロパチー 28% (1%)
- 高血圧 39% (12%)
- 呼吸困難 35% (3%)
- 尿路感染 23% (7%)
各プロトコル
適格基準
GOG 281/LOGS試験³⁾の主な適格基準
- 18歳以上
- 組織学的に確認された低異型度漿液性卵巣癌
- 少なくとも1つの白金併用化学療法歴あり
- ECOG PS 0–1
- 好中球数≧1500/μL
- 血小板数≧10万/μL
- Hb≧9.0g/dL
- 肝機能 : T-Bil≦1.5×ULN、 AST/ALT≦2.5×ULN
用量レベル

0.5mg錠と2mg錠の生物学的同等性は示されていないため、 2mgを投与する際は0.5mg錠を使用しないこと¹⁾。
腎障害患者に対する用量調整
腎機能障害 (eGFR 15~89mL/min/1.73m²) は、 トラメチニブの曝露量に臨床的に重要な影響を及ぼさない。
U.S. Food and Drug Administration. MEKINIST® (trametinib) tablets: Full Prescribing Information. Revised June 2022. Reference ID: 5002951.
有害事象発現時の減量・休薬・中止基準
電子添文情報¹⁾ :

GOG 281/LOGS試験のプロトコル³⁾ :

GOG 281/LOGS試験³⁾のプロトコルを基に編集部作成
レジメンの特徴と注意点
本レジメンの位置付け
遺伝子変異型によらず、 がん化学療法後に増悪した低異型度漿液性卵巣癌 (腹膜癌、 卵管癌及び卵巣癌) に対して有効性が期待できる⁴⁾。
他の抗悪性腫瘍剤との併用及び手術の補助療法における本剤の有効性及び安全性は確立していない。
作用機序の特徴
トラメチニブは、 MEK1及びMEK2の活性化並びにキナーゼ活性を阻害し、 A375P F11細胞株を皮下移植したマウスの腫瘍組織において、 MEKの基質であるERKのリン酸化を阻害した。
レジメン適用時の注意事項
心臓障害 : LVEF低下、 心不全等があらわれることがあるため、 本剤投与開始前及び投与中は、 心機能検査 (心エコー等) を定期的に実施する。
眼障害 : 網膜静脈閉塞症、 網膜剥離等の眼障害があらわれることがあるため、 視力異常等の異常が認められた場合には速やかに眼科医による検査を受けるよう患者に指導する。
肝機能障害 : 肝機能障害があらわれることがあるため、 定期的に肝機能検査を行う。
発熱 : 高頻度に認められ、 重度の脱水や低血圧を伴う例も報告されている。 患者の状態を十分に観察し、 異常が認められた場合は減量、 休薬、 解熱剤投与など適切に対応し、 感染症等の有無を評価する。 解熱剤で効果不十分な場合は、 経口ステロイド剤の投与を検討する。
横紋筋融解症 : 筋肉痛、 脱力感、 CK上昇等に注意し、 異常が認められた場合には適切な処置を行う。
好中球減少症、 白血球減少症 : 定期的に血液検査を実施するなど十分に観察する。
RMP【重要な特定されたリスク】
メキニスト®RMP : 医薬品リスク管理計画書
- 心臓障害
- 眼障害
- 肝機能障害
- 横紋筋融解症
- 発熱
- 好中球減少症・白血球減少症
監修医からのコメント
日本医科大学 武蔵小杉病院 腫瘍内科 勝俣 範之先生
低異形度漿液性腺癌は、 上皮性卵巣癌の約5%を占める希少疾患である。 増殖が比較的緩徐である一方、 化学療法の奏効率は高くなく、 長らく標準治療が確立していなかった。 加えて、 これまで再発した低異形度漿液性腺癌に承認された薬剤は存在しなかった。 こうした背景から、 MAPK経路異常を特徴とする本腫瘍に対して、 MEK阻害薬トラメチニブが期待されていた。
米国GOGを主体とする医師主導治験として実施されたGOG281/LOGS試験では、 前述のとおりトラメチニブ群でPFSの有意な延長が示され、 OSも良好な傾向を示した。 この結果を受け、 米国NCCNガイドラインにも記載された。
日本では、 日本臨床腫瘍学会、 日本婦人科腫瘍学会、 卵巣がん体験者の会スマイリーの3者からの要望を受け、 公知申請 (日本での治験成績がなくても、 海外の有力なエビデンスに基づいて承認する制度) により、 2026年2月19日に承認された。 要望書提出から3年を経ての承認であり、 低異形度漿液性腺癌の患者にとって朗報といえる。
出典
1) ノバルティスファーマ株式会社. メキニスト®電子添文情報 2026年2月改訂 第8版.
2) 準備中
3) Lancet. 2022;399(10324):541-553.
4) 公知申請への該当性に係る報告書. トラメチニブ ジメチルスルホキシド付加物. 再発した低異型度漿液性卵巣癌または腹膜癌
最終更新 : 2026年3月13日
執筆 : HOKUTO編集部 がん専門・指導薬剤師
監修医師 : 日本医科大学 武蔵小杉病院 腫瘍内科 勝俣 範之
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
がん薬物療法における治療計画をまとめたものです。
主要論文や適正使用ガイドをもとにした用量調整プロトコール、 有害事象対応をご紹介します。
なお、 本ツールは医師向けの教育用資料であり、 実臨床での使用は想定しておりません。 最新の添付文書やガイドラインを必ずご確認下さい。
また、 一般の方への情報提供ではないことを予めご了承ください。