2022年5月26日に新たに 「PD-L1陽性の非小細胞肺癌における術後補助療法」 に適応が追加された
本コンテンツは特定の治療法を推奨するものではありません。 個々の患者の病態や、 実際の薬剤情報やガイドラインを確認の上、 利用者の判断と責任でご利用ください。
薬剤情報
テセントリク®点滴静注 (アテゾリズマブ)
*中外製薬株式会社の外部サイトへ遷移します
投与スケジュール
【1コース】21日
【催吐性】 軽度催吐性
【FN発症】低リスク

1回1200mgを60分かけて3週間ごとに点滴静注し、 初回投与の忍容性が良好であれば2回目以降は投与時間を30分まで短縮できる。
※PD-L1陽性NSCLCにおける術後補助療法の場合、 投与期間は12ヵ月間まで
2025年9月19日、 1回1680mgを4週間ごとに点滴静注する用法・用量が追加承認された。
👨⚕️q4wの追加承認により、 単剤療法の利便性が向上した。 一方で、 併用療法においてはq4w投与が未承認である点に留意が必要である。
和歌山県立医科大学附属病院 赤松弘朗先生
KeyData|臨床試験結果
📊IMpower010試験³⁾
プラチナ製剤を含む術後補助療法後の術後病理病期IB (腫瘍径≥4cm) ~ⅢA (UICC/AJCC病期分類第7版) のNSCLC患者1005例 (日本人117例を含む) を対象に、 アテゾリズマブの有効性及び安全性を支持療法 (BSC) と比較した第Ⅲ相試験。 うち、 PD-L1陽性 (腫瘍細胞におけるPD-L1発現率 (TC) が1%以上) のⅡ又はⅢA期集団、 アテゾリズマブ投与群 (248例) とBSC群 (228例) との比較結果
【有効性】PD-L1陽性 (TC≧1%) のⅡ-ⅢA期
- mDFS : 未達 [主要評価項目]
BSC群 35.3ヵ月、 HR 0.66 (95%CI 0.50-0.88)、 P=0.0039
- mOS : 未達
【安全性】
本剤が投与された495例 (日本人56例を含む) において335例 (67.7%) に副作用が認められた。 主な副作用 (5%以上) は、 甲状腺機能低下症53例 (10.7%)、 そう痒症43例 (8.7%)、 発疹40例 (8.1%)、 AST増加37例 (7.5%)、 ALT増加36例 (7.3%)、 甲状腺機能亢進症29例 (5.9%)、 発熱27例 (5.5%)、 関節痛26例 (5.3%) 等であった。
アテゾリズマブ関連のGrade3、 4 の有害事象は495人の患者中53人 (11%) で発生し、 Grade5の有害事象は4人の患者 (1%) で発生した
各プロトコル
投与開始基準
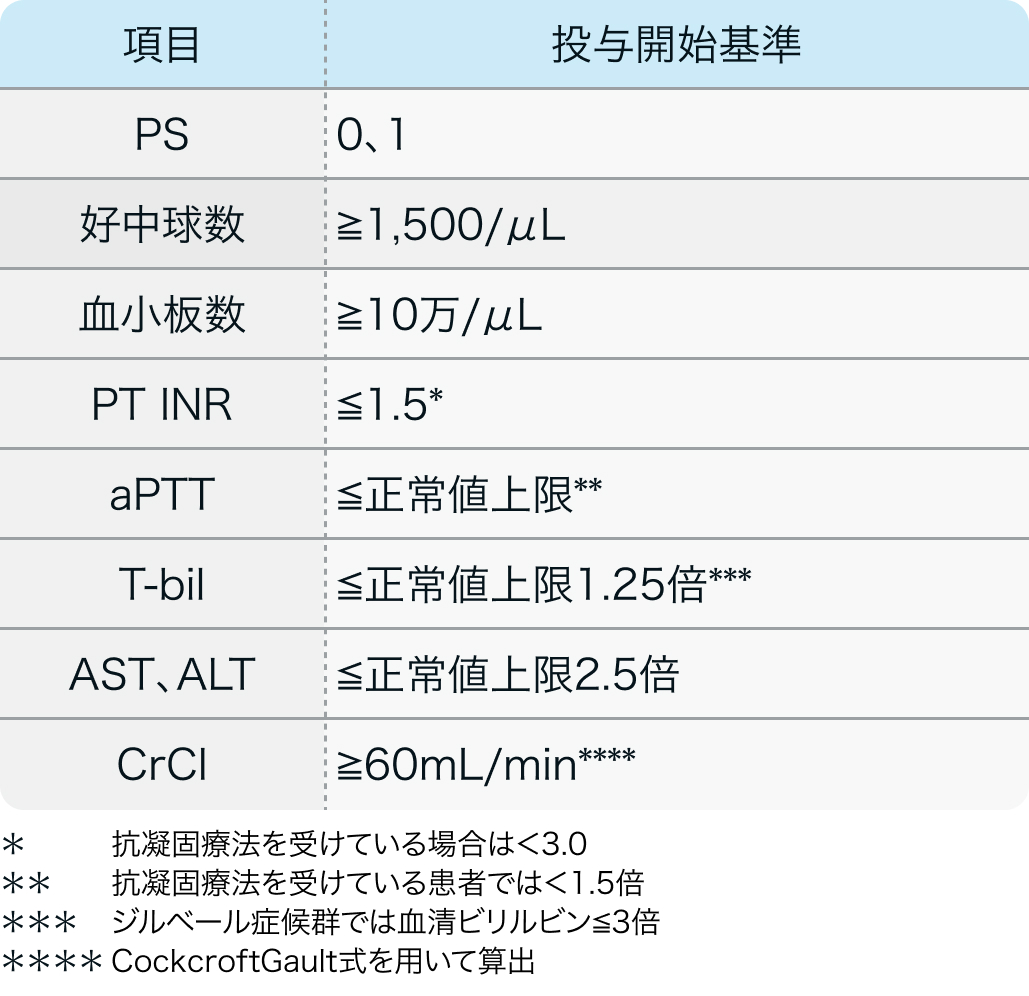
テセントリク®︎適正使用ガイド²⁾より引用
休薬・中止基準
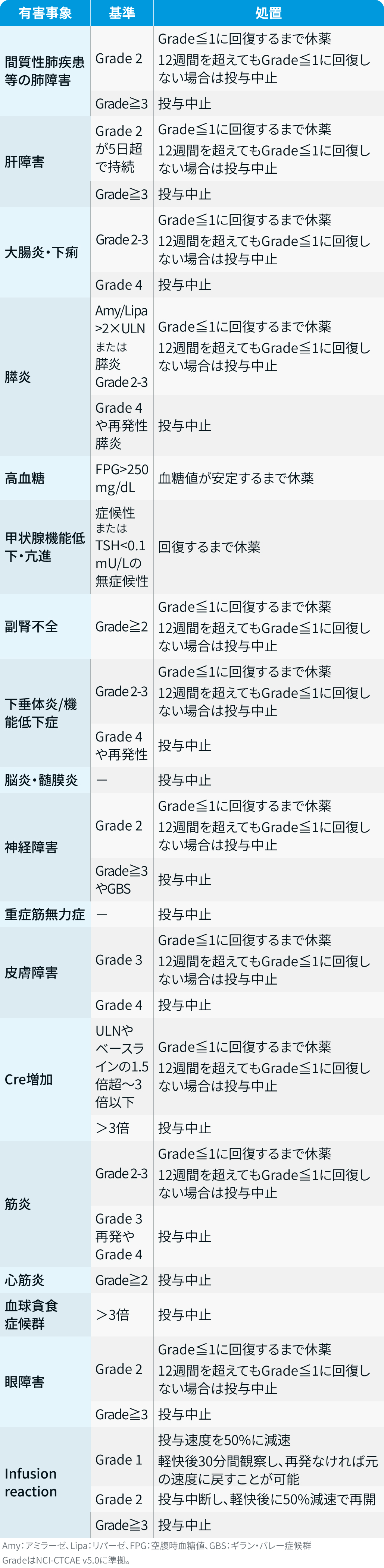
テセントリク®︎適正使用ガイド²⁾より引用
レジメンの特徴と注意点
PD-L1>1%で承認されているが、 PD-L1 1-49%ではOS延長は示されていない³⁾。
肺癌診療ガイドライン2025の推奨⁴⁾
術後病理病期ⅡA–ⅢB期 (第9版)* 完全切除例では、 腫瘍細胞のPD-L1発現50%以上例に対して、 シスプラチン併用化学療法後のアテゾリズマブ単剤療法追加が弱く推奨されている (2C)。 一方、 PD-L1発現1%以上50%未満例では、 勧めるだけの明確な根拠はない。
*ⅡAはN1のみ/ⅢBはN3を除く
出典
1) 中外製薬株式会社. テセントリク®電子添文 (2025年12月改訂 第12版)
2) 中外製薬株式会社. テセントリク®適正使用ガイド (2025年12月改訂)
4) 日本肺癌学会. 肺癌診療ガイドライン-胸膜中皮腫・ 胸腺腫瘍含む-2025年版
最終更新日 : 2026年1月7日
監修医師 : HOKUTO編集部監修医師
Atezolizumab
2022年5月26日に新たに 「PD-L1陽性の非小細胞肺癌における術後補助療法」 に適応が追加された
本コンテンツは特定の治療法を推奨するものではありません。 個々の患者の病態や、 実際の薬剤情報やガイドラインを確認の上、 利用者の判断と責任でご利用ください。
薬剤情報
テセントリク®点滴静注 (アテゾリズマブ)
*中外製薬株式会社の外部サイトへ遷移します
投与スケジュール
【1コース】21日
【催吐性】 軽度催吐性
【FN発症】低リスク

1回1200mgを60分かけて3週間ごとに点滴静注し、 初回投与の忍容性が良好であれば2回目以降は投与時間を30分まで短縮できる。
※PD-L1陽性NSCLCにおける術後補助療法の場合、 投与期間は12ヵ月間まで
2025年9月19日、 1回1680mgを4週間ごとに点滴静注する用法・用量が追加承認された。
👨⚕️q4wの追加承認により、 単剤療法の利便性が向上した。 一方で、 併用療法においてはq4w投与が未承認である点に留意が必要である。
和歌山県立医科大学附属病院 赤松弘朗先生
KeyData|臨床試験結果
📊IMpower010試験³⁾
プラチナ製剤を含む術後補助療法後の術後病理病期IB (腫瘍径≥4cm) ~ⅢA (UICC/AJCC病期分類第7版) のNSCLC患者1005例 (日本人117例を含む) を対象に、 アテゾリズマブの有効性及び安全性を支持療法 (BSC) と比較した第Ⅲ相試験。 うち、 PD-L1陽性 (腫瘍細胞におけるPD-L1発現率 (TC) が1%以上) のⅡ又はⅢA期集団、 アテゾリズマブ投与群 (248例) とBSC群 (228例) との比較結果
【有効性】PD-L1陽性 (TC≧1%) のⅡ-ⅢA期
- mDFS : 未達 [主要評価項目]
BSC群 35.3ヵ月、 HR 0.66 (95%CI 0.50-0.88)、 P=0.0039
- mOS : 未達
【安全性】
本剤が投与された495例 (日本人56例を含む) において335例 (67.7%) に副作用が認められた。 主な副作用 (5%以上) は、 甲状腺機能低下症53例 (10.7%)、 そう痒症43例 (8.7%)、 発疹40例 (8.1%)、 AST増加37例 (7.5%)、 ALT増加36例 (7.3%)、 甲状腺機能亢進症29例 (5.9%)、 発熱27例 (5.5%)、 関節痛26例 (5.3%) 等であった。
アテゾリズマブ関連のGrade3、 4 の有害事象は495人の患者中53人 (11%) で発生し、 Grade5の有害事象は4人の患者 (1%) で発生した
各プロトコル
投与開始基準

テセントリク®︎適正使用ガイド²⁾より引用
休薬・中止基準

テセントリク®︎適正使用ガイド²⁾より引用
レジメンの特徴と注意点
PD-L1>1%で承認されているが、 PD-L1 1-49%ではOS延長は示されていない³⁾。
肺癌診療ガイドライン2025の推奨⁴⁾
術後病理病期ⅡA–ⅢB期 (第9版)* 完全切除例では、 腫瘍細胞のPD-L1発現50%以上例に対して、 シスプラチン併用化学療法後のアテゾリズマブ単剤療法追加が弱く推奨されている (2C)。 一方、 PD-L1発現1%以上50%未満例では、 勧めるだけの明確な根拠はない。
*ⅡAはN1のみ/ⅢBはN3を除く
出典
1) 中外製薬株式会社. テセントリク®電子添文 (2025年12月改訂 第12版)
2) 中外製薬株式会社. テセントリク®適正使用ガイド (2025年12月改訂)
4) 日本肺癌学会. 肺癌診療ガイドライン-胸膜中皮腫・ 胸腺腫瘍含む-2025年版
最終更新日 : 2026年1月7日
監修医師 : HOKUTO編集部監修医師
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
がん薬物療法における治療計画をまとめたものです。
主要論文や適正使用ガイドをもとにした用量調整プロトコール、 有害事象対応をご紹介します。
なお、 本ツールは医師向けの教育用資料であり、 実臨床での使用は想定しておりません。 最新の添付文書やガイドラインを必ずご確認下さい。
また、 一般の方への情報提供ではないことを予めご了承ください。