本コンテンツは特定の治療法を推奨するものではございません. 個々の患者の病態や、 実際の薬剤情報やガイドラインを確認の上、 利用者の判断と責任でご利用ください.
薬剤情報
イレッサ®錠 (ゲフィチニブ)
*アストラゼネカ株式会社の外部サイトへ遷移します
投与スケジュール
【1コース】21日
【催吐性】 中等度催吐性*
【FN発症】低リスク
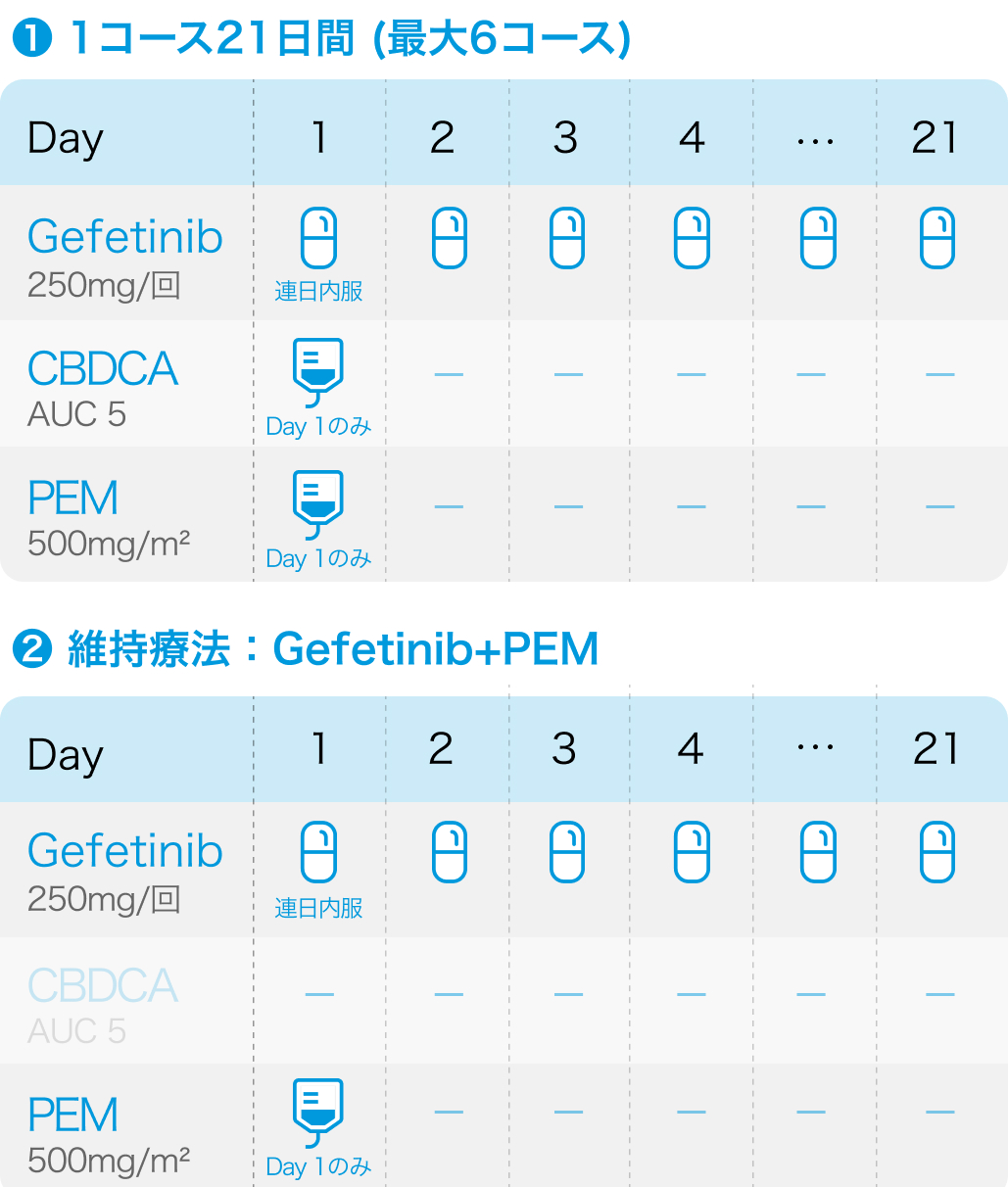
1コース21日間で最大6コース施行、 その後は維持療法としてGefetinib+PEM継続
*制吐薬適正使用GL2023 第3版においてCBDCA+PEMが中等度催吐性レジメンであるが、 CBDCA併用レジメンは、 CBDCA AUC≧4の場合、 5-HT3受容体拮抗薬、 デキサメタゾン、 NK1受容体拮抗薬を併用する。
KeyData|臨床試験結果
📊 NEJ009試験 [国内第Ⅲ相試験]¹⁾²⁾
J Clin Oncol. 2020 Jan 10;38(2):115-23.
J Clin Oncol. 2022 Nov 1;40(31):3587-92.
PS 0~1で、 EGFR変異陽性 IIIB~IV期、 または術後再発で根治的放射線治療及び外科的治療の適応がないNSCLC患者 (Stage IIIA を含む)を対象に、 ゲフィチニブ+CBDCA+PEM併用療法とゲフィチニブ単剤療法を比較有効性
【有効性】本レジメン群
- ORR : 84%
- mPFS : 20.9ヵ月
- mOS : 49.0ヵ月
各プロトコル
開始基準例 (NEJ009試験¹⁾²⁾)
EGFR遺伝子変異陽性 (エクソン19欠失、 L858R、L861Q、G719A、G719C、 G719S) で、 IIIB期/Ⅳ期または術後再発の非扁平上皮非小細胞肺癌 (PS0~1、化学療法未治療、20~75歳)
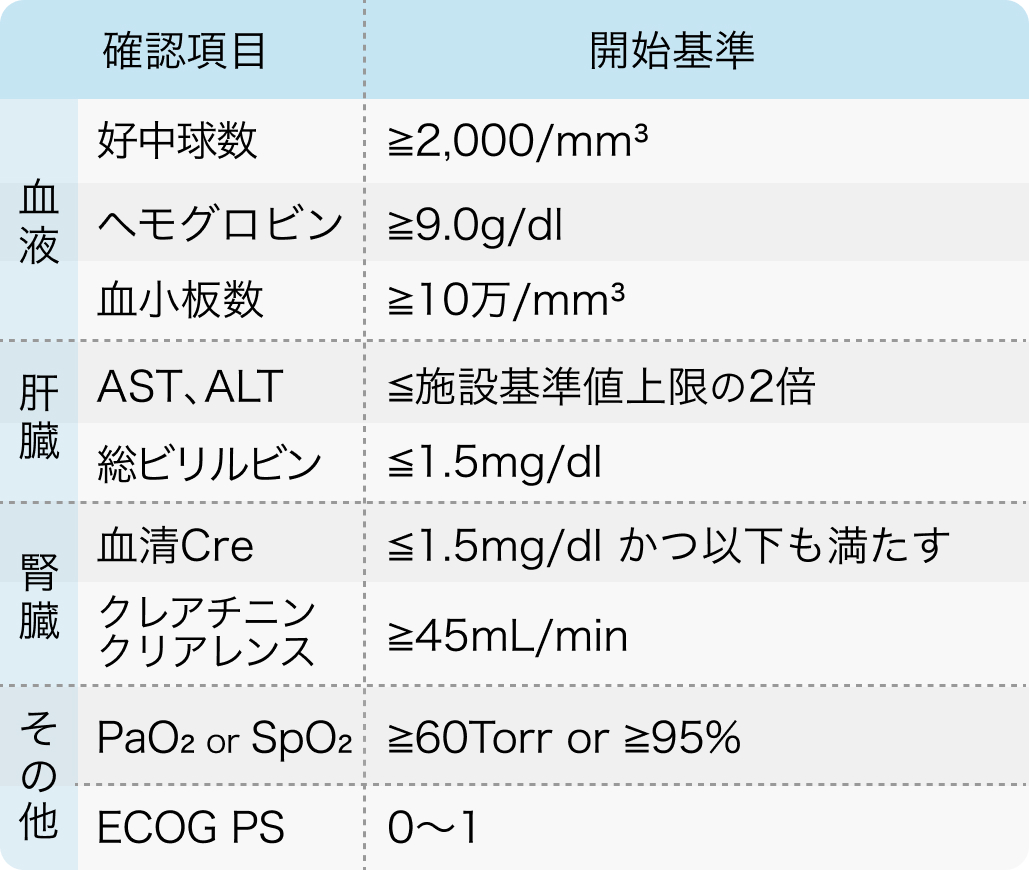
J Clin Oncol. 2020 Jan 10;38(2):115-123. より作図
その他の詳細な開始・除外基準はプロトコールを参照すること
減量時の投与量 (NEJ009試験¹⁾²⁾)
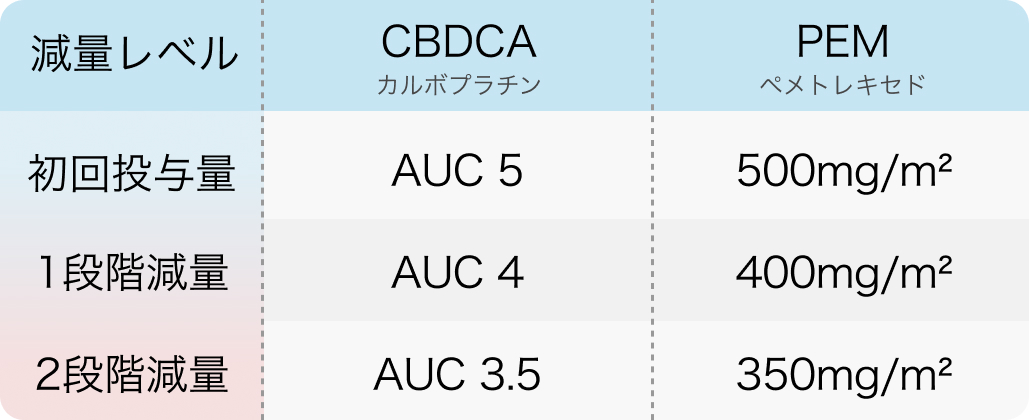
J Clin Oncol. 2020 Jan 10;38(2):115-123. より作図
継続基準例 (NEJ009試験¹⁾²⁾)

J Clin Oncol. 2020 Jan 10;38(2):115-123. より作図
AUC投与量計算
🔢カルボプラチンAUC投与量計算より算出可
レジメンの特徴と注意点
遺伝子パネル検査・コンパニオン診断
日本肺癌学会の各種手引きやHOKUTO編集部のまとめコンテンツを参照ください。
肺癌遺伝子パネル検査・コンパニオン診断薬一覧ページへ遷移
PEMとNSAIDs併用は控える
PEMの血中濃度が上昇し、 有害事象が増強する可能性があるため、 半減期の長いNSAIDsにおいてはPEM投与5日前から投与2日後の8日間はできるかぎり併用を控えた方が良い。 また、 半減期の短いNSAIDsにおいては軽度から中等度の腎機能障害の場合、 PEM投与2日前から投与2日後の5日間はできるかぎり併用を控えた方が良い。
アリムタ®適正使用ガイド (2022年6月作成)より引用
PEM投与時の推奨前投薬
投与1週間以上前に、 Vit.B12 1000mg 筋注、 葉酸1g日 投与。 それぞれVit.B12は9週ごと、 葉酸は毎日継続する。
肺癌診療ガイドライン2025の推奨³⁾
2025年版からは推奨記載が削除された。
出典
3) 日本肺癌学会. 肺癌診療ガイドライン-胸膜中皮腫・ 胸腺腫瘍含む-2025年版
4) アストラゼネカ株式会社. 「イレッサ®︎総合製品情報概要」 2024年12月作成 [最終閲覧 2025/10/5]
*アストラゼネカ株式会社の外部サイトへ遷移します
最終更新日 : 2025年11月13日
HOKUTO編集部医師監修
Gefitinib+CBDCA+PEM
本コンテンツは特定の治療法を推奨するものではございません. 個々の患者の病態や、 実際の薬剤情報やガイドラインを確認の上、 利用者の判断と責任でご利用ください.
薬剤情報
イレッサ®錠 (ゲフィチニブ)
*アストラゼネカ株式会社の外部サイトへ遷移します
投与スケジュール
【1コース】21日
【催吐性】 中等度催吐性*
【FN発症】低リスク

1コース21日間で最大6コース施行、 その後は維持療法としてGefetinib+PEM継続
*制吐薬適正使用GL2023 第3版においてCBDCA+PEMが中等度催吐性レジメンであるが、 CBDCA併用レジメンは、 CBDCA AUC≧4の場合、 5-HT3受容体拮抗薬、 デキサメタゾン、 NK1受容体拮抗薬を併用する。
KeyData|臨床試験結果
📊 NEJ009試験 [国内第Ⅲ相試験]¹⁾²⁾
J Clin Oncol. 2020 Jan 10;38(2):115-23.
J Clin Oncol. 2022 Nov 1;40(31):3587-92.
PS 0~1で、 EGFR変異陽性 IIIB~IV期、 または術後再発で根治的放射線治療及び外科的治療の適応がないNSCLC患者 (Stage IIIA を含む)を対象に、 ゲフィチニブ+CBDCA+PEM併用療法とゲフィチニブ単剤療法を比較有効性
【有効性】本レジメン群
- ORR : 84%
- mPFS : 20.9ヵ月
- mOS : 49.0ヵ月
各プロトコル
開始基準例 (NEJ009試験¹⁾²⁾)
EGFR遺伝子変異陽性 (エクソン19欠失、 L858R、L861Q、G719A、G719C、 G719S) で、 IIIB期/Ⅳ期または術後再発の非扁平上皮非小細胞肺癌 (PS0~1、化学療法未治療、20~75歳)

J Clin Oncol. 2020 Jan 10;38(2):115-123. より作図
その他の詳細な開始・除外基準はプロトコールを参照すること
減量時の投与量 (NEJ009試験¹⁾²⁾)

J Clin Oncol. 2020 Jan 10;38(2):115-123. より作図
継続基準例 (NEJ009試験¹⁾²⁾)

J Clin Oncol. 2020 Jan 10;38(2):115-123. より作図
AUC投与量計算
🔢カルボプラチンAUC投与量計算より算出可
レジメンの特徴と注意点
遺伝子パネル検査・コンパニオン診断
日本肺癌学会の各種手引きやHOKUTO編集部のまとめコンテンツを参照ください。
肺癌遺伝子パネル検査・コンパニオン診断薬一覧ページへ遷移
PEMとNSAIDs併用は控える
PEMの血中濃度が上昇し、 有害事象が増強する可能性があるため、 半減期の長いNSAIDsにおいてはPEM投与5日前から投与2日後の8日間はできるかぎり併用を控えた方が良い。 また、 半減期の短いNSAIDsにおいては軽度から中等度の腎機能障害の場合、 PEM投与2日前から投与2日後の5日間はできるかぎり併用を控えた方が良い。
アリムタ®適正使用ガイド (2022年6月作成)より引用
PEM投与時の推奨前投薬
投与1週間以上前に、 Vit.B12 1000mg 筋注、 葉酸1g日 投与。 それぞれVit.B12は9週ごと、 葉酸は毎日継続する。
肺癌診療ガイドライン2025の推奨³⁾
2025年版からは推奨記載が削除された。
出典
3) 日本肺癌学会. 肺癌診療ガイドライン-胸膜中皮腫・ 胸腺腫瘍含む-2025年版
4) アストラゼネカ株式会社. 「イレッサ®︎総合製品情報概要」 2024年12月作成 [最終閲覧 2025/10/5]
*アストラゼネカ株式会社の外部サイトへ遷移します
最終更新日 : 2025年11月13日
HOKUTO編集部医師監修
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
がん薬物療法における治療計画をまとめたものです。
主要論文や適正使用ガイドをもとにした用量調整プロトコール、 有害事象対応をご紹介します。
なお、 本ツールは医師向けの教育用資料であり、 実臨床での使用は想定しておりません。 最新の添付文書やガイドラインを必ずご確認下さい。
また、 一般の方への情報提供ではないことを予めご了承ください。