治療スケジュール
概要
監修医師
Pirtobrutinib:ピルトブルチニブ(ジャイパーカ®)
| 投与量 | コース | 投与日 |
|---|---|---|
| 1日1回 200mg | 1~ | Day 1~ |
| 連日経口 | - | - |
前投薬
| なし. |
その他
| 他のBTK阻害剤に抵抗性又は不耐容の再発又は難治性のマントル細胞リンパ腫に保険適用. |
| 200mgを1日1回経口投与. |
| 患者の状態により適宜減量. |
2024年8月21日、 「他のBTK阻害剤に抵抗性又は不耐容の再発又は難治性のマントル細胞リンパ腫」 に対して薬価収載 (100mg1錠 1万9465.80円 / 1日薬価 3万8931.60円)
本コンテンツは特定の治療法を推奨するものではございません. 個々の患者の病態や、 実際の薬剤情報やガイドラインを確認の上、 利用者の判断と責任でご利用ください.
薬剤情報
ジャイパーカ® (ピルトブルチニブ)
*日本新薬株式会社の外部サイトへ遷移します
主な有害事象
BRUIN-18001試験¹⁾より引用 (全体集団).
骨髄抑制
- 貧血 (13.9%、 ≧Grade3 7.7%)
- 好中球数減少 (12.3%、 ≧Grade3 10.6%)
- 血小板数減少 (10.2%、 ≧Grade3 4.8%)
主な有害事象
- 疲労 (26.3%、 ≧Grade3 1.7%)
- 下痢 (22.1%、 ≧Grade3 0.8%)
- 挫傷 (19.0%、 ≧Grade3 0.0%)
- 悪心 (14.9%、 ≧Grade3 0.1%)
- 咳嗽 (14.8%、 ≧Grade3 0.0%)
- 呼吸困難 (13.7%、 ≧Grade3 1.0%)
- 関節痛 (13.0%、 ≧Grade3 0.4%)
- 便秘 (12.8%、 ≧Grade3 0.3%)
- 背部痛 (12.6%、 ≧Grade3 0.6%)
- 頭痛 (12.1%、 ≧Grade3 0.3%)
- 発熱 (12.0%、 ≧Grade3 0.8%)
- 末梢性浮腫 (11.4%、 ≧Grade3 0.1%)
- 腹痛 (11.0%、 ≧Grade3 0.8%)
その他重大な有害事象
インタビューフォームより引用.
- 感染症 (3.0%)
- 消化管出血 (0.6%)
- 頭蓋内出血 (頻度不明)
特徴と注意点
適応
- 他のBTK阻害剤に抵抗性又は不耐容の再発又は難治性のマントル細胞リンパ腫.
特徴と注意点
- 他の抗悪性腫瘍剤との併用について、 有効性及び安全性は確立していない.
- 外科的処置に伴って大量出血が生じる可能性があることから、 投与中に手術や侵襲的手技を実施する患者に対しては、 術前術後の3~5日程度は投与中断を考慮する.
- 骨髄抑制が出現することがあるので、 定期的に血液検査を行う.
- 主にCYP3A4によって代謝され、 CYP2C8、 CYP2C19、 CYP3A、 P-gp及びBCRPの阻害作用を示すため、 関連する相互作用に注意.
作用機序
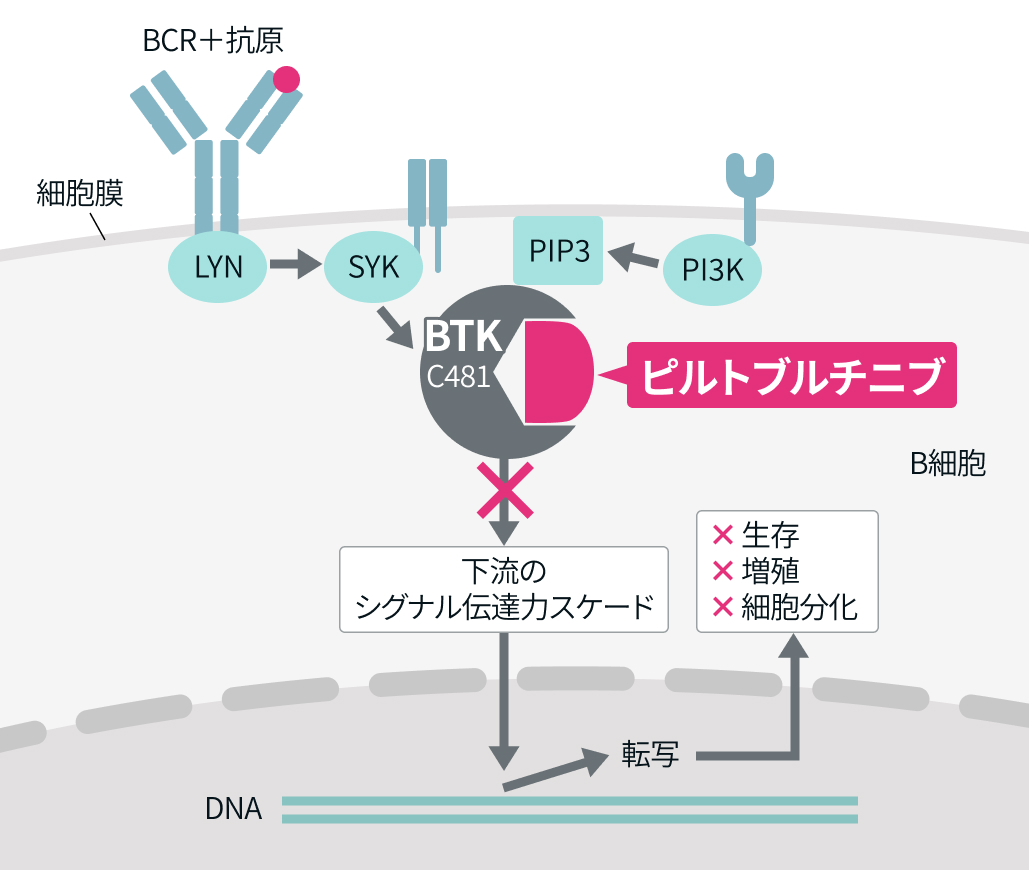
日本新薬株式会社の医療関係者向けサイトの図をもとにHOKUTO編集部で作成
- ブルトン型チロシンキナーゼ (BTK) に対し可逆的な非共有結合型の阻害作用を有する.
- 共有結合型BTK阻害剤はBTKのATP結合ポケット内にあるC481に共有結合するが、 ピルトブルチニブはATP結合ポケット内でC481とは異なる複数のアミノ酸に非共有結合することでBTKのキナーゼ活性を阻害し、 B細胞性腫瘍の増殖を抑制する. 従ってC481S変異が生じた場合でもBTK経路を阻害する.
用法・用量
- 200mgを1日1回経口投与.
- 患者状態により適宜減量.
用量調節
- Grade3*以上の有害事象が発現した場合、 ベースライン又はGrade1以下に回復するまで休薬.
- 再開時の用量は以下の用量調節の目安を参照.
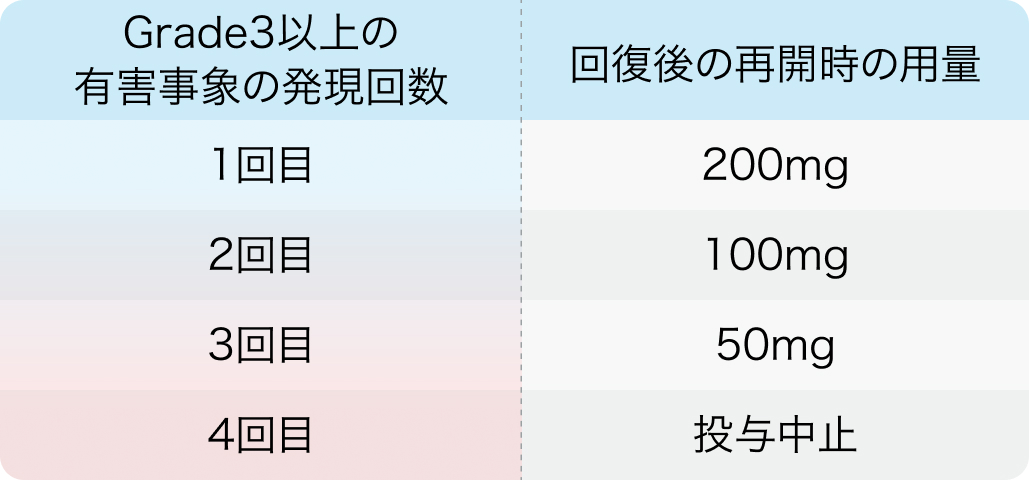
*GradeはNCI-CTCAEver.5.0に準じる.
関連する臨床試験の結果
BRUIN-18001試験¹⁾
- 試験デザイン : 非盲検、 多施設共同、 第I/II相、 国際共同臨床試験.
<第Ⅰ相パート>
- 目的 : 前治療歴のあるマントル細胞リンパ腫 (MCL) を含むB細胞性非ホジキンリンパ腫 (B-NHL) 患者におけるピルトブルチニブ経口投与時の最大耐量 (MTD) 及び第Ⅱ相推奨用量 (RP2D) を決定する.
※日本人のみ : 海外で決定されたピルトブルチニブのRP2Dの安全性プロファイル及び忍容性を、 同じ基準を用いて日本人患者で確認.
- 対象 : MCLを含むB-NHL患者.
- 投与方法 (用法漸増及び用量拡大パート) : ピルトブルチニブ 25、 50、 100、 150、 200、 250、 300mgを1日1回経口投与. 1サイクルは28日間.
- 主要評価項目 : MTD、 RP2D
- 副次評価項目 : 安全性 (有害事象及び臨床検査)、 薬物動態等
- 目的 : 各コホート (全7コホート) において、 B-NHL患者におけるピルトブルチニブの有効性及び安全性を検討.
- 対象 : MCLを含むB-NHL患者
- 投与方法 : ピルトブルチニブ200mgを1日1回経口投与. 1サイクルは28日間.
- 主要評価項目 : ORR
- 副次評価項目 : BOR、 DOR、 PFS、 OS、 安全性
ORR : 奏効率 (CR+PR)、 BOR : 最良総合効果、 DOR : 奏効期間、 PFS : 無増悪生存期間、 OS : 全生存期間
CR : 完全奏効、 PR : 部分奏効、 SD : 安定、 PD : 病勢進行、 NE : 評価不能
- MCLを含むB-NHL患者を以下コホートに登録
- コホート1 : BTK阻害剤を含む前治療歴がある非芽球様細胞性MCL患者.
- コホート2 : BTK阻害剤を含む2剤以上の前治療歴がある慢性リンパ性白血病/小リンパ球性リンパ腫 (CLL/SLL) 患者.
- コホート3 : 前治療歴がないCLL/SLL患者.
- コホート4 : BTK阻害剤による治療歴のない前治療歴があるCLL/SLL患者.
- コホート5 : BTK阻害剤を含む前治療歴がある原発性マクログロブリン血症 (WM) 患者.
- コホート6 : BTK阻害剤を含む前治療歴がある辺縁帯リンパ腫 (MZL) 患者.
- コホート7 : 分類不能な患者 (コホート1~6に分類されないCLL/SLL又はリヒター形質転換、 形質転換を伴う低悪性度NHL、 芽球様細胞性MCL、 もしくは中枢神経系 (CNS) 浸潤又は原発性CNSリンパ腫の既往がある患者を含む)
結果
MCL集団の有効性 (第Ⅰ/Ⅱ相パート) ※海外データ
- ORR : 56.9% (95%CI 44.0-69.2).
- BORの内訳 : CR 20.0%、 PR 36.9%、 SD 13.8%、 PD 15.4%、 NE 13.8%.
- DOR : 未到達 (95%CI 8.31ヵ月-未到達). ※18ヵ月時点の奏効持続割合は57.6%.
- PFS中央値 : 6.90ヵ月 (95%CI 3.98ヵ月-未到達). ※18ヵ月時点のPFSは36.9%.
- OS中央値 : 未到達 (95%CI 34ヵ月-未到達). ※18ヵ月時点のOSは58.9%.
日本人MCL集団の有効性 (第Ⅱ相パート) ※計8例
- ORR達成は4例 (ORRの95%CI : 15.7~84.3).
- BORの内訳 : CR 2例、 PR 2例、 SD 3例、 PD 1例、 NE 0例.
芽球様細胞性MCLの有効性 (第Ⅰ/Ⅱ相パート) ※計15例
- ORR : 46.7% (95%CI 21.3-73.4).
- BORの内訳 : CR 1例 (6.7%)、 PR 6例 (40.0%)、 SD 3例 (20.0%)、 PD 4例 (26.7%)、 NE 1例 (6.7%).
参考文献
1) Lancet.2021Mar6;397 (10277):892-901.
最終更新 : 2025年12月9日
執筆担当 : 小澤病院薬剤部 長剛広
監修医師 : 東海大学血液腫瘍内科 扇屋大輔
Pirtobrutinib
ピルトブルチニブ (ジャイパーカ®)
悪性リンパ腫 > マントル細胞リンパ腫
2025年12月09日更新
Pirtobrutinib:ピルトブルチニブ(ジャイパーカ®)
| 投与量 | コース | 投与日 |
|---|---|---|
| 1日1回 200mg | 1~ | Day 1~ |
| 連日経口 | - | - |
前投薬
| なし. |
その他
| 他のBTK阻害剤に抵抗性又は不耐容の再発又は難治性のマントル細胞リンパ腫に保険適用. |
| 200mgを1日1回経口投与. |
| 患者の状態により適宜減量. |
概要
2024年8月21日、 「他のBTK阻害剤に抵抗性又は不耐容の再発又は難治性のマントル細胞リンパ腫」 に対して薬価収載 (100mg1錠 1万9465.80円 / 1日薬価 3万8931.60円)
本コンテンツは特定の治療法を推奨するものではございません. 個々の患者の病態や、 実際の薬剤情報やガイドラインを確認の上、 利用者の判断と責任でご利用ください.
薬剤情報
ジャイパーカ® (ピルトブルチニブ)
*日本新薬株式会社の外部サイトへ遷移します
主な有害事象
BRUIN-18001試験¹⁾より引用 (全体集団).
骨髄抑制
- 貧血 (13.9%、 ≧Grade3 7.7%)
- 好中球数減少 (12.3%、 ≧Grade3 10.6%)
- 血小板数減少 (10.2%、 ≧Grade3 4.8%)
主な有害事象
- 疲労 (26.3%、 ≧Grade3 1.7%)
- 下痢 (22.1%、 ≧Grade3 0.8%)
- 挫傷 (19.0%、 ≧Grade3 0.0%)
- 悪心 (14.9%、 ≧Grade3 0.1%)
- 咳嗽 (14.8%、 ≧Grade3 0.0%)
- 呼吸困難 (13.7%、 ≧Grade3 1.0%)
- 関節痛 (13.0%、 ≧Grade3 0.4%)
- 便秘 (12.8%、 ≧Grade3 0.3%)
- 背部痛 (12.6%、 ≧Grade3 0.6%)
- 頭痛 (12.1%、 ≧Grade3 0.3%)
- 発熱 (12.0%、 ≧Grade3 0.8%)
- 末梢性浮腫 (11.4%、 ≧Grade3 0.1%)
- 腹痛 (11.0%、 ≧Grade3 0.8%)
その他重大な有害事象
インタビューフォームより引用.
- 感染症 (3.0%)
- 消化管出血 (0.6%)
- 頭蓋内出血 (頻度不明)
特徴と注意点
適応
- 他のBTK阻害剤に抵抗性又は不耐容の再発又は難治性のマントル細胞リンパ腫.
特徴と注意点
- 他の抗悪性腫瘍剤との併用について、 有効性及び安全性は確立していない.
- 外科的処置に伴って大量出血が生じる可能性があることから、 投与中に手術や侵襲的手技を実施する患者に対しては、 術前術後の3~5日程度は投与中断を考慮する.
- 骨髄抑制が出現することがあるので、 定期的に血液検査を行う.
- 主にCYP3A4によって代謝され、 CYP2C8、 CYP2C19、 CYP3A、 P-gp及びBCRPの阻害作用を示すため、 関連する相互作用に注意.
作用機序

日本新薬株式会社の医療関係者向けサイトの図をもとにHOKUTO編集部で作成
- ブルトン型チロシンキナーゼ (BTK) に対し可逆的な非共有結合型の阻害作用を有する.
- 共有結合型BTK阻害剤はBTKのATP結合ポケット内にあるC481に共有結合するが、 ピルトブルチニブはATP結合ポケット内でC481とは異なる複数のアミノ酸に非共有結合することでBTKのキナーゼ活性を阻害し、 B細胞性腫瘍の増殖を抑制する. 従ってC481S変異が生じた場合でもBTK経路を阻害する.
用法・用量

- 200mgを1日1回経口投与.
- 患者状態により適宜減量.
用量調節
- Grade3*以上の有害事象が発現した場合、 ベースライン又はGrade1以下に回復するまで休薬.
- 再開時の用量は以下の用量調節の目安を参照.

*GradeはNCI-CTCAEver.5.0に準じる.
関連する臨床試験の結果
BRUIN-18001試験¹⁾
- 試験デザイン : 非盲検、 多施設共同、 第I/II相、 国際共同臨床試験.
<第Ⅰ相パート>
- 目的 : 前治療歴のあるマントル細胞リンパ腫 (MCL) を含むB細胞性非ホジキンリンパ腫 (B-NHL) 患者におけるピルトブルチニブ経口投与時の最大耐量 (MTD) 及び第Ⅱ相推奨用量 (RP2D) を決定する.
※日本人のみ : 海外で決定されたピルトブルチニブのRP2Dの安全性プロファイル及び忍容性を、 同じ基準を用いて日本人患者で確認.
- 対象 : MCLを含むB-NHL患者.
- 投与方法 (用法漸増及び用量拡大パート) : ピルトブルチニブ 25、 50、 100、 150、 200、 250、 300mgを1日1回経口投与. 1サイクルは28日間.
- 主要評価項目 : MTD、 RP2D
- 副次評価項目 : 安全性 (有害事象及び臨床検査)、 薬物動態等
- 目的 : 各コホート (全7コホート) において、 B-NHL患者におけるピルトブルチニブの有効性及び安全性を検討.
- 対象 : MCLを含むB-NHL患者
- 投与方法 : ピルトブルチニブ200mgを1日1回経口投与. 1サイクルは28日間.
- 主要評価項目 : ORR
- 副次評価項目 : BOR、 DOR、 PFS、 OS、 安全性
ORR : 奏効率 (CR+PR)、 BOR : 最良総合効果、 DOR : 奏効期間、 PFS : 無増悪生存期間、 OS : 全生存期間
CR : 完全奏効、 PR : 部分奏効、 SD : 安定、 PD : 病勢進行、 NE : 評価不能
- MCLを含むB-NHL患者を以下コホートに登録
- コホート1 : BTK阻害剤を含む前治療歴がある非芽球様細胞性MCL患者.
- コホート2 : BTK阻害剤を含む2剤以上の前治療歴がある慢性リンパ性白血病/小リンパ球性リンパ腫 (CLL/SLL) 患者.
- コホート3 : 前治療歴がないCLL/SLL患者.
- コホート4 : BTK阻害剤による治療歴のない前治療歴があるCLL/SLL患者.
- コホート5 : BTK阻害剤を含む前治療歴がある原発性マクログロブリン血症 (WM) 患者.
- コホート6 : BTK阻害剤を含む前治療歴がある辺縁帯リンパ腫 (MZL) 患者.
- コホート7 : 分類不能な患者 (コホート1~6に分類されないCLL/SLL又はリヒター形質転換、 形質転換を伴う低悪性度NHL、 芽球様細胞性MCL、 もしくは中枢神経系 (CNS) 浸潤又は原発性CNSリンパ腫の既往がある患者を含む)
結果
MCL集団の有効性 (第Ⅰ/Ⅱ相パート) ※海外データ
- ORR : 56.9% (95%CI 44.0-69.2).
- BORの内訳 : CR 20.0%、 PR 36.9%、 SD 13.8%、 PD 15.4%、 NE 13.8%.
- DOR : 未到達 (95%CI 8.31ヵ月-未到達). ※18ヵ月時点の奏効持続割合は57.6%.
- PFS中央値 : 6.90ヵ月 (95%CI 3.98ヵ月-未到達). ※18ヵ月時点のPFSは36.9%.
- OS中央値 : 未到達 (95%CI 34ヵ月-未到達). ※18ヵ月時点のOSは58.9%.
日本人MCL集団の有効性 (第Ⅱ相パート) ※計8例
- ORR達成は4例 (ORRの95%CI : 15.7~84.3).
- BORの内訳 : CR 2例、 PR 2例、 SD 3例、 PD 1例、 NE 0例.
芽球様細胞性MCLの有効性 (第Ⅰ/Ⅱ相パート) ※計15例
- ORR : 46.7% (95%CI 21.3-73.4).
- BORの内訳 : CR 1例 (6.7%)、 PR 6例 (40.0%)、 SD 3例 (20.0%)、 PD 4例 (26.7%)、 NE 1例 (6.7%).
参考文献
1) Lancet.2021Mar6;397 (10277):892-901.
最終更新 : 2025年12月9日
執筆担当 : 小澤病院薬剤部 長剛広
監修医師 : 東海大学血液腫瘍内科 扇屋大輔
こちらの記事の監修医師
HOKUTO編集部
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
HOKUTO編集部
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
レジメン(血液)
がん薬物療法における治療計画をまとめたものです。
主要論文や適正使用ガイドをもとにした用量調整プロトコール、 有害事象対応をご紹介します。
なお、 本ツールは医師向けの教育用資料であり、 実臨床での使用は想定しておりません。 最新の添付文書やガイドラインを必ずご確認下さい。
また、 一般の方への情報提供ではないことを予めご了承ください。
