治療スケジュール
概要
監修医師
BV:ブレンツキシマブベドチン(アドセトリス®)
| 投与量 | コース | 投与日 |
|---|---|---|
| 1.8mg/kg 点滴静注 | 1~ | Day 1 |
CPA:シクロホスファミド(エンドキサン®)
| 投与量 | コース | 投与日 |
|---|---|---|
| 750mg/m² 点滴静注 | 1~ | Day 1 |
DXR:ドキソルビシン(アドリアシン®)
| 投与量 | コース | 投与日 |
|---|---|---|
| 50mg/m² 点滴静注 | 1~ | Day 1 |
PSL:プレドニゾロン(プレドニン®)
| 投与量 | コース | 投与日 |
|---|---|---|
| 100mg/body 経口or点滴静注 | 1~ | Day 1~5 |
前投薬
| 5-HT3受容体拮抗薬 |
| アプレピタント (悪心/嘔吐の程度、 各施設の方針による) |
その他
| 1コースは21日間. 6~8コース行う. |
| DXRは静注も可能. 各施設の運用方針による. |
| PSLは100mg/bodyが基本. 65歳以上では40mg/m²へ減量. |
| PSLは糖尿病など合併症を考慮して用量を決定. |
本コンテンツは特定の治療法を推奨するものではございません. 個々の患者の病態や、 実際の薬剤情報やガイドラインを確認の上、 利用者の判断と責任でご利用ください.
薬剤情報
*適正使用ガイドは「武田薬品工業株式会社」 の外部サイトへ遷移します.
主な有害事象
ECHELON-2試験¹⁾より引用
【骨髄抑制】
- 好中球減少 (≧Grade3 35%)
- 貧血 (≧Grade3 13%)
- 血小板減少症 (≧Grade3 6%)
- リンパ球減少 (≧Grade3 1%)
【主な有害事象】
- 感染症 (52%)
- 悪心 (46%)
- 末梢性感覚神経障害 (45%)
- 下痢 (38%)
- 便秘 (29%)
- 脱毛症 (26%)
- 発熱 (26%)
- 嘔吐 (26%)
- 疲労 (24%)
- 発熱性好中球減少症 (18%)
- 食欲減退 (17%)
- 呼吸困難 (14%)
- 頭痛 (14%)
- 浮動性めまい (13%)
- 咳嗽 (12%)
- 低カリウム血症 (12%)
- 口内炎 (12%)
- 無力症 (12%)
- 体重減少 (12%)
- 不眠症 (11%)
- 筋肉痛 (11%)
- 末梢性浮腫 (11%)
- 発疹 (10%)
【その他重要な有害事象】
- Infusion reaction (4%)
- 末梢性運動神経障害 (4%)
特徴と注意点
背景
- ALK陽性ALCLではCHOP療法が標準療法.
- PTCL-NOS、 AITL、 ALK陰性ALCLでは、 CHOP (or CHOP類似) 療法が行われているが標準療法としては確立していない.
- 未治療のCD30陽性の末梢性T細胞リンパ腫ではA-CHP療法を考慮する.
ブレンツキシマブベドチン (BV)
- BVは抗CD30モノクローナル抗体に強力な微小管阻害薬MMAEを結合した抗体薬物複合体.
- 免疫組織化学法等によりCD30陽性を確認した上で使用.
- ブレオマイシンの投与中でないことを確認.
- Infusion reaction予防のための前投薬は必須ではないが、 重度症状出現に備えた対応を.
- 重度腎障害 (CrCL<30mL/min) や肝障害では減量を考慮.
- MMAEの代謝は主にCYP3A4が関与. CYP3A4阻害剤との併用によるMMAE血中濃度増加の可能性あり.
- 避妊を指導 (男女ともに投与中及び投与終了後6ヵ月間). 乳汁中への移行も不明.
- その他BV投与に伴う重大な副作用として、 末梢神経障害、 感染症、 進行性多巣性白質脳症 (PML)、 骨髄抑制、 Infusion reaction、 腫瘍崩壊症候群、 皮膚粘膜眼症候群 (Stevens-Johnson症候群)、 急性膵炎、 劇症肝炎、 肝機能障害、 肺障害に注意する.
- 調整後の希釈液を30分以上かけて点滴静注. 急速投与は行わない.
末梢神経障害発現時の用量調節の目安
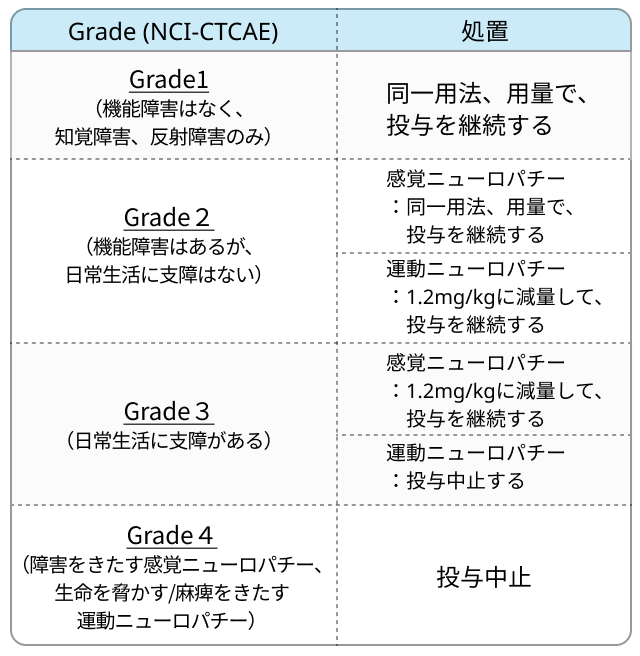
その他の副作用と対策
- 腫瘍量が多い場合、 腫瘍崩壊症候群が出現するため、 十分な予防が必要.
- 好中球数<1,000/µlとなった時、 ベースライン又は1,000/µl以上に回復するまで休薬.
- HBV再活性化リスクを考慮し、 適切なスクリーニング検査とモニタリングを行う.
- ニューモシスチス、 カンジダ、 ヘルペス含め日和見感染に注意.
関連する臨床試験の結果
ECHELON-2試験 (SGN35-014試験)¹⁾
概要
- 国際共同ランダム化第3相試験 (二重盲検、 ダブルダミー).
- 対象:CD30陽性の未治療PTCL患者 452例 (1:1 割り付け)
- 治療:BV (1.8mg/m2)併用CHP (A-CHP) 6-8コース vs CHOP 6-8コース
- プライマリーエンドポイント:PFS
- セカンダリーエンドポイント:OS
PFS:無増悪生存期間 OS:全生存期間
結果
- PFS中央値:A-CHP群 48.2ヵ月 vs CHOP群 20.8ヵ月 (HR 0.71、 95%CI 0.54-0.93、 p=0.0110)
- A-CHP群の死亡リスク減少率:34% (HR 0.66、 95%CI 0.46-0.95、 p=0.0244).
- 75パーセンタイルOS中央値:A-CHP群 未到達 vs CHOP群 17.5ヵ月.
- 主な有害事象 (BV+CHP群 vs CHOP群で記載):発熱性好中球減少症 (18% vs 15%)、 末梢神経障害 (52% vs 55%)、 致死的な有害事象 (3% vs 4%).
結論
- CD30陽性PTCLに対するA-CHP療法は、 CHOP療法と比較してPFS、 OSを改善した.
- 有害事象も管理可能であった.
- サブグループ解析においてALK陽性及びALK陰性ともにALCLでは有意にPFSを改善したが、 AITLにおいてはCHOPの方が良い傾向にあった. PTCL-NOSにおいてはHR 0.75であるが有意差は認めなかった.
ECHELON-2試験のフォローアップ解析²⁾
- 観察期間中央値:47.6ヵ月
- 5年PFS:A-CHP群 51.4% vs CHOP群 43.0% (HR 0.70、 95%CI 0.53-0.91).
- 5年OS:A-CHP群 70.1% vs CHOP群 61.0% (HR 0.72、 95%CI 0.53-0.99).
- 末梢神経障害改善率:A-CHP群 72% vs CHOP群 78%.
- 再発もしくはBVによる継続治療が行われた際の奏効率:A-CHP群 59% vs CHOP群 50%.
参考文献
最終更新:2022年2月3日
監修医師:東海大学血液腫瘍内科 扇屋大輔
A-CHP
BV併用CHP
悪性リンパ腫 > 末梢性T細胞リンパ腫
2023年05月27日更新
BV:ブレンツキシマブベドチン(アドセトリス®)
| 投与量 | コース | 投与日 |
|---|---|---|
| 1.8mg/kg 点滴静注 | 1~ | Day 1 |
CPA:シクロホスファミド(エンドキサン®)
| 投与量 | コース | 投与日 |
|---|---|---|
| 750mg/m² 点滴静注 | 1~ | Day 1 |
DXR:ドキソルビシン(アドリアシン®)
| 投与量 | コース | 投与日 |
|---|---|---|
| 50mg/m² 点滴静注 | 1~ | Day 1 |
PSL:プレドニゾロン(プレドニン®)
| 投与量 | コース | 投与日 |
|---|---|---|
| 100mg/body 経口or点滴静注 | 1~ | Day 1~5 |
前投薬
| 5-HT3受容体拮抗薬 |
| アプレピタント (悪心/嘔吐の程度、 各施設の方針による) |
その他
| 1コースは21日間. 6~8コース行う. |
| DXRは静注も可能. 各施設の運用方針による. |
| PSLは100mg/bodyが基本. 65歳以上では40mg/m²へ減量. |
| PSLは糖尿病など合併症を考慮して用量を決定. |
概要
本コンテンツは特定の治療法を推奨するものではございません. 個々の患者の病態や、 実際の薬剤情報やガイドラインを確認の上、 利用者の判断と責任でご利用ください.
薬剤情報
*適正使用ガイドは「武田薬品工業株式会社」 の外部サイトへ遷移します.
主な有害事象
ECHELON-2試験¹⁾より引用
【骨髄抑制】
- 好中球減少 (≧Grade3 35%)
- 貧血 (≧Grade3 13%)
- 血小板減少症 (≧Grade3 6%)
- リンパ球減少 (≧Grade3 1%)
【主な有害事象】
- 感染症 (52%)
- 悪心 (46%)
- 末梢性感覚神経障害 (45%)
- 下痢 (38%)
- 便秘 (29%)
- 脱毛症 (26%)
- 発熱 (26%)
- 嘔吐 (26%)
- 疲労 (24%)
- 発熱性好中球減少症 (18%)
- 食欲減退 (17%)
- 呼吸困難 (14%)
- 頭痛 (14%)
- 浮動性めまい (13%)
- 咳嗽 (12%)
- 低カリウム血症 (12%)
- 口内炎 (12%)
- 無力症 (12%)
- 体重減少 (12%)
- 不眠症 (11%)
- 筋肉痛 (11%)
- 末梢性浮腫 (11%)
- 発疹 (10%)
【その他重要な有害事象】
- Infusion reaction (4%)
- 末梢性運動神経障害 (4%)
特徴と注意点
背景
- ALK陽性ALCLではCHOP療法が標準療法.
- PTCL-NOS、 AITL、 ALK陰性ALCLでは、 CHOP (or CHOP類似) 療法が行われているが標準療法としては確立していない.
- 未治療のCD30陽性の末梢性T細胞リンパ腫ではA-CHP療法を考慮する.
ブレンツキシマブベドチン (BV)
- BVは抗CD30モノクローナル抗体に強力な微小管阻害薬MMAEを結合した抗体薬物複合体.
- 免疫組織化学法等によりCD30陽性を確認した上で使用.
- ブレオマイシンの投与中でないことを確認.
- Infusion reaction予防のための前投薬は必須ではないが、 重度症状出現に備えた対応を.
- 重度腎障害 (CrCL<30mL/min) や肝障害では減量を考慮.
- MMAEの代謝は主にCYP3A4が関与. CYP3A4阻害剤との併用によるMMAE血中濃度増加の可能性あり.
- 避妊を指導 (男女ともに投与中及び投与終了後6ヵ月間). 乳汁中への移行も不明.
- その他BV投与に伴う重大な副作用として、 末梢神経障害、 感染症、 進行性多巣性白質脳症 (PML)、 骨髄抑制、 Infusion reaction、 腫瘍崩壊症候群、 皮膚粘膜眼症候群 (Stevens-Johnson症候群)、 急性膵炎、 劇症肝炎、 肝機能障害、 肺障害に注意する.
- 調整後の希釈液を30分以上かけて点滴静注. 急速投与は行わない.
末梢神経障害発現時の用量調節の目安

その他の副作用と対策
- 腫瘍量が多い場合、 腫瘍崩壊症候群が出現するため、 十分な予防が必要.
- 好中球数<1,000/µlとなった時、 ベースライン又は1,000/µl以上に回復するまで休薬.
- HBV再活性化リスクを考慮し、 適切なスクリーニング検査とモニタリングを行う.
- ニューモシスチス、 カンジダ、 ヘルペス含め日和見感染に注意.
関連する臨床試験の結果
ECHELON-2試験 (SGN35-014試験)¹⁾
概要
- 国際共同ランダム化第3相試験 (二重盲検、 ダブルダミー).
- 対象:CD30陽性の未治療PTCL患者 452例 (1:1 割り付け)
- 治療:BV (1.8mg/m2)併用CHP (A-CHP) 6-8コース vs CHOP 6-8コース
- プライマリーエンドポイント:PFS
- セカンダリーエンドポイント:OS
PFS:無増悪生存期間 OS:全生存期間
結果
- PFS中央値:A-CHP群 48.2ヵ月 vs CHOP群 20.8ヵ月 (HR 0.71、 95%CI 0.54-0.93、 p=0.0110)
- A-CHP群の死亡リスク減少率:34% (HR 0.66、 95%CI 0.46-0.95、 p=0.0244).
- 75パーセンタイルOS中央値:A-CHP群 未到達 vs CHOP群 17.5ヵ月.
- 主な有害事象 (BV+CHP群 vs CHOP群で記載):発熱性好中球減少症 (18% vs 15%)、 末梢神経障害 (52% vs 55%)、 致死的な有害事象 (3% vs 4%).
結論
- CD30陽性PTCLに対するA-CHP療法は、 CHOP療法と比較してPFS、 OSを改善した.
- 有害事象も管理可能であった.
- サブグループ解析においてALK陽性及びALK陰性ともにALCLでは有意にPFSを改善したが、 AITLにおいてはCHOPの方が良い傾向にあった. PTCL-NOSにおいてはHR 0.75であるが有意差は認めなかった.
ECHELON-2試験のフォローアップ解析²⁾
- 観察期間中央値:47.6ヵ月
- 5年PFS:A-CHP群 51.4% vs CHOP群 43.0% (HR 0.70、 95%CI 0.53-0.91).
- 5年OS:A-CHP群 70.1% vs CHOP群 61.0% (HR 0.72、 95%CI 0.53-0.99).
- 末梢神経障害改善率:A-CHP群 72% vs CHOP群 78%.
- 再発もしくはBVによる継続治療が行われた際の奏効率:A-CHP群 59% vs CHOP群 50%.
参考文献
最終更新:2022年2月3日
監修医師:東海大学血液腫瘍内科 扇屋大輔
こちらの記事の監修医師
HOKUTO編集部
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
HOKUTO編集部
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
レジメン(血液)
がん薬物療法における治療計画をまとめたものです。
主要論文や適正使用ガイドをもとにした用量調整プロトコール、 有害事象対応をご紹介します。
なお、 本ツールは医師向けの教育用資料であり、 実臨床での使用は想定しておりません。 最新の添付文書やガイドラインを必ずご確認下さい。
また、 一般の方への情報提供ではないことを予めご了承ください。