「内分泌療法後に増悪したESR1遺伝子変異を有するホルモン受容体陽性かつHER2陰性の手術不能又は再発乳癌」 を対象として、 2025年12月22日に正式承認された。
本コンテンツは特定の治療法を推奨するものではありません。 個々の患者の病態や、 実際の薬剤情報やガイドラインを確認の上、 利用者の判断と責任でご利用ください。
薬剤情報
イムルリオ®錠 (イムルネストラント)
投与スケジュール
【1コース】 28日間
【催吐性】不明
【FN発症】 低リスク*
*EMBER-3試験のFN発症率0.3%を基に編集部が評価
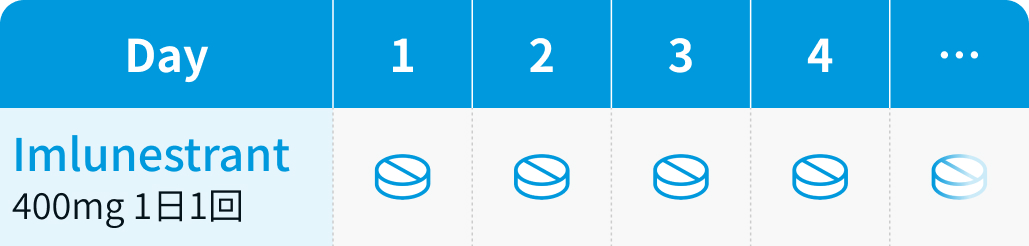
1日1回400mgを空腹時 (食前2時間以上、 または食後1時間以上) に経口投与
閉経前乳癌および男性には、 LH-RHアゴニスト投与下で使用
Key Data|臨床試験結果
📊 EMBER-3試験
N Engl J Med. 2025;392(12):1189-1202.
アロマターゼ阻害剤を含む内分泌療法歴のあるER陽性かつHER2陰性の手術不能又は再発乳癌患者を対象とした第III相無作為化比較試験。 イムルネストラント群331例、 対照群 (フルベストラント又はエキセメスタン) 330例、 イムルネストラント+アベマシクリブ併用群213例に1:1:1に割り付け、 主要評価項目はESR1遺伝子変異陽性集団、 全体集団および併用群のPFSとされた。
【有効性】イムルネストラント群 (vs 対照群)
ESR1変異あり :
- PFS中央値 5.5ヵ月 (vs 3.8ヵ月)
- 制限付き平均生存期間 (19.4ヵ月時点) 7.9ヵ月 (vs 5.4ヵ月)
- 差2.6ヵ月 (95%CI 1.2–3.9、 p<0.001)
治療群間でのイベント発生率が時間経過を通じて一定の比率を保たないことが示されたことを理由に代替指標として制限付き平均生存期間 (RMST) 解析が実施
- ORR 14.3% (vs 7.7%)
- CBR* 46.4% (vs 36.4%)
*Clinical benefit rate (CBR) : 全患者における完全奏効、 部分奏効または安定疾患が24週間以上持続した患者、 もしくは非完全奏効/疾患進行なしが24週間以上持続した患者の割合
全患者 :
- PFS中央値 5.6ヵ月 (vs 5.5ヵ月)
- HR 0.87 (95%CI 0.72–1.04、 p=0.12)
- ORR 12.2% (vs 8.4%)
- CBR 46.8% (vs 45.5%)
【安全性】主な有害事象 : 全Grade (Grade≧3)
- 倦怠感 22.6% (0.3%)
- 下痢 21.4% (0.3%)
- 悪心 17.1% (0.3%)
- 関節痛 14.1% (0.6%)
- AST増加 12.5% (0.9%)
- 背部痛 10.7% (0.6%)
- ALT増加 10.4% (0.3%)
- 貧血 10.1% (2.1%)
- 腹痛 8.9% (0.3%)
- 嘔吐 8.9% (0.6%)
- 食欲減退 8.0% (0.3%)
- 血小板減少症 5.5% (0.9%)
- 好中球減少症 5.2% (2.1%)
- 白血球減少症 5.2% (0.6%)
- 発疹 2.8% (0%)
各プロトコル
EMBER-3試験²⁾の主な適格基準
- 18歳以上
- ECOG PS 0–1
- 好中球≧1500/mm³
- 血小板≧10万/mm³
- ヘモグロビン≧9.0g/dL
- 腎機能 : Cre ≦1.5×ULNまたはCrCl≧50mL/分
- 肝機能 : T-Bil ≦1.5×ULN、 AST/ALT≦3×ULN
用量レベル
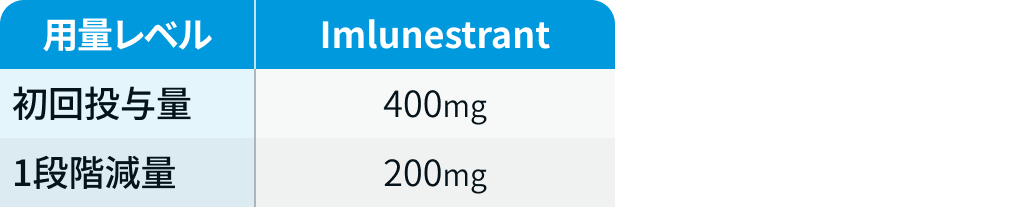
腎障害患者に対する用量調整
尿中排泄率は0.28%と低く腎クリアランスの寄与は小さいため、 腎障害時の用量調整は不要と考えられる²⁾。
肝障害患者に対する用量調整
Child-Pugh BまたはC : 200mgに減量¹⁾²⁾
HOKUTO計算ツールに遷移します
CYP3A4阻害剤との併用
強いCYP3A4阻害薬の併用 : 200mgに減量¹⁾²⁾
HOKUTOコンテンツに遷移します
有害事象発現時の減量・休薬・中止基準
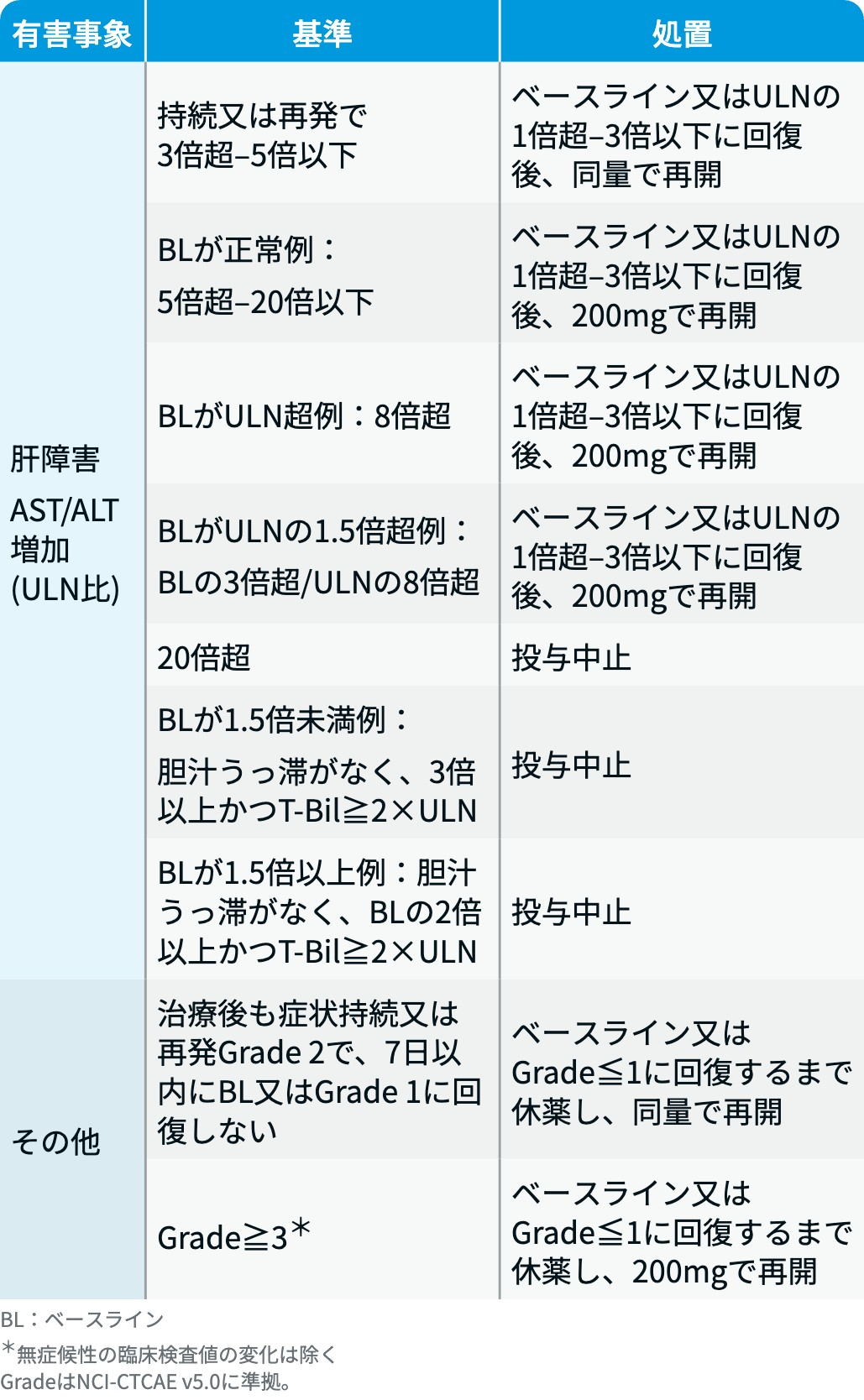
イムルリオ®電子添文情報¹⁾を基に編集部作成
EMBER-3試験³⁾では、 下記の対応も規定されていた。
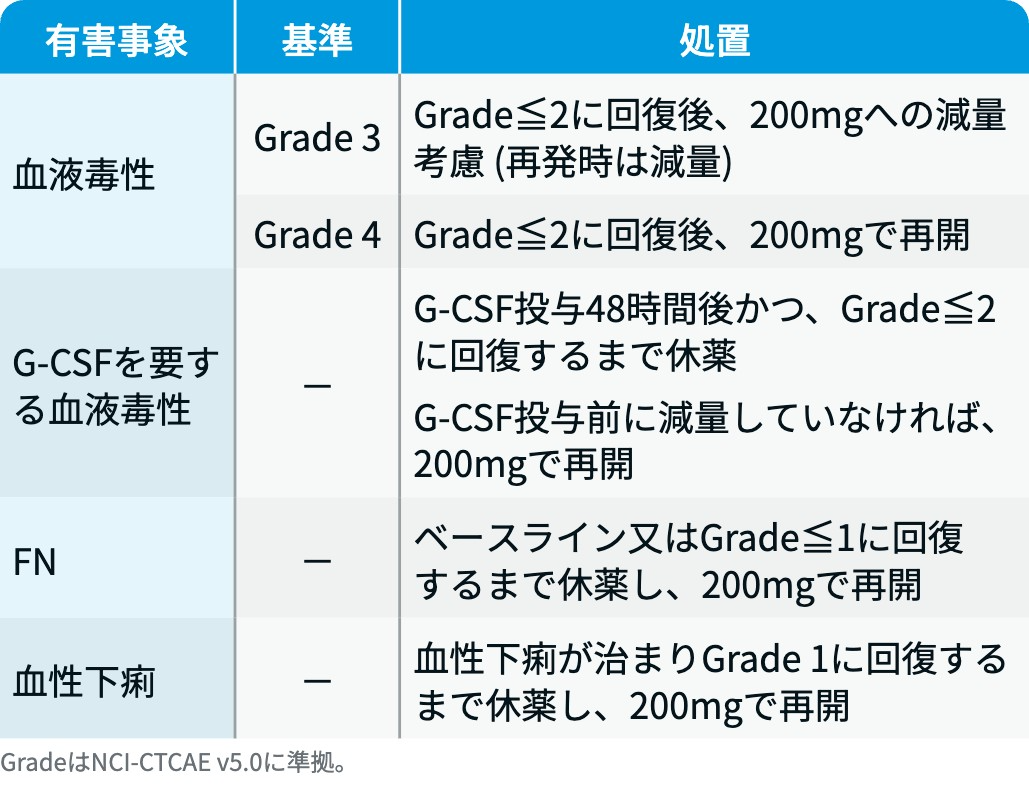
EMBER-3試験³⁾のプロトコルを基に編集部作成
レジメンの特徴と注意点
🧑⚕️世界的に開発競争が激化している経口SERDですが、 日本で初めて承認された経口SERDがこのイムルネストラントです。 CDK4/6阻害薬併用内分泌療法耐性後、 2次内分泌療法以降での標準的選択肢の一つとなります。 ESR1変異が確認されている必要があること、 また単剤での使用のみが承認されていることが留意点です。
がん研有明病院 乳腺内科副部長 尾崎由記範先生
本レジメンの位置付け
内分泌療法後に増悪したESR1遺伝子変異陽性のホルモン受容体陽性かつHER2陰性の手術不能又は再発乳癌を対象とする。 なお、 術前・術後薬物療法としての有効性及び安全性は確立していない。
作用機序の特徴
イムルネストラントは野生型及び変異型エストロゲン受容体α (ERα) に結合する選択的エストロゲン受容体分解剤 (SERD) であり、 ERαを分解してER依存性遺伝子の転写を阻害することで、 ESR1遺伝子変異陽性乳癌に対して腫瘍増殖抑制作用を示す。
レジメン適用時の注意事項
光線過敏症 : in vitroおよびin vivo光毒性試験で光毒性が示されており、 EMBER-3試験では治療期間中および最終投与後少なくとも5日間、 直射日光・日焼けサロンを避け、 曝露時は日焼け止め・遮光衣類・サングラスの使用が推奨されていた (光毒性は未報告)²⁾。
RMP【重要な特定されたリスク】
イムルリオ®医薬品リスク管理計画書 (RMP)
該当なし
コンパニオン診断薬の情報
本剤の適応判定に利用可能なコンパニオン診断薬は以下のとおり。
- Guardant360® CDx がん遺伝子パネル
出典
1) 日本イーライリリー株式会社. イムルリオ錠200mg 電子添文 2025年12月作成 第1版.
2) 日本イーライリリー株式会社. イムルリオ錠200mg 適正使用ガイド. 2025年12月作成.
3) N Engl J Med. 2025;392(12):1189-1202.
最終更新 : 2026年2月25日
執筆 : 京都桂病院薬剤科 塩飽英二
監修医師 : がん研究会有明病院 乳腺内科 尾崎由記範
Imlunestrant
「内分泌療法後に増悪したESR1遺伝子変異を有するホルモン受容体陽性かつHER2陰性の手術不能又は再発乳癌」 を対象として、 2025年12月22日に正式承認された。
本コンテンツは特定の治療法を推奨するものではありません。 個々の患者の病態や、 実際の薬剤情報やガイドラインを確認の上、 利用者の判断と責任でご利用ください。
薬剤情報
イムルリオ®錠 (イムルネストラント)
投与スケジュール
【1コース】 28日間
【催吐性】不明
【FN発症】 低リスク*
*EMBER-3試験のFN発症率0.3%を基に編集部が評価

1日1回400mgを空腹時 (食前2時間以上、 または食後1時間以上) に経口投与
閉経前乳癌および男性には、 LH-RHアゴニスト投与下で使用
Key Data|臨床試験結果
📊 EMBER-3試験
N Engl J Med. 2025;392(12):1189-1202.
アロマターゼ阻害剤を含む内分泌療法歴のあるER陽性かつHER2陰性の手術不能又は再発乳癌患者を対象とした第III相無作為化比較試験。 イムルネストラント群331例、 対照群 (フルベストラント又はエキセメスタン) 330例、 イムルネストラント+アベマシクリブ併用群213例に1:1:1に割り付け、 主要評価項目はESR1遺伝子変異陽性集団、 全体集団および併用群のPFSとされた。
【有効性】イムルネストラント群 (vs 対照群)
ESR1変異あり :
- PFS中央値 5.5ヵ月 (vs 3.8ヵ月)
- 制限付き平均生存期間 (19.4ヵ月時点) 7.9ヵ月 (vs 5.4ヵ月)
- 差2.6ヵ月 (95%CI 1.2–3.9、 p<0.001)
治療群間でのイベント発生率が時間経過を通じて一定の比率を保たないことが示されたことを理由に代替指標として制限付き平均生存期間 (RMST) 解析が実施
- ORR 14.3% (vs 7.7%)
- CBR* 46.4% (vs 36.4%)
*Clinical benefit rate (CBR) : 全患者における完全奏効、 部分奏効または安定疾患が24週間以上持続した患者、 もしくは非完全奏効/疾患進行なしが24週間以上持続した患者の割合
全患者 :
- PFS中央値 5.6ヵ月 (vs 5.5ヵ月)
- HR 0.87 (95%CI 0.72–1.04、 p=0.12)
- ORR 12.2% (vs 8.4%)
- CBR 46.8% (vs 45.5%)
【安全性】主な有害事象 : 全Grade (Grade≧3)
- 倦怠感 22.6% (0.3%)
- 下痢 21.4% (0.3%)
- 悪心 17.1% (0.3%)
- 関節痛 14.1% (0.6%)
- AST増加 12.5% (0.9%)
- 背部痛 10.7% (0.6%)
- ALT増加 10.4% (0.3%)
- 貧血 10.1% (2.1%)
- 腹痛 8.9% (0.3%)
- 嘔吐 8.9% (0.6%)
- 食欲減退 8.0% (0.3%)
- 血小板減少症 5.5% (0.9%)
- 好中球減少症 5.2% (2.1%)
- 白血球減少症 5.2% (0.6%)
- 発疹 2.8% (0%)
各プロトコル
EMBER-3試験²⁾の主な適格基準
- 18歳以上
- ECOG PS 0–1
- 好中球≧1500/mm³
- 血小板≧10万/mm³
- ヘモグロビン≧9.0g/dL
- 腎機能 : Cre ≦1.5×ULNまたはCrCl≧50mL/分
- 肝機能 : T-Bil ≦1.5×ULN、 AST/ALT≦3×ULN
用量レベル

腎障害患者に対する用量調整
尿中排泄率は0.28%と低く腎クリアランスの寄与は小さいため、 腎障害時の用量調整は不要と考えられる²⁾。
肝障害患者に対する用量調整
Child-Pugh BまたはC : 200mgに減量¹⁾²⁾
HOKUTO計算ツールに遷移します
CYP3A4阻害剤との併用
強いCYP3A4阻害薬の併用 : 200mgに減量¹⁾²⁾
HOKUTOコンテンツに遷移します
有害事象発現時の減量・休薬・中止基準

イムルリオ®電子添文情報¹⁾を基に編集部作成
EMBER-3試験³⁾では、 下記の対応も規定されていた。

EMBER-3試験³⁾のプロトコルを基に編集部作成
レジメンの特徴と注意点
🧑⚕️世界的に開発競争が激化している経口SERDですが、 日本で初めて承認された経口SERDがこのイムルネストラントです。 CDK4/6阻害薬併用内分泌療法耐性後、 2次内分泌療法以降での標準的選択肢の一つとなります。 ESR1変異が確認されている必要があること、 また単剤での使用のみが承認されていることが留意点です。
がん研有明病院 乳腺内科副部長 尾崎由記範先生
本レジメンの位置付け
内分泌療法後に増悪したESR1遺伝子変異陽性のホルモン受容体陽性かつHER2陰性の手術不能又は再発乳癌を対象とする。 なお、 術前・術後薬物療法としての有効性及び安全性は確立していない。
作用機序の特徴
イムルネストラントは野生型及び変異型エストロゲン受容体α (ERα) に結合する選択的エストロゲン受容体分解剤 (SERD) であり、 ERαを分解してER依存性遺伝子の転写を阻害することで、 ESR1遺伝子変異陽性乳癌に対して腫瘍増殖抑制作用を示す。
レジメン適用時の注意事項
光線過敏症 : in vitroおよびin vivo光毒性試験で光毒性が示されており、 EMBER-3試験では治療期間中および最終投与後少なくとも5日間、 直射日光・日焼けサロンを避け、 曝露時は日焼け止め・遮光衣類・サングラスの使用が推奨されていた (光毒性は未報告)²⁾。
RMP【重要な特定されたリスク】
イムルリオ®医薬品リスク管理計画書 (RMP)
該当なし
コンパニオン診断薬の情報
本剤の適応判定に利用可能なコンパニオン診断薬は以下のとおり。
- Guardant360® CDx がん遺伝子パネル
出典
1) 日本イーライリリー株式会社. イムルリオ錠200mg 電子添文 2025年12月作成 第1版.
2) 日本イーライリリー株式会社. イムルリオ錠200mg 適正使用ガイド. 2025年12月作成.
3) N Engl J Med. 2025;392(12):1189-1202.
最終更新 : 2026年2月25日
執筆 : 京都桂病院薬剤科 塩飽英二
監修医師 : がん研究会有明病院 乳腺内科 尾崎由記範
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
がん薬物療法における治療計画をまとめたものです。
主要論文や適正使用ガイドをもとにした用量調整プロトコール、 有害事象対応をご紹介します。
なお、 本ツールは医師向けの教育用資料であり、 実臨床での使用は想定しておりません。 最新の添付文書やガイドラインを必ずご確認下さい。
また、 一般の方への情報提供ではないことを予めご了承ください。