本コンテンツは特定の治療法を推奨するものではありません。 個々の患者の病態や、 実際の薬剤情報やガイドラインを確認の上、 利用者の判断と責任でご利用ください。
薬剤情報
ヒストン脱アセチル化酵素 (HDAC) 阻害薬 ボリノスタット
*大鵬薬品工業株式会社の外部サイトへ遷移します
用法・用量
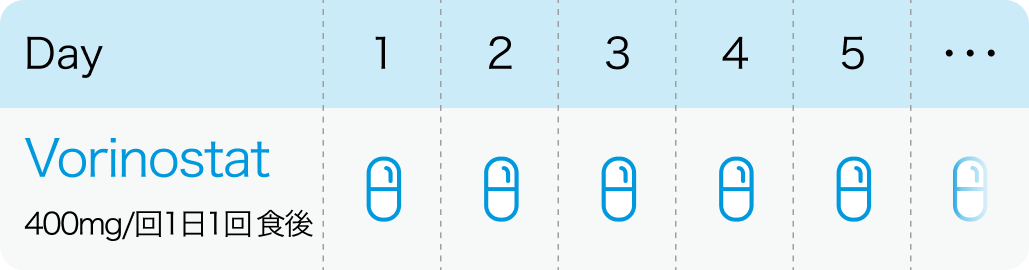
通常、 成人にはボリノスタットとして1日1回400mgを食後経口投与する。 なお、 患者の状態により適宜減量する。
ゾリンザカプセル添付文書 (2021年2月改訂第1版)より引用
エキスパートによるワンポイント
2次治療以降の選択肢で、経口投与可能
Skin-directed therapy抵抗性の早期菌状息肉症および進行期菌状息肉症/セザリー症候群において、 2次治療以降で使用される薬剤である。
治験では、 少なくとも1回以上の全身療法を受けたうえで、 進行性または再発性のステージIIB以上の菌状息肉症/セザリー症候群の患者が対象とされている。 2次治療の薬剤の中でも、 通常はモガムリズマブやブレンツキシマブベドチンより後に使用されるが、 これらの薬剤が静脈投与であるのに対して、 ボリノスタットは経口投与であるため、 患者によっては利便性が高い。
解説 : 近畿大学皮膚科 藤井 一恭先生
用量、 減量・休薬・中止基準
ボリノスタットの標準的な投与方法は、 1日400 mgを経口投与することである¹⁾。 日本の治験データでもこの投与量が基本とされており、 投与期間中にGrade 3以上の副作用が発現した場合には、 Grade 1以下に回復するまで最大2週間休薬し、 その後減量して再開する。
ただし、 貧血と血小板減少に関してはGrade 3でも必ずしも休薬する必要はない。 一方、 消化器症状についてはGrade 2でも内服継続が困難なことがある。 減量に当たっては、 1回目の減量は1日1回300mgとし、 2回目の減量は1日1回300 mgを5日間継続し、 その後2日間休薬することが推奨されている。
過去の主要な臨床試験の有効性と安全性
国内第Ⅰ相試験 (Wadaら)³⁾
日本におけるPhase 1試験では、 約40%の患者が部分寛解を達成し、 特に進行期患者に対する有効性が確認された。 副作用として最も多く報告されたのは血小板減少や消化器症状 (下痢、 食欲不振) であるが、 これらは適切な投与量調整や休薬により管理可能であった。
海外第Ⅱb相試験 (Olsenら)⁴⁾
海外の臨床試験でも、 ボリノスタットが他の治療に反応しなかったCTCL患者に対して有効であることが示され、 全体の30%近くの患者で部分寛解または完全寛解が確認されている。 特に、 皮膚病変の改善やかゆみの緩和が報告されており、 患者のQOL向上にも寄与することが示されている。
血小板減少や消化器症状への対応
ボリノスタットの使用中には、 特に血小板減少や消化器症状に対する適切な管理が必要である。 日本のデータにおいてもこれらの副作用が多く報告されているため、 治療中は定期的な血液検査と副作用のモニタリングが推奨される。
特に高齢者や体力が低下している患者には、 より慎重な管理が求められる。 下痢や脱水症状が発生する可能性があるため、 適切な水分補給や消化器症状に対する対策が重要である。 また、 抗凝固薬を併用している患者には、 出血リスクを考慮し、 プロトロンビン時間やINRの定期的なチェックが推奨されている。
出典
1) MSD株式会社/大鵬薬品工業株式会社. ゾリンザカプセル100mg添付文書 (2021年2月改訂第1版) [最終閲覧 : 2024/10/15]
2) MSD株式会社/大鵬薬品工業株式会社. ゾリンザカプセル100mg適正使用ガイド (2021年5月改訂) [最終閲覧 : 2024/10/15]
最終更新日 : 2024年10月15日
監修医師 : 近畿大学皮膚科 藤井 一恭先生
Vorinostat
本コンテンツは特定の治療法を推奨するものではありません。 個々の患者の病態や、 実際の薬剤情報やガイドラインを確認の上、 利用者の判断と責任でご利用ください。
薬剤情報
ヒストン脱アセチル化酵素 (HDAC) 阻害薬 ボリノスタット
*大鵬薬品工業株式会社の外部サイトへ遷移します
用法・用量

通常、 成人にはボリノスタットとして1日1回400mgを食後経口投与する。 なお、 患者の状態により適宜減量する。
ゾリンザカプセル添付文書 (2021年2月改訂第1版)より引用
エキスパートによるワンポイント
2次治療以降の選択肢で、経口投与可能
Skin-directed therapy抵抗性の早期菌状息肉症および進行期菌状息肉症/セザリー症候群において、 2次治療以降で使用される薬剤である。
治験では、 少なくとも1回以上の全身療法を受けたうえで、 進行性または再発性のステージIIB以上の菌状息肉症/セザリー症候群の患者が対象とされている。 2次治療の薬剤の中でも、 通常はモガムリズマブやブレンツキシマブベドチンより後に使用されるが、 これらの薬剤が静脈投与であるのに対して、 ボリノスタットは経口投与であるため、 患者によっては利便性が高い。
解説 : 近畿大学皮膚科 藤井 一恭先生
用量、 減量・休薬・中止基準
ボリノスタットの標準的な投与方法は、 1日400 mgを経口投与することである¹⁾。 日本の治験データでもこの投与量が基本とされており、 投与期間中にGrade 3以上の副作用が発現した場合には、 Grade 1以下に回復するまで最大2週間休薬し、 その後減量して再開する。
ただし、 貧血と血小板減少に関してはGrade 3でも必ずしも休薬する必要はない。 一方、 消化器症状についてはGrade 2でも内服継続が困難なことがある。 減量に当たっては、 1回目の減量は1日1回300mgとし、 2回目の減量は1日1回300 mgを5日間継続し、 その後2日間休薬することが推奨されている。
過去の主要な臨床試験の有効性と安全性
国内第Ⅰ相試験 (Wadaら)³⁾
日本におけるPhase 1試験では、 約40%の患者が部分寛解を達成し、 特に進行期患者に対する有効性が確認された。 副作用として最も多く報告されたのは血小板減少や消化器症状 (下痢、 食欲不振) であるが、 これらは適切な投与量調整や休薬により管理可能であった。
海外第Ⅱb相試験 (Olsenら)⁴⁾
海外の臨床試験でも、 ボリノスタットが他の治療に反応しなかったCTCL患者に対して有効であることが示され、 全体の30%近くの患者で部分寛解または完全寛解が確認されている。 特に、 皮膚病変の改善やかゆみの緩和が報告されており、 患者のQOL向上にも寄与することが示されている。
血小板減少や消化器症状への対応
ボリノスタットの使用中には、 特に血小板減少や消化器症状に対する適切な管理が必要である。 日本のデータにおいてもこれらの副作用が多く報告されているため、 治療中は定期的な血液検査と副作用のモニタリングが推奨される。
特に高齢者や体力が低下している患者には、 より慎重な管理が求められる。 下痢や脱水症状が発生する可能性があるため、 適切な水分補給や消化器症状に対する対策が重要である。 また、 抗凝固薬を併用している患者には、 出血リスクを考慮し、 プロトロンビン時間やINRの定期的なチェックが推奨されている。
出典
1) MSD株式会社/大鵬薬品工業株式会社. ゾリンザカプセル100mg添付文書 (2021年2月改訂第1版) [最終閲覧 : 2024/10/15]
2) MSD株式会社/大鵬薬品工業株式会社. ゾリンザカプセル100mg適正使用ガイド (2021年5月改訂) [最終閲覧 : 2024/10/15]
最終更新日 : 2024年10月15日
監修医師 : 近畿大学皮膚科 藤井 一恭先生
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
がん薬物療法における治療計画をまとめたものです。
主要論文や適正使用ガイドをもとにした用量調整プロトコール、 有害事象対応をご紹介します。
なお、 本ツールは医師向けの教育用資料であり、 実臨床での使用は想定しておりません。 最新の添付文書やガイドラインを必ずご確認下さい。
また、 一般の方への情報提供ではないことを予めご了承ください。