L-OHP:Oxaliplatin(エルプラット®)
| 投与量 | コース | 投与日 |
|---|---|---|
| 100mg/m² 点滴 | 1~ | Day1 |
l-LV:Levofolinate(アイソボリン®)
| 投与量 | コース | 投与日 |
|---|---|---|
| 400mg/m² 点滴 | 1~ | Day1 |
5-FU:Fluorouracil(フルオロウラシル®)
| 投与量 | コース | 投与日 |
|---|---|---|
| 400mg/m² 急速静注 | 1~ | Day1 |
| 2,400mg/m² 持続静注 | 1~ | Day1~3 |
前投薬
| パロノセトロン0.75mg day1 点滴、 デキサメタゾン 6.6mg day1 点滴、 8.0mg day2-4 経口 |
その他
| 1コース14日間。 |
| L-OHP+l-LV+5-FUをFOLFOX療法と呼ぶ。 |
本コンテンツは特定の治療法を推奨するものではありません。 個々の患者の病態や、 実際の薬剤情報やガイドラインを確認の上、 利用者の判断と責任でご利用ください。
薬剤情報
用法用量
国際第Ⅱ相試験⁴⁾のプロトコル
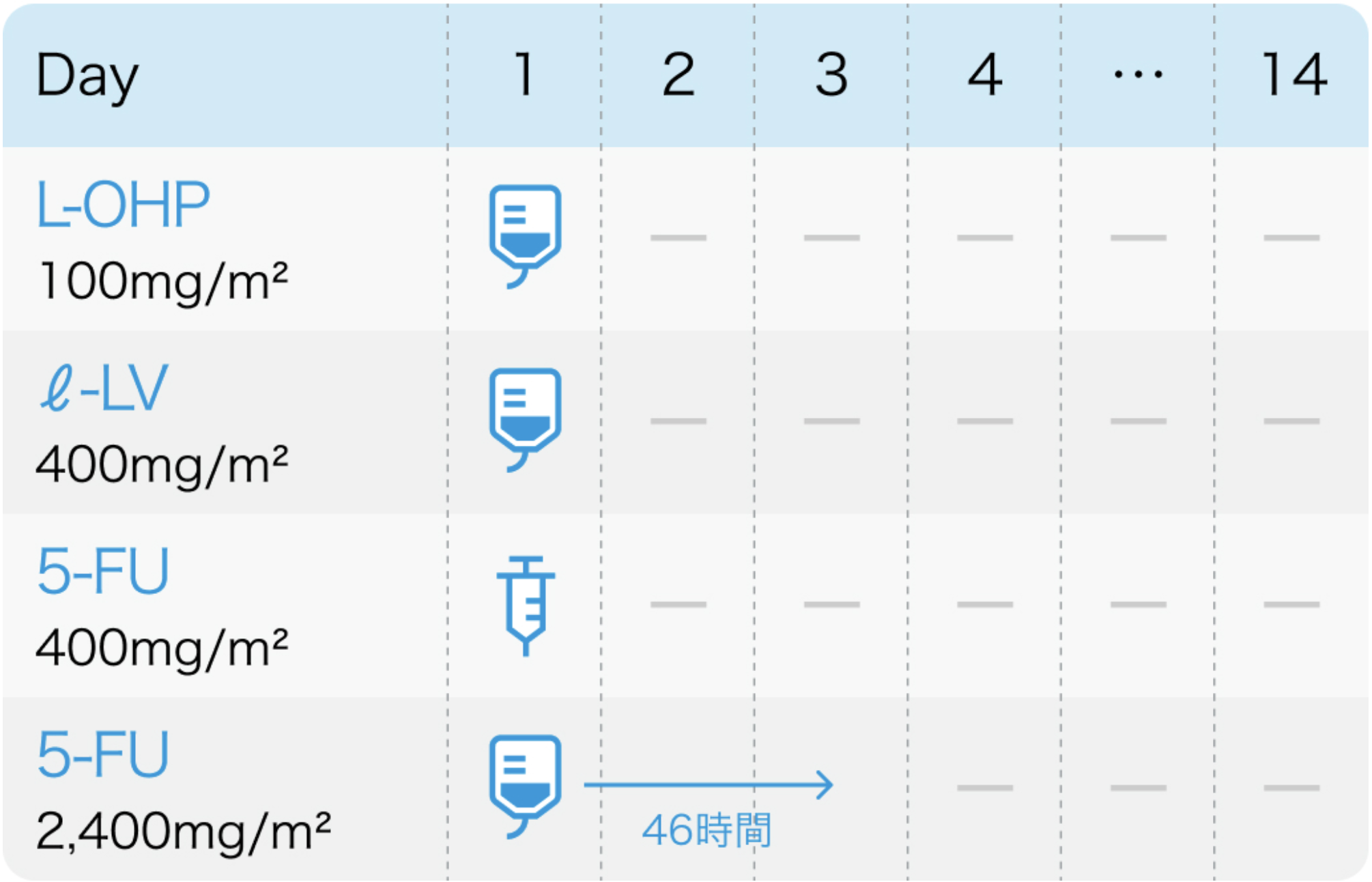
Cancer Chemother Pharmacol. 2013 Apr;71(4):905-11⁴⁾より作図
前投薬
MECレジメンとして扱う。
- パロノセトロン0.75mg day1 点滴
- デキサメタゾン 6.6mg day1 点滴、 8.0mg day2-4 経口
執筆 : 神奈川県立がんセンター消化器内科 古田 光寛先生
投与開始基準
国際第Ⅱ相試験⁴⁾のプロトコル

Cancer Chemother Pharmacol. 2013 Apr;71(4):905-11⁴⁾より作図
減量・休薬基準
国際第Ⅱ相試験⁴⁾のプロトコル

Cancer Chemother Pharmacol. 2013 Apr;71(4):905-11⁴⁾より作図
主な有害事象
国際第Ⅱ相試験⁴⁾
主な有害事象 (カッコ内はGrade3~4)
- 好中球減少症 80.3% (35.7%)
- 白血球減少症 76.8% (28.6%)
- 貧血 35.7% (10.7%)
- 血小板減少症 30.4% (10.7%)
- AST/ALT上昇 16.1% (0%)
- 発熱性好中球減少症 7.1% (7.1%)
- 倦怠感 60.7% (5%)
- 粘膜炎 57.1% (0%)
- 悪心/嘔吐 51.8% (0%)
- 下痢 10.7% (0%)
注意すべき有害事象 (カッコ内はGrade3~4)
- 脱毛症 10.7% (0%)
Cancer Chemother Pharmacol. 2013 Apr;71(4):905-11⁴⁾より引用
上手に使うためのワンポイント
他のレジメンとの使い分け
FP±Nivo/PemやIPI+Nivoとの使い分けが問題となる。 エビデンスレベルからはFP±Nivo/PemやIPI+Nivoを第1選択とし、 FOLFOXはこれらの治療レジメンが不適格の症例を対象とする。 具体的には心疾患、 腎障害、 外来での通院希望例、 自己免疫疾患を有する症例などである。
腎機能について
オキサリプラチンの投与量は腎機能CrClを参考に決定する。 CrClの計算はCockcroft-Gault式を用い、 CrCl≧30mL/minでは減量不要である。 欧州の添付文書ではCrCl<30mL/minは禁忌とされているが、 米国NCI Organ Dysfunction Working GroupによるとCrCl≧20mL/minで投与可能と報告されている⁵⁾。
執筆 : 神奈川県立がんセンター消化器内科 古田 光寛先生
特徴と注意点
オキサリプラチンは末梢神経障害が問題となる。 累積投与量が850mg/m²に達するとGrade3の末梢神経障害が約10%に出現する⁶⁾。 またオキサリプラチンの末梢神経障害は中止後も増悪するcoastingが見られるため、 症状が増悪してから中止しても手遅れとなりQOLを著しく悪化させる可能性があるため注意を要する。 累積投与量が850mg/m²を目安に中止を検討する。
執筆 : 神奈川県立がんセンター消化器内科 古田 光寛先生
出典
- 協和キリン株式会社. 5-FU®電子添文 (2024年6月改訂 第4版) [最終閲覧 : 2024/08/15]
- ファイザー・ファーマ株式会社. アイソボリン®電子添文 (2023年3月改訂 第1版) [最終閲覧 : 2024/04/10]
- ヤクルト本社. エルプラット®電子添文 (2024年4月改訂 第4版) [最終閲覧 : 2024/04/10]
- A phase II study of oxaliplatin in combination with leucovorin and fluorouracil as first-line chemotherapy in patients with metastatic squamous cell carcinoma of esophagus. Cancer Chemother Pharmacol. 2013 Apr;71(4):905-11. PMID: 23370661
- Dose-escalating and pharmacological study of oxaliplatin in adult cancer patients with impaired renal function: a National Cancer Institute Organ Dysfunction Working Group Study. J Clin Oncol. 2003 Jul 15;21(14):2664-72. PMID: 12860942
- Oxaliplatin-safety profile: neurotoxicity. Semin Oncol. 2003 Aug;30(4 Suppl 15):5-13. PMID: 14523789
最終更新日 : 2024年8月21日
執筆医 : 神奈川県立がんセンター消化器内科 古田 光寛先生
監修医師 : 神奈川県立がんセンター消化器内科部長 町田望先生
FOLFOX
L-OHP:Oxaliplatin(エルプラット®)
| 投与量 | コース | 投与日 |
|---|---|---|
| 100mg/m² 点滴 | 1~ | Day1 |
l-LV:Levofolinate(アイソボリン®)
| 投与量 | コース | 投与日 |
|---|---|---|
| 400mg/m² 点滴 | 1~ | Day1 |
5-FU:Fluorouracil(フルオロウラシル®)
| 投与量 | コース | 投与日 |
|---|---|---|
| 400mg/m² 急速静注 | 1~ | Day1 |
| 2,400mg/m² 持続静注 | 1~ | Day1~3 |
前投薬
| パロノセトロン0.75mg day1 点滴、 デキサメタゾン 6.6mg day1 点滴、 8.0mg day2-4 経口 |
その他
| 1コース14日間。 |
| L-OHP+l-LV+5-FUをFOLFOX療法と呼ぶ。 |
概要
本コンテンツは特定の治療法を推奨するものではありません。 個々の患者の病態や、 実際の薬剤情報やガイドラインを確認の上、 利用者の判断と責任でご利用ください。
薬剤情報
用法用量
国際第Ⅱ相試験⁴⁾のプロトコル

Cancer Chemother Pharmacol. 2013 Apr;71(4):905-11⁴⁾より作図
前投薬
MECレジメンとして扱う。
- パロノセトロン0.75mg day1 点滴
- デキサメタゾン 6.6mg day1 点滴、 8.0mg day2-4 経口
執筆 : 神奈川県立がんセンター消化器内科 古田 光寛先生
投与開始基準
国際第Ⅱ相試験⁴⁾のプロトコル

Cancer Chemother Pharmacol. 2013 Apr;71(4):905-11⁴⁾より作図
減量・休薬基準
国際第Ⅱ相試験⁴⁾のプロトコル

Cancer Chemother Pharmacol. 2013 Apr;71(4):905-11⁴⁾より作図
主な有害事象
国際第Ⅱ相試験⁴⁾
主な有害事象 (カッコ内はGrade3~4)
- 好中球減少症 80.3% (35.7%)
- 白血球減少症 76.8% (28.6%)
- 貧血 35.7% (10.7%)
- 血小板減少症 30.4% (10.7%)
- AST/ALT上昇 16.1% (0%)
- 発熱性好中球減少症 7.1% (7.1%)
- 倦怠感 60.7% (5%)
- 粘膜炎 57.1% (0%)
- 悪心/嘔吐 51.8% (0%)
- 下痢 10.7% (0%)
注意すべき有害事象 (カッコ内はGrade3~4)
- 脱毛症 10.7% (0%)
Cancer Chemother Pharmacol. 2013 Apr;71(4):905-11⁴⁾より引用
上手に使うためのワンポイント
他のレジメンとの使い分け
FP±Nivo/PemやIPI+Nivoとの使い分けが問題となる。 エビデンスレベルからはFP±Nivo/PemやIPI+Nivoを第1選択とし、 FOLFOXはこれらの治療レジメンが不適格の症例を対象とする。 具体的には心疾患、 腎障害、 外来での通院希望例、 自己免疫疾患を有する症例などである。
腎機能について
オキサリプラチンの投与量は腎機能CrClを参考に決定する。 CrClの計算はCockcroft-Gault式を用い、 CrCl≧30mL/minでは減量不要である。 欧州の添付文書ではCrCl<30mL/minは禁忌とされているが、 米国NCI Organ Dysfunction Working GroupによるとCrCl≧20mL/minで投与可能と報告されている⁵⁾。
執筆 : 神奈川県立がんセンター消化器内科 古田 光寛先生
特徴と注意点
オキサリプラチンは末梢神経障害が問題となる。 累積投与量が850mg/m²に達するとGrade3の末梢神経障害が約10%に出現する⁶⁾。 またオキサリプラチンの末梢神経障害は中止後も増悪するcoastingが見られるため、 症状が増悪してから中止しても手遅れとなりQOLを著しく悪化させる可能性があるため注意を要する。 累積投与量が850mg/m²を目安に中止を検討する。
執筆 : 神奈川県立がんセンター消化器内科 古田 光寛先生
出典
- 協和キリン株式会社. 5-FU®電子添文 (2024年6月改訂 第4版) [最終閲覧 : 2024/08/15]
- ファイザー・ファーマ株式会社. アイソボリン®電子添文 (2023年3月改訂 第1版) [最終閲覧 : 2024/04/10]
- ヤクルト本社. エルプラット®電子添文 (2024年4月改訂 第4版) [最終閲覧 : 2024/04/10]
- A phase II study of oxaliplatin in combination with leucovorin and fluorouracil as first-line chemotherapy in patients with metastatic squamous cell carcinoma of esophagus. Cancer Chemother Pharmacol. 2013 Apr;71(4):905-11. PMID: 23370661
- Dose-escalating and pharmacological study of oxaliplatin in adult cancer patients with impaired renal function: a National Cancer Institute Organ Dysfunction Working Group Study. J Clin Oncol. 2003 Jul 15;21(14):2664-72. PMID: 12860942
- Oxaliplatin-safety profile: neurotoxicity. Semin Oncol. 2003 Aug;30(4 Suppl 15):5-13. PMID: 14523789
最終更新日 : 2024年8月21日
執筆医 : 神奈川県立がんセンター消化器内科 古田 光寛先生
監修医師 : 神奈川県立がんセンター消化器内科部長 町田望先生
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
がん薬物療法における治療計画をまとめたものです。
主要論文や適正使用ガイドをもとにした用量調整プロトコール、 有害事象対応をご紹介します。
なお、 本ツールは医師向けの教育用資料であり、 実臨床での使用は想定しておりません。 最新の添付文書やガイドラインを必ずご確認下さい。
また、 一般の方への情報提供ではないことを予めご了承ください。
