治療スケジュール
概要
監修医師
Bmab:Bevacizumab(アバスチン®)
| 投与量 | コース | 投与日 |
|---|---|---|
| 5mg/kg 点滴 | 1~ | Day1 |
CPT-11:Irinotecan(トポテシン®)
| 投与量 | コース | 投与日 |
|---|---|---|
| 165mg/m² 点滴 | 1~ | Day1 |
l-LV:Levofolinate(アイソボリン®)
| 投与量 | コース | 投与日 |
|---|---|---|
| 200mg/m² 点滴 | 1~ | Day1 |
L-OHP:Oxaliplatin(エルプラット®)
| 投与量 | コース | 投与日 |
|---|---|---|
| 85mg/m² 点滴 | 1~ | Day1 |
5-FU:Fluorouracil(フルオロウラシル®)
| 投与量 | コース | 投与日 |
|---|---|---|
| 3,200mg/m² 持続静注 | 1~ | Day1~3 |
その他
| 1コース14日間。 |
| CPT-11+L-OHP+l-LV+5-FUでFOLFOXIRI療法と呼ぶ。 |
本コンテンツは特定の治療法を推奨するものではありません。 個々の患者の病態や、 実際の薬剤情報やガイドラインを確認の上、 利用者の判断と責任でご利用ください。
薬剤情報
*中外製薬株式会社の外部サイトへ遷移します
用法用量
第Ⅲ相試験⁷⁾のプロトコル
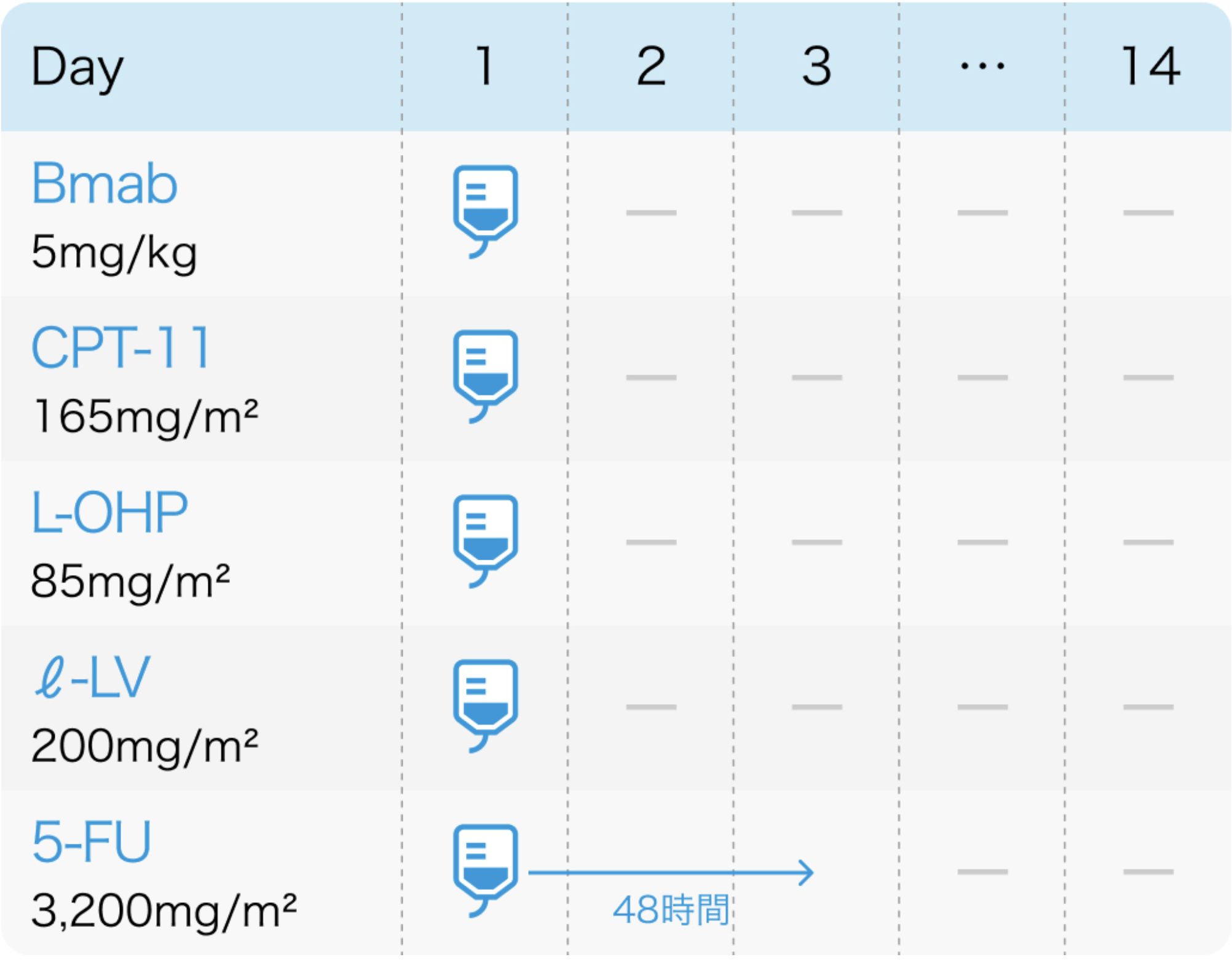
N Engl J Med. 2014 Oct 23;371(17):1609-18⁷⁾より作図
投与開始基準
第Ⅲ相試験⁷⁾のプロトコル

CrCl、 血中Creはどちらか一方を満たせば可
N Engl J Med. 2014 Oct 23;371(17):1609-18⁷⁾より作図
減量基準
第Ⅲ相試験⁷⁾のプロトコル
FOLFOXIRI減量基準
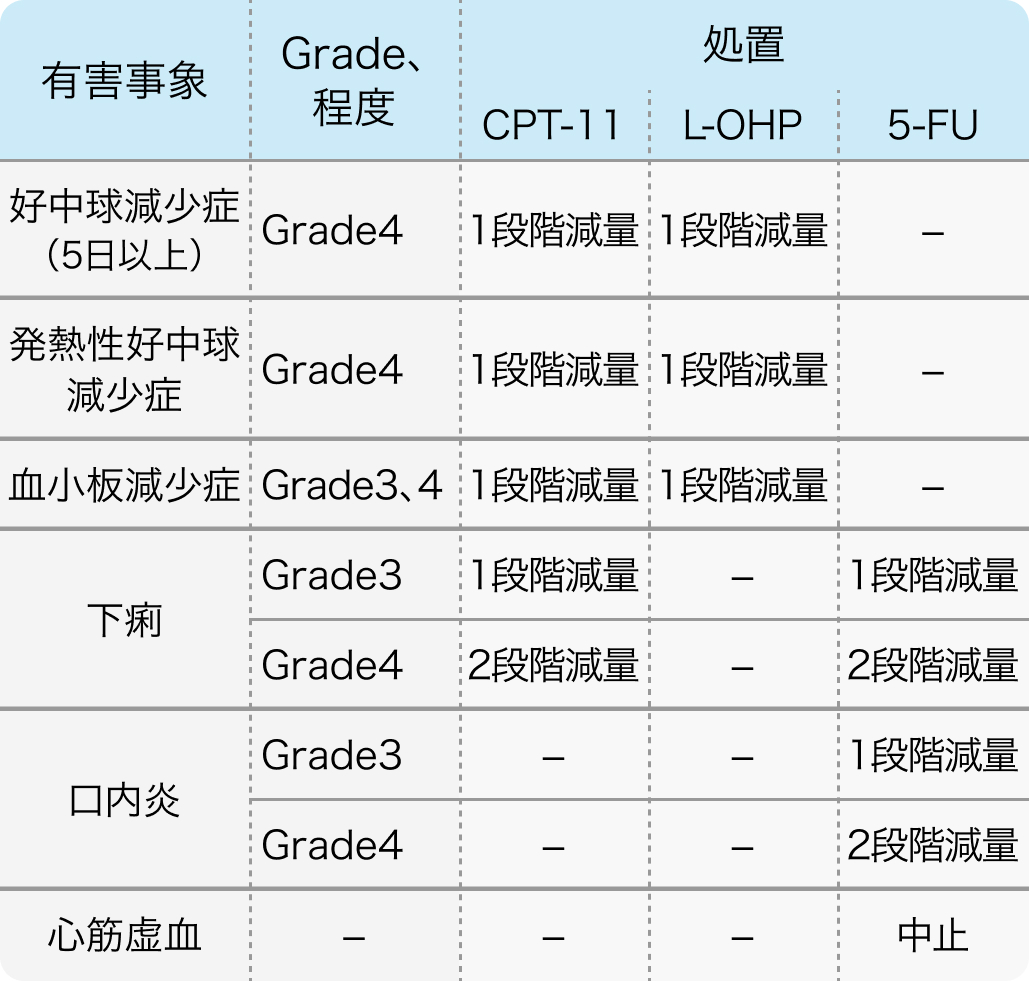
N Engl J Med. 2014 Oct 23;371(17):1609-18⁷⁾より作図
初回基準量と減量レベル
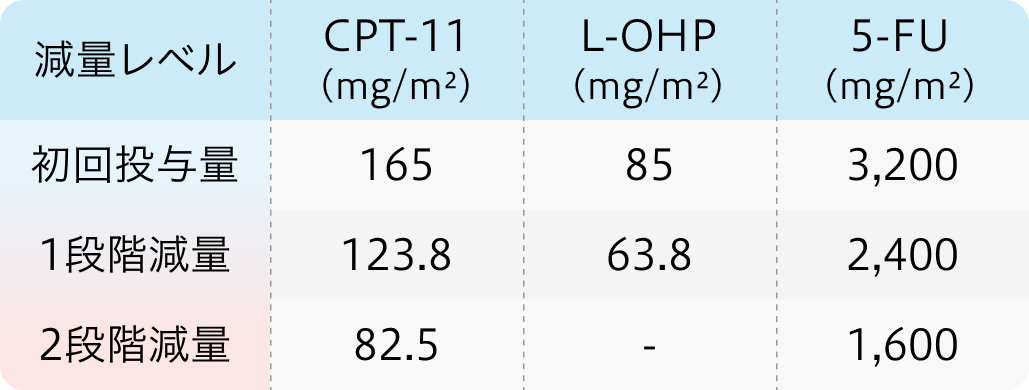
N Engl J Med. 2014 Oct 23;371(17):1609-18⁷⁾より作図
FOLFOXIRI休薬・中止基準
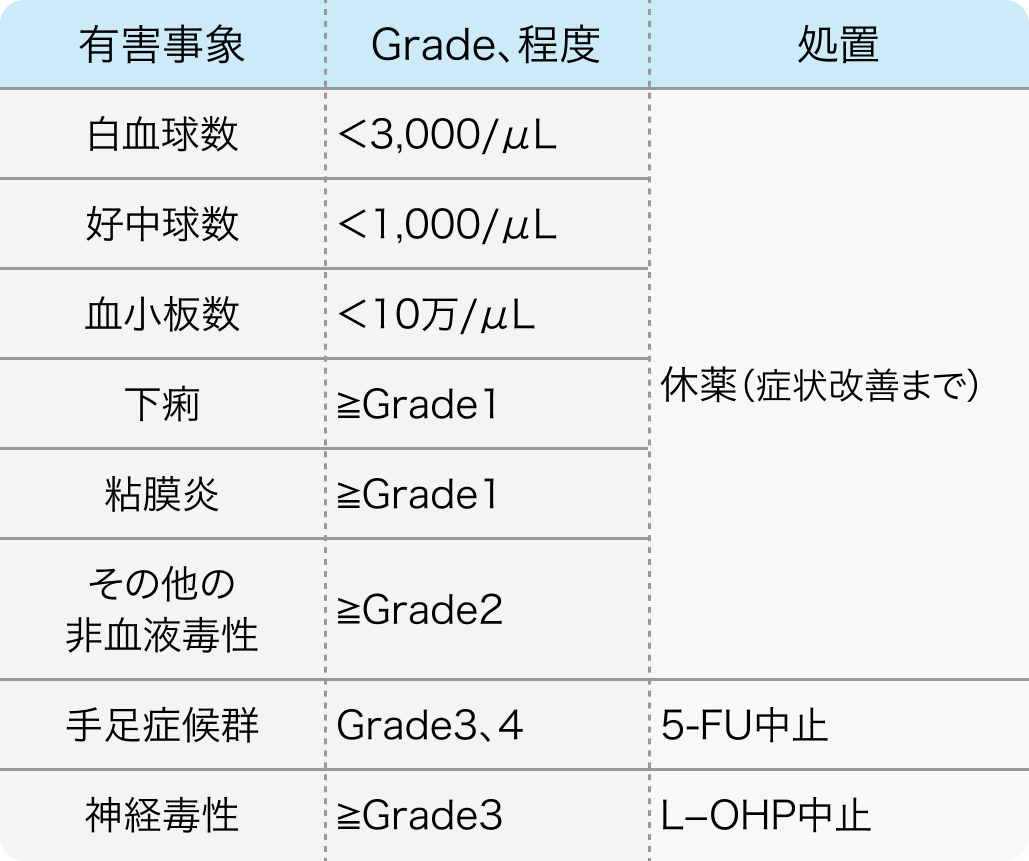
N Engl J Med. 2014 Oct 23;371(17):1609-18⁷⁾より作図
ベバシズマブ休薬・中止基準
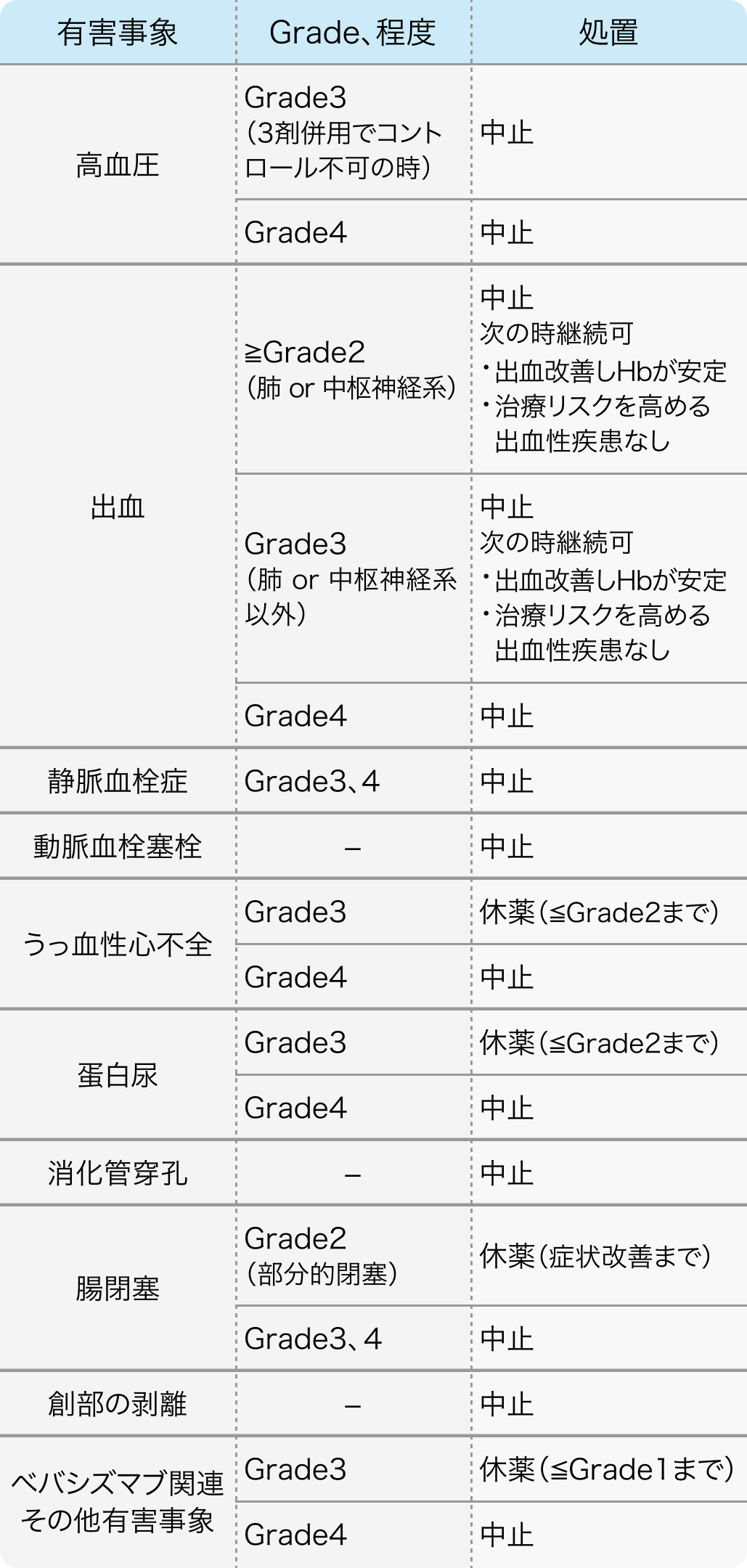
N Engl J Med. 2014 Oct 23;371(17):1609-18⁷⁾より作図
主な有害事象
第Ⅲ相試験⁷⁾
主な有害事象 (Grade3~4)
- 好中球減少症 50.0%
- 発熱性好中球減少症 8.8%
- 下痢 18.8%
- 口内炎 8.8%
- 嘔吐 4.4%
- 悪心 2.8%
注意すべき有害事象 (Grade3~4)
- 末梢神経障害 5.2%
- 高血圧 5.2%
N Engl J Med. 2014 Oct 23;371(17):1609-18⁷⁾より引用
上手に使うためのワンポイント
- 1-2コース中に好中球減少などの血液毒性の初回出現が予想されるため最初は週毎の血液検査実施を考慮する。
- 導入化学療法の期間について、 TRIBE試験やQUATTRO試験、 modified FOLFOXIRIのJACCRO CC-11試験では12コースに設定されていたが、 TRIBE2試験では8コースに設定されている。 またQUATTRO2試験でも原則8コースに設定しつつ最大12コースまで投与できるようなプロトコルになっている。 延命を目的とした場合には末梢性感覚ニューロパチー悪化を意識して8コースで終了を基本と考えたほうが良いかもしれない。
- 使用理由や実際の腫瘍縮小効果にもよるが、 毒性による治療延期を繰り返しDose intensityが低下するケースでは導入化学療法期間でもdoubletへ切り替えることも選択肢の一つである。
監修 : 神奈川県立がんセンター消化器内科部長 町田望先生
特徴と注意点
- 大腸癌治療ガイドライン2022年版では、 RAS/RAF野生型の右側・RAS変異型・BRAF変異型において治療選択肢とされている。 複数試験の統合解析では、 BRAF変異型における有効性について、 doubletと比較してOSでは差がないもののORRとPFSでは優れる結果であるため、 病状により適用を検討する必要がある。
- 治療前にUGT1A1の結果が、 628いずれかのホモ接合体、 もしくは両者の複合ヘテロ接合体かどうかの確認をすること。
監修 : 神奈川県立がんセンター消化器内科部長 町田望先生
関連する臨床試験
第Ⅲ相試験⁷⁾
未治療の転移性結腸直腸癌患者508人を、 FOLFIRIとベバシズマブの併用 (対照群) またはFOLFOXIRIとベバシズマブの投与 (実験群) を比較した試験。 主要評価項目は無増悪生存期間 (PFS) で、 副次評価項目には奏効率、 全生存率 (OS)、 転移切除率、 有害事象発生率などとされた。
N Engl J Med. 2014 Oct 23;371(17):1609-18. PMID: 25337750
出典
- アルフレッサ ファーマ株式会社. トポテシン®電子添文 (2023年8月改訂 第1版) [最終閲覧 : 2024/6/15]
- ヤクルト本社. エルプラット®電子添文 (2024年4月改訂 第4版) [最終閲覧 : 2024/5/10]
- ファイザー・ファーマ株式会社. アイソボリン®電子添文 (2023年3月改訂 第1版) [最終閲覧 : 2024/04/15]
- 協和キリン株式会社. 5-FU®電子添文 (2024年6月改訂 第4版) [最終閲覧 : 2024/08/26]
- 中外製薬株式会社. アバスチン®電子添文 (2024年3月改訂 第5版) [最終閲覧 : 2024/04/17]
- 中外製薬株式会社. アバスチン®適正使用ガイド (2023年11月改訂) [最終閲覧 : 2024/04/17]
- Initial therapy with FOLFOXIRI and bevacizumab for metastatic colorectal cancer. N Engl J Med. 2014 Oct 23;371(17):1609-18. PMID: 25337750
最終更新日 : 2024年8月27日
監修医師 : 神奈川県立がんセンター消化器内科部長 町田望先生
FOLFOXIRI + Bmab
イリノテカン + オキサリプラチン + レボホリナート + フルオロウラシル + ベバシズマブ
大腸癌 > 一次、 二次治療
2024年08月27日更新
Bmab:Bevacizumab(アバスチン®)
| 投与量 | コース | 投与日 |
|---|---|---|
| 5mg/kg 点滴 | 1~ | Day1 |
CPT-11:Irinotecan(トポテシン®)
| 投与量 | コース | 投与日 |
|---|---|---|
| 165mg/m² 点滴 | 1~ | Day1 |
l-LV:Levofolinate(アイソボリン®)
| 投与量 | コース | 投与日 |
|---|---|---|
| 200mg/m² 点滴 | 1~ | Day1 |
L-OHP:Oxaliplatin(エルプラット®)
| 投与量 | コース | 投与日 |
|---|---|---|
| 85mg/m² 点滴 | 1~ | Day1 |
5-FU:Fluorouracil(フルオロウラシル®)
| 投与量 | コース | 投与日 |
|---|---|---|
| 3,200mg/m² 持続静注 | 1~ | Day1~3 |
その他
| 1コース14日間。 |
| CPT-11+L-OHP+l-LV+5-FUでFOLFOXIRI療法と呼ぶ。 |
概要
本コンテンツは特定の治療法を推奨するものではありません。 個々の患者の病態や、 実際の薬剤情報やガイドラインを確認の上、 利用者の判断と責任でご利用ください。
薬剤情報
*中外製薬株式会社の外部サイトへ遷移します
用法用量
第Ⅲ相試験⁷⁾のプロトコル

N Engl J Med. 2014 Oct 23;371(17):1609-18⁷⁾より作図
投与開始基準
第Ⅲ相試験⁷⁾のプロトコル

CrCl、 血中Creはどちらか一方を満たせば可
N Engl J Med. 2014 Oct 23;371(17):1609-18⁷⁾より作図
減量基準
第Ⅲ相試験⁷⁾のプロトコル
FOLFOXIRI減量基準

N Engl J Med. 2014 Oct 23;371(17):1609-18⁷⁾より作図
初回基準量と減量レベル

N Engl J Med. 2014 Oct 23;371(17):1609-18⁷⁾より作図
FOLFOXIRI休薬・中止基準

N Engl J Med. 2014 Oct 23;371(17):1609-18⁷⁾より作図
ベバシズマブ休薬・中止基準

N Engl J Med. 2014 Oct 23;371(17):1609-18⁷⁾より作図
主な有害事象
第Ⅲ相試験⁷⁾
主な有害事象 (Grade3~4)
- 好中球減少症 50.0%
- 発熱性好中球減少症 8.8%
- 下痢 18.8%
- 口内炎 8.8%
- 嘔吐 4.4%
- 悪心 2.8%
注意すべき有害事象 (Grade3~4)
- 末梢神経障害 5.2%
- 高血圧 5.2%
N Engl J Med. 2014 Oct 23;371(17):1609-18⁷⁾より引用
上手に使うためのワンポイント
- 1-2コース中に好中球減少などの血液毒性の初回出現が予想されるため最初は週毎の血液検査実施を考慮する。
- 導入化学療法の期間について、 TRIBE試験やQUATTRO試験、 modified FOLFOXIRIのJACCRO CC-11試験では12コースに設定されていたが、 TRIBE2試験では8コースに設定されている。 またQUATTRO2試験でも原則8コースに設定しつつ最大12コースまで投与できるようなプロトコルになっている。 延命を目的とした場合には末梢性感覚ニューロパチー悪化を意識して8コースで終了を基本と考えたほうが良いかもしれない。
- 使用理由や実際の腫瘍縮小効果にもよるが、 毒性による治療延期を繰り返しDose intensityが低下するケースでは導入化学療法期間でもdoubletへ切り替えることも選択肢の一つである。
監修 : 神奈川県立がんセンター消化器内科部長 町田望先生
特徴と注意点
- 大腸癌治療ガイドライン2022年版では、 RAS/RAF野生型の右側・RAS変異型・BRAF変異型において治療選択肢とされている。 複数試験の統合解析では、 BRAF変異型における有効性について、 doubletと比較してOSでは差がないもののORRとPFSでは優れる結果であるため、 病状により適用を検討する必要がある。
- 治療前にUGT1A1の結果が、 628いずれかのホモ接合体、 もしくは両者の複合ヘテロ接合体かどうかの確認をすること。
監修 : 神奈川県立がんセンター消化器内科部長 町田望先生
関連する臨床試験
第Ⅲ相試験⁷⁾
未治療の転移性結腸直腸癌患者508人を、 FOLFIRIとベバシズマブの併用 (対照群) またはFOLFOXIRIとベバシズマブの投与 (実験群) を比較した試験。 主要評価項目は無増悪生存期間 (PFS) で、 副次評価項目には奏効率、 全生存率 (OS)、 転移切除率、 有害事象発生率などとされた。
N Engl J Med. 2014 Oct 23;371(17):1609-18. PMID: 25337750
出典
- アルフレッサ ファーマ株式会社. トポテシン®電子添文 (2023年8月改訂 第1版) [最終閲覧 : 2024/6/15]
- ヤクルト本社. エルプラット®電子添文 (2024年4月改訂 第4版) [最終閲覧 : 2024/5/10]
- ファイザー・ファーマ株式会社. アイソボリン®電子添文 (2023年3月改訂 第1版) [最終閲覧 : 2024/04/15]
- 協和キリン株式会社. 5-FU®電子添文 (2024年6月改訂 第4版) [最終閲覧 : 2024/08/26]
- 中外製薬株式会社. アバスチン®電子添文 (2024年3月改訂 第5版) [最終閲覧 : 2024/04/17]
- 中外製薬株式会社. アバスチン®適正使用ガイド (2023年11月改訂) [最終閲覧 : 2024/04/17]
- Initial therapy with FOLFOXIRI and bevacizumab for metastatic colorectal cancer. N Engl J Med. 2014 Oct 23;371(17):1609-18. PMID: 25337750
最終更新日 : 2024年8月27日
監修医師 : 神奈川県立がんセンター消化器内科部長 町田望先生
こちらの記事の監修医師
HOKUTO編集部
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
HOKUTO編集部
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
レジメン(消化器)
がん薬物療法における治療計画をまとめたものです。
主要論文や適正使用ガイドをもとにした用量調整プロトコール、 有害事象対応をご紹介します。
なお、 本ツールは医師向けの教育用資料であり、 実臨床での使用は想定しておりません。 最新の添付文書やガイドラインを必ずご確認下さい。
また、 一般の方への情報提供ではないことを予めご了承ください。

