「がん化学療法後に増悪したPIK3CA遺伝子変異を有する卵巣明細胞癌」 を対象に、 2025年8月15日に承認申請され、 2026年3月23日に正式承認された。
本コンテンツは特定の治療法を推奨するものではありません。 個々の患者の病態や、 実際の薬剤情報やガイドラインを確認の上、 利用者の判断と責任でご利用ください。
薬剤情報
ハイツエキシン®錠 (リソバリシブ)
添付文書¹⁾ / 適正使用情報 (準備中)²⁾
*海和製薬株式会社の外部サイトへ遷移します
投与スケジュール
【1コース】連日投与
【催吐性】不明
【FN発症】未報告¹⁾
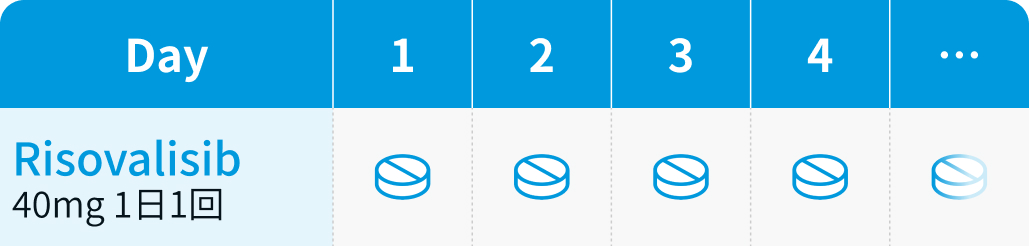
リソバリシブ : 40mgを1日1回空腹時に経口投与
食後投与の場合、 Cmax及びAUCが上昇するとの報告があるため、 食事の1時間前から食後2時間までの間の服用は避ける。
ハイツエキシン®電子添文情報¹⁾より引用
Key Data|臨床試験結果
📊 CYH33-G201試験¹⁾
化学療法歴のあるPIK3CA遺伝子変異陽性卵巣明細胞癌患者93例 (日本人52例を含む) を対象とした国際共同第II相単群試験。 PIK3CA遺伝子エクソン9または20の変異が確認された患者に、 リソバリシブを1日1回経口投与した。 主要評価項目は、 独立中央評価機関の評価によるORRであり、 有効性評価対象は84例 (日本人46例を含む) であった。
【有効性】
- ORR 34.5% (95%CI 24.6–45.7)
【安全性】主な副作用 (全Grade)
- 高血糖 89.2%
- 発疹 72.0%
- 口内炎 68.8%
- 悪心 52.7%
- 疲労 41.9%
- 食欲減退 38.7%
- 下痢 36.6%
- 血小板減少 35.5%
- 体重減少 35.5%
- 末梢性浮腫 26.9%
- 顔面浮腫 15.1%
- 間質性肺疾患 8.6%
- 低アルブミン血症 5.4%
- QT間隔延長 2.2%
- 多形紅斑 2.2%
- 糖尿病性ケトアシドーシス (DKA) 1.1%
- ニューモシスチス・イロベチイ肺炎 1.1%
- 腹水 1.1%
各プロトコル
適格基準
CYH33-G201試験の主な適格基準¹⁾
- 白金剤を含む化学療法歴のある患者
- PIK3CA遺伝子エクソン9又は20に変異が確認された卵巣明細胞癌
- 対象変異 : E542K, E545A, E545D, E545G, E545K, Q546E, Q546K, Q546L, Q546R, H1047L, H1047R, H1047Y
糖尿病患者、 空腹時血糖値>110mg/dL、 HbA1c>ULNの患者は除外
用量レベル
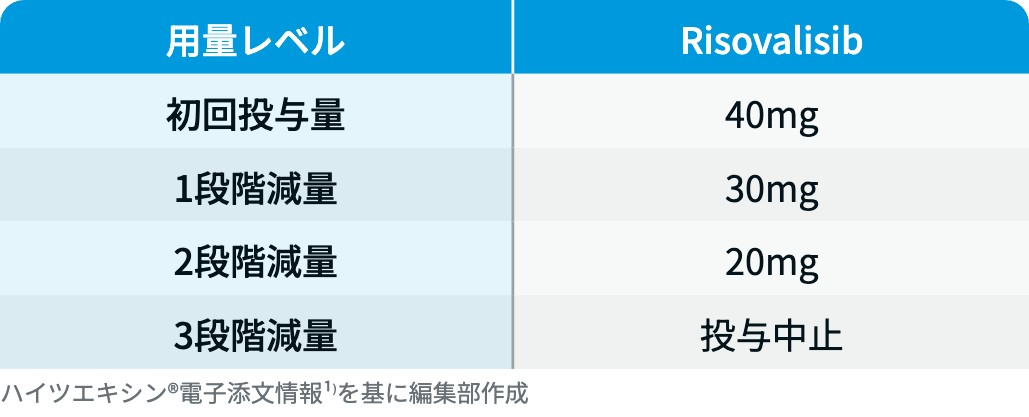
腎障害患者に対する用量調整
軽度腎機能障害患者 (CrCl 60~90mL/min) では、 腎機能正常患者に対するAUC0-24hの幾何平均値の比は0.83であった¹⁾。
有害事象発現時の減量・休薬・中止基準
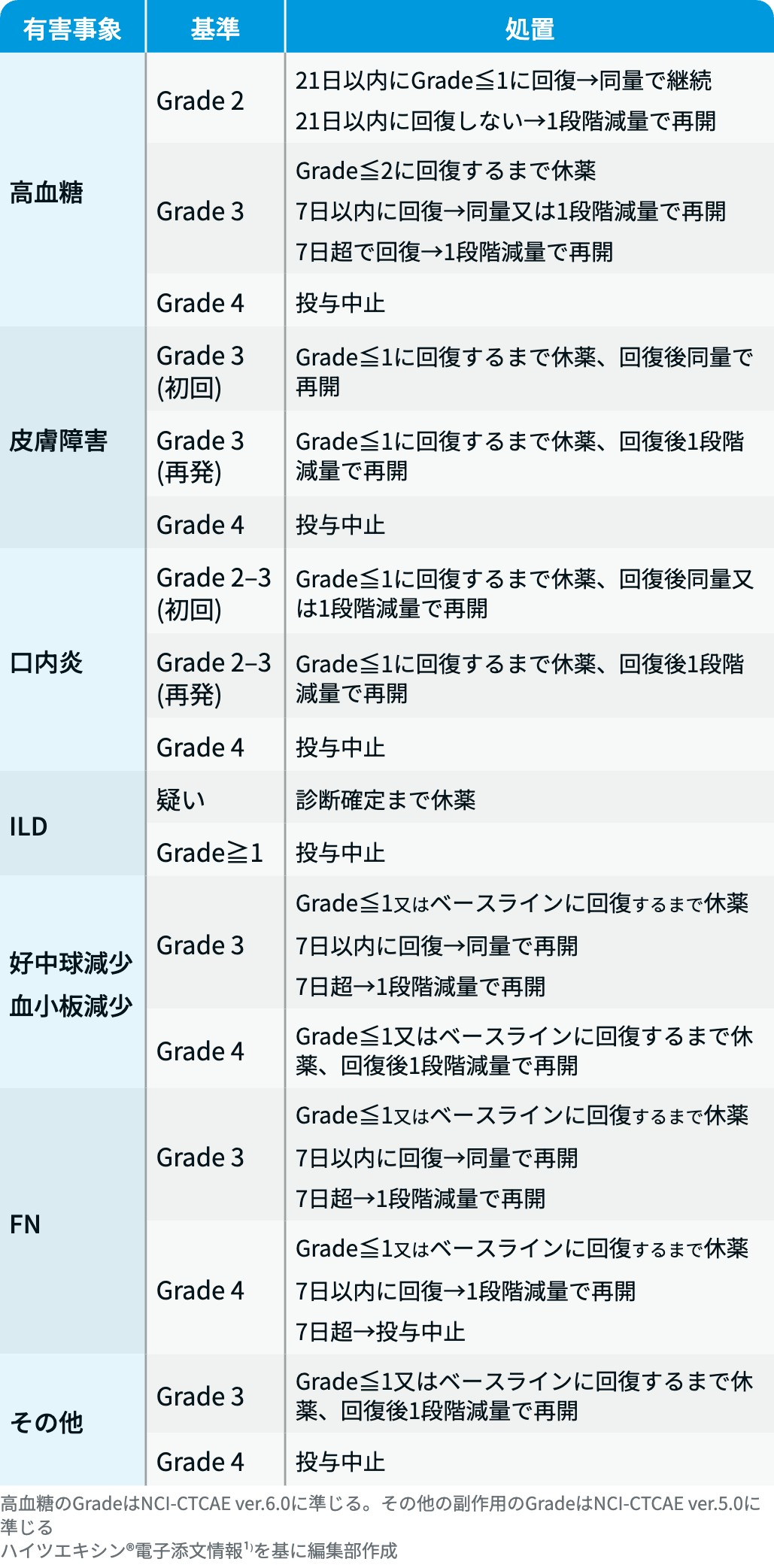
レジメンの特徴と注意点
作用機序の特徴
リソバリシブは、 PI3KαのATP結合部位に結合しキナーゼ活性を阻害する。 PI3Kシグナル伝達経路の下流分子であるAKTのリン酸化を阻害することにより、 腫瘍増殖抑制作用を示す¹⁾。
レジメン適用時の注意事項
ハイツエキシン®電子添文¹⁾ 「重要な基本的注意」 の要約
間質性肺疾患 : 間質性肺疾患があらわれることがあるため、 初期症状の確認や定期的な胸部画像検査を行い、 十分に観察する。 初期症状がみられた場合は、 速やかに医療機関を受診するよう患者へ指導する。
高血糖 : 高血糖があらわれ、 DKAに至ることがあるため、 投与開始前および投与中は空腹時血糖値、 HbA1cを定期的に測定する。 投与中はこれらに加えて、 ケトン体の測定も望ましい。 高血糖について十分に説明し、 口渇、 頻尿、 多尿、 体重減少などの症状がみられた場合は、 速やかに医療機関を受診するよう患者へ指導する。
血小板減少 : 血小板減少症があらわれることがあるため、 投与前および投与中は定期的に血液検査を行い、 患者の状態を十分に観察する。
電解質異常 : 電解質異常があらわれることがあるため、 投与前および投与中は定期的に電解質検査 (カリウムなど) を行い、 患者の状態を十分に観察する。 投与中の電解質検査は、 最初の1ヵ月間は週1回、 その後は3週間に1回を目安に実施する。 異常が認められた場合は速やかに適切な処置を行い、 必要に応じて補正する。
QT間隔延長 : QT間隔延長があらわれることがあるため、 投与前および投与中は定期的に心電図検査を行い、 患者の状態を十分に観察する。 投与中の心電図検査は、 最初の1ヵ月間は週1回、 その後は3週間に1回を目安に実施し、 異常が認められた場合は速やかに適切な処置を行う。
RMP【重要な特定されたリスク】
準備中
コンパニオン診断薬の情報
本剤の適応判定に利用可能なコンパニオン診断薬は以下のとおり。
- AmoyDx PIK3CA 変異検出キット
出典
1) 海和製薬株式会社. ハイツエキシン®錠10mg 電子添文. 2026年3月作成 第1版.
2) 準備中
最終更新 : 2026年4月3日
執筆 : HOKUTO編集部 がん専門・指導薬剤師
監修医師 : 日本医科大学 武蔵小杉病院 腫瘍内科 勝俣 範之
Risovalisib
「がん化学療法後に増悪したPIK3CA遺伝子変異を有する卵巣明細胞癌」 を対象に、 2025年8月15日に承認申請され、 2026年3月23日に正式承認された。
本コンテンツは特定の治療法を推奨するものではありません。 個々の患者の病態や、 実際の薬剤情報やガイドラインを確認の上、 利用者の判断と責任でご利用ください。
薬剤情報
ハイツエキシン®錠 (リソバリシブ)
添付文書¹⁾ / 適正使用情報 (準備中)²⁾
*海和製薬株式会社の外部サイトへ遷移します
投与スケジュール
【1コース】連日投与
【催吐性】不明
【FN発症】未報告¹⁾

リソバリシブ : 40mgを1日1回空腹時に経口投与
食後投与の場合、 Cmax及びAUCが上昇するとの報告があるため、 食事の1時間前から食後2時間までの間の服用は避ける。
ハイツエキシン®電子添文情報¹⁾より引用
Key Data|臨床試験結果
📊 CYH33-G201試験¹⁾
化学療法歴のあるPIK3CA遺伝子変異陽性卵巣明細胞癌患者93例 (日本人52例を含む) を対象とした国際共同第II相単群試験。 PIK3CA遺伝子エクソン9または20の変異が確認された患者に、 リソバリシブを1日1回経口投与した。 主要評価項目は、 独立中央評価機関の評価によるORRであり、 有効性評価対象は84例 (日本人46例を含む) であった。
【有効性】
- ORR 34.5% (95%CI 24.6–45.7)
【安全性】主な副作用 (全Grade)
- 高血糖 89.2%
- 発疹 72.0%
- 口内炎 68.8%
- 悪心 52.7%
- 疲労 41.9%
- 食欲減退 38.7%
- 下痢 36.6%
- 血小板減少 35.5%
- 体重減少 35.5%
- 末梢性浮腫 26.9%
- 顔面浮腫 15.1%
- 間質性肺疾患 8.6%
- 低アルブミン血症 5.4%
- QT間隔延長 2.2%
- 多形紅斑 2.2%
- 糖尿病性ケトアシドーシス (DKA) 1.1%
- ニューモシスチス・イロベチイ肺炎 1.1%
- 腹水 1.1%
各プロトコル
適格基準
CYH33-G201試験の主な適格基準¹⁾
- 白金剤を含む化学療法歴のある患者
- PIK3CA遺伝子エクソン9又は20に変異が確認された卵巣明細胞癌
- 対象変異 : E542K, E545A, E545D, E545G, E545K, Q546E, Q546K, Q546L, Q546R, H1047L, H1047R, H1047Y
糖尿病患者、 空腹時血糖値>110mg/dL、 HbA1c>ULNの患者は除外
用量レベル

腎障害患者に対する用量調整
軽度腎機能障害患者 (CrCl 60~90mL/min) では、 腎機能正常患者に対するAUC0-24hの幾何平均値の比は0.83であった¹⁾。
有害事象発現時の減量・休薬・中止基準

レジメンの特徴と注意点
作用機序の特徴
リソバリシブは、 PI3KαのATP結合部位に結合しキナーゼ活性を阻害する。 PI3Kシグナル伝達経路の下流分子であるAKTのリン酸化を阻害することにより、 腫瘍増殖抑制作用を示す¹⁾。
レジメン適用時の注意事項
ハイツエキシン®電子添文¹⁾ 「重要な基本的注意」 の要約
間質性肺疾患 : 間質性肺疾患があらわれることがあるため、 初期症状の確認や定期的な胸部画像検査を行い、 十分に観察する。 初期症状がみられた場合は、 速やかに医療機関を受診するよう患者へ指導する。
高血糖 : 高血糖があらわれ、 DKAに至ることがあるため、 投与開始前および投与中は空腹時血糖値、 HbA1cを定期的に測定する。 投与中はこれらに加えて、 ケトン体の測定も望ましい。 高血糖について十分に説明し、 口渇、 頻尿、 多尿、 体重減少などの症状がみられた場合は、 速やかに医療機関を受診するよう患者へ指導する。
血小板減少 : 血小板減少症があらわれることがあるため、 投与前および投与中は定期的に血液検査を行い、 患者の状態を十分に観察する。
電解質異常 : 電解質異常があらわれることがあるため、 投与前および投与中は定期的に電解質検査 (カリウムなど) を行い、 患者の状態を十分に観察する。 投与中の電解質検査は、 最初の1ヵ月間は週1回、 その後は3週間に1回を目安に実施する。 異常が認められた場合は速やかに適切な処置を行い、 必要に応じて補正する。
QT間隔延長 : QT間隔延長があらわれることがあるため、 投与前および投与中は定期的に心電図検査を行い、 患者の状態を十分に観察する。 投与中の心電図検査は、 最初の1ヵ月間は週1回、 その後は3週間に1回を目安に実施し、 異常が認められた場合は速やかに適切な処置を行う。
RMP【重要な特定されたリスク】
準備中
コンパニオン診断薬の情報
本剤の適応判定に利用可能なコンパニオン診断薬は以下のとおり。
- AmoyDx PIK3CA 変異検出キット
出典
1) 海和製薬株式会社. ハイツエキシン®錠10mg 電子添文. 2026年3月作成 第1版.
2) 準備中
最終更新 : 2026年4月3日
執筆 : HOKUTO編集部 がん専門・指導薬剤師
監修医師 : 日本医科大学 武蔵小杉病院 腫瘍内科 勝俣 範之
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
がん薬物療法における治療計画をまとめたものです。
主要論文や適正使用ガイドをもとにした用量調整プロトコール、 有害事象対応をご紹介します。
なお、 本ツールは医師向けの教育用資料であり、 実臨床での使用は想定しておりません。 最新の添付文書やガイドラインを必ずご確認下さい。
また、 一般の方への情報提供ではないことを予めご了承ください。