本コンテンツは特定の治療法を推奨するものではありません。 個々の患者の病態や、 実際の薬剤情報やガイドラインを確認の上、 利用者の判断と責任でご利用ください。
薬剤情報
【催吐性】 中等度催吐性
【FN発症】低リスク (<10%)
- タキソール® (添付文書¹⁾)
- パラプラチン® (添付文書²⁾)
用法用量
国際第III相試験³⁾のプロトコル
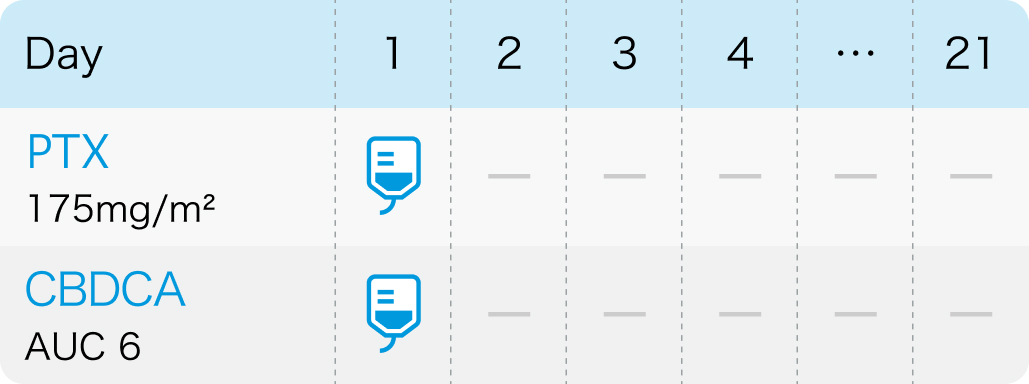
J Clin Oncol. 2009 Mar 20;27(9):1419-25³⁾より作図
電子添文の用法および用量
パクリタキセル : 1日1回210mg/m² を3時間かけて点滴静注し、 少なくとも3週間休薬。 タキソール®電子添文 (2023年7月改訂 第2版)¹⁾より引用
カルボプラチン : 1日1回300~400mg/m²を投与し、 少なくとも4週間休薬。 パラプラチン®電子添文 (2023年5月改訂 第3版)²⁾より引用
前投薬・投与スケジュール例
- DEX 9.9mg+ファモチジン 50mg+ 抗ヒスタミン薬+生食 100ml
- NK₁阻害剤+5HT₃拮抗剤+生食 50ml (30分)
- PTX 175mg/m²+5%ブ糖液 500mL (3時間)
- CBDCA+5%ブ糖液 250mL (30-60分)
日本医科大学 武蔵小杉病院 腫瘍内科教授 勝俣 範之先生提供
参考 : パクリタキセル電子添文¹⁾
投与約30分前までに投与を終了するように、 デキサメタゾンリン酸エステルナトリウム注射液 (デキサメタゾンとして8mg) 及びラニチジン塩酸塩注射液 (ラニチジンとして50mg) または注射用ファモチジン (ファモチジンとして20mg) を静脈内投与、 ジフェンヒドラミン塩酸塩錠 (ジフェンヒドラミン塩酸塩として50mg) を経口投与すること。
デキサメタゾンは初回投与時8mgとし、 次回投与時までに過敏症状の発現がみられなかった場合または臨床上特に問題のない過敏症状の場合は、 2週目の投与より半量 (4mg) に減量し投与してもよい。 以降の投与週においても同様の場合、 半量ずつ最低1mgまで減量し投与してもよい。
タキソール®電子添文 (2023年7月改訂 第2版)¹⁾より引用
投与開始基準
国際第III相試験³⁾のプロトコル
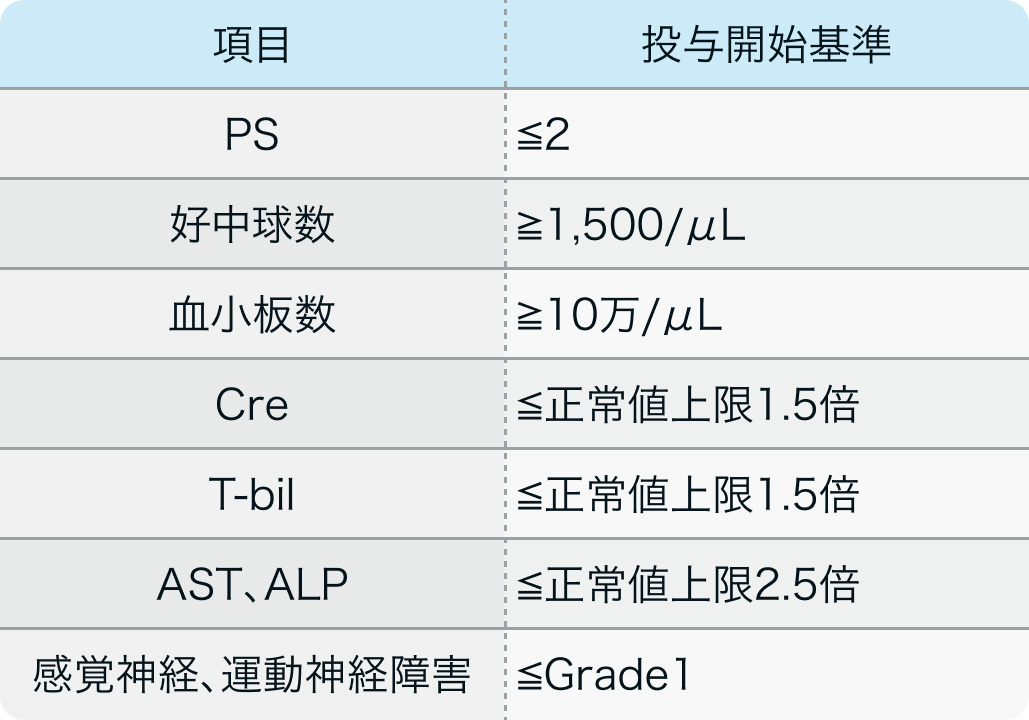
J Clin Oncol. 2009 Mar 20;27(9):1419-25³⁾より作図
KeyData|臨床試験結果
国際第III相試験³⁾⁴⁾
対象: ステージ III-IVの進行期上皮性卵巣癌および原発性腹膜癌患者4,312例
方法: TC (PTX+CBDCA)群
【有効性】 TC群
- mPFS 16.0ヵ月
- mOS 44.1ヵ月
【安全性】≧Grade3の主な有害事象
- 白血球数減少 50.8%
- 好中球数減少 86.9%
- 血小板数減少 22.4%
- 貧血 11.8%
- その他の血液疾患 18.1%
- アレルギー 4.4%
- 聴覚 0.6%
- 心臓血管 2.3%
- 凝固系 0.6%
- 全身状態 6.3%
- 皮膚 1.5%
- 胃腸 10.4%
- 泌尿生殖器/腎臓 1.0%
- 出血 0.9%
- 肝臓 1.5%
- 感染症/発熱 8.8%
- 代謝 7.1%
- 筋骨格 0.8%
- 神経学的 3.9%
- 末梢神経 5.2%
- 眼球/視覚 0.1%
- 痛み 6.1%
- 肺 2.2%
- 二次原発腫瘍 3.9%
J Clin Oncol. 2009 Mar 20;27(9):1419-25³⁾、 ClinicalTrials.gov (NCT00011986) ⁴⁾より引用
エキスパートによるワンポイント
初回治療の国際的標準
3週ごと6サイクルが基本的スケジュールです (第6回卵巣がん国際コンセンサスカンファレンス⁵⁾)
外来治療が可能
このレジメンで入院は不要です。 特に合併症があったりやPS不良でない限りは、 初回から外来治療がよいと思います。
監修 : 日本医科大学 武蔵小杉病院 腫瘍内科教授 勝俣 範之先生
出典
- クリニジェン株式会社. タキソール®電子添文 (2023年7月改訂 第2版) [最終閲覧 : 2024/03/27]
- クリニジェン株式会社. パラプラチン®電子添文 (2023年5月改訂 第3版) [最終閲覧 : 2024/03/27]
- Evaluation of new platinum-based treatment regimens in advanced-stage ovarian cancer: a Phase III Trial of the Gynecologic Cancer Intergroup. J Clin Oncol. 2009 Mar 20;27(9):1419-25. PMID: 19224846
- ClinicalTrials.gov (NCT00011986)
- Correction to Lancet Oncol 2022; 23: e374-84. Lancet Oncol. 2022 Sep;23(9):e404. PMID: 36055305
最終更新日 : 2024年8月3日
監修医師 : 日本医科大学 武蔵小杉病院 腫瘍内科教授 勝俣 範之先生
TC (PTX + CBDCA)
本コンテンツは特定の治療法を推奨するものではありません。 個々の患者の病態や、 実際の薬剤情報やガイドラインを確認の上、 利用者の判断と責任でご利用ください。
薬剤情報
【催吐性】 中等度催吐性
【FN発症】低リスク (<10%)
- タキソール® (添付文書¹⁾)
- パラプラチン® (添付文書²⁾)
用法用量
国際第III相試験³⁾のプロトコル

J Clin Oncol. 2009 Mar 20;27(9):1419-25³⁾より作図
電子添文の用法および用量
パクリタキセル : 1日1回210mg/m² を3時間かけて点滴静注し、 少なくとも3週間休薬。 タキソール®電子添文 (2023年7月改訂 第2版)¹⁾より引用
カルボプラチン : 1日1回300~400mg/m²を投与し、 少なくとも4週間休薬。 パラプラチン®電子添文 (2023年5月改訂 第3版)²⁾より引用
前投薬・投与スケジュール例
- DEX 9.9mg+ファモチジン 50mg+ 抗ヒスタミン薬+生食 100ml
- NK₁阻害剤+5HT₃拮抗剤+生食 50ml (30分)
- PTX 175mg/m²+5%ブ糖液 500mL (3時間)
- CBDCA+5%ブ糖液 250mL (30-60分)
日本医科大学 武蔵小杉病院 腫瘍内科教授 勝俣 範之先生提供
参考 : パクリタキセル電子添文¹⁾
投与約30分前までに投与を終了するように、 デキサメタゾンリン酸エステルナトリウム注射液 (デキサメタゾンとして8mg) 及びラニチジン塩酸塩注射液 (ラニチジンとして50mg) または注射用ファモチジン (ファモチジンとして20mg) を静脈内投与、 ジフェンヒドラミン塩酸塩錠 (ジフェンヒドラミン塩酸塩として50mg) を経口投与すること。
デキサメタゾンは初回投与時8mgとし、 次回投与時までに過敏症状の発現がみられなかった場合または臨床上特に問題のない過敏症状の場合は、 2週目の投与より半量 (4mg) に減量し投与してもよい。 以降の投与週においても同様の場合、 半量ずつ最低1mgまで減量し投与してもよい。
タキソール®電子添文 (2023年7月改訂 第2版)¹⁾より引用
投与開始基準
国際第III相試験³⁾のプロトコル

J Clin Oncol. 2009 Mar 20;27(9):1419-25³⁾より作図
KeyData|臨床試験結果
国際第III相試験³⁾⁴⁾
対象: ステージ III-IVの進行期上皮性卵巣癌および原発性腹膜癌患者4,312例
方法: TC (PTX+CBDCA)群
【有効性】 TC群
- mPFS 16.0ヵ月
- mOS 44.1ヵ月
【安全性】≧Grade3の主な有害事象
- 白血球数減少 50.8%
- 好中球数減少 86.9%
- 血小板数減少 22.4%
- 貧血 11.8%
- その他の血液疾患 18.1%
- アレルギー 4.4%
- 聴覚 0.6%
- 心臓血管 2.3%
- 凝固系 0.6%
- 全身状態 6.3%
- 皮膚 1.5%
- 胃腸 10.4%
- 泌尿生殖器/腎臓 1.0%
- 出血 0.9%
- 肝臓 1.5%
- 感染症/発熱 8.8%
- 代謝 7.1%
- 筋骨格 0.8%
- 神経学的 3.9%
- 末梢神経 5.2%
- 眼球/視覚 0.1%
- 痛み 6.1%
- 肺 2.2%
- 二次原発腫瘍 3.9%
J Clin Oncol. 2009 Mar 20;27(9):1419-25³⁾、 ClinicalTrials.gov (NCT00011986) ⁴⁾より引用
エキスパートによるワンポイント
初回治療の国際的標準
3週ごと6サイクルが基本的スケジュールです (第6回卵巣がん国際コンセンサスカンファレンス⁵⁾)
外来治療が可能
このレジメンで入院は不要です。 特に合併症があったりやPS不良でない限りは、 初回から外来治療がよいと思います。
監修 : 日本医科大学 武蔵小杉病院 腫瘍内科教授 勝俣 範之先生
出典
- クリニジェン株式会社. タキソール®電子添文 (2023年7月改訂 第2版) [最終閲覧 : 2024/03/27]
- クリニジェン株式会社. パラプラチン®電子添文 (2023年5月改訂 第3版) [最終閲覧 : 2024/03/27]
- Evaluation of new platinum-based treatment regimens in advanced-stage ovarian cancer: a Phase III Trial of the Gynecologic Cancer Intergroup. J Clin Oncol. 2009 Mar 20;27(9):1419-25. PMID: 19224846
- ClinicalTrials.gov (NCT00011986)
- Correction to Lancet Oncol 2022; 23: e374-84. Lancet Oncol. 2022 Sep;23(9):e404. PMID: 36055305
最終更新日 : 2024年8月3日
監修医師 : 日本医科大学 武蔵小杉病院 腫瘍内科教授 勝俣 範之先生
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
がん薬物療法における治療計画をまとめたものです。
主要論文や適正使用ガイドをもとにした用量調整プロトコール、 有害事象対応をご紹介します。
なお、 本ツールは医師向けの教育用資料であり、 実臨床での使用は想定しておりません。 最新の添付文書やガイドラインを必ずご確認下さい。
また、 一般の方への情報提供ではないことを予めご了承ください。