本コンテンツは特定の治療法を推奨するものではございません。 個々の患者の病態や、 実際の薬剤情報やガイドラインを確認の上、 利用者の判断と責任でご利用ください。
薬剤情報
タグリッソ®錠 (オシメルチニブ)
*アストラゼネカ株式会社の外部サイトへ遷移します
投与スケジュール
【1コース】連日内服投与
【催吐性】 最小度催吐性
【FN発症】低リスク
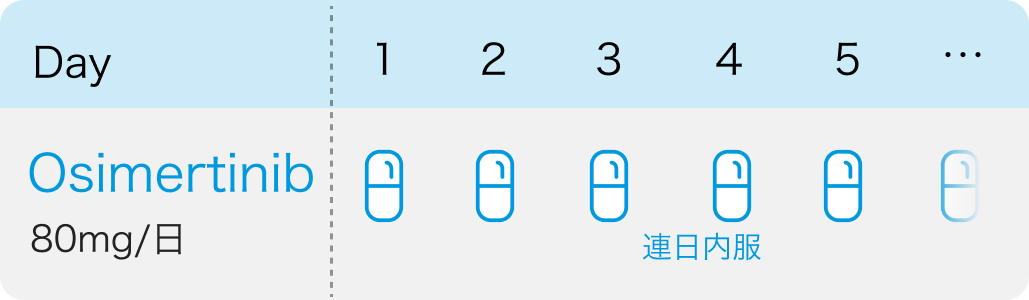
通常、 成人にはオシメルチニブとして80mgを1日1回経口投与。 患者の状態により適宜減量。
タグリッソ®電子添文¹⁾適正使用ガイド²⁾より作図
KeyData|臨床試験結果
FLAURA試験³⁾⁴⁾|1次治療
EGFR遺伝子変異陽性NSCLCの1次治療として、オシメルチニブと標準治療であるゲフィチニブまたはエルロチニブの有効性を比較した国際第Ⅲ相試験 (オシメルチニブ群 279例 vs 標準治療群 277例)
【有効性】オシメルチニブ群
- ORR : 80%
うち未治療T790M変異陽性7例中6例でPR
- mPFS : 18.9ヵ月
- mOS : 38.6ヵ月
【安全性】主な有害事象 (括弧内はGrade3~4)
- すべての有害事象 98% (32%)
- 皮疹またはざ瘡様皮疹 58% (1%)
- 下痢 58% (2%)
- 皮膚乾燥 36% (2%)
- 爪囲炎 35% (<1%)
- 口内炎 29% (<1%)
- 食欲不振 20% (3%)
- 掻痒症 17% (<1%)
- 咳嗽 10% (0%)
- 便秘 15% (0%)
- 悪心 14% (0%)
- 疲労 14% (1%)
- 呼吸困難 13% (<1%)
- 貧血12% (1%)
- 頭痛 12% (<1%)
- 嘔吐 11% (0%)
- 上気道感染 10% (0%)
- 発熱 10% (0%)
- QT延長 10% (3%)
AURA3試験⁵⁾⁶⁾|2次治療~T790M陽性
EGFR-TKI耐性後 T790M変異陽性となった進行NSCLC患者を対象に、 オシメルチニブとプラチナ製剤併用療法 (CDDP/CBDCA+PEM) を比較した国際第Ⅲ相試験 (オシメルチニブ群 279例 vs プラチナ製剤併用群 140例)
【有効性】オシメルチニブ群
- ORR : 71.0%
- mPFS : 10.1ヵ月
- mOS : 22.7ヵ月
【安全性】主な有害事象 (括弧内はGrade3~4)
- 下痢 41% (1%)
- 皮疹 34% (1%)
- 皮膚乾燥 23% (0%)
- 爪囲炎 22% (0%)
- 悪心 16% (1%)
- 食欲不振 18% (1%)
- 便秘 14% (0%)
- 貧血 8% (1%)
各プロトコル
適格基準例
投与開始前に、 間質性肺炎、 肝機能障害、 QT延長がないことを確認する。
参考 : AURA、AURA2、AURA3試験の骨髄・臓器機能基準

タグリッソ®適正使用ガイド²⁾より作図
減量の目安

初回投与量80mg/日、1段階減量40mg/日
タグリッソ®電子添文情報¹⁾を基に編集部作表
有害事象発現時の用量調節基準
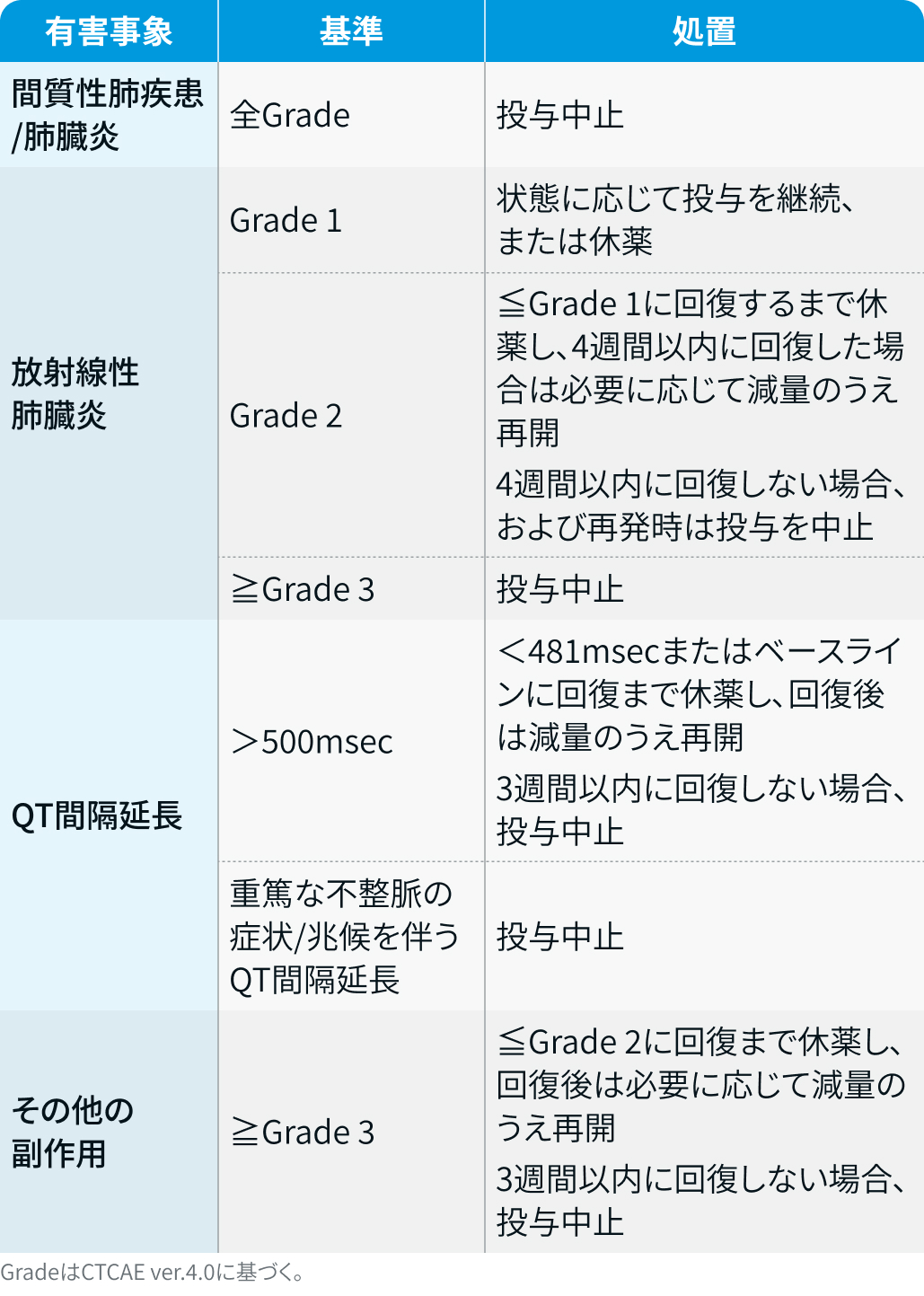
タグリッソ®電子添文情報¹⁾を基に編集部作表
レジメンの特徴と注意点
効能又は効果
1次治療としての推奨だけでなく、 AURA3試験より「他のEGFR-TKI使用後に、T790M耐性遺伝子変異が出現したNSCLC*」 にも有効性が示されている。
*他のEGFR-TKI使用後では再生検もしくはリキッドバイオプシーでT790M変異を検出した症例例のみ使用可
遺伝子パネル検査・コンパニオン診断
日本肺癌学会の各種手引きやHOKUTO編集部のまとめコンテンツを参照すること。
肺癌遺伝子パネル検査・コンパニオン診断薬一覧ページへ遷移
有害事象の特徴
日本人の薬剤性肺障害の発現割合は全集団より高い傾向が見られた。 また、 ICI投与歴がある場合、 薬剤性肺障害の発現率が高いことや一過性無症候性肺陰影 (TAPO) が報告されている。
Chest 2022 : オシメルチニブ起因の薬剤性肺炎発症率18%、半数はTAPO の記事を読む
肺癌診療ガイドライン2025⁹⁾
オシメルチニブ単剤療法は、 EGFR遺伝子変異陽性かつPS 0–1の1次治療として「強く推奨」(1A) されている。 また、 エクソン18–21遺伝子変異陽性例および未治療T790M変異陽性例には「弱く推奨」(2C)、 1次治療以降の耐性化または増悪後のT790M変異陽性例には「強く推奨」(2D) されている。
出典
- アストラゼネカ株式会社. タグリッソ®電子添文. 2026年01月改訂 第8版.
- アストラゼネカ株式会社. タグリッソ®適正使用ガイド. 2025年10月作成
- N Engl J Med. 2018;378(2):113-125.
- N Engl J Med. 2020;382(1):41-50.
- N Engl J Med. 2017;376(7):629-640.
- Ann Oncol. 2020;31(11):1536-1544.
- J Clin Oncol. 2023;41(10):1830-1840.
- N Engl J Med. 2023;389(2):137-147.
- 日本肺癌学会. 肺癌診療ガイドライン-胸膜中皮腫・ 胸腺腫瘍含む-2025年版
最終更新日 : 2026年1月13日
監修・作図 : HOKUTO編集部専門医
Osimertinib
本コンテンツは特定の治療法を推奨するものではございません。 個々の患者の病態や、 実際の薬剤情報やガイドラインを確認の上、 利用者の判断と責任でご利用ください。
薬剤情報
タグリッソ®錠 (オシメルチニブ)
*アストラゼネカ株式会社の外部サイトへ遷移します
投与スケジュール
【1コース】連日内服投与
【催吐性】 最小度催吐性
【FN発症】低リスク

通常、 成人にはオシメルチニブとして80mgを1日1回経口投与。 患者の状態により適宜減量。
タグリッソ®電子添文¹⁾適正使用ガイド²⁾より作図
KeyData|臨床試験結果
FLAURA試験³⁾⁴⁾|1次治療
EGFR遺伝子変異陽性NSCLCの1次治療として、オシメルチニブと標準治療であるゲフィチニブまたはエルロチニブの有効性を比較した国際第Ⅲ相試験 (オシメルチニブ群 279例 vs 標準治療群 277例)
【有効性】オシメルチニブ群
- ORR : 80%
うち未治療T790M変異陽性7例中6例でPR
- mPFS : 18.9ヵ月
- mOS : 38.6ヵ月
【安全性】主な有害事象 (括弧内はGrade3~4)
- すべての有害事象 98% (32%)
- 皮疹またはざ瘡様皮疹 58% (1%)
- 下痢 58% (2%)
- 皮膚乾燥 36% (2%)
- 爪囲炎 35% (<1%)
- 口内炎 29% (<1%)
- 食欲不振 20% (3%)
- 掻痒症 17% (<1%)
- 咳嗽 10% (0%)
- 便秘 15% (0%)
- 悪心 14% (0%)
- 疲労 14% (1%)
- 呼吸困難 13% (<1%)
- 貧血12% (1%)
- 頭痛 12% (<1%)
- 嘔吐 11% (0%)
- 上気道感染 10% (0%)
- 発熱 10% (0%)
- QT延長 10% (3%)
AURA3試験⁵⁾⁶⁾|2次治療~T790M陽性
EGFR-TKI耐性後 T790M変異陽性となった進行NSCLC患者を対象に、 オシメルチニブとプラチナ製剤併用療法 (CDDP/CBDCA+PEM) を比較した国際第Ⅲ相試験 (オシメルチニブ群 279例 vs プラチナ製剤併用群 140例)
【有効性】オシメルチニブ群
- ORR : 71.0%
- mPFS : 10.1ヵ月
- mOS : 22.7ヵ月
【安全性】主な有害事象 (括弧内はGrade3~4)
- 下痢 41% (1%)
- 皮疹 34% (1%)
- 皮膚乾燥 23% (0%)
- 爪囲炎 22% (0%)
- 悪心 16% (1%)
- 食欲不振 18% (1%)
- 便秘 14% (0%)
- 貧血 8% (1%)
各プロトコル
適格基準例
投与開始前に、 間質性肺炎、 肝機能障害、 QT延長がないことを確認する。
参考 : AURA、AURA2、AURA3試験の骨髄・臓器機能基準

タグリッソ®適正使用ガイド²⁾より作図
減量の目安

初回投与量80mg/日、1段階減量40mg/日
タグリッソ®電子添文情報¹⁾を基に編集部作表
有害事象発現時の用量調節基準

タグリッソ®電子添文情報¹⁾を基に編集部作表
レジメンの特徴と注意点
効能又は効果
1次治療としての推奨だけでなく、 AURA3試験より「他のEGFR-TKI使用後に、T790M耐性遺伝子変異が出現したNSCLC*」 にも有効性が示されている。
*他のEGFR-TKI使用後では再生検もしくはリキッドバイオプシーでT790M変異を検出した症例例のみ使用可
遺伝子パネル検査・コンパニオン診断
日本肺癌学会の各種手引きやHOKUTO編集部のまとめコンテンツを参照すること。
肺癌遺伝子パネル検査・コンパニオン診断薬一覧ページへ遷移
有害事象の特徴
日本人の薬剤性肺障害の発現割合は全集団より高い傾向が見られた。 また、 ICI投与歴がある場合、 薬剤性肺障害の発現率が高いことや一過性無症候性肺陰影 (TAPO) が報告されている。
Chest 2022 : オシメルチニブ起因の薬剤性肺炎発症率18%、半数はTAPO の記事を読む
肺癌診療ガイドライン2025⁹⁾
オシメルチニブ単剤療法は、 EGFR遺伝子変異陽性かつPS 0–1の1次治療として「強く推奨」(1A) されている。 また、 エクソン18–21遺伝子変異陽性例および未治療T790M変異陽性例には「弱く推奨」(2C)、 1次治療以降の耐性化または増悪後のT790M変異陽性例には「強く推奨」(2D) されている。
出典
- アストラゼネカ株式会社. タグリッソ®電子添文. 2026年01月改訂 第8版.
- アストラゼネカ株式会社. タグリッソ®適正使用ガイド. 2025年10月作成
- N Engl J Med. 2018;378(2):113-125.
- N Engl J Med. 2020;382(1):41-50.
- N Engl J Med. 2017;376(7):629-640.
- Ann Oncol. 2020;31(11):1536-1544.
- J Clin Oncol. 2023;41(10):1830-1840.
- N Engl J Med. 2023;389(2):137-147.
- 日本肺癌学会. 肺癌診療ガイドライン-胸膜中皮腫・ 胸腺腫瘍含む-2025年版
最終更新日 : 2026年1月13日
監修・作図 : HOKUTO編集部専門医
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
がん薬物療法における治療計画をまとめたものです。
主要論文や適正使用ガイドをもとにした用量調整プロトコール、 有害事象対応をご紹介します。
なお、 本ツールは医師向けの教育用資料であり、 実臨床での使用は想定しておりません。 最新の添付文書やガイドラインを必ずご確認下さい。
また、 一般の方への情報提供ではないことを予めご了承ください。