HOKUTO編集部
2年前
【解説】乳癌周術期治療の最新トピックス~ESMO報告のKN-522のOS最終解析を受けて~

9月13~17日に開催された欧州臨床腫瘍学会 (ESMO 2024) では、 乳癌領域における注目演題が多数報告されました。 本稿では注目演題をがん研有明病院乳腺内科医長の尾崎由記範先生にご解説いただきました。
ESMO 2024 乳癌領域の重要演題
周術期、 転移再発例ともに以下のように多くの興味深い発表があった。 本稿では、 ESMO 2024でアップデートがあったKEYNOTE-522試験の報告を中心に、 乳癌周術期治療の最新トピックスについて紹介したい。
周術期
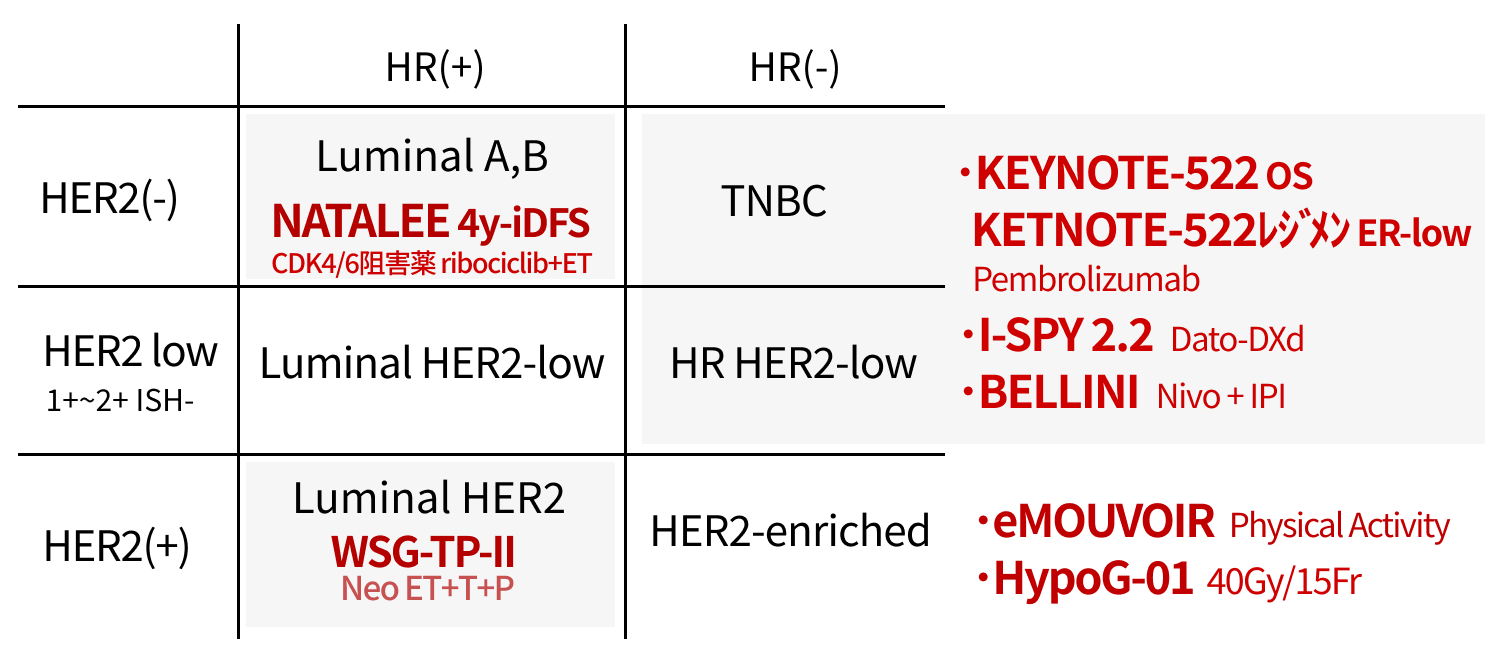
現時点では保険外の内容も含む(各試験を参考に尾崎氏作成)
転移・再発
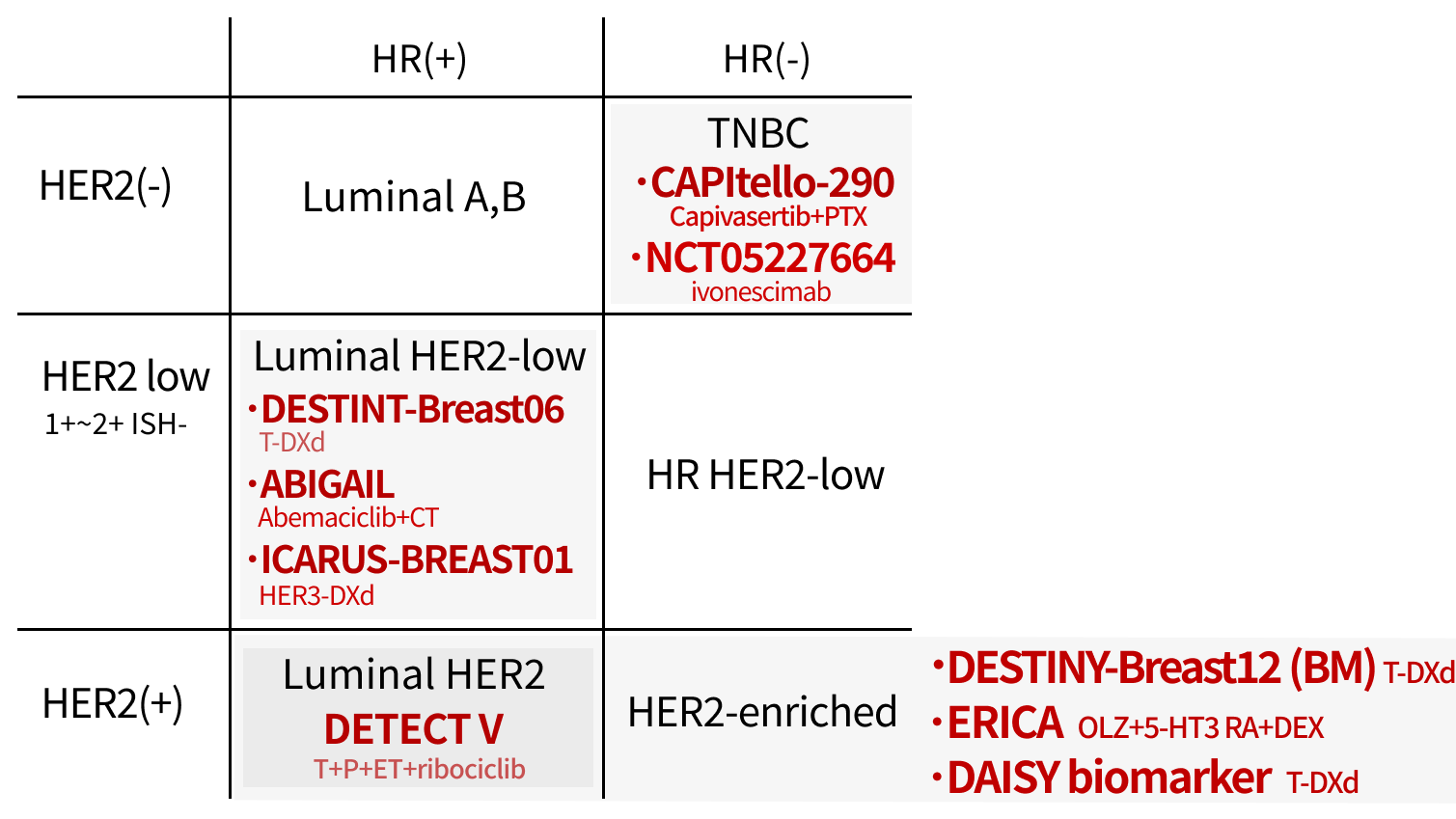
現時点では保険外の内容も含む(各試験を参考に尾崎氏作成)
周術期治療の変遷
KN-522の結果から、 周術期ペムブロリズマブが切除可能TNBCの標準治療に
切除可能TNBCに対する標準薬物療法としては、 アントラサイクリン系 / タキサン系を中心とした術前または術後化学療法がある。 近年では、 術前化学療法後、 病理学的に残存病変がある患者に対するカペシタビンやPARP阻害薬オラパリブ投与の有効性が示され、 世界的に標準治療となっている。
さらに最近では、 第Ⅲ相KEYNOTE-522試験の結果を受けて、 術前・術後ペムブロリズマブ投与の有効性が示され、 ICIを用いた周術期治療が標準治療となった。
KN-522のOS最終解析結果が報告
既報結果を基に本邦でも2022年9月承認
KEYNOTE-522試験の対象は、 cT1c N1-2、 T2-4 N0-2 (主にStage II-III) の再発高リスクTNBCであり、 1,174例が以下の2群に2:1で無作為に割り付けられた。
・ペムブロリズマブ群
パクリタキセル+カルボプラチン+ペムブロリズマブ→ドキソルビシン+シクロホスファミド(AC)またはエピルビシン+シクロホスファミド(EC)+ペムブロリズマブ→手術→ペムブロリズマブ
・プラセボ群
パクリタキセル+カルボプラチン+プラセボ→ACまたはEC+プラセボ→手術→プラセボ
主要評価項目は病理学的完全奏効 (pCR)率および無イベント生存期間 (EFS)だった。
試験の結果、 pCR率はペムブロリズマブ群64.8%、 プラセボ群51.2% (p=0.00055)、 EFSもHR0.63 (95% CI 0.48-0.82) と、 いずれも有意に改善した。 この結果から、 日本においても術前ペムブロリズマブ+化学療法と術後ペムブロリズマブ単剤療法の治療レジメンは2022年9月に承認されている。
6年以上の長期成績でも死亡リスクを34%低減、 周術期ICIをさらに支持
ESMO 2024では、 主要副次評価項目であるOSの最終結果について、 追跡期間中央値75.1ヵ月の長期成績が報告された。
OSはHR 0.66 (95%CI 0.50-0.87、 p=0.0015)であり、 ペムブロリズマブ群で有意に改善した。 5年OS率はペムブロリズマブ群が86.6%で、 プラセボ群 (81.7%) に比べ約5%㌽の差があった。
OSのサブグループ解析では、 リンパ節転移の有無、 腫瘍径、 カルボプラチンのスケジュール、 PD-L1などの因子に関わらず、 ペムブロリズマブ群におけるOSの改善効果が一貫して示された。 また、 ペムブロリズマブ群の免疫関連有害事象 (irAE) の発現率は、 Grade3以上が13%、 全Gradeが35%で、 治療中止に至った頻度は7.7%と報告された。
主要評価項目であるEFSの結果から、 再発高リスクTNBCに対する術前・術後ペムブロリズマブは既に世界の標準治療となっているが、 ESMO 2024のOSデータから、 さらにその臨床的意義が大きいものになったと考える。
追加解析の臨床試験が現在も進行中
なお、 さらなる予後改善を目的として、 pCR症例に対する術後ペムブロリズマブの省略や、 non-pCR症例に対する強化治療などを評価する臨床試験が現在も複数進行中であり、 結果が待たれる。 また、 irAEのマネジメントや予測、 患者選択などに対するさらなる研究も期待されている。
その他の周術期ICIに関する臨床試験も進行中
ペムブロリズマブ以外のICIを用いた代表的な試験として、 抗PD-L1抗体アテゾリズマブの術前投与の有効性を評価したIMpassion031試験、 および同薬の術後投与の有効性を評価したIMpassion030試験が挙げられる。 両試験について概説する。
術前アテゾリズマブ上乗せはpCRを達成もEFS改善せず : IMpassion031
IMpassion031試験は、 Stage II-IIIの早期TNBCを対象とした第III相無作為化比較試験である。 333例が登録され、 アテゾリズマブ群 (ナブパクリタキセル+アテゾリズマブ→dose dense AC療法+アテゾリズマブ→手術→アテゾリズマブ) とプラセボ群 (ナブパクリタキセル+プラセボ→dose dense AC療法+プラセボ→手術→経過観察) の2群に1:1で無作為に割り付けられた。
主要評価項目であるpCR率はアテゾリズマブ群が57.6%であり、 プラセボ群の41.1%に比べて有意な改善を示した (p=0.0044)。 ただし、 EFSはHR 0.76 (95%CI 0.40-1.44)と有意差が示されなかった。
術後アテゾリズマブ上乗せはiDFSを改善せず : IMpassion030
IMpassion030試験は、 IMpassion031試験と同様にStage II-IIIの早期TNBCを対象とした第Ⅲ相無作為化比較試験である。 2,199例が登録され、 アテゾリズマブ群 (術後パクリタキセル+アテゾリズマブ→dose dense AC/EC療法+アテゾリズマブ) と化学療法群 (術後パクリタキセル→dose dense AC/EC療法) の2群に1:1で無作為に割り付けられた。
観察期間中央値25ヵ月時点において、 主要評価項目である無浸潤疾患生存期間 (iDFS) はHR 1.12 (95%CI 0.87-1.45)と報告され、 これを受けて同試験は中止された。 なお、 本結果はサンアントニオ乳癌シンポジウム (SABCS) 2023にて報告された。
周術期アテゾリズマブの有効性は現在も検証中
これらの結果から、 TNBCにおける周術期アテゾリズマブは依然として承認に至っていないが、 現在、 術前・術後アテゾリズマブの有効性を評価する第III相二重盲検無作為化比較試験GeparDouze/NSABP B-59が進行中であり、 結果が期待されている。
解説医師

関連コンテンツ



編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。