HOKUTO編集部
1年前
【特集】造血器腫瘍遺伝子パネル 「実装への期待と課題」

2025年3月1日、 国内初の造血器腫瘍専用の遺伝子パネル検査 「ヘムサイト®」 が大塚製薬より発売されました。 いよいよ始まる造血器腫瘍ゲノム診療について、 福井大学の今村善宣先生に解説いただきました。
はじめに
ヘムサイト®が保険適用を取得し、 国内で本格的な造血器腫瘍ゲノム診療が始まる。 造血器腫瘍に対するがんゲノムプロファイリング検査は、 固形がん以上に診断や予後予測、 治療選択に大きく貢献し、 特に急性白血病など致死的な進行をたどりやすい疾患においては待望のツールといえる。
本稿では、 保険適用となった造血器腫瘍パネルのメリットや想定される患者フロー、 運用上の課題と今後の展望を示す。
造血器腫瘍ゲノム診療の意義
造血器腫瘍におけるゲノム検査の必要性
造血器腫瘍では、 固形がんと比較して診断や予後予測にゲノム情報が強く関わる。 例えば急性骨髄性白血病 (AML) や急性リンパ性白血病 (ALL)、 骨髄異形成症候群 (MDS) などの疾患は、 特定の遺伝子異常が治療方針や造血幹細胞移植適応に直結する。
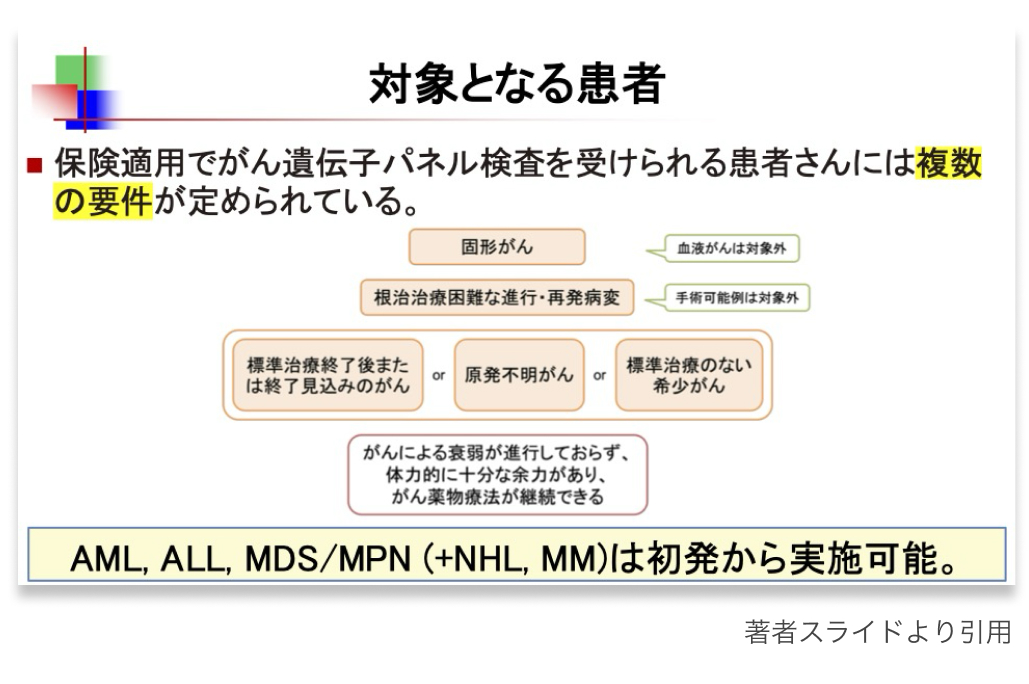
ヘムサイト®の登場により、 AMLやALL、 MDS、 骨髄増殖性疾患、 非ホジキンリンパ腫、 多発性骨髄腫などを対象に、 初発時や再発時、 原因不明の血球減少例でも検査実施が可能となった。 これにより、 初発時からの包括的な遺伝子解析が可能となり、 鑑別困難症例や原因不明の血球減少症例でも、 造血器腫瘍の確定診断にゲノム情報を活用できるようになる。
ヘムサイト®の概要

造血器腫瘍専用の次世代シーケンス (NGS) パネルとして開発されたヘムサイト®は、 体外診断用医薬品 (ヘムサイト診断薬) と医療機器プログラム (ヘムサイト解析プログラム) から構成されており、 造血器腫瘍の腫瘍細胞や骨髄液など多彩な検体に対応できる点が特長である。
2025年3月時点で、 がんゲノム医療中核拠点病院・拠点病院・連携病院である279病院で導入の準備が進められている。
ヘムサイト®の保険適用の対象や条件、 点数などの基本情報を以下に示す。
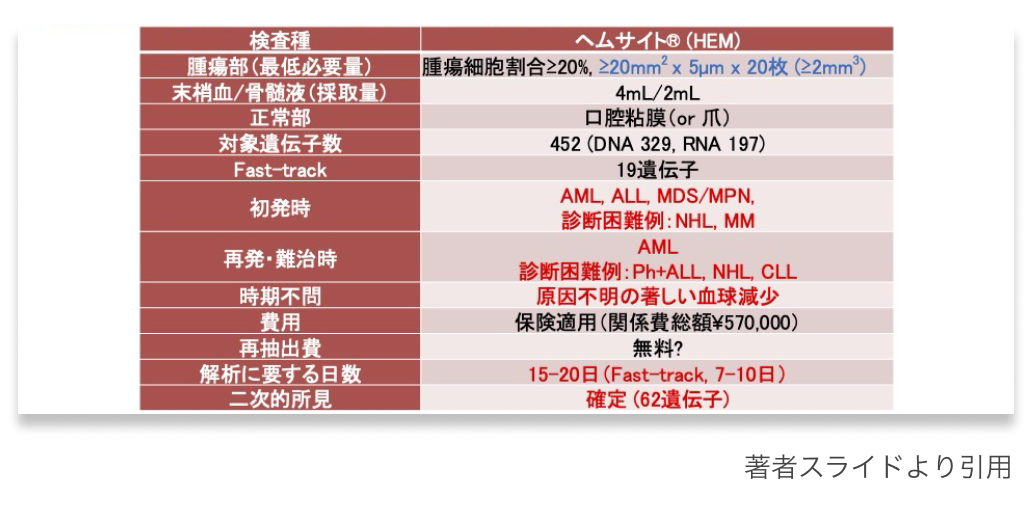
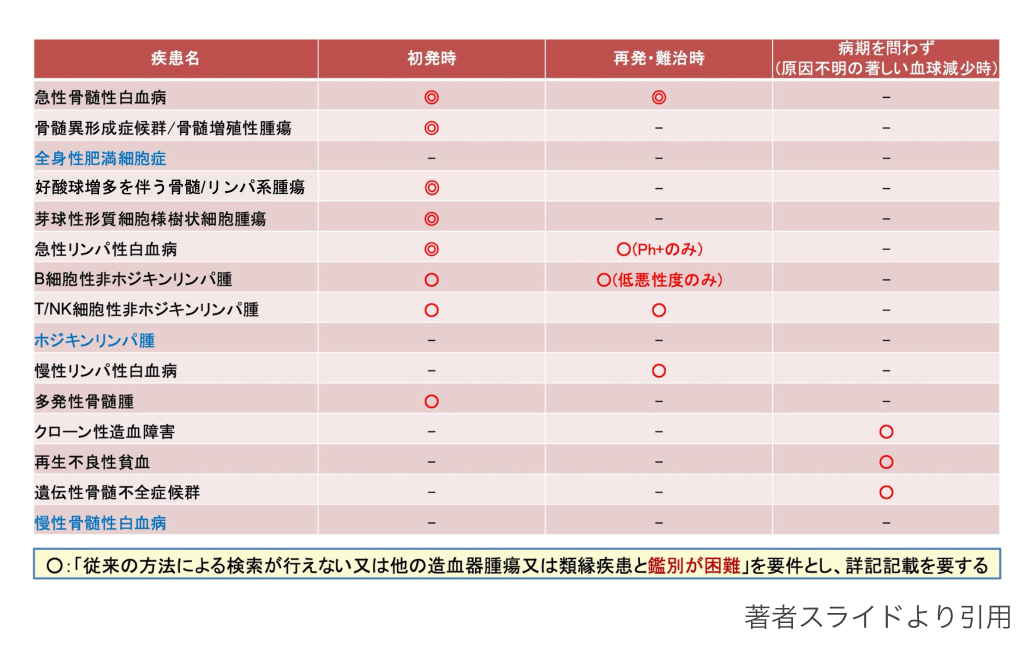
遺伝子パネル検査の概要と運用
3つの主要な役割
遺伝子パネル検査は①診断、 ②予後予測、 ③治療選択という3つの役割を担っているが、 造血器腫瘍遺伝子パネル検査は固形がんと異なり①と②の比重が高い。
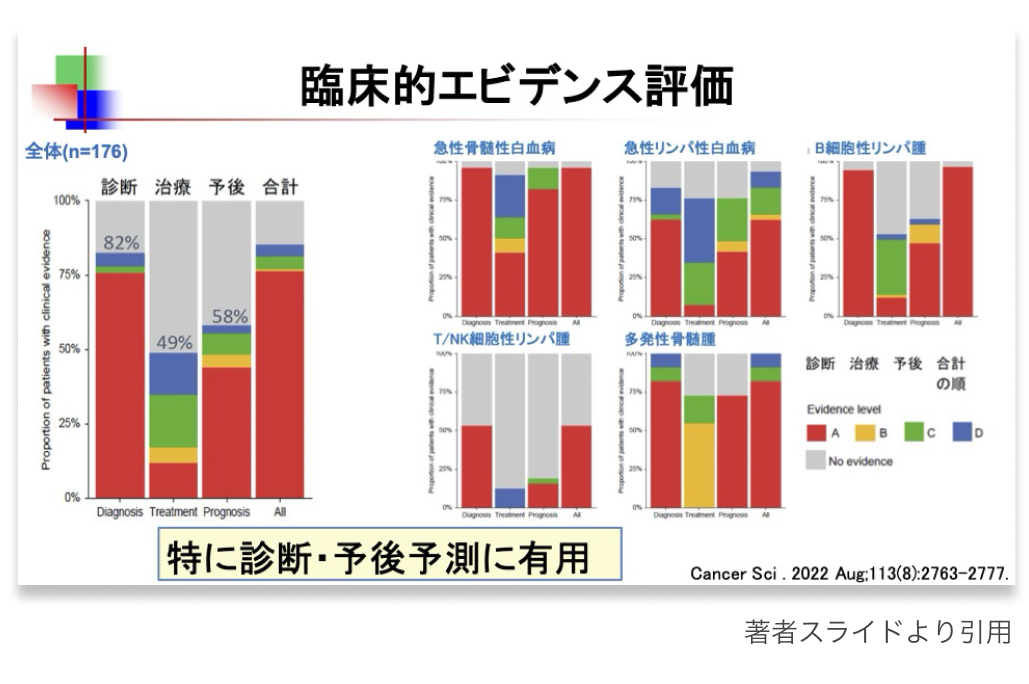
これらの情報は、 造血器腫瘍の治療計画の策定において非常に重要であり、 特に移植適応の判断や分子標的薬の適用可否の決定に直結する。 遺伝子パネル検査の導入によって、 治療の個別化が一層進むことが期待される。
①診断 : 原因不明の血球減少
実臨床では、 原因不明の汎血球減少や骨髄異常所見がみられる場合、 再生不良性貧血やMDS、 先天性骨髄不全症候群など複数の鑑別疾患を想定する。 しかし、 形態学的評価や個別遺伝子検査のみでは確定に至らない症例もある。
本パネルの包括的な変異検索によって、 これらをより的確に絞り込み、 適切な治療方針を迅速に立案しやすくなる。

②予後予測 : AMLの移植適応判断
AMLは、 特定の遺伝子異常が移植適応や予後層別に直結する。 白血病キメラ遺伝子スクリーニング検査などに加え、 網羅的な遺伝子パネル解析を用いることで、 より幅広い遺伝子異常の有無を把握でき、 再発リスクや治療反応性をより精緻に評価できる。
「強度の高い治療を実施するか否か」 という重要な判断において、 より確かな臨床的根拠を提供することができる。

③治療選択 : 分子標的薬の適応決定
近年、 AMLにおけるFLT3阻害薬やIDH阻害薬、 リンパ腫におけるEZH2阻害薬など、 造血器腫瘍の分子標的薬が相次いで登場している。
本パネルにより、 こうした重要なドライバー遺伝子変異を一括で探索できる点は大きなメリットである。
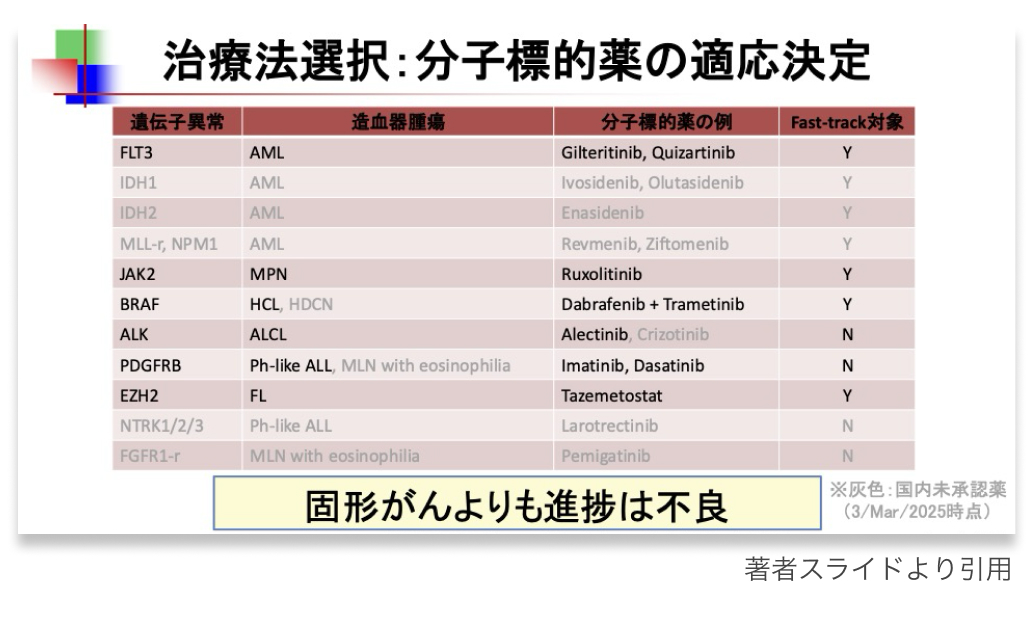
なお、 本パネルでは、 臨床上重要とされる19のFast-track対象遺伝子異常*が設定されており、 これらの異常に関しては7~10日程度で速報が得られる。
*日本血液学会が策定した 「造血器腫瘍ゲノム検査ガイドライン 2023年度版」 において、 「迅速結果返却が望ましい遺伝子異常」 と定義された遺伝子異常。 なお、 「造血器腫瘍ゲノム検査ガイドライン」 はアップデートが予定されているため、 随時確認が必要である。
急性期の診療が必要な症例において、 標準検査では把握できなかった情報を早期に取得し、 治療方針を迅速に決定できる意義は大きい。


検査実施フローと検体管理
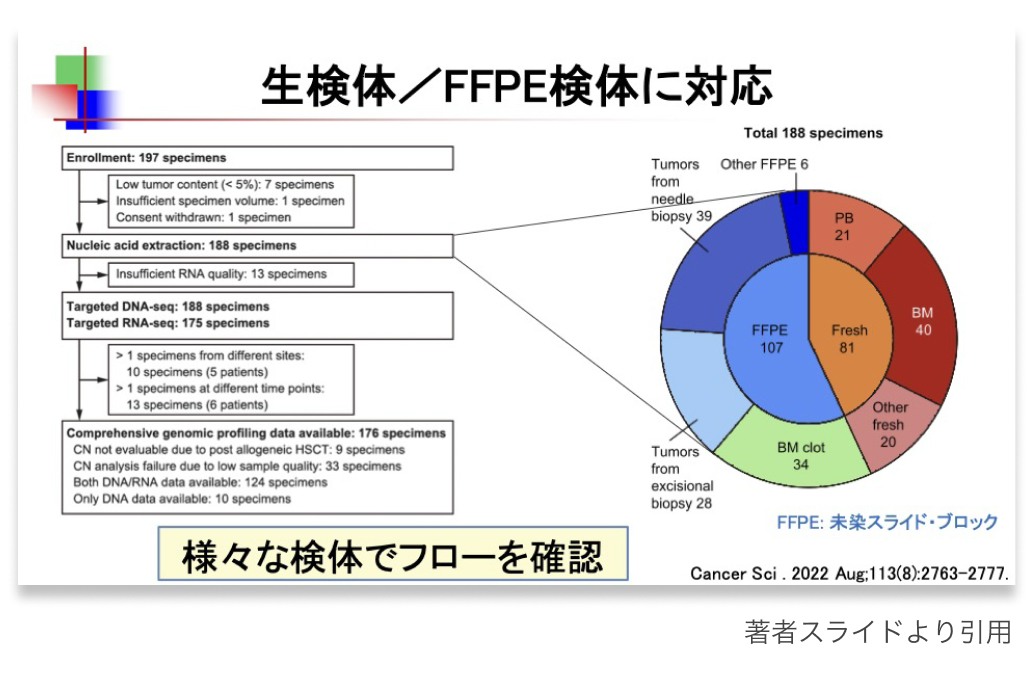
造血器腫瘍では、 骨髄検査やリンパ節生検だけでなく、 末梢血や体腔液、 過去のFFPE検体など、 多様な検体が使用される。 そのため、 検体採取手順や保管方法を施設全体で統一し、 検査部門と連携して運用フローを整備することが求められる。
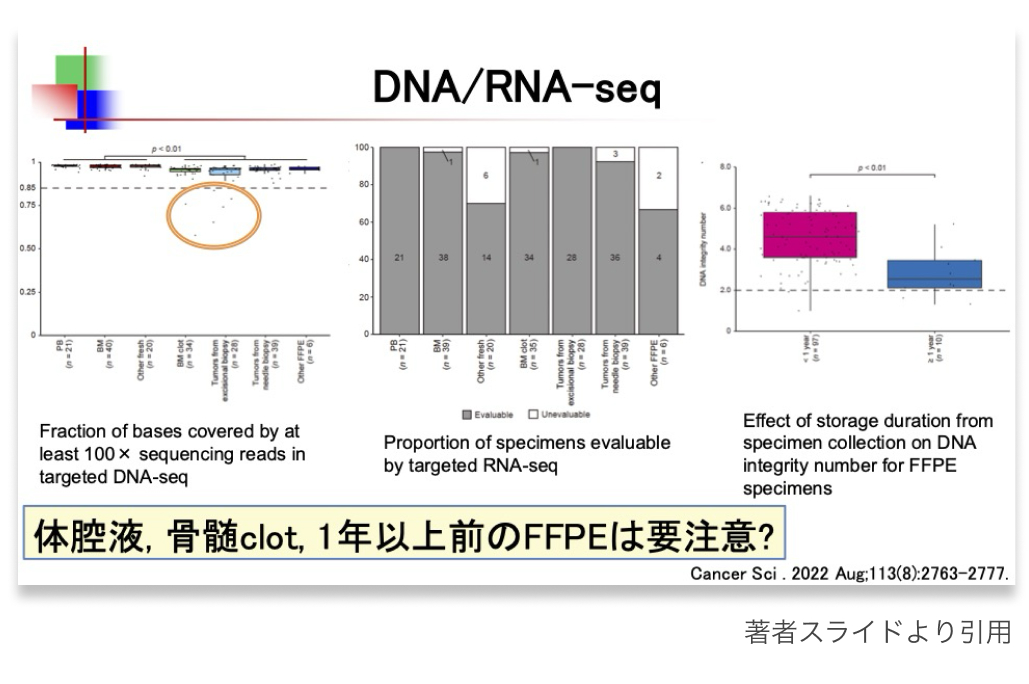
特に骨髄クロットや1年以上前のFFPEブロックはDNA/RNAの品質が低下しやすく、 結果の再現性が下がる恐れがあるため注意が必要である。
保険算定とDPC特例
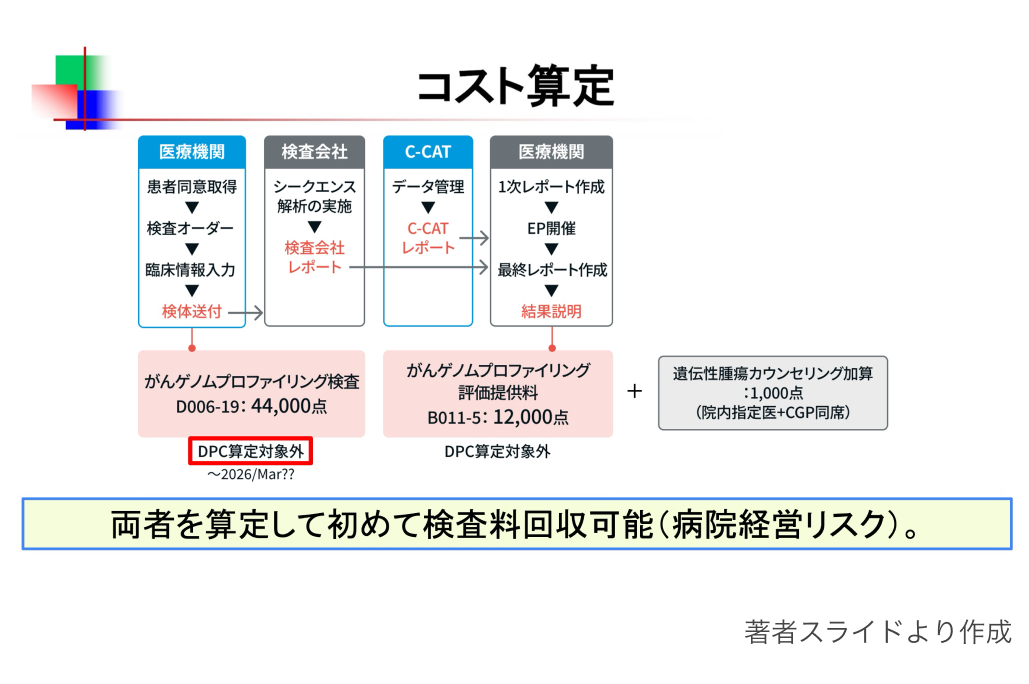
造血器腫瘍遺伝子パネル検査は、 2025年3月1日より4万4,000点での保険算定が可能となり、 従来のがんゲノムプロファイリング検査 (D006-19) を準用する形で請求が行える。
ただし、 造血器腫瘍は固形がんと異なり、 急速に進行し致死的な経過をたどる症例が多いことから、 入院下での検査実施の必要性が高い。 このため、 造血器腫瘍遺伝子パネル検査ではDPC対象外になる見通しである*。
*急性白血病 (130010)、 非ホジキンリンパ腫 (130030)、 多発性骨髄腫 (130040)、 骨髄増殖性腫瘍 (130050)、 骨髄異形成症候群 (130060)、 再生不良性貧血 (130080) などの診断群分類に該当する患者については、 次期診療報酬改定までの間、 特例的に出来高算定が認められる。
今後、 本検査の普及に伴い、 診療報酬体系のさらなる調整や、 DPC制度における算定基準の見直しが進められる可能性がある。 特に、 エキスパートパネル (EP) を含む検討体制の構築や、 検査結果を迅速に治療方針へ反映させるための運用改善が求められる。
造血器腫瘍パネルの課題
固形がんゲノム医療との相違点
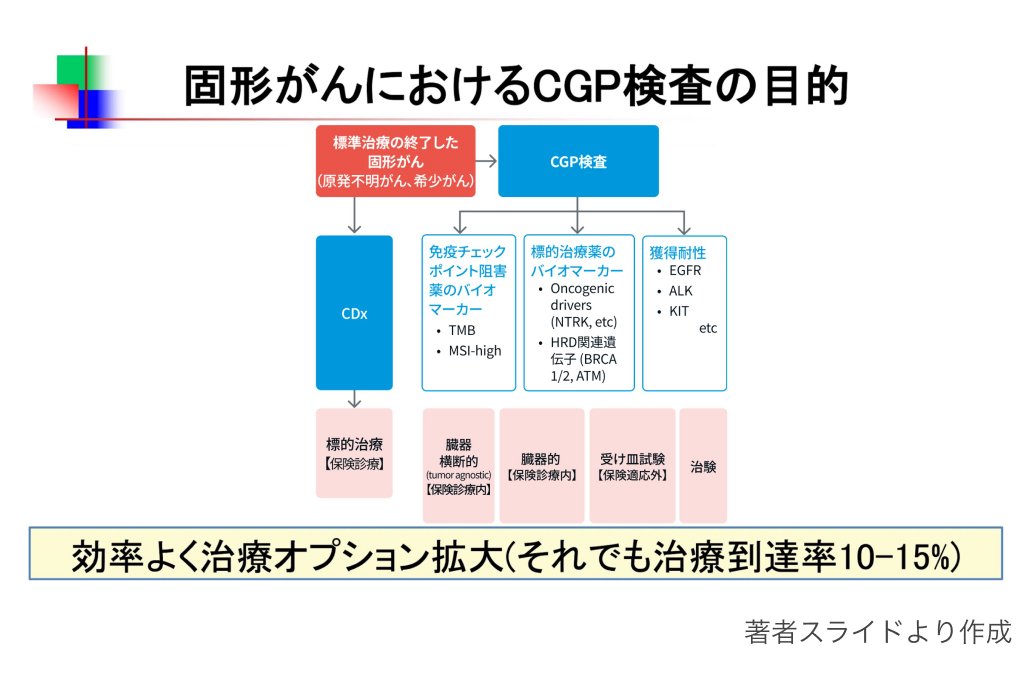
造血器腫瘍ゲノム検査が初発時から診断・予後の層別化に大きく寄与するのに対し、 固形がんゲノム検査では、 主に 「標準治療が適用できない患者の新たな治療選択肢の探索」 を目的とすることが多い。 したがって、 造血器腫瘍とは検査実施のタイミングや目的が大きく異なるといえる。
一方で、 いずれの領域においてもゲノム情報に基づく新規薬剤の開発余地は大きく、 新薬や治験体制のさらなる充実が求められる。
運用上の課題
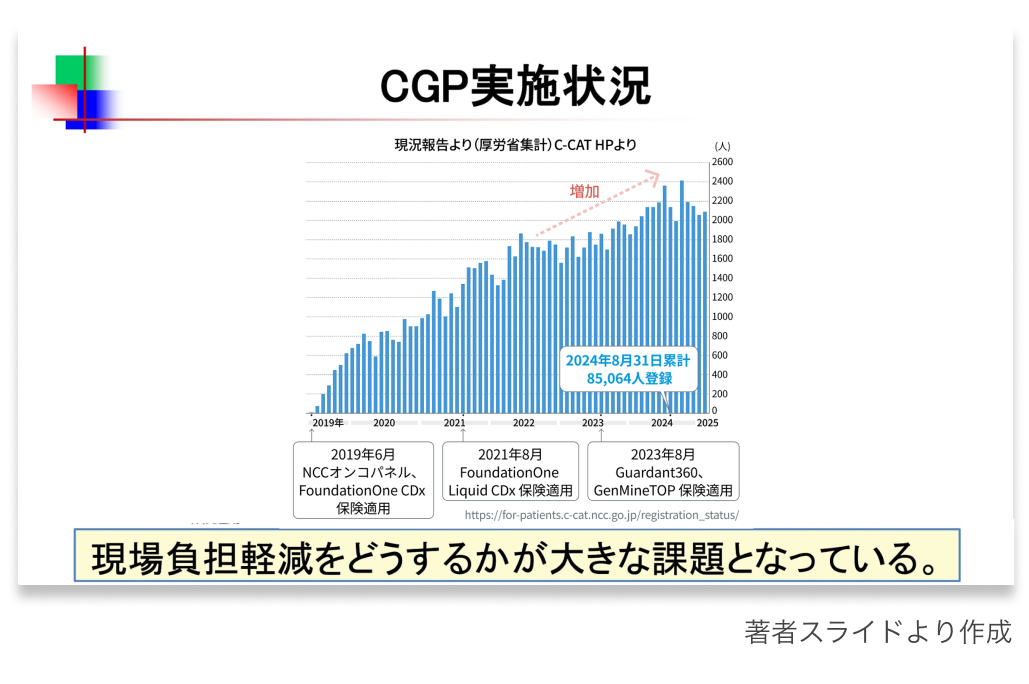
①ゲノム外来・検体受付体制
急性に進行する症例が少なくない造血器腫瘍では、 検査依頼から結果開示までの時間を可能な限り短縮し、 遅滞なく対応できる体制の整備が不可欠である。
実際、 患者フロー (入院/外来) や検体フロー (腫瘍組織 : 末梢血・骨髄液・FFPE検体・その他、 正常組織 : 口腔ぬぐい液・爪など) は多岐にわたり複雑であり、 それらを円滑に処理する運用設計が求められる。
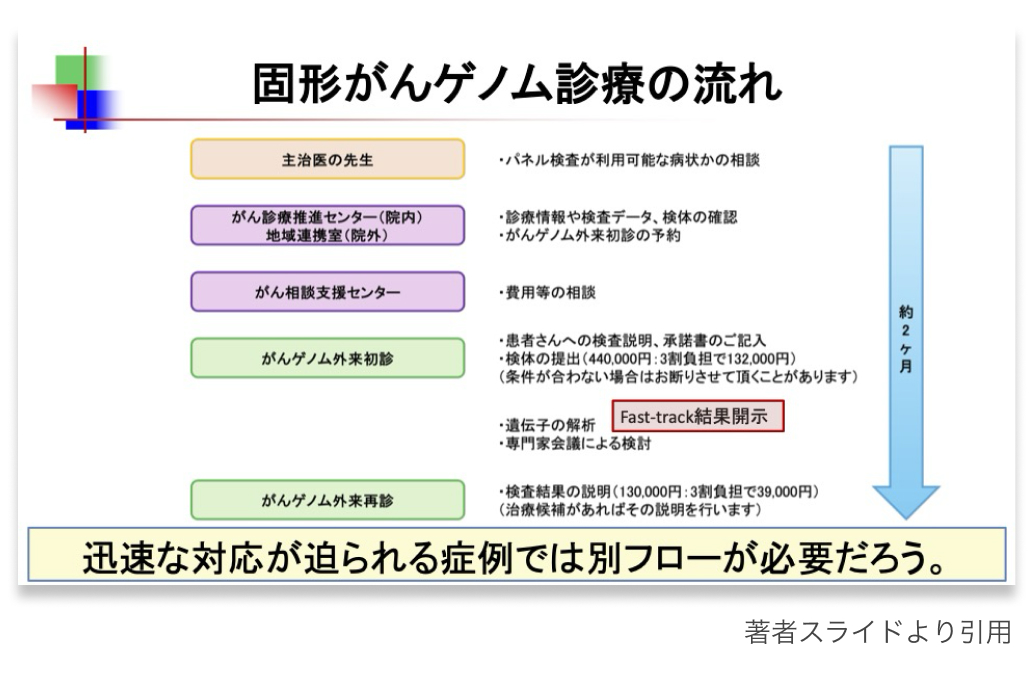

②エキスパートパネル (EP) の役割
検出された遺伝子変異の臨床的意義を評価し、 治療提案に反映させるために、 多職種が集まる専門家会議を設ける点は、 固形がんでも造血器腫瘍でも共通している。 ただし、 造血器腫瘍では急性期対応が多いことから、 検討回数の増加や検討サイクルの短縮も検討される。
また、 固形がんで 「がん薬物療法の専門医」 が必須構成員とされていたように、 造血器腫瘍では 「造血器腫瘍の専門医」 が中心的な役割を担うこととなる。


③C-CAT (がんゲノム情報レポジトリ) 入力
がんゲノム検査の結果に加えて、 患者の臨床情報や治療情報をC-CATに集約する流れは固形がんと共通している。 しかし造血器腫瘍ゲノムでは、 血液検査やリスクスコア、 細胞表面抗原などの特有の情報も入力対象となるため、 現場では固形がん以上に入力内容の把握と対応が求められる。
また、 造血器腫瘍ゲノム検査開始による対象患者数の増加に伴い、 今後さらに入力作業の負担が増すことが予想される。 臨床現場の負担軽減とデータ品質向上を両立する体制づくりが重要である。
固形がんとの対比について以下の表にまとめる。 類似点より相違点の方が多い。

今後の展望
今回の造血器腫瘍ゲノムパネル検査の保険償還は、 診療現場に大きな変革をもたらすと考えられる。
診断・予後予測・治療法選択を幅広く支援する一方で、 検体採取や検査部門との連携、 EPの開催、 C-CATへの登録など、 医療機関側の運用体制整備が急務である。
特に急性期患者が多い領域であるだけに、 迅速性と精度を両立する院内システムを構築することが重要である。 さらに、 病院間の連携体制を整備し、 情報共有を円滑に行うことで、 患者にとって最適な医療提供が可能となる。
今後はFast-track対応を含むさらなる研究開発や適切な治験導入により、 分子標的薬の適応拡大が期待される。 固形がんゲノム診療で培われた知見を活かしつつ、 造血器腫瘍に特化した運用モデルを確立することが重要である。
<参考文献>
・日本血液学会 : 造血器腫瘍ゲノム検査ガイドライン (2023年年度版)
・日本血液学会 : 造血器腫瘍における遺伝子パネル検査体制のあり方とその使用指針 (2023年 5月31日更新)
・中央社会保険医療協議会 総会 (第604回) 議事次第
・大塚製薬 : 国内初の造血器腫瘍遺伝子パネル検査 「ヘムサイト®」 新発売- 2025年3月1日より保険適用開始 -

編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。
編集・作図:編集部、 監修:所属専門医師。各領域の第一線の専門医が複数在籍。最新トピックに関する独自記事を配信中。